新人教版 化学课件:4.1.1《金属矿物的开发利用》
文档属性
| 名称 | 新人教版 化学课件:4.1.1《金属矿物的开发利用》 |

|
|
| 格式 | rar | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-01 00:00:00 | ||
图片预览






文档简介
课件26张PPT。 第一节
开发利用金属矿物和海水资源
第1课时 金属矿物的开发利用 绝大多数金属元素以什么形态 存在于自然界中?大多数金属元素: 化合态, 如Na、Fe
极少数金属元素: 游离态, 如Au、Pt一、金属的冶炼方法
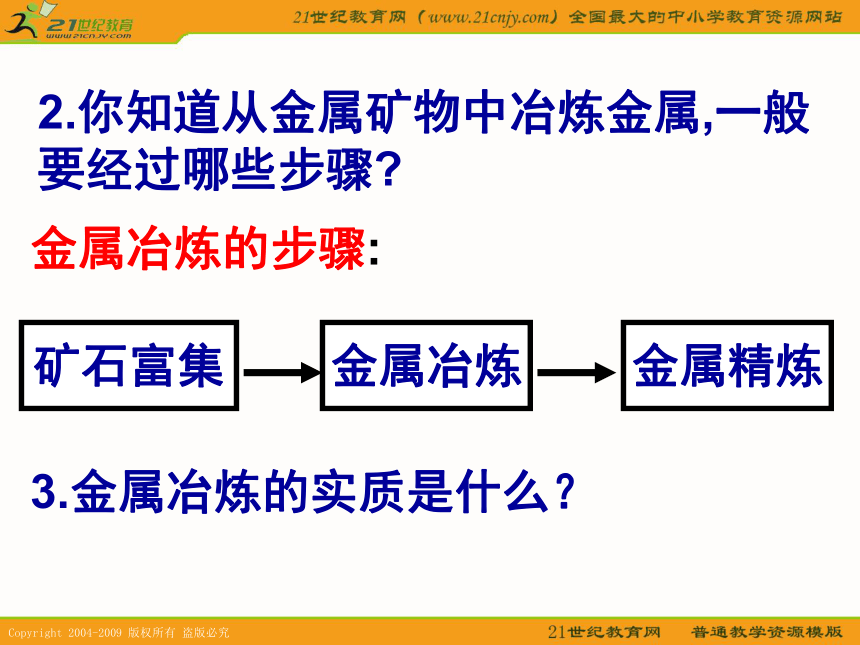
1. 金属的存在形态:金属矿石黄铜矿 CuFeS2菱镁矿 MgCO3 萤石 CaF2 现代—铝、铁合金等多样化的材料自行车不锈钢器具不锈钢器具金条首饰2.你知道从金属矿物中冶炼金属,一般
要经过哪些步骤?矿石富集金属冶炼金属精炼金属冶炼的步骤:3.金属冶炼的实质是什么? 金属冶炼的实质
金属元素:化合态
金属冶炼方法的依据为:
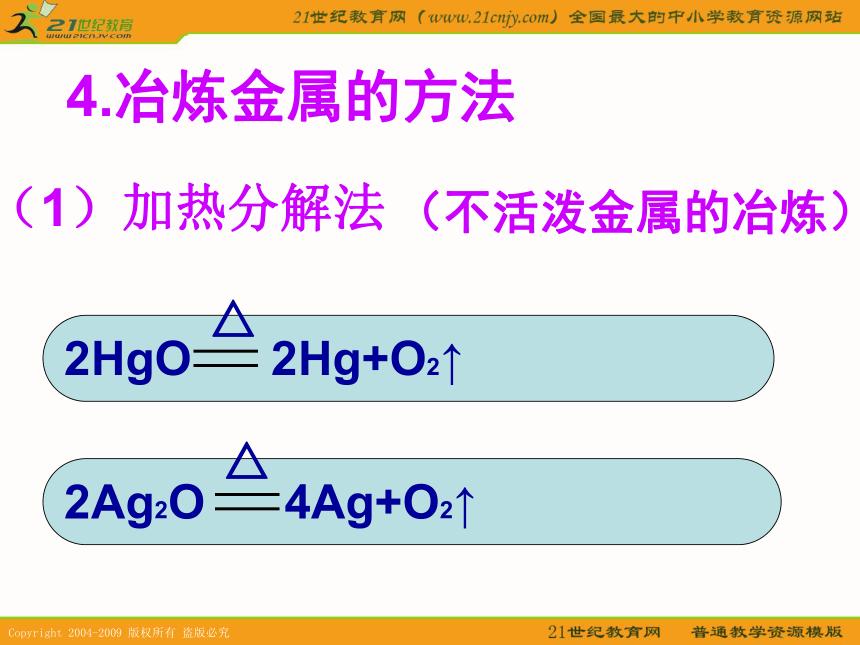
金属活动性得到电子游离态2HgO 2Hg+O2↑△2Ag2O 4Ag+O2↑△(不活泼金属的冶炼)(1)加热分解法4.冶炼金属的方法(2).电解法(非常活泼金属的冶炼)冰晶石:Na3AlF6(3).热还原法 常用的还原剂:H2、CO、C、活泼金属
高温
H2+CuO Cu+H2O
高温
Fe2O3+3CO 2Fe+3CO2
(较活泼金属的冶炼)小结:请结合金属活泼性顺序表总结
金属冶炼方法的一般规律:强弱强弱电解法热还原法热分解法二、铝热反应 活泼金属也可以做还原剂,把相对不活泼的金属置换出来,例如:铝
高温
Fe2O3+2Al == 2Fe+Al2O3
实验4-1 铝热反应
现象原理镁条剧烈燃烧,发出白光,导致混合物
剧烈反应,发出强光,有红热的熔融物生成。2Al+Fe2O3===2Fe+Al2O3高温镁条为引燃剂
氯酸钾为助燃剂
铝热剂:铝与氧化铁的混合物其它铝热反应 铝热反应的应用?????? 铝热反应的原理可以应用在生产上,如用于焊接钢轨等;在冶金工业上也常用这一反应原理,冶炼钒、铬、锰等熔点高的金属。表4-1 常见金属的冶炼原理金属冶炼原理FeFe2O3+3CO===2Fe+3CO2(高炉炼铁)
Fe2O3+2Al===2Fe+Al2O3(铝热法炼铁)高温高温CuCu2S+O2===2Cu+SO2(火法炼铜)
Fe+CuSO4===FeSO4+Cu(湿法炼铜)高温MgMgO+C===Mg+CO↑
MgCl2(熔融)===Mg+Cl2↑高温Al2Al2O3(熔融)===4Al+3O2↑电解冰晶石Na2NaCl(熔融)===2Na+Cl2↑
电解电解讨论1、人类先进入青铜器时代,还是
先进入铁器时代,为什么?
2、从能量转化和环保的角度讨论,
为什么要合理利用金属资源?
怎样合理利用?
金属资源的合理利用1、提高金属矿物的利用率
2、减少金属的使用量
3、加强金属资源的回收和再利用
4、使用其他材料代替金属材料三、金属的回收和环境保护回收金属的意义:
(1)节约矿物资源;
(2)节约能源;
(3)减少环境污染K Ca Na Mg Al Zn Fe…Cu Hg Ag Pt Au电解法热还原法热分解法金属活动顺序与金属冶炼方法的关系:思考总结:达标练习1.在冶金工业上,均不能用通常化学 还原剂制得的金属组是 ( )
A.Na、Mg 、Al
B.Na、K 、Zn
C.Fe、Cu、Ag
D.Na、Ca、Cu
A2.目前,工业上冶炼铝
通常采用的方法是 ( )
A.CO或氢气还原法
B.铝热反应法
C.电解法
D.热分解法C3.下列叙述正确的是( )
A.工业上用电解熔融氯化钠的
方法制取钠
B.钠加入氯化镁的饱和溶液中
可以制取金属镁
C.电解冶炼铝的原料是氯化铝
D.碳在高温下能还原氧化铝中的铝A4.下列说法正确的是( )
A.Mg可以用置换法和电解法
冶炼得到
B.Cu可以用电解法冶炼得到
C.Al可以用直接加热法冶炼得到
D.Fe可以用铝热法冶炼得到
D谢 谢!
开发利用金属矿物和海水资源
第1课时 金属矿物的开发利用 绝大多数金属元素以什么形态 存在于自然界中?大多数金属元素: 化合态, 如Na、Fe
极少数金属元素: 游离态, 如Au、Pt一、金属的冶炼方法
1. 金属的存在形态:金属矿石黄铜矿 CuFeS2菱镁矿 MgCO3 萤石 CaF2 现代—铝、铁合金等多样化的材料自行车不锈钢器具不锈钢器具金条首饰2.你知道从金属矿物中冶炼金属,一般
要经过哪些步骤?矿石富集金属冶炼金属精炼金属冶炼的步骤:3.金属冶炼的实质是什么? 金属冶炼的实质
金属元素:化合态
金属冶炼方法的依据为:
金属活动性得到电子游离态2HgO 2Hg+O2↑△2Ag2O 4Ag+O2↑△(不活泼金属的冶炼)(1)加热分解法4.冶炼金属的方法(2).电解法(非常活泼金属的冶炼)冰晶石:Na3AlF6(3).热还原法 常用的还原剂:H2、CO、C、活泼金属
高温
H2+CuO Cu+H2O
高温
Fe2O3+3CO 2Fe+3CO2
(较活泼金属的冶炼)小结:请结合金属活泼性顺序表总结
金属冶炼方法的一般规律:强弱强弱电解法热还原法热分解法二、铝热反应 活泼金属也可以做还原剂,把相对不活泼的金属置换出来,例如:铝
高温
Fe2O3+2Al == 2Fe+Al2O3
实验4-1 铝热反应
现象原理镁条剧烈燃烧,发出白光,导致混合物
剧烈反应,发出强光,有红热的熔融物生成。2Al+Fe2O3===2Fe+Al2O3高温镁条为引燃剂
氯酸钾为助燃剂
铝热剂:铝与氧化铁的混合物其它铝热反应 铝热反应的应用?????? 铝热反应的原理可以应用在生产上,如用于焊接钢轨等;在冶金工业上也常用这一反应原理,冶炼钒、铬、锰等熔点高的金属。表4-1 常见金属的冶炼原理金属冶炼原理FeFe2O3+3CO===2Fe+3CO2(高炉炼铁)
Fe2O3+2Al===2Fe+Al2O3(铝热法炼铁)高温高温CuCu2S+O2===2Cu+SO2(火法炼铜)
Fe+CuSO4===FeSO4+Cu(湿法炼铜)高温MgMgO+C===Mg+CO↑
MgCl2(熔融)===Mg+Cl2↑高温Al2Al2O3(熔融)===4Al+3O2↑电解冰晶石Na2NaCl(熔融)===2Na+Cl2↑
电解电解讨论1、人类先进入青铜器时代,还是
先进入铁器时代,为什么?
2、从能量转化和环保的角度讨论,
为什么要合理利用金属资源?
怎样合理利用?
金属资源的合理利用1、提高金属矿物的利用率
2、减少金属的使用量
3、加强金属资源的回收和再利用
4、使用其他材料代替金属材料三、金属的回收和环境保护回收金属的意义:
(1)节约矿物资源;
(2)节约能源;
(3)减少环境污染K Ca Na Mg Al Zn Fe…Cu Hg Ag Pt Au电解法热还原法热分解法金属活动顺序与金属冶炼方法的关系:思考总结:达标练习1.在冶金工业上,均不能用通常化学 还原剂制得的金属组是 ( )
A.Na、Mg 、Al
B.Na、K 、Zn
C.Fe、Cu、Ag
D.Na、Ca、Cu
A2.目前,工业上冶炼铝
通常采用的方法是 ( )
A.CO或氢气还原法
B.铝热反应法
C.电解法
D.热分解法C3.下列叙述正确的是( )
A.工业上用电解熔融氯化钠的
方法制取钠
B.钠加入氯化镁的饱和溶液中
可以制取金属镁
C.电解冶炼铝的原料是氯化铝
D.碳在高温下能还原氧化铝中的铝A4.下列说法正确的是( )
A.Mg可以用置换法和电解法
冶炼得到
B.Cu可以用电解法冶炼得到
C.Al可以用直接加热法冶炼得到
D.Fe可以用铝热法冶炼得到
D谢 谢!
