氧气的实验室制法
图片预览



文档简介
课件18张PPT。2.2(2)氧气的制法出示药品高锰酸钾(KMnO4) 氯酸钾(KClO3)、二氧化锰(MnO2)、氧气是由什么物质反应生成的?实验设计:实验过程实验探究氯酸钾熔化后产生氧气没有氧气生成加热不久就产生氧气结论:氧气由氯酸钾反应放出二氧化锰作用:加快反应速率一、催化剂:在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有变化的物质。催化作用:催化剂在化学反应中所起的作用。指加快或减慢一个改变两个不变质量和化学性质1、方法一:加热氯酸钾和二氧化锰的混合物
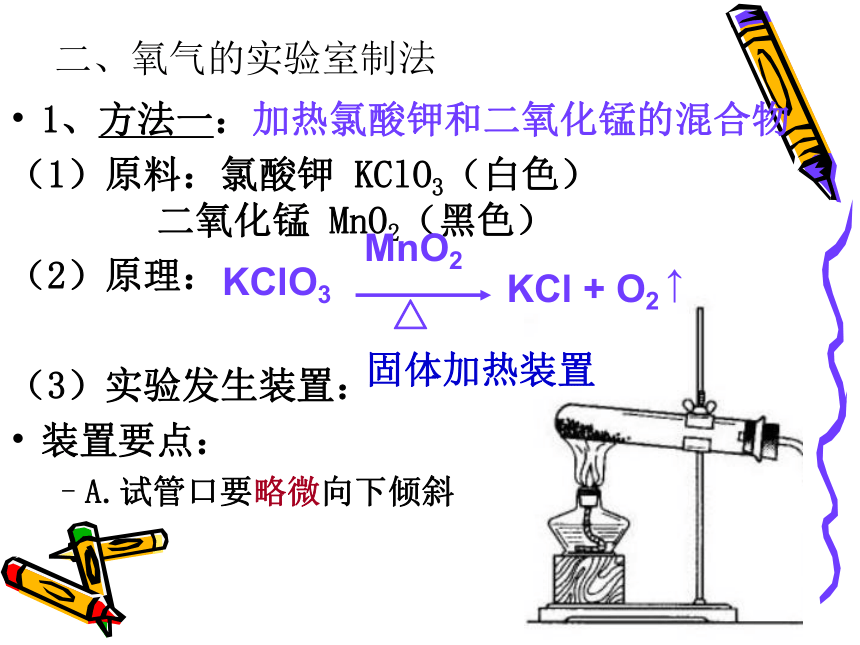
(1)原料:氯酸钾 KClO3(白色) 二氧化锰 MnO2(黑色)
(2)原理:
(3)实验发生装置:
装置要点:
A.试管口要略微向下倾斜
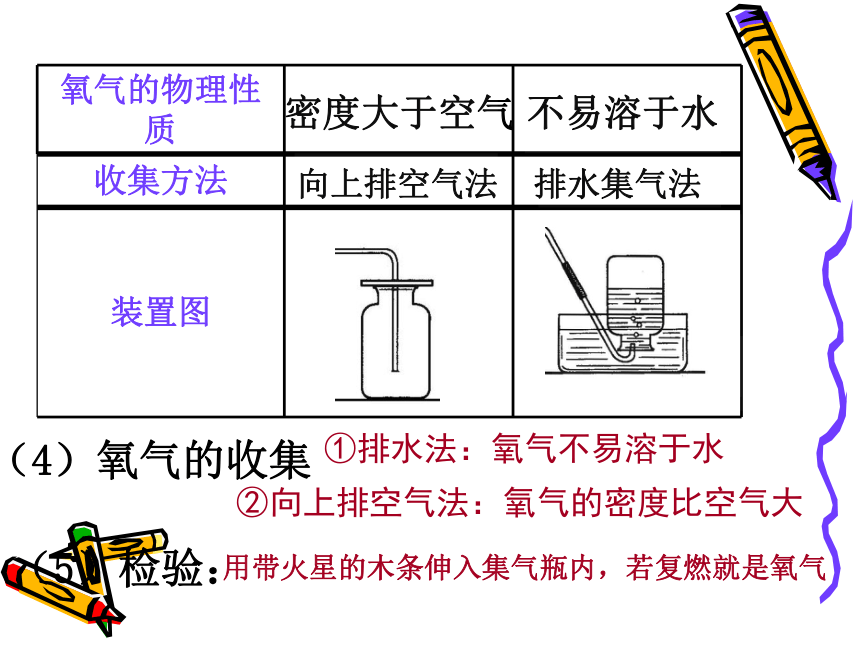
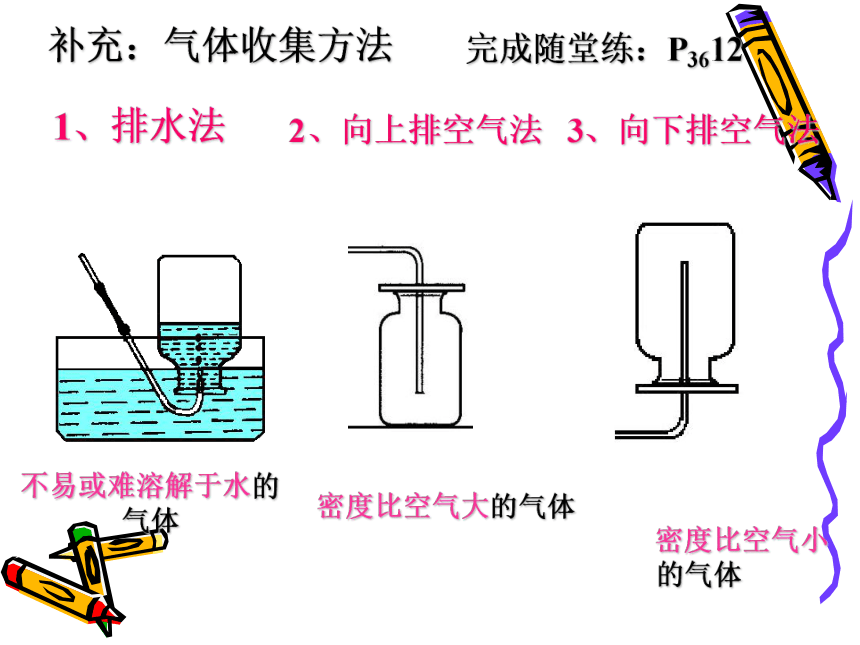
固体加热装置二、氧气的实验室制法KClO3MnO2KCl + O2△↑(4)氧气的收集向上排空气法排水集气法密度大于空气不易溶于水②向上排空气法:氧气的密度比空气大①排水法:氧气不易溶于水(5)检验:用带火星的木条伸入集气瓶内,若复燃就是氧气补充:气体收集方法1、排水法不易或难溶解于水的气体2、向上排空气法密度比空气大的气体密度比空气小的气体3、向下排空气法完成随堂练:P3612加热氯酸钾和二氧化锰混合物制取氧气的操作过程及要点查检查装置气密性装填装药品(KClO3、MnO2)定固定装置点点燃酒精灯收收集氧气(导管口有 大量气泡冒出再收集)离导管离开水槽熄熄灭酒精灯??为什么要等导管口有大量气泡冒出再收集?为什么先取出水槽中的导管,再熄灭酒精灯?开始时,试管内有空气,所以开始的气泡并不是氧气,或者是含杂质的氧气。先熄灭酒精灯,试管内气体冷却后收缩,会将水倒吸入试管,引起试管破裂。问题解决氯酸钾和二氧化锰共热制氧气化学反应式KClO3MnO2KCl + O2从剩余固体中回收MnO2的步骤:
注:MnO2不溶于水, KCl溶于水分析1、剩余固体的成分2、各成分的性质3、使用的方法△?↑KCl 与 MnO2KCl可溶,MnO2不溶溶解:KCl溶解于水中,MnO2不溶过滤:MnO2留在滤纸上,KCl溶液在烧杯中。溶解过滤(MnO2)蒸发(KCl)2、方法二:双氧水(过氧化氢H2O2)
(1)原料:双氧水(过氧化氢)、MnO2
(2)原理:
(3)实验发生装置:
固加液不加热装置注:长颈漏斗下端应浸入液面以下防止生成的气体从长颈漏斗中逸出 H2O2MnO2H2O + O2↑(4)验满:用带火星的木条放在集气瓶口,若复燃就证明收集满*方法三:
原料:高锰酸钾 KMnO4
实验发生装置:
化学反应式:KMnO4K2MnO4 + MnO2 + O2↑三、分解反应由一种物质生成两种或两种以上新物质的反应↑↑分解反应:由一种物质生成两种或两种以上
其他物质的反应。AB → A + B化合反应:A + B → AB(多变一)(一变多)知识对比原料: 空气-200℃-183℃-195℃液态空气N2气化O2气化四、工业制氧方法:分离
液态空气
(利用沸点不同)属于物理变化制取气体小结1、发生装置1、排水法2、向上排空气法3、向下排空气法固加液不加热装置固体加热装置2、收集装置7.判断下图是否有错误?如果有,请指出错误并加以改正。试管口要略向下倾斜导管只需突出胶塞少许铁夹应夹在试管中上部应对准药品加热导管口只能插在集气瓶口附近应加酒精2、氧气的收集向上排空气法排水集气法导管伸到容器底部带火星的木条放在瓶口复燃有气泡从瓶口逸出密度大于空气难溶于水
(1)原料:氯酸钾 KClO3(白色) 二氧化锰 MnO2(黑色)
(2)原理:
(3)实验发生装置:
装置要点:
A.试管口要略微向下倾斜
固体加热装置二、氧气的实验室制法KClO3MnO2KCl + O2△↑(4)氧气的收集向上排空气法排水集气法密度大于空气不易溶于水②向上排空气法:氧气的密度比空气大①排水法:氧气不易溶于水(5)检验:用带火星的木条伸入集气瓶内,若复燃就是氧气补充:气体收集方法1、排水法不易或难溶解于水的气体2、向上排空气法密度比空气大的气体密度比空气小的气体3、向下排空气法完成随堂练:P3612加热氯酸钾和二氧化锰混合物制取氧气的操作过程及要点查检查装置气密性装填装药品(KClO3、MnO2)定固定装置点点燃酒精灯收收集氧气(导管口有 大量气泡冒出再收集)离导管离开水槽熄熄灭酒精灯??为什么要等导管口有大量气泡冒出再收集?为什么先取出水槽中的导管,再熄灭酒精灯?开始时,试管内有空气,所以开始的气泡并不是氧气,或者是含杂质的氧气。先熄灭酒精灯,试管内气体冷却后收缩,会将水倒吸入试管,引起试管破裂。问题解决氯酸钾和二氧化锰共热制氧气化学反应式KClO3MnO2KCl + O2从剩余固体中回收MnO2的步骤:
注:MnO2不溶于水, KCl溶于水分析1、剩余固体的成分2、各成分的性质3、使用的方法△?↑KCl 与 MnO2KCl可溶,MnO2不溶溶解:KCl溶解于水中,MnO2不溶过滤:MnO2留在滤纸上,KCl溶液在烧杯中。溶解过滤(MnO2)蒸发(KCl)2、方法二:双氧水(过氧化氢H2O2)
(1)原料:双氧水(过氧化氢)、MnO2
(2)原理:
(3)实验发生装置:
固加液不加热装置注:长颈漏斗下端应浸入液面以下防止生成的气体从长颈漏斗中逸出 H2O2MnO2H2O + O2↑(4)验满:用带火星的木条放在集气瓶口,若复燃就证明收集满*方法三:
原料:高锰酸钾 KMnO4
实验发生装置:
化学反应式:KMnO4K2MnO4 + MnO2 + O2↑三、分解反应由一种物质生成两种或两种以上新物质的反应↑↑分解反应:由一种物质生成两种或两种以上
其他物质的反应。AB → A + B化合反应:A + B → AB(多变一)(一变多)知识对比原料: 空气-200℃-183℃-195℃液态空气N2气化O2气化四、工业制氧方法:分离
液态空气
(利用沸点不同)属于物理变化制取气体小结1、发生装置1、排水法2、向上排空气法3、向下排空气法固加液不加热装置固体加热装置2、收集装置7.判断下图是否有错误?如果有,请指出错误并加以改正。试管口要略向下倾斜导管只需突出胶塞少许铁夹应夹在试管中上部应对准药品加热导管口只能插在集气瓶口附近应加酒精2、氧气的收集向上排空气法排水集气法导管伸到容器底部带火星的木条放在瓶口复燃有气泡从瓶口逸出密度大于空气难溶于水
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
