高一开学初初中化学方程式和化学实验基本操作复习
文档属性
| 名称 | 高一开学初初中化学方程式和化学实验基本操作复习 |

|
|
| 格式 | zip | ||
| 文件大小 | 41.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-11 00:00:00 | ||
图片预览




文档简介
初中内容复习
初中化学方程式(写出下列反应方程式)
(一) 物质与氧气的反应:
(1)单质与氧气的反应:
1. 镁在空气中燃烧:
2. 铁在氧气中燃烧:
3. 氢气中空气中燃烧:
4. 红磷在空气中燃烧:
5、碳在氧气中充分燃烧:
6. 碳在氧气中不充分燃烧
(2)化合物与氧气的反应:
7. 一氧化碳在氧气中燃烧:
8. 甲烷在空气中燃烧:
9. 酒精在空气中燃烧:
(二).几个分解反应:
10. 水在直流电的作用下分解:
11. 加热碱式碳酸铜:
12. 加热氯酸钾(有少量的二氧化锰):
13. 加热高锰酸钾:
14. 碳酸不稳定而分解:
15. 高温煅烧石灰石:
(三).几个氧化还原反应:
16. 氢气还原氧化铜:
17. 木炭还原氧化铜:
18. 焦炭还原氧化铁:
19. 一氧化碳还原氧化铜:
20. 一氧化碳还原氧化铁:
(四).单质、氧化物、酸、碱、盐的相互关系
(1)金属单质 + 酸 ----- 盐 + 氢气 (置换反应)
21. 锌和稀硫酸;
22. 铁和稀硫酸
23. 镁和稀硫酸
24. 铝和稀硫酸
25. 锌和稀盐酸
26. 铁和稀盐酸
27. 镁和稀盐酸
28. 铝和稀盐酸
(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐
29. 铁和硫酸铜溶液反应:
30. 锌和硫酸铜溶液反应:
31. 铜和硝酸银溶液反应:
(3)碱性氧化物 +酸 ------ 盐 + 水
32.. 氧化铁和稀盐酸反应:
33.. 氧化铁和稀硫酸反应:
34.. 氧化铜和稀盐酸反应:
35 . 氧化铜和稀硫酸反应:
氧化镁和稀硫酸反应:
(4)酸性氧化物 +碱 -------- 盐 + 水
37.苛性钠暴露在空气中变质:
38.消石灰放在空气中变质
(5)酸 + 碱 -------- 盐 + 水
39.盐酸和烧碱起反应 :
40.盐酸和氢氧化钾反应:
41.盐酸和氢氧化铜反应:
42.盐酸和氢氧化钙反应:
43.盐酸和氢氧化铁反应
44.氢氧化铝药物治疗胃酸过多:
45.硫酸和烧碱反应:
46.硫酸和氢氧化钾反应:
47.硫酸和氢氧化铜反应:
48.硫酸和氢氧化铁反应:
49.硝酸和烧碱反应:
(6)酸 + 盐 -------- 另一种酸 + 另一种盐
50.大理石与稀盐酸反应:
51.碳酸钠与稀盐酸反应:
52.碳酸镁与稀盐酸反应:
53.盐酸和硝酸银溶液反应:
54.硫酸和碳酸钠反应:
55.硫酸和氯化钡溶液反应:
(7)碱 + 盐 -------- 另一种碱 + 另一种盐
56.氢氧化钠与硫酸铜:
57.氢氧化钠与氯化铁:
58.氢氧化钠与氯化镁:
59. 氢氧化钠与氯化铜:
60.氢氧化钙与碳酸钠:
(8)盐 + 盐 ----- 两种新盐
61.氯化钠溶液和硝酸银溶液:
62.硫酸钠和氯化钡:
五.其它反应:
63.二氧化碳溶解于水:
64.生石灰溶于水:
65.氧化钠溶于水:
二、九年级实验基本操作
第一节 化学实验基本方法
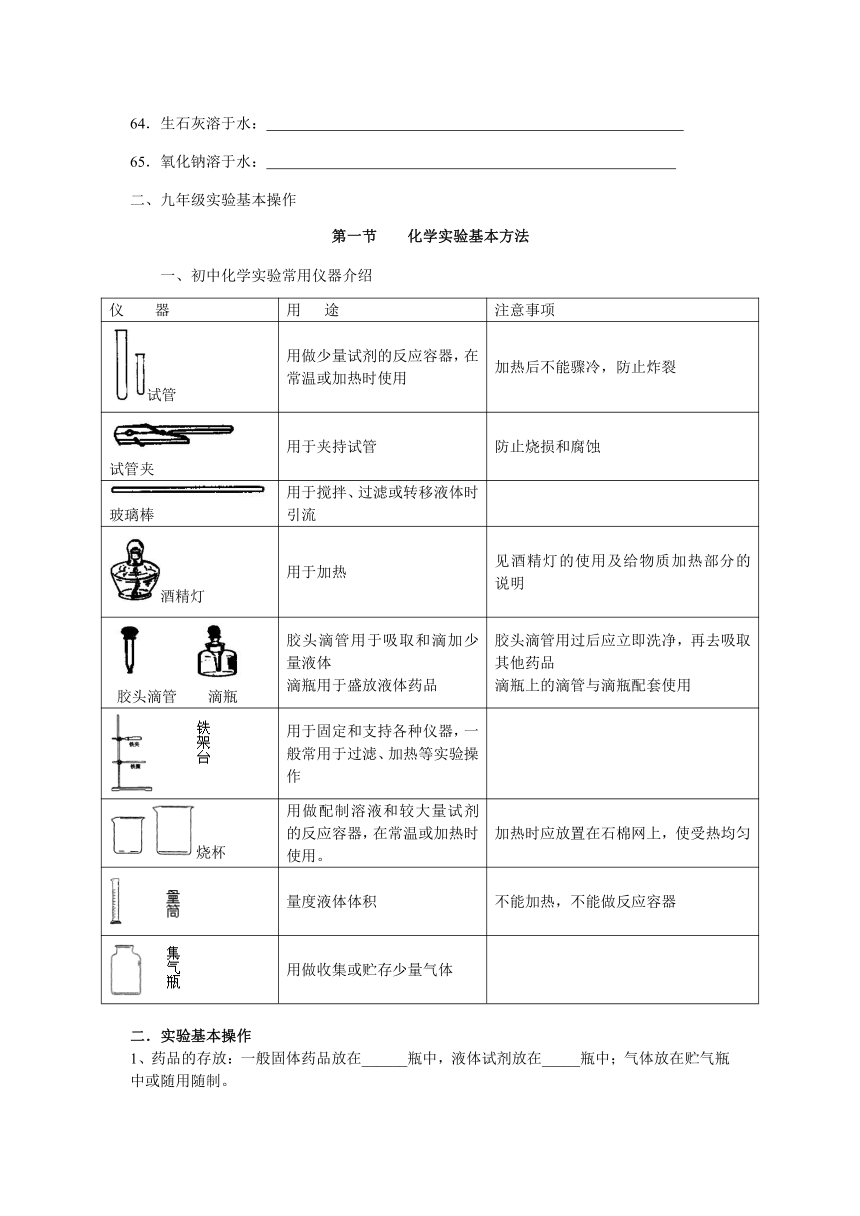
一、初中化学实验常用仪器介绍
仪 器 用 途 注意事项
试管 用做少量试剂的反应容器,在常温或加热时使用 加热后不能骤冷,防止炸裂
试管夹 用于夹持试管 防止烧损和腐蚀
玻璃棒 用于搅拌、过滤或转移液体时引流
酒精灯 用于加热 见酒精灯的使用及给物质加热部分的说明
胶头滴管 滴瓶 胶头滴管用于吸取和滴加少量液体滴瓶用于盛放液体药品 胶头滴管用过后应立即洗净,再去吸取其他药品滴瓶上的滴管与滴瓶配套使用
用于固定和支持各种仪器,一般常用于过滤、加热等实验操作
烧杯 用做配制溶液和较大量试剂的反应容器,在常温或加热时使用。 加热时应放置在石棉网上,使受热均匀
量度液体体积 不能加热,不能做反应容器
用做收集或贮存少量气体
二.实验基本操作
1、药品的存放:一般固体药品放在______瓶中,液体试剂放在_____瓶中;气体放在贮气瓶中或随用随制。
2、药品的取用
(1)取用药品遵守“三不”原则:___________________________________________________________。
(2)药品没有具体说明取用量时,一般按______取用:液体取_____毫升,固体____________________。
(3)用剩的药品要做到“三不一要”:_______________________________________________________。
(4)固体药品的取用:块状固体用_______,粉末状或细晶体用_______取,必要时可用纸槽取。
操作:______________________________________________。
(5)液体药品的取用:瓶塞_______,试剂瓶的标签________,瓶靠试管口,倒完后盖紧瓶塞,将剂瓶放回原处。
①定量取用液体操作:量筒放平,视线与______________________,再读出液体的体积数(若仰视会使读数_______,俯视会使读数________)。
②吸取和滴加少量液体用滴管:胶头在上,滴管不要接触反应容器内壁或放在实验台上,以免沾污滴管。
(6)浓酸,浓碱的使用:浓酸,浓碱都具有强腐蚀性,使用时要格外小心。
3、物品称量:用____________(左物右码)
4、物质的加热:
(1)酒精灯的使用:酒精量为酒精灯容积的_____-_________。
“三不”:__________________________________________________________________________。
(2)加热时所用仪器:固体用试管,蒸发皿; 液体用试管,烧杯,蒸发皿,烧瓶。
(3)加热操作:
用酒精灯的__________焰。
固体物质:先__________试管,再把酒精灯固定在放固体物质的部位用_________加热。
液体物质:(液体不超过试管容积的________)先均匀受热,再固定加热。不对着自己和他人。
一、化学实验安全:
1、遵守实验室规则:
了解安全措施:
掌握正确的操作方法。
重视并逐步熟悉污染物和废弃物的处理方法。
【模拟试题】
1. 判断镁在空气中燃烧属于化学变化的依据是( )
A. 发出耀眼的强光 B. 放出大量的热 C. 生成了氧化镁 D. 固体质量增加了
2. 固体氧化铜的颜色是( ) A. 绿色 B. 蓝色 C. 红色 D. 黑色
3. 做完实验后,对于用过的废酸,你认为正确的处理方法是( )
A.拿出实验室 B.留在实验台上,准备下次实验用 C.倒入废液缸中 D.放回原试剂瓶
4. 用托盘天平称量某物体的质量,如图所示,则物体的质量为( )
A. 4.5g B. 5g C. 5.5g D. 无法确定
5. 检查装置气密性的步骤为:(1)用手掌紧贴容器外壁;(2)导气管口有气泡冒出(说明气密性良好);(3)把导气管的一端浸入水中;(4)移开手后,导气管内形成一段水柱。其正确的操作顺序是( )
A.(1)(2)(3)(4) B.(2)(3)(4)(1) C.(3)(1)(2)(4) D.(4)(3)(2)(1)
6. 下列化学实验的操作不正确的是( )
A.给烧杯加热时,要垫上石棉网
B.给试管里的液体加热,液体体积不超过试管容积的三分之一
C.用托盘天平称量易潮解的药品时,药品应该放在玻璃器皿里称量
D.实验中剩余的药品都要放回原试剂瓶
7. 下列实验操作或记录正确的是( )
A. 用10mL量筒量取了8.65mL的水
B. 把氯化钠固体直接放在天平的托盘上称量
C. 稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌
D. 实验时未经洗净的滴管可直接再吸取别的试剂
8. 现有如下仪器:a. 量筒,b. 玻璃棒,c. 药匙,d. 托盘天平,e. 蒸发皿,f. 胶头滴管,请回答。
(1)称量固体药品的是_______________; (2)取用固体药品的是_______________;
(3)量取液体体积的是_______________; (4)可用于搅拌液体的是_______________;
(5)用于给液体加热的是_______________;(6)用于吸取和滴加少量液体的是_______________。
9. 下列做法符合操作规范的是_______________。(填写序号)
(1)为了节约药品,将实验用剩的药品放回原试剂瓶中
(2)使用托盘天平称量时,用镊子取放砝码
(3)给试管中的液体加热时,液体的量不超过试管容积的1/3
(4)过滤时,为了加快过滤速度,用玻璃棒搅动漏斗里的液体
(5)不慎将浓碱溶液沾在皮肤上,立即用大量水冲洗,再涂上硼酸溶液
10.某纪念币外观有银白色的金属光泽,一些同学认为它可能是铁制成的。在讨论时,有同学提出:“我们可以先拿磁铁来吸一下”。就“拿磁铁来吸一下”这一过程而言,属于科学探究中的( )
A. 实验 B. 假设 C. 观察 D. 做结论
11. 下列图示的操作中,正确的是( )
12. 2004年春,我国新发现的“非典”病例源于实验室感染,可见实验室的严格管理和规范操作十分重要。在下图所示实验操作中,正确的是( )
13. 下列实验操作正确的是( )
14. 下图是实验室中常见的化学仪器,相信你已多次使用过。
请按下列要求把仪器的名称填在横线上:
少量溶液相互反应时,需要用_____________;
(2)吸取和滴加少量的液体时,需要用__________;
配制溶液,溶解一定量的溶质时,需要用_____________;
(4)蒸发溶液时,需要用_____________。
15. 下列变化属于化学变化的是( )
16. NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能。NO难溶于水,通常条件下极易与氧气反应。实验室收集NO的装置是( )
17. 在一些科普读物中常见下列词汇。其中的颜色不是用来描述相关物质真实颜色的是( )
A. 蓝色晶体 B. 黑色粉末 C. 绿色食品 D. 银白色金属
18. 实验证明点燃的镁条在CO2气体中可以燃烧,生成氧化镁和炭黑(碳单质)。下列说法中错误的是( )
A. 金属镁着火不能用灭火器灭火
B. 镁在二氧化碳中燃烧的化学方程式是
C. 镁条在空气中燃烧时只与发生了化学反应
D. 不是一切物质的燃烧都要在空气或氧气中才能进行
【思考与交流】(1)同学们都听过“吹尽黄沙始见金”,你知道淘金者是利用什么方法和性质将黄金从沙里分离出来的吗?
(2)如果有铁和铜的混合物,你能用哪些方法将铁铜分离
你还能举出几种生活中混合物分离和提纯的例子吗?它们是怎么分开的?
二、混合物的分离提纯
自然界的物质绝大部分是以 混合物 的形式存在。 将混合物中各物质经过物理(或化学)变化,将其彼此分开 的操作叫做物质的分离提纯。分离物质提纯的方法依据是各成份性质的差别,可以是 物理 方法,也可是 化学 方法。
1、过滤和蒸发
【思考与交流】(1).粗盐的提纯所用到的仪器有哪些?
.在粗盐的提纯实验中,应注意哪些问题?
.粗盐的提纯实验的步骤是?每步操作的目的是
.在粗盐的提纯实验中,几次用到了玻璃棒,其作用和目的是什么?
小结:1、过滤和蒸发:
(1)过滤是
过滤时应注意:
①一贴、二低、三靠;
②根据实验要求不同,有时要对过滤出的沉淀物进行洗涤;
③洗涤方法是在过滤器中加蒸馏水浸没沉淀物,待其自然过滤干为一次洗涤,直至洗净为止;
④洗净的标准为取洗涤时的最后滤出液,检验其中是否含有可溶性物质。
(2)蒸发 。 (注: 加热时用玻璃棒不断搅动,防止局部温度过高,造成液滴飞溅。 )
2、物质的检验
【思考与交流】:(1).若粗盐中除含有不溶性的泥沙外,还含有可溶性的CaCl2、MgCl2以及一些硫酸盐等。你认为通过上述操作得到的是比较纯的氯化钠吗?可能还有什么杂质没有除去?
(2).在水溶液中NaCl和各种杂质以什么形式存在?
(3).如何检验Mg2+、Ca2+、SO42-?
【思考与交流】:(1).如果要除去粗盐中含有的可溶性杂质CaCl2、MgCl2及一些硫酸盐,应加入什么试剂
杂质 加入的试剂 化学方程式
硫酸盐
MgCl2
CaCl2
(2).在实际操作中,还要考虑所加试剂的先后顺序、试剂用量,以及试剂过量后如何处理等。你设计的除去离子的方法中有没有引入其他离子?想一想可用什么方法把它们除去?
小结:如何除去物质中的杂质?如果含有多种杂质时在除去时要注意什么问题?
初中化学方程式(写出下列反应方程式)
(一) 物质与氧气的反应:
(1)单质与氧气的反应:
1. 镁在空气中燃烧:
2. 铁在氧气中燃烧:
3. 氢气中空气中燃烧:
4. 红磷在空气中燃烧:
5、碳在氧气中充分燃烧:
6. 碳在氧气中不充分燃烧
(2)化合物与氧气的反应:
7. 一氧化碳在氧气中燃烧:
8. 甲烷在空气中燃烧:
9. 酒精在空气中燃烧:
(二).几个分解反应:
10. 水在直流电的作用下分解:
11. 加热碱式碳酸铜:
12. 加热氯酸钾(有少量的二氧化锰):
13. 加热高锰酸钾:
14. 碳酸不稳定而分解:
15. 高温煅烧石灰石:
(三).几个氧化还原反应:
16. 氢气还原氧化铜:
17. 木炭还原氧化铜:
18. 焦炭还原氧化铁:
19. 一氧化碳还原氧化铜:
20. 一氧化碳还原氧化铁:
(四).单质、氧化物、酸、碱、盐的相互关系
(1)金属单质 + 酸 ----- 盐 + 氢气 (置换反应)
21. 锌和稀硫酸;
22. 铁和稀硫酸
23. 镁和稀硫酸
24. 铝和稀硫酸
25. 锌和稀盐酸
26. 铁和稀盐酸
27. 镁和稀盐酸
28. 铝和稀盐酸
(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐
29. 铁和硫酸铜溶液反应:
30. 锌和硫酸铜溶液反应:
31. 铜和硝酸银溶液反应:
(3)碱性氧化物 +酸 ------ 盐 + 水
32.. 氧化铁和稀盐酸反应:
33.. 氧化铁和稀硫酸反应:
34.. 氧化铜和稀盐酸反应:
35 . 氧化铜和稀硫酸反应:
氧化镁和稀硫酸反应:
(4)酸性氧化物 +碱 -------- 盐 + 水
37.苛性钠暴露在空气中变质:
38.消石灰放在空气中变质
(5)酸 + 碱 -------- 盐 + 水
39.盐酸和烧碱起反应 :
40.盐酸和氢氧化钾反应:
41.盐酸和氢氧化铜反应:
42.盐酸和氢氧化钙反应:
43.盐酸和氢氧化铁反应
44.氢氧化铝药物治疗胃酸过多:
45.硫酸和烧碱反应:
46.硫酸和氢氧化钾反应:
47.硫酸和氢氧化铜反应:
48.硫酸和氢氧化铁反应:
49.硝酸和烧碱反应:
(6)酸 + 盐 -------- 另一种酸 + 另一种盐
50.大理石与稀盐酸反应:
51.碳酸钠与稀盐酸反应:
52.碳酸镁与稀盐酸反应:
53.盐酸和硝酸银溶液反应:
54.硫酸和碳酸钠反应:
55.硫酸和氯化钡溶液反应:
(7)碱 + 盐 -------- 另一种碱 + 另一种盐
56.氢氧化钠与硫酸铜:
57.氢氧化钠与氯化铁:
58.氢氧化钠与氯化镁:
59. 氢氧化钠与氯化铜:
60.氢氧化钙与碳酸钠:
(8)盐 + 盐 ----- 两种新盐
61.氯化钠溶液和硝酸银溶液:
62.硫酸钠和氯化钡:
五.其它反应:
63.二氧化碳溶解于水:
64.生石灰溶于水:
65.氧化钠溶于水:
二、九年级实验基本操作
第一节 化学实验基本方法
一、初中化学实验常用仪器介绍
仪 器 用 途 注意事项
试管 用做少量试剂的反应容器,在常温或加热时使用 加热后不能骤冷,防止炸裂
试管夹 用于夹持试管 防止烧损和腐蚀
玻璃棒 用于搅拌、过滤或转移液体时引流
酒精灯 用于加热 见酒精灯的使用及给物质加热部分的说明
胶头滴管 滴瓶 胶头滴管用于吸取和滴加少量液体滴瓶用于盛放液体药品 胶头滴管用过后应立即洗净,再去吸取其他药品滴瓶上的滴管与滴瓶配套使用
用于固定和支持各种仪器,一般常用于过滤、加热等实验操作
烧杯 用做配制溶液和较大量试剂的反应容器,在常温或加热时使用。 加热时应放置在石棉网上,使受热均匀
量度液体体积 不能加热,不能做反应容器
用做收集或贮存少量气体
二.实验基本操作
1、药品的存放:一般固体药品放在______瓶中,液体试剂放在_____瓶中;气体放在贮气瓶中或随用随制。
2、药品的取用
(1)取用药品遵守“三不”原则:___________________________________________________________。
(2)药品没有具体说明取用量时,一般按______取用:液体取_____毫升,固体____________________。
(3)用剩的药品要做到“三不一要”:_______________________________________________________。
(4)固体药品的取用:块状固体用_______,粉末状或细晶体用_______取,必要时可用纸槽取。
操作:______________________________________________。
(5)液体药品的取用:瓶塞_______,试剂瓶的标签________,瓶靠试管口,倒完后盖紧瓶塞,将剂瓶放回原处。
①定量取用液体操作:量筒放平,视线与______________________,再读出液体的体积数(若仰视会使读数_______,俯视会使读数________)。
②吸取和滴加少量液体用滴管:胶头在上,滴管不要接触反应容器内壁或放在实验台上,以免沾污滴管。
(6)浓酸,浓碱的使用:浓酸,浓碱都具有强腐蚀性,使用时要格外小心。
3、物品称量:用____________(左物右码)
4、物质的加热:
(1)酒精灯的使用:酒精量为酒精灯容积的_____-_________。
“三不”:__________________________________________________________________________。
(2)加热时所用仪器:固体用试管,蒸发皿; 液体用试管,烧杯,蒸发皿,烧瓶。
(3)加热操作:
用酒精灯的__________焰。
固体物质:先__________试管,再把酒精灯固定在放固体物质的部位用_________加热。
液体物质:(液体不超过试管容积的________)先均匀受热,再固定加热。不对着自己和他人。
一、化学实验安全:
1、遵守实验室规则:
了解安全措施:
掌握正确的操作方法。
重视并逐步熟悉污染物和废弃物的处理方法。
【模拟试题】
1. 判断镁在空气中燃烧属于化学变化的依据是( )
A. 发出耀眼的强光 B. 放出大量的热 C. 生成了氧化镁 D. 固体质量增加了
2. 固体氧化铜的颜色是( ) A. 绿色 B. 蓝色 C. 红色 D. 黑色
3. 做完实验后,对于用过的废酸,你认为正确的处理方法是( )
A.拿出实验室 B.留在实验台上,准备下次实验用 C.倒入废液缸中 D.放回原试剂瓶
4. 用托盘天平称量某物体的质量,如图所示,则物体的质量为( )
A. 4.5g B. 5g C. 5.5g D. 无法确定
5. 检查装置气密性的步骤为:(1)用手掌紧贴容器外壁;(2)导气管口有气泡冒出(说明气密性良好);(3)把导气管的一端浸入水中;(4)移开手后,导气管内形成一段水柱。其正确的操作顺序是( )
A.(1)(2)(3)(4) B.(2)(3)(4)(1) C.(3)(1)(2)(4) D.(4)(3)(2)(1)
6. 下列化学实验的操作不正确的是( )
A.给烧杯加热时,要垫上石棉网
B.给试管里的液体加热,液体体积不超过试管容积的三分之一
C.用托盘天平称量易潮解的药品时,药品应该放在玻璃器皿里称量
D.实验中剩余的药品都要放回原试剂瓶
7. 下列实验操作或记录正确的是( )
A. 用10mL量筒量取了8.65mL的水
B. 把氯化钠固体直接放在天平的托盘上称量
C. 稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌
D. 实验时未经洗净的滴管可直接再吸取别的试剂
8. 现有如下仪器:a. 量筒,b. 玻璃棒,c. 药匙,d. 托盘天平,e. 蒸发皿,f. 胶头滴管,请回答。
(1)称量固体药品的是_______________; (2)取用固体药品的是_______________;
(3)量取液体体积的是_______________; (4)可用于搅拌液体的是_______________;
(5)用于给液体加热的是_______________;(6)用于吸取和滴加少量液体的是_______________。
9. 下列做法符合操作规范的是_______________。(填写序号)
(1)为了节约药品,将实验用剩的药品放回原试剂瓶中
(2)使用托盘天平称量时,用镊子取放砝码
(3)给试管中的液体加热时,液体的量不超过试管容积的1/3
(4)过滤时,为了加快过滤速度,用玻璃棒搅动漏斗里的液体
(5)不慎将浓碱溶液沾在皮肤上,立即用大量水冲洗,再涂上硼酸溶液
10.某纪念币外观有银白色的金属光泽,一些同学认为它可能是铁制成的。在讨论时,有同学提出:“我们可以先拿磁铁来吸一下”。就“拿磁铁来吸一下”这一过程而言,属于科学探究中的( )
A. 实验 B. 假设 C. 观察 D. 做结论
11. 下列图示的操作中,正确的是( )
12. 2004年春,我国新发现的“非典”病例源于实验室感染,可见实验室的严格管理和规范操作十分重要。在下图所示实验操作中,正确的是( )
13. 下列实验操作正确的是( )
14. 下图是实验室中常见的化学仪器,相信你已多次使用过。
请按下列要求把仪器的名称填在横线上:
少量溶液相互反应时,需要用_____________;
(2)吸取和滴加少量的液体时,需要用__________;
配制溶液,溶解一定量的溶质时,需要用_____________;
(4)蒸发溶液时,需要用_____________。
15. 下列变化属于化学变化的是( )
16. NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能。NO难溶于水,通常条件下极易与氧气反应。实验室收集NO的装置是( )
17. 在一些科普读物中常见下列词汇。其中的颜色不是用来描述相关物质真实颜色的是( )
A. 蓝色晶体 B. 黑色粉末 C. 绿色食品 D. 银白色金属
18. 实验证明点燃的镁条在CO2气体中可以燃烧,生成氧化镁和炭黑(碳单质)。下列说法中错误的是( )
A. 金属镁着火不能用灭火器灭火
B. 镁在二氧化碳中燃烧的化学方程式是
C. 镁条在空气中燃烧时只与发生了化学反应
D. 不是一切物质的燃烧都要在空气或氧气中才能进行
【思考与交流】(1)同学们都听过“吹尽黄沙始见金”,你知道淘金者是利用什么方法和性质将黄金从沙里分离出来的吗?
(2)如果有铁和铜的混合物,你能用哪些方法将铁铜分离
你还能举出几种生活中混合物分离和提纯的例子吗?它们是怎么分开的?
二、混合物的分离提纯
自然界的物质绝大部分是以 混合物 的形式存在。 将混合物中各物质经过物理(或化学)变化,将其彼此分开 的操作叫做物质的分离提纯。分离物质提纯的方法依据是各成份性质的差别,可以是 物理 方法,也可是 化学 方法。
1、过滤和蒸发
【思考与交流】(1).粗盐的提纯所用到的仪器有哪些?
.在粗盐的提纯实验中,应注意哪些问题?
.粗盐的提纯实验的步骤是?每步操作的目的是
.在粗盐的提纯实验中,几次用到了玻璃棒,其作用和目的是什么?
小结:1、过滤和蒸发:
(1)过滤是
过滤时应注意:
①一贴、二低、三靠;
②根据实验要求不同,有时要对过滤出的沉淀物进行洗涤;
③洗涤方法是在过滤器中加蒸馏水浸没沉淀物,待其自然过滤干为一次洗涤,直至洗净为止;
④洗净的标准为取洗涤时的最后滤出液,检验其中是否含有可溶性物质。
(2)蒸发 。 (注: 加热时用玻璃棒不断搅动,防止局部温度过高,造成液滴飞溅。 )
2、物质的检验
【思考与交流】:(1).若粗盐中除含有不溶性的泥沙外,还含有可溶性的CaCl2、MgCl2以及一些硫酸盐等。你认为通过上述操作得到的是比较纯的氯化钠吗?可能还有什么杂质没有除去?
(2).在水溶液中NaCl和各种杂质以什么形式存在?
(3).如何检验Mg2+、Ca2+、SO42-?
【思考与交流】:(1).如果要除去粗盐中含有的可溶性杂质CaCl2、MgCl2及一些硫酸盐,应加入什么试剂
杂质 加入的试剂 化学方程式
硫酸盐
MgCl2
CaCl2
(2).在实际操作中,还要考虑所加试剂的先后顺序、试剂用量,以及试剂过量后如何处理等。你设计的除去离子的方法中有没有引入其他离子?想一想可用什么方法把它们除去?
小结:如何除去物质中的杂质?如果含有多种杂质时在除去时要注意什么问题?
