(高一化学)第一节 物质的分类(第一课时)导学案
文档属性
| 名称 | (高一化学)第一节 物质的分类(第一课时)导学案 |
|
|
| 格式 | rar | ||
| 文件大小 | 15.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-11 00:00:00 | ||
图片预览



文档简介
(高一化学)第一节 物质的分类(第一课时)
一、简单分类法及其应用
1、物质的分类
⑴交叉分类法
请同学们连线下列物质,并指明分类依据。
例一:交叉分类法
Na2SO4 含氧酸盐 Na2SO4分类依据1:_________________
K2SO4 无氧酸盐 Na2SO4分类依据2:_________________
NaCl 钠盐 Na2SO4分类依据3:___________________
BaSO4 硫酸盐
⑵树状分类法
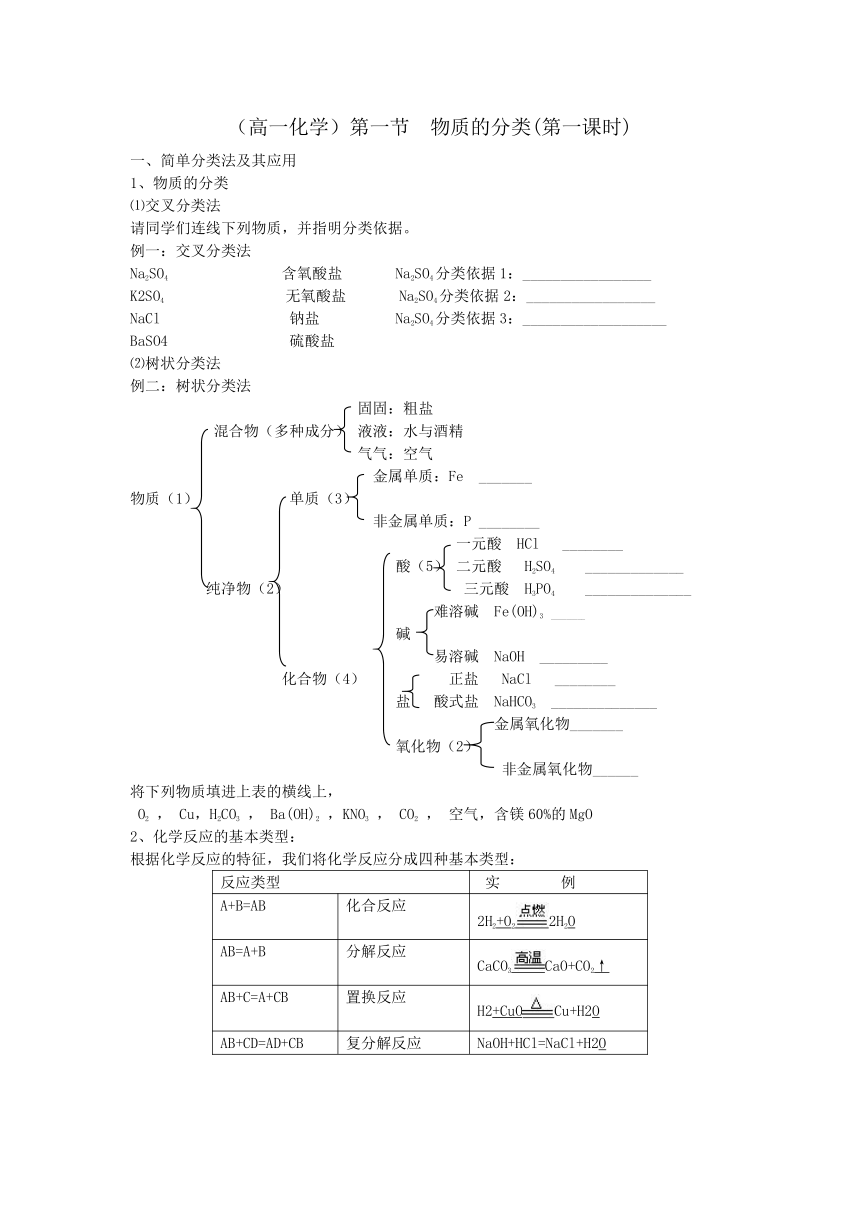
例二:树状分类法
固固:粗盐
混合物(多种成分) 液液:水与酒精
气气:空气
金属单质:Fe _______
物质(1) 单质(3)
非金属单质:P ________
一元酸 HCl ________
酸(5) 二元酸 H2SO4 _____________
纯净物(2) 三元酸 H3PO4 ______________
难溶碱 Fe(OH)3 _________
碱
易溶碱 NaOH _________
化合物(4) 正盐 NaCl ________
盐 酸式盐 NaHCO3 ______________
金属氧化物_______
氧化物(2)
非金属氧化物______
将下列物质填进上表的横线上,
O2 , Cu,H2CO3 , Ba(OH)2 ,KNO3 , CO2 , 空气,含镁60%的MgO
2、化学反应的基本类型:
根据化学反应的特征,我们将化学反应分成四种基本类型:
反应类型 实 例
A+B=AB 化合反应 2H2+O22H2O
AB=A+B 分解反应 CaCO3CaO+CO2↑
AB+C=A+CB 置换反应 H2+CuOCu+H2O
AB+CD=AD+CB 复分解反应 NaOH+HCl=NaCl+H2O
【同步练习】
1、每组物质都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来。
(1)NaCl、KCl、NaClO、BaCl2
(2)HClO3、KClO3、Cl2、NaClO3
(3)H3PO4、H4SiO4、HCl、H2SO4
*(4)浊液、溶液、胶体、水
(5)空气、N2、HCl、CuSO4·5H2O、
(6)铜、金、汞、钠
2.下列物质是你在生活中经常遇到的物质,其中属于纯净物是( )
A.煤 B.生铁 C.蒸馏水 D.矿泉水
3、环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于( )
A无机物 B有机物 C盐类 D非金属单质
4、经分析,某种物质只含一种元素,则此物质( )
A.一定是一种单质 B.一定是纯净物
C.一定是混合物 D.可能是纯净物,也可能是混合物
5、对于下列反应的反应类型的判断,不正确的是( )
A、CO2+H2O=H2CO3 化合反应 B、Cu(OH)2ΔCuO+H2O 分解反应
C、Fe2O3+3CO高温2Fe+3CO2 置换反应 D、NaCl+AgNO3=AgCl↓+NaNO3 复分解反应
6、从铁、盐酸、氧气、水、硝酸银溶液五种物质中选出一种或两种作反应物,按下列要求的反应类型各写一个化学方程式
化合反应___________________________
分解反应________ ________
置换反应____________ ____________
复分解反应_________________________
【课时同步练习】
1.下列物质中,肯定是纯净物的是( )
A.只由一种元素组成的物质
B.只由一种原子组成的物质
C.只由一种分子组成的物质
D.只由一种元素的阳离子跟另一种元素的阴离子组成的物质
2. 根据物质的分类,水不属于( )
A、氧化物 B、单质 C、化合物 D、纯净物
3.下列说法正确的是( )
A.纯净物是指由同种元素组成的物质 B.由同种元素组成的纯净物叫单质
C.由不同种分子组成的物质叫化合物 D.一种元素只能组成一种单质
4. 在高空中有一层臭氧层,它吸收了太阳光中绝大部分紫外线,使地球上的生物免受紫外线伤害,臭氧的化学式是O3,它是一种( )
A、混合物 B、氧化物 C、单质 D、化合物
5. 下列各组物质都是氧化物的是( )
A、KClO3、O2、MnO2 B、SO2、CaO、Fe2O3
C、NaOH、H2SO4、CaO D、H2O、MgO、C5H6O
6. 双氧水(H2O2)是隐形眼镜洗液的主要成分,下列说法正确的是( )
A、它是由氢气和氧气组成 B、它是由两个氢元素和2个氧元素组成
C、它是由氢元素和氧元素组成 D、它是由2个氢原子和2个氧原子组成
7. 单质与化合物的根本区别是( )
A、单质是一种物质,化合物至少含两种物质
B、单质是纯净物,化合物是混合物
C、单质只含一种元素,化合物至少含两种元素
D、单质是气体,化合物是固体
8.下列说法不正确的是( )
A、对于Na2SO4从组成上看既属于钠盐、又属于硫酸盐
B、对于Na2SO4和Na2S从组成上看都可以看作钠盐,又可以看作硫酸盐
C、每一种元素都可以在一定条件下以单质或化合物的形态存在
D、血糖属于混合物
9、下列关于酸、碱、盐元素组成的说法中,正确的是( )
A.酸、碱一定含有氢,盐一定不含氢
B.酸、碱、盐可能都不含金属元素
C.碱、盐可能含氧,酸一定含氧
D.盐、碱一定含有金属元素,酸一定不含金属元素
10、下列关于物质的分类正确的组合是( )
分 类组 合 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 盐酸 烧碱 氧化铝 二氧化氮
B 烧碱 硫酸 食盐 氧化镁 一氧化碳
C 苛性钠 醋酸 硝酸 过氧化钠 二氧化硫
D 苛性钾 硫酸 苏打 氧化钠 硫酸酐
11.在①海水②镁粉③高锰酸钾④冰水⑤空气⑥氧化镁⑦氯化钠⑧白磷⑨碳酸氢铵⑩液氧中,属于混合物的是(填物质代号) ,属于纯净物的是 ,属于单质的是 ,属于化合物的是 ,属于氧化物的是 。
12 . 膨化食品的包装袋中,经常有一个小纸袋,上面写着“干燥剂”、其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可用作干燥剂的理由是(用化学方程式表示)
(3)生石灰可以跟哪些类别的物质发生化学反应?举三例(用化学方程式表示)
、 、
(4)小纸袋中的物质能否长期持续地作干燥剂? ;原因
第一节 物质的分类(第二课时)
一、物质的分散体系
【思考】:混合物如何分类?
混合物(????) 酸
物质 纯净物 单质 碱
化合物 盐
氧化物
举例:请举例说明你生活中见到的混合物?
阅读: 了解什么是分散系?什么是分散质?什么是分散剂?
九种分散体系——按分散剂、分散质分别为固、液、气三态来分类
讨论:将下列分散系填入下表:汽水、自来水、白酒、牛奶,豆浆、食盐水、糖水、泡沫塑料、湿砖块、珍珠、云、雾、烟、尘。
分散质 分散剂 实 例
气 液
液 液
固 液
气 固
液 固
固 固
气 气
液 气
固 气
2、按分散质粒子的大小再分类
分散系 粒子大小
溶液
胶体
浊液
注:1nm=10-9m
二、胶体的性质
【实验探究】:溶液、胶体、浊液三种分散系的特点
分散系 溶液 胶体 浊液
实例 CuSO4溶液 Fe(OH)3胶体 泥水
稳定性
均一性
激光笔照射
透过滤纸的情况
半透膜
[小结]:溶液,胶体,浊液的本质区别是 ,区别溶液和胶体的简便方法是 。
【思考】1、为什么一束光射向胶体和溶液时,会出现这样不同的现象?
如何制取Fe(OH)3胶体
生活中还有哪些常见的丁达尔效应,胶体还有哪些性质
【小结】.胶体的知识在生活、生产和科研等方面有着重要用途,如常见的有:
①盐卤点豆腐 ②肥皂的制取分离 ③明矾、Fe(SO4)3溶液净水
④FeCl3溶液用于伤口止血 ⑤江河入海口形成的沙洲 ⑥水泥硬化
⑦冶金厂大量烟尘用高压电除去 ⑧土壤胶体中离子的吸附和交换过程,保肥
【针对练习】
1、(06全国高考卷2)下列叙述正确的是( )
A. 直径介于 1nm~10nm之间的微粒称为胶体
B. 电泳现象可证明胶体属于电解质溶液
C. 利用丁达尔效应可以区别溶液与胶体
D. 胶体粒子很小,可以透过半透膜
2 .下列分散系最稳定的是( )
A.悬浊液 B.乳浊液 C.胶体 D.溶液
3、胶体最本质的特征是( )
A、丁达尔效应 B、可以通过滤纸
C、布朗运动 D、分散质颗粒的直径在1~100nm之间
4.(04年上海)氢氧化铁胶体稳定存在的主要原因是( )
A.胶粒直径小于1nm B.胶粒作布郎运动
C.胶粒带正电荷 D.胶粒不能通过半透膜
5.(02年上海卷)氯化铁溶液与氢氧化铁胶体具有的共同性质是
A.分散质颗粒直径都在1~100nm之间 B.能透过半透膜
C.都会产生丁达尔现象 D.呈红褐色
6、(05年清远)下列有关胶体和溶液的比较中正确的是( )
A。溶液呈电中性,胶体带有电荷
B。溶液中溶质粒子运动有规律,胶体粒子运动无规律
C。溶液中通过光束没有特殊现象,胶体中通过光束有丁达尔现象
D。胶体粒子的直径比溶液中溶质粒子的直径小
7、溶液、胶体和浊液这三种分散质的根本区别是( )
A、是否为大量分子或离子的集合体
B、分散质微粒直径的大小
C、能否透过滤纸或半透膜
D、是否均一、稳定透明
8、下列关于胶体的说法中正确的是( )
A、胶体外观不均匀 B、胶体不能通过滤纸
C、胶粒做不停的、无秩序的运动 D、胶体不稳定,静置后容易产生沉淀
9、(2002年上海高考).将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是( )
A 冷水 B 沸水 C NaOH浓溶液 D NaCl浓溶液
【课时同步练习】
1、关于制备氢氧化铁胶体的正确操作方法( )
A.在氯化铁溶液中滴入氢氧化钠溶液 B.加热煮沸氯化铁溶液
C.把氯化铁溶液滴入热水中 D.把饱和的氯化铁溶液滴入到沸水中
2、Fe(OH)3胶体和MgCl2溶液共同具备的性质是( )
A、都比较稳定,密闭放置不产生沉淀 B、两者均有丁达尔现象
C、加入盐酸先产生沉淀,后溶解 D、分散质微粒可通过滤纸
3、用特殊方法把固体物质加工到纳米级(1~100nm,1nm=10—9m)的超细粉末微粒,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是(
A、溶液 B、悬浊液 C、胶体 D、乳浊液
4、下列分散系能发生丁达尔现象的是( )
A.CH3CH2OH水溶液 B.雾
C.含有尘埃的空气 D.饱和食盐水
5、血液中重要的蛋白质是一种胶体,在实验中不慎手被玻璃划破,可用FeCl3溶液紧急止血,其主要原因可能是( ) ( http: / / www. / course / 40722 / yx / HX_22_02_015 / )
A.FeCl3溶液具有杀菌消毒作用
B.FeCl3溶液能使血液凝聚
C.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口
D.FeCl3能使血液发生化学变化
6、不能用有关胶体的观点解释的现象是 ( )
A、在江河入海处易形成三角洲
B、0.01mol/LAgNO3溶液中滴入同浓度NaI溶液,看不到黄色沉淀
C、在NaF溶液中滴入AgNO3溶液看不到沉淀
D、同一钢笔同时使用不同牌号的墨水易发生堵塞
7.关于胶体和溶液的叙述中正确的是 ( )
A.胶体带电荷,而溶液呈电中性
B.胶体加入电解质可产生沉淀,而溶液不能
C.胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系
D.胶体能够发生丁达尔现象,而溶液则不能
8.胶体区别于其它分散系的特征是 ( )
A.胶体粒子直径在1-100nm之间 B.胶体粒子带电荷
C.胶体粒子不能穿过半透膜 D.胶体粒子能够发生布朗运动
9.在水泥厂、冶金厂常用高压电作用于气溶胶,以除去大量烟尘,减少烟尘对空气的污染。这种除尘法的原理是 ( )
A.渗析 B.电泳 C.凝聚 D.丁达尔现象
一、简单分类法及其应用
1、物质的分类
⑴交叉分类法
请同学们连线下列物质,并指明分类依据。
例一:交叉分类法
Na2SO4 含氧酸盐 Na2SO4分类依据1:_________________
K2SO4 无氧酸盐 Na2SO4分类依据2:_________________
NaCl 钠盐 Na2SO4分类依据3:___________________
BaSO4 硫酸盐
⑵树状分类法
例二:树状分类法
固固:粗盐
混合物(多种成分) 液液:水与酒精
气气:空气
金属单质:Fe _______
物质(1) 单质(3)
非金属单质:P ________
一元酸 HCl ________
酸(5) 二元酸 H2SO4 _____________
纯净物(2) 三元酸 H3PO4 ______________
难溶碱 Fe(OH)3 _________
碱
易溶碱 NaOH _________
化合物(4) 正盐 NaCl ________
盐 酸式盐 NaHCO3 ______________
金属氧化物_______
氧化物(2)
非金属氧化物______
将下列物质填进上表的横线上,
O2 , Cu,H2CO3 , Ba(OH)2 ,KNO3 , CO2 , 空气,含镁60%的MgO
2、化学反应的基本类型:
根据化学反应的特征,我们将化学反应分成四种基本类型:
反应类型 实 例
A+B=AB 化合反应 2H2+O22H2O
AB=A+B 分解反应 CaCO3CaO+CO2↑
AB+C=A+CB 置换反应 H2+CuOCu+H2O
AB+CD=AD+CB 复分解反应 NaOH+HCl=NaCl+H2O
【同步练习】
1、每组物质都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来。
(1)NaCl、KCl、NaClO、BaCl2
(2)HClO3、KClO3、Cl2、NaClO3
(3)H3PO4、H4SiO4、HCl、H2SO4
*(4)浊液、溶液、胶体、水
(5)空气、N2、HCl、CuSO4·5H2O、
(6)铜、金、汞、钠
2.下列物质是你在生活中经常遇到的物质,其中属于纯净物是( )
A.煤 B.生铁 C.蒸馏水 D.矿泉水
3、环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于( )
A无机物 B有机物 C盐类 D非金属单质
4、经分析,某种物质只含一种元素,则此物质( )
A.一定是一种单质 B.一定是纯净物
C.一定是混合物 D.可能是纯净物,也可能是混合物
5、对于下列反应的反应类型的判断,不正确的是( )
A、CO2+H2O=H2CO3 化合反应 B、Cu(OH)2ΔCuO+H2O 分解反应
C、Fe2O3+3CO高温2Fe+3CO2 置换反应 D、NaCl+AgNO3=AgCl↓+NaNO3 复分解反应
6、从铁、盐酸、氧气、水、硝酸银溶液五种物质中选出一种或两种作反应物,按下列要求的反应类型各写一个化学方程式
化合反应___________________________
分解反应________ ________
置换反应____________ ____________
复分解反应_________________________
【课时同步练习】
1.下列物质中,肯定是纯净物的是( )
A.只由一种元素组成的物质
B.只由一种原子组成的物质
C.只由一种分子组成的物质
D.只由一种元素的阳离子跟另一种元素的阴离子组成的物质
2. 根据物质的分类,水不属于( )
A、氧化物 B、单质 C、化合物 D、纯净物
3.下列说法正确的是( )
A.纯净物是指由同种元素组成的物质 B.由同种元素组成的纯净物叫单质
C.由不同种分子组成的物质叫化合物 D.一种元素只能组成一种单质
4. 在高空中有一层臭氧层,它吸收了太阳光中绝大部分紫外线,使地球上的生物免受紫外线伤害,臭氧的化学式是O3,它是一种( )
A、混合物 B、氧化物 C、单质 D、化合物
5. 下列各组物质都是氧化物的是( )
A、KClO3、O2、MnO2 B、SO2、CaO、Fe2O3
C、NaOH、H2SO4、CaO D、H2O、MgO、C5H6O
6. 双氧水(H2O2)是隐形眼镜洗液的主要成分,下列说法正确的是( )
A、它是由氢气和氧气组成 B、它是由两个氢元素和2个氧元素组成
C、它是由氢元素和氧元素组成 D、它是由2个氢原子和2个氧原子组成
7. 单质与化合物的根本区别是( )
A、单质是一种物质,化合物至少含两种物质
B、单质是纯净物,化合物是混合物
C、单质只含一种元素,化合物至少含两种元素
D、单质是气体,化合物是固体
8.下列说法不正确的是( )
A、对于Na2SO4从组成上看既属于钠盐、又属于硫酸盐
B、对于Na2SO4和Na2S从组成上看都可以看作钠盐,又可以看作硫酸盐
C、每一种元素都可以在一定条件下以单质或化合物的形态存在
D、血糖属于混合物
9、下列关于酸、碱、盐元素组成的说法中,正确的是( )
A.酸、碱一定含有氢,盐一定不含氢
B.酸、碱、盐可能都不含金属元素
C.碱、盐可能含氧,酸一定含氧
D.盐、碱一定含有金属元素,酸一定不含金属元素
10、下列关于物质的分类正确的组合是( )
分 类组 合 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 盐酸 烧碱 氧化铝 二氧化氮
B 烧碱 硫酸 食盐 氧化镁 一氧化碳
C 苛性钠 醋酸 硝酸 过氧化钠 二氧化硫
D 苛性钾 硫酸 苏打 氧化钠 硫酸酐
11.在①海水②镁粉③高锰酸钾④冰水⑤空气⑥氧化镁⑦氯化钠⑧白磷⑨碳酸氢铵⑩液氧中,属于混合物的是(填物质代号) ,属于纯净物的是 ,属于单质的是 ,属于化合物的是 ,属于氧化物的是 。
12 . 膨化食品的包装袋中,经常有一个小纸袋,上面写着“干燥剂”、其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可用作干燥剂的理由是(用化学方程式表示)
(3)生石灰可以跟哪些类别的物质发生化学反应?举三例(用化学方程式表示)
、 、
(4)小纸袋中的物质能否长期持续地作干燥剂? ;原因
第一节 物质的分类(第二课时)
一、物质的分散体系
【思考】:混合物如何分类?
混合物(????) 酸
物质 纯净物 单质 碱
化合物 盐
氧化物
举例:请举例说明你生活中见到的混合物?
阅读: 了解什么是分散系?什么是分散质?什么是分散剂?
九种分散体系——按分散剂、分散质分别为固、液、气三态来分类
讨论:将下列分散系填入下表:汽水、自来水、白酒、牛奶,豆浆、食盐水、糖水、泡沫塑料、湿砖块、珍珠、云、雾、烟、尘。
分散质 分散剂 实 例
气 液
液 液
固 液
气 固
液 固
固 固
气 气
液 气
固 气
2、按分散质粒子的大小再分类
分散系 粒子大小
溶液
胶体
浊液
注:1nm=10-9m
二、胶体的性质
【实验探究】:溶液、胶体、浊液三种分散系的特点
分散系 溶液 胶体 浊液
实例 CuSO4溶液 Fe(OH)3胶体 泥水
稳定性
均一性
激光笔照射
透过滤纸的情况
半透膜
[小结]:溶液,胶体,浊液的本质区别是 ,区别溶液和胶体的简便方法是 。
【思考】1、为什么一束光射向胶体和溶液时,会出现这样不同的现象?
如何制取Fe(OH)3胶体
生活中还有哪些常见的丁达尔效应,胶体还有哪些性质
【小结】.胶体的知识在生活、生产和科研等方面有着重要用途,如常见的有:
①盐卤点豆腐 ②肥皂的制取分离 ③明矾、Fe(SO4)3溶液净水
④FeCl3溶液用于伤口止血 ⑤江河入海口形成的沙洲 ⑥水泥硬化
⑦冶金厂大量烟尘用高压电除去 ⑧土壤胶体中离子的吸附和交换过程,保肥
【针对练习】
1、(06全国高考卷2)下列叙述正确的是( )
A. 直径介于 1nm~10nm之间的微粒称为胶体
B. 电泳现象可证明胶体属于电解质溶液
C. 利用丁达尔效应可以区别溶液与胶体
D. 胶体粒子很小,可以透过半透膜
2 .下列分散系最稳定的是( )
A.悬浊液 B.乳浊液 C.胶体 D.溶液
3、胶体最本质的特征是( )
A、丁达尔效应 B、可以通过滤纸
C、布朗运动 D、分散质颗粒的直径在1~100nm之间
4.(04年上海)氢氧化铁胶体稳定存在的主要原因是( )
A.胶粒直径小于1nm B.胶粒作布郎运动
C.胶粒带正电荷 D.胶粒不能通过半透膜
5.(02年上海卷)氯化铁溶液与氢氧化铁胶体具有的共同性质是
A.分散质颗粒直径都在1~100nm之间 B.能透过半透膜
C.都会产生丁达尔现象 D.呈红褐色
6、(05年清远)下列有关胶体和溶液的比较中正确的是( )
A。溶液呈电中性,胶体带有电荷
B。溶液中溶质粒子运动有规律,胶体粒子运动无规律
C。溶液中通过光束没有特殊现象,胶体中通过光束有丁达尔现象
D。胶体粒子的直径比溶液中溶质粒子的直径小
7、溶液、胶体和浊液这三种分散质的根本区别是( )
A、是否为大量分子或离子的集合体
B、分散质微粒直径的大小
C、能否透过滤纸或半透膜
D、是否均一、稳定透明
8、下列关于胶体的说法中正确的是( )
A、胶体外观不均匀 B、胶体不能通过滤纸
C、胶粒做不停的、无秩序的运动 D、胶体不稳定,静置后容易产生沉淀
9、(2002年上海高考).将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是( )
A 冷水 B 沸水 C NaOH浓溶液 D NaCl浓溶液
【课时同步练习】
1、关于制备氢氧化铁胶体的正确操作方法( )
A.在氯化铁溶液中滴入氢氧化钠溶液 B.加热煮沸氯化铁溶液
C.把氯化铁溶液滴入热水中 D.把饱和的氯化铁溶液滴入到沸水中
2、Fe(OH)3胶体和MgCl2溶液共同具备的性质是( )
A、都比较稳定,密闭放置不产生沉淀 B、两者均有丁达尔现象
C、加入盐酸先产生沉淀,后溶解 D、分散质微粒可通过滤纸
3、用特殊方法把固体物质加工到纳米级(1~100nm,1nm=10—9m)的超细粉末微粒,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是(
A、溶液 B、悬浊液 C、胶体 D、乳浊液
4、下列分散系能发生丁达尔现象的是( )
A.CH3CH2OH水溶液 B.雾
C.含有尘埃的空气 D.饱和食盐水
5、血液中重要的蛋白质是一种胶体,在实验中不慎手被玻璃划破,可用FeCl3溶液紧急止血,其主要原因可能是( ) ( http: / / www. / course / 40722 / yx / HX_22_02_015 / )
A.FeCl3溶液具有杀菌消毒作用
B.FeCl3溶液能使血液凝聚
C.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口
D.FeCl3能使血液发生化学变化
6、不能用有关胶体的观点解释的现象是 ( )
A、在江河入海处易形成三角洲
B、0.01mol/LAgNO3溶液中滴入同浓度NaI溶液,看不到黄色沉淀
C、在NaF溶液中滴入AgNO3溶液看不到沉淀
D、同一钢笔同时使用不同牌号的墨水易发生堵塞
7.关于胶体和溶液的叙述中正确的是 ( )
A.胶体带电荷,而溶液呈电中性
B.胶体加入电解质可产生沉淀,而溶液不能
C.胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系
D.胶体能够发生丁达尔现象,而溶液则不能
8.胶体区别于其它分散系的特征是 ( )
A.胶体粒子直径在1-100nm之间 B.胶体粒子带电荷
C.胶体粒子不能穿过半透膜 D.胶体粒子能够发生布朗运动
9.在水泥厂、冶金厂常用高压电作用于气溶胶,以除去大量烟尘,减少烟尘对空气的污染。这种除尘法的原理是 ( )
A.渗析 B.电泳 C.凝聚 D.丁达尔现象
