等效平衡等效平衡
图片预览




文档简介
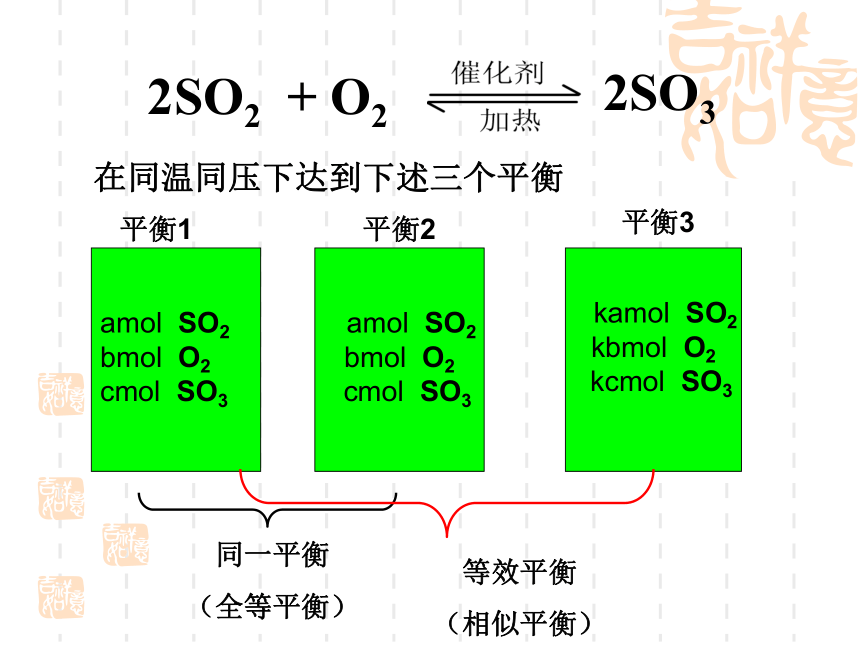
课件14张PPT。等 效 平 衡2019年2月24日星期日等效平衡:在一定条件下,可逆反应只要起始浓度相当,无论经过何种途径,但达到化学平衡时,只要同种物质的体积分数相同,这样的平衡称为等效平衡。在同温同压下达到下述三个平衡 起始: 2mol 1mol 0
Δt内改变:2amol amol 2amol
t时后: (2-2a)mol (1-a)mol 2amol
t1时刻后平衡:xmol ymol zmol(1):起始等效,建立全等平衡状态分析:在同温同体积密闭容器中,起始时加入
(1)2molSO2+1molO2 (2) (2-2a)molSO2+(1-a)molO2+2amolSO3 达到平衡时所建立平衡全等 起始: 2mol 1mol 0
平衡时物质的量:xmol ymol zmol
平衡时体积分数: a% b% c%
若起始: 4mol 2mol 04mol SO2
2mol O2SO2
2xmol
O2
2ymol
SO3
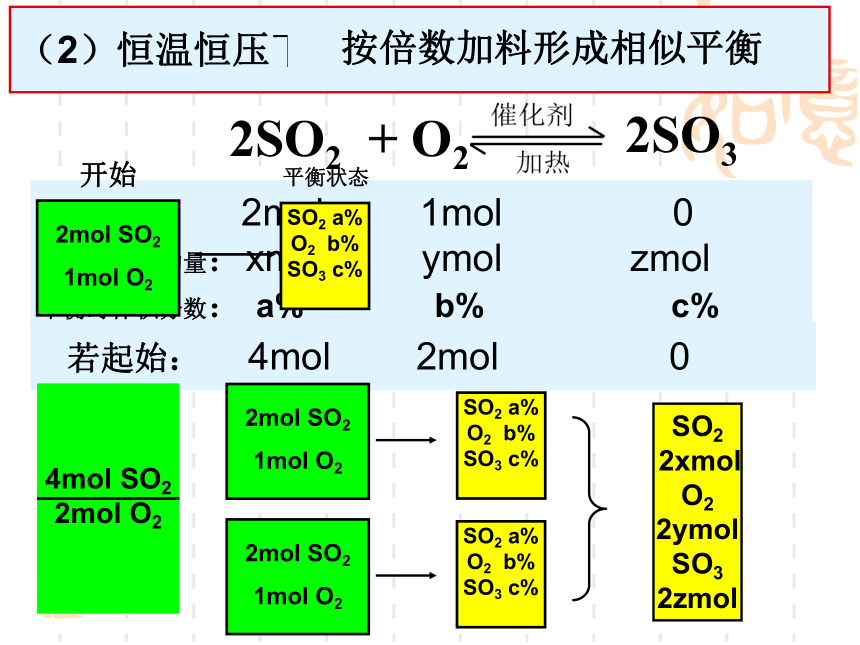
2zmol(2)恒温恒压下,按倍数加料形成相似平衡等效平衡问题1.5a00.52g-8m(g-3m)a 起始: 2mol 1mol 0
平衡时物质的量:xmol ymol zmol
平衡时体积分数: a% b% c%
若起始: 4mol 2mol 0SO2 a%
O2 b%
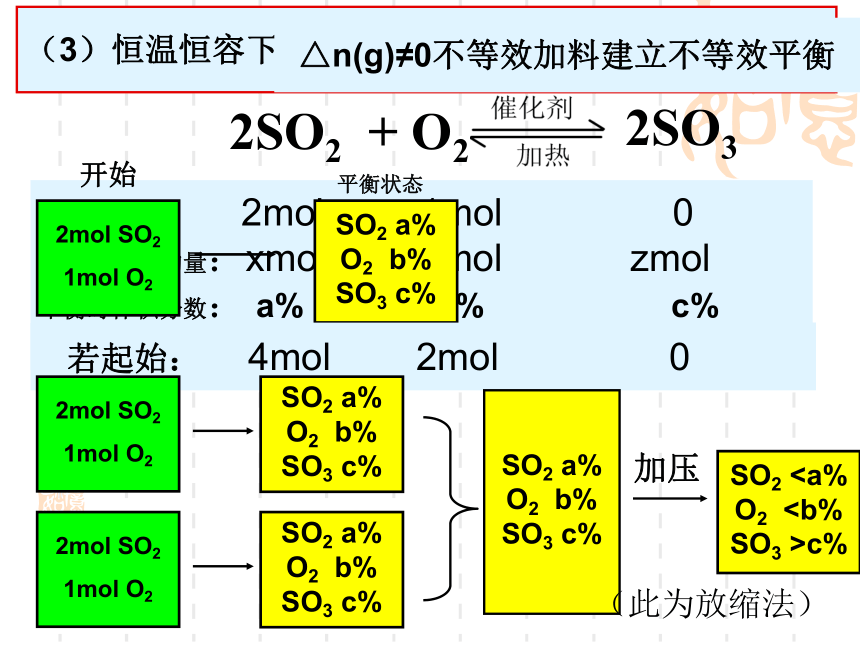
SO3 c%(3)恒温恒容下,SO2O2 SO3 >c%△n(g)≠0不等效加料建立不等效平衡(此为放缩法) 若起始: 2mol 2mol 0 起始: 1mol 1mol 0
平衡时物质的量:xmol ymol zmol
平衡时体积分数: a% b% c%H2 a%
I2 b%
HI c%(3)恒温恒容下,△n(g)=0按倍数加料形成等效平衡等效平衡小结等效平衡问题1.在一个固定体积的密闭容器中,加入2molA和1molB,发生反应:
2A(气) + B(气) 3C(气) + D(气)
达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
A. 4molA+2molB
B. 2molA+1molB+3molC+1molD
C. 3molC+1molD+1molB
D. 3molC+1molDD2、在固定体积的密闭容器内,加入2mol A、1mol B,发生反应:
A(气)+B(气) 2C(气)达 到平衡时,C的质量分数为W。在相同(T、V)条件下,按下列情况充入物质达到平衡时C的质量分数仍为W的是
A.2mol C
B.3mol C
C.4mol A、2mol B
D.1mol A、2mol CAB3.在一恒容的容器中充入2 mol A和1 mol B,发生反应2 A(g) + B(g) x C(g),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为0.6 mol,B为0.3 mol,C为1.4 mol充入容器,达到平衡后,C的体积分数仍为W%,则x的值为 ( )
A .只能为2 B.只能为3
C.可能是2,也可能是3
D.无法确定C4、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:
3A(气)+2B(气) xC(气)+yD(气)
达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则X,Y的值分别为( )
A x=3 y=1 B x=4 y=1
C x=5 y =1 D x=10 y=2 ﹏CDN2 + 3H2 2NH3mgxm+ x/2g +3x/20:g - 4m==x/2x==2g-8mm+ x/2==m+ x/2m+ (2g-8m)/2==g - 3m
Δt内改变:2amol amol 2amol
t时后: (2-2a)mol (1-a)mol 2amol
t1时刻后平衡:xmol ymol zmol(1):起始等效,建立全等平衡状态分析:在同温同体积密闭容器中,起始时加入
(1)2molSO2+1molO2 (2) (2-2a)molSO2+(1-a)molO2+2amolSO3 达到平衡时所建立平衡全等 起始: 2mol 1mol 0
平衡时物质的量:xmol ymol zmol
平衡时体积分数: a% b% c%
若起始: 4mol 2mol 04mol SO2
2mol O2SO2
2xmol
O2
2ymol
SO3
2zmol(2)恒温恒压下,按倍数加料形成相似平衡等效平衡问题1.5a00.52g-8m(g-3m)a 起始: 2mol 1mol 0
平衡时物质的量:xmol ymol zmol
平衡时体积分数: a% b% c%
若起始: 4mol 2mol 0SO2 a%
O2 b%
SO3 c%(3)恒温恒容下,SO2
平衡时物质的量:xmol ymol zmol
平衡时体积分数: a% b% c%H2 a%
I2 b%
HI c%(3)恒温恒容下,△n(g)=0按倍数加料形成等效平衡等效平衡小结等效平衡问题1.在一个固定体积的密闭容器中,加入2molA和1molB,发生反应:
2A(气) + B(气) 3C(气) + D(气)
达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
A. 4molA+2molB
B. 2molA+1molB+3molC+1molD
C. 3molC+1molD+1molB
D. 3molC+1molDD2、在固定体积的密闭容器内,加入2mol A、1mol B,发生反应:
A(气)+B(气) 2C(气)达 到平衡时,C的质量分数为W。在相同(T、V)条件下,按下列情况充入物质达到平衡时C的质量分数仍为W的是
A.2mol C
B.3mol C
C.4mol A、2mol B
D.1mol A、2mol CAB3.在一恒容的容器中充入2 mol A和1 mol B,发生反应2 A(g) + B(g) x C(g),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为0.6 mol,B为0.3 mol,C为1.4 mol充入容器,达到平衡后,C的体积分数仍为W%,则x的值为 ( )
A .只能为2 B.只能为3
C.可能是2,也可能是3
D.无法确定C4、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:
3A(气)+2B(气) xC(气)+yD(气)
达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则X,Y的值分别为( )
A x=3 y=1 B x=4 y=1
C x=5 y =1 D x=10 y=2 ﹏CDN2 + 3H2 2NH3mgxm+ x/2g +3x/20:g - 4m==x/2x==2g-8mm+ x/2==m+ x/2m+ (2g-8m)/2==g - 3m
