鲁科版选修三第一章第二节 原子结构与元素周期表(练习)
文档属性
| 名称 | 鲁科版选修三第一章第二节 原子结构与元素周期表(练习) |

|
|
| 格式 | zip | ||
| 文件大小 | 27.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-14 00:00:00 | ||
图片预览


文档简介
第二节 原子结构与元素周期表
高考资源网【基础检测】
1.下列四种元素中,其单质氧化性最强的是 ( )
A.原子含有未成对电子最多的第二周期元素
B.位于周期表中第三周期ⅢA族的元素
C.原子最外电子层排布为2s22p6的元素
D.原子最外电子层排布为3s23P5的元素
2.某元素有6个电子处于n=3,l=2的能级上,根据洪特规则推测它在d轨道上未成对电子数为 ( )
A.3 B.4 C.5 D.2
3.在多电子原子中,各电子具有下列量子数,其中能量最高的电子是 ( )
A. B.
C. D.
4.在多电子原子中,轨道能量是由谁决定。 ( )
A. n B. n和m C. n和l D. n、l、m
5.以下元素的原子半径递变规律是( )
A. Be<B<Na<Mg B. B<Be<Mg<Na
C. Be<B<Mg<Na D. B<Be<Na<Mg
6.价电子满足4s和3d为半满的元素是( )
A. Ca B. V C. Cr D.Cu
7.写出下列基态原子的核外电子排布
⑴ 17Cl ;
⑵ 24Cr ;
⑶ 34Se ;
⑷ 81Tl 。
8.指出下列元素是主族元素还是副族元素?位于周期表中第几周期?第几族?
⑴ 1s22s22p63s23p4 ;
(2) [Kr] 4d105s25p2 ;
(3) [Ar] 3d34s2 ;
(4) [Ar] 3d104s1 。
9.氢原子的电子能级由 决定,而锂原子的电子能级由 共同决定。
10.在周期表中可分为 、 、 、 、 五个区,各区的价电子排布为 、 、 、 、 。
11.具有下列价电子排布的元素位于周期表中哪个区?是金属元素还是非金属元素?
⑴ ns2(n≠1) ;
⑵ ns2np4 ;
⑶ (n-1)d5ns2 ;
⑷ (n-1)d8ns2 。
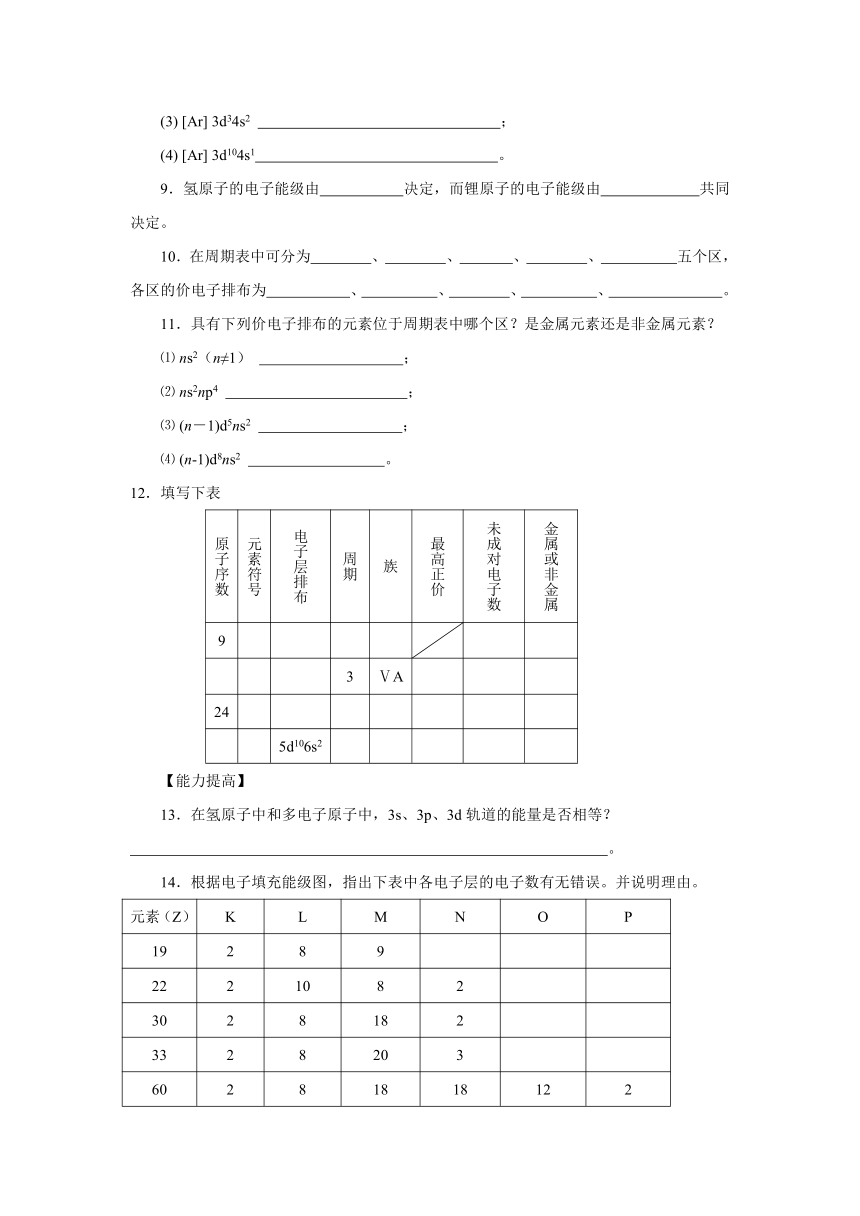
12.填写下表
原子序数 元素符号 电子层排布 周期 族 最高正价 未成对电子数 金属或非金属
9
3 ⅤA
24
5d106s2
【能力提高】
13.在氢原子中和多电子原子中,3s、3p、3d轨道的能量是否相等?
。
14.根据电子填充能级图,指出下表中各电子层的电子数有无错误。并说明理由。
元素(Z) K L M N O P
19 2 8 9
22 2 10 8 2
30 2 8 18 2
33 2 8 20 3
60 2 8 18 18 12 2
15.某元素原子序数为33,则
⑴ 此元素原子的电子总数是 ,有 个未成对电子。
⑵ 有 各电子层, 个能级, 个原子轨道。
⑶ 它的价电子排布为 。
16.满足下列条件之一的是哪一族或哪一种元素?
⑴ 最外层具有6个p电子: 。
⑵ 价电子数是n=4、l=0的轨道上有2个电子和n=3、l=2的轨道上有5个电子: 。
⑶ 次外层d轨道全满,最外层有一个s电子: 。
⑷ 某元素+3价离子和氩原子的电子排布相同: 。
⑸ 某元素+3价离子的3d轨道半充满: 。
17.若元素原子最外层仅有一个电子,它的量子数为:n=4、l=0、m=0、ms=。
⑴ 符合上述条件的元素可以有几种?原子序数各为多少?
⑵ 写出相应元素原子的电子排布,并指出在周期表中的位置(周期、族、区)、最高正价、金属或非金属。
18.已知甲、乙、丙丁四种元素,其中甲为第4周期元素与丁能形成原子比为1∶1的化合物。乙为第4周期d区元素,其最高正价为+7。丙与甲同周期,并具有相同的最高正化合价。丁为所有元素中最活泼的非金属元素。填写下表:
元素 价电子排布 周期 族 金属或非金属
甲
乙
丙
丁
19.设X、Y、Z代表3种元素。已知:①X+和Y-两种离子具有相同的电子层结构; ②Z元素原子核内质子数比Y元素原子核内质子数少9个;
③Y和Z两元素可以形成四核42个电子的负一价阴离子。据此,请填空:
⑴Y元素是 ,Z元素是 。
⑵由X、Y、Z三元素所形成的含68个电子的盐类化合物之化学式是
20.短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、
D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径
最大的主族元素。试回答下列问题:
(1)A的元素符号 ;D的原子结构示意图 。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是 。
(3)A、B、C、D形成的化合物B2A2、CD2、D2A、DA2中,各原子都满足最外层8电子结构的是 (请填写具体的化学式)
(4)CA2与D元素的单质在水溶液中反应的化学方程式是 。
【综合探究】
21.A元素的单质的化学性质活泼,A元素的原子在本周期中原子半径最大.B元素的氧化物2.0g恰好跟100mL0.50mol/L硫酸完全反应.B元素单质跟D元素单质反应生成化合物BD2.根据以上事实填写下列空白:
A的原子结构示意图 ;C原子的电子排布式 ;BD2的电子式 .
若向C的氧化物的水化物中加入A的氧化物的水化物,则溶液显碱性.C的氧化物的水化物化学式是 。
22.请用四个量子数表示原子序数为24的元素的每个价电子的运动状态.
参考答案
【基础检测】
1. D 2. B 3. D 4. C 5. B 6. C
7.(1)1s22s22p63s23p5或[Ne]3s23p5
(2) 1s22s22p63s23p63d54s1或[Ar]3d54s1
(3)1s22s22p63s23p63d104s24p4或[Ar] 3d104s24p4
(4) 1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p1或[Xe]4f145d106s26p1
8.(1)第3周期第ⅥA 族
(2)第5周期第ⅣA族
(3)第4周期第ⅤB族
(4)第4周期第ⅠB族
9.主量子数(n), 主量子数(n)及角量子数(l)
10.s区、p区、d区、ds区、f区;ns1-2、ns2np1-6、(n-1)d1-9ns1-2、(n-1)d10ns1-2、(n-2)f0-14(n-1)d0-2ns2
11.(1)s区、金属
(2)p区、非金属(n≥6为金属)
(3)d区、金属
(4)d区、金属
12.
原子序数 元素符号 电子层排布 周期 族 最高正价 未成对电子数 金属或非金属
9 F [He]2s22p5 2 ⅦA 1 非金属
15 P [Ne]3s23p3 3 ⅤA +5 3 非金属
24 Cr [Ar]3d54s1 4 ⅥB +6 6 金属
80 Hg [Xe]5d106s2 6 ⅡB +2 0 金属
【能力提高】
13.在氢原子中 E3s=E3p=E3d , 在多电子原子中E3s<E3p<E3d
14.Z=19,(2、8、9)有错误,因为最外层不能超过8个电子。应为2、8、8、1。
Z=22,(2、10、8、2)有错误,因为每一电子层最多可容纳2n2个电子,所以L层电子数应为8,不能为10,应为2、8、10、2。
Z=30无错误。
Z=33,(2、8、20、3)有错误,因为次外层不能超过18个电子。应为2、8、18、5。
Z=60,(2、8、18、18、12、2)有错误,因为当n=6时,E6s<E4f<E5d<E6p ,填5d前要填4f,次外层为12个电子即有d电子,则倒三层必有f电子,即倒三层电子数必大于18,应为2、8、18、22、8、2。
15.该元素原子的电子层排布为:1s22s22p63s23p63d104s24p3
(1)33,3(2)4,8,18(3)4s24p3
16.( 1)具有p6(即np6)排布的是稀有气体元素(He除外)。
(2)符合n=4,l=0(即4s)轨道上2个电子和n=3,l=2轨道(即3d)上有5个电子的排布是锰Mn。
(3)具有(n-1)d10ns1排布的元素是ⅠB族元素。
(4)该元素是钪Sc。
(5)该元素是Fe。
17.⑴ 根据题意知这类元素原子最外层电子排布为4s1,所以它们可能是K、Cr、Cu三种元素,其原子序数是19、24、29。
⑵ K:1s22s22p63s23p64s1,第4周期,ⅠA族,s区,最高正价+1,是金属元素。
Cr:1s22s22p63s23p63d54s1,第4周期,ⅥB族,d区,最高正价+6,是金属元素。
Cu:1s22s22p63s23p63d104s1,第4周期,ⅠB族,ds区,最高正价+3,是金属元素。
18.
元素 价电子排布 周期 族 金属或非金属
甲 4s1 4 ⅠA 金属
乙 3d54s2 4 ⅦB 金属
丙 4s24p5 4 ⅦA 非金属
丁 2s22p5 2 ⅦA 非金属
19.⑴Cl(氯),O(氧) ⑵ KClO3
20.(1)O;
(2)S2->O2->Na+
(3)Na2O2、SCl2、Cl2O
(4)SO2+Cl2+2H2O=2HCl+H2SO
【综合探究】
21.A:
22.24号元素为Cr,价电子结构为 3d54s1.
3d轨道: n l m ms
3 2 -2 + (或全为- )
3 2 -1 +
3 2 0 +
3 2 +1 +
3 2 +2 +
4s轨道: 4 0 0 + (或为- )
www.
+17
8
2
7
+11
8
2
1
高考资源网【基础检测】
1.下列四种元素中,其单质氧化性最强的是 ( )
A.原子含有未成对电子最多的第二周期元素
B.位于周期表中第三周期ⅢA族的元素
C.原子最外电子层排布为2s22p6的元素
D.原子最外电子层排布为3s23P5的元素
2.某元素有6个电子处于n=3,l=2的能级上,根据洪特规则推测它在d轨道上未成对电子数为 ( )
A.3 B.4 C.5 D.2
3.在多电子原子中,各电子具有下列量子数,其中能量最高的电子是 ( )
A. B.
C. D.
4.在多电子原子中,轨道能量是由谁决定。 ( )
A. n B. n和m C. n和l D. n、l、m
5.以下元素的原子半径递变规律是( )
A. Be<B<Na<Mg B. B<Be<Mg<Na
C. Be<B<Mg<Na D. B<Be<Na<Mg
6.价电子满足4s和3d为半满的元素是( )
A. Ca B. V C. Cr D.Cu
7.写出下列基态原子的核外电子排布
⑴ 17Cl ;
⑵ 24Cr ;
⑶ 34Se ;
⑷ 81Tl 。
8.指出下列元素是主族元素还是副族元素?位于周期表中第几周期?第几族?
⑴ 1s22s22p63s23p4 ;
(2) [Kr] 4d105s25p2 ;
(3) [Ar] 3d34s2 ;
(4) [Ar] 3d104s1 。
9.氢原子的电子能级由 决定,而锂原子的电子能级由 共同决定。
10.在周期表中可分为 、 、 、 、 五个区,各区的价电子排布为 、 、 、 、 。
11.具有下列价电子排布的元素位于周期表中哪个区?是金属元素还是非金属元素?
⑴ ns2(n≠1) ;
⑵ ns2np4 ;
⑶ (n-1)d5ns2 ;
⑷ (n-1)d8ns2 。
12.填写下表
原子序数 元素符号 电子层排布 周期 族 最高正价 未成对电子数 金属或非金属
9
3 ⅤA
24
5d106s2
【能力提高】
13.在氢原子中和多电子原子中,3s、3p、3d轨道的能量是否相等?
。
14.根据电子填充能级图,指出下表中各电子层的电子数有无错误。并说明理由。
元素(Z) K L M N O P
19 2 8 9
22 2 10 8 2
30 2 8 18 2
33 2 8 20 3
60 2 8 18 18 12 2
15.某元素原子序数为33,则
⑴ 此元素原子的电子总数是 ,有 个未成对电子。
⑵ 有 各电子层, 个能级, 个原子轨道。
⑶ 它的价电子排布为 。
16.满足下列条件之一的是哪一族或哪一种元素?
⑴ 最外层具有6个p电子: 。
⑵ 价电子数是n=4、l=0的轨道上有2个电子和n=3、l=2的轨道上有5个电子: 。
⑶ 次外层d轨道全满,最外层有一个s电子: 。
⑷ 某元素+3价离子和氩原子的电子排布相同: 。
⑸ 某元素+3价离子的3d轨道半充满: 。
17.若元素原子最外层仅有一个电子,它的量子数为:n=4、l=0、m=0、ms=。
⑴ 符合上述条件的元素可以有几种?原子序数各为多少?
⑵ 写出相应元素原子的电子排布,并指出在周期表中的位置(周期、族、区)、最高正价、金属或非金属。
18.已知甲、乙、丙丁四种元素,其中甲为第4周期元素与丁能形成原子比为1∶1的化合物。乙为第4周期d区元素,其最高正价为+7。丙与甲同周期,并具有相同的最高正化合价。丁为所有元素中最活泼的非金属元素。填写下表:
元素 价电子排布 周期 族 金属或非金属
甲
乙
丙
丁
19.设X、Y、Z代表3种元素。已知:①X+和Y-两种离子具有相同的电子层结构; ②Z元素原子核内质子数比Y元素原子核内质子数少9个;
③Y和Z两元素可以形成四核42个电子的负一价阴离子。据此,请填空:
⑴Y元素是 ,Z元素是 。
⑵由X、Y、Z三元素所形成的含68个电子的盐类化合物之化学式是
20.短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、
D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径
最大的主族元素。试回答下列问题:
(1)A的元素符号 ;D的原子结构示意图 。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是 。
(3)A、B、C、D形成的化合物B2A2、CD2、D2A、DA2中,各原子都满足最外层8电子结构的是 (请填写具体的化学式)
(4)CA2与D元素的单质在水溶液中反应的化学方程式是 。
【综合探究】
21.A元素的单质的化学性质活泼,A元素的原子在本周期中原子半径最大.B元素的氧化物2.0g恰好跟100mL0.50mol/L硫酸完全反应.B元素单质跟D元素单质反应生成化合物BD2.根据以上事实填写下列空白:
A的原子结构示意图 ;C原子的电子排布式 ;BD2的电子式 .
若向C的氧化物的水化物中加入A的氧化物的水化物,则溶液显碱性.C的氧化物的水化物化学式是 。
22.请用四个量子数表示原子序数为24的元素的每个价电子的运动状态.
参考答案
【基础检测】
1. D 2. B 3. D 4. C 5. B 6. C
7.(1)1s22s22p63s23p5或[Ne]3s23p5
(2) 1s22s22p63s23p63d54s1或[Ar]3d54s1
(3)1s22s22p63s23p63d104s24p4或[Ar] 3d104s24p4
(4) 1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p1或[Xe]4f145d106s26p1
8.(1)第3周期第ⅥA 族
(2)第5周期第ⅣA族
(3)第4周期第ⅤB族
(4)第4周期第ⅠB族
9.主量子数(n), 主量子数(n)及角量子数(l)
10.s区、p区、d区、ds区、f区;ns1-2、ns2np1-6、(n-1)d1-9ns1-2、(n-1)d10ns1-2、(n-2)f0-14(n-1)d0-2ns2
11.(1)s区、金属
(2)p区、非金属(n≥6为金属)
(3)d区、金属
(4)d区、金属
12.
原子序数 元素符号 电子层排布 周期 族 最高正价 未成对电子数 金属或非金属
9 F [He]2s22p5 2 ⅦA 1 非金属
15 P [Ne]3s23p3 3 ⅤA +5 3 非金属
24 Cr [Ar]3d54s1 4 ⅥB +6 6 金属
80 Hg [Xe]5d106s2 6 ⅡB +2 0 金属
【能力提高】
13.在氢原子中 E3s=E3p=E3d , 在多电子原子中E3s<E3p<E3d
14.Z=19,(2、8、9)有错误,因为最外层不能超过8个电子。应为2、8、8、1。
Z=22,(2、10、8、2)有错误,因为每一电子层最多可容纳2n2个电子,所以L层电子数应为8,不能为10,应为2、8、10、2。
Z=30无错误。
Z=33,(2、8、20、3)有错误,因为次外层不能超过18个电子。应为2、8、18、5。
Z=60,(2、8、18、18、12、2)有错误,因为当n=6时,E6s<E4f<E5d<E6p ,填5d前要填4f,次外层为12个电子即有d电子,则倒三层必有f电子,即倒三层电子数必大于18,应为2、8、18、22、8、2。
15.该元素原子的电子层排布为:1s22s22p63s23p63d104s24p3
(1)33,3(2)4,8,18(3)4s24p3
16.( 1)具有p6(即np6)排布的是稀有气体元素(He除外)。
(2)符合n=4,l=0(即4s)轨道上2个电子和n=3,l=2轨道(即3d)上有5个电子的排布是锰Mn。
(3)具有(n-1)d10ns1排布的元素是ⅠB族元素。
(4)该元素是钪Sc。
(5)该元素是Fe。
17.⑴ 根据题意知这类元素原子最外层电子排布为4s1,所以它们可能是K、Cr、Cu三种元素,其原子序数是19、24、29。
⑵ K:1s22s22p63s23p64s1,第4周期,ⅠA族,s区,最高正价+1,是金属元素。
Cr:1s22s22p63s23p63d54s1,第4周期,ⅥB族,d区,最高正价+6,是金属元素。
Cu:1s22s22p63s23p63d104s1,第4周期,ⅠB族,ds区,最高正价+3,是金属元素。
18.
元素 价电子排布 周期 族 金属或非金属
甲 4s1 4 ⅠA 金属
乙 3d54s2 4 ⅦB 金属
丙 4s24p5 4 ⅦA 非金属
丁 2s22p5 2 ⅦA 非金属
19.⑴Cl(氯),O(氧) ⑵ KClO3
20.(1)O;
(2)S2->O2->Na+
(3)Na2O2、SCl2、Cl2O
(4)SO2+Cl2+2H2O=2HCl+H2SO
【综合探究】
21.A:
22.24号元素为Cr,价电子结构为 3d54s1.
3d轨道: n l m ms
3 2 -2 + (或全为- )
3 2 -1 +
3 2 0 +
3 2 +1 +
3 2 +2 +
4s轨道: 4 0 0 + (或为- )
www.
+17
8
2
7
+11
8
2
1
