(鲁科版选修4)第一章第三节 化学能转化为电能--原电池(课件)
文档属性
| 名称 | (鲁科版选修4)第一章第三节 化学能转化为电能--原电池(课件) |

|
|
| 格式 | rar | ||
| 文件大小 | 286.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-15 00:00:00 | ||
图片预览


文档简介
课件19张PPT。 第三节 化学能转化为电能
--------原电池实验现象:锌片上有气泡产生
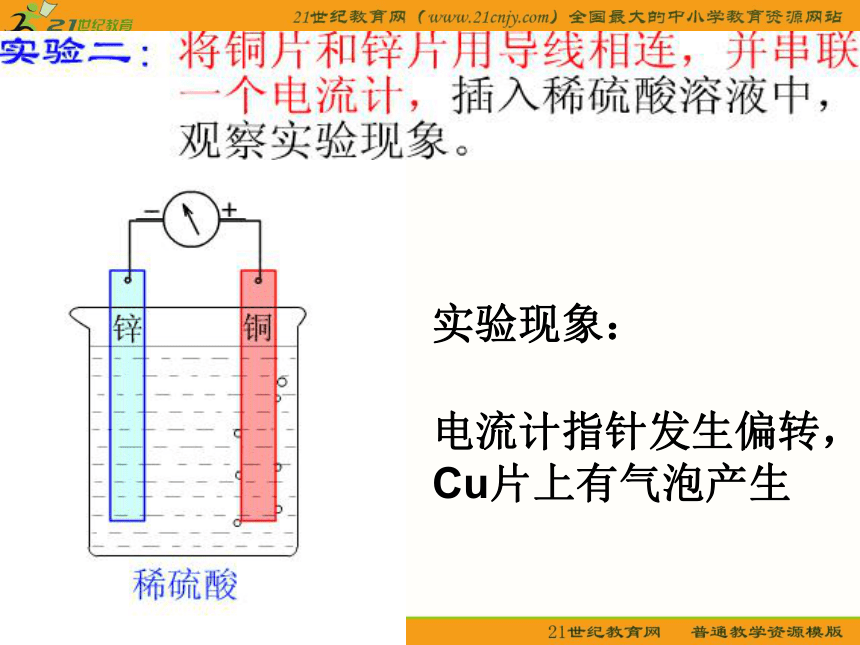
而铜片上没有实验现象:电流计指针发生偏转,
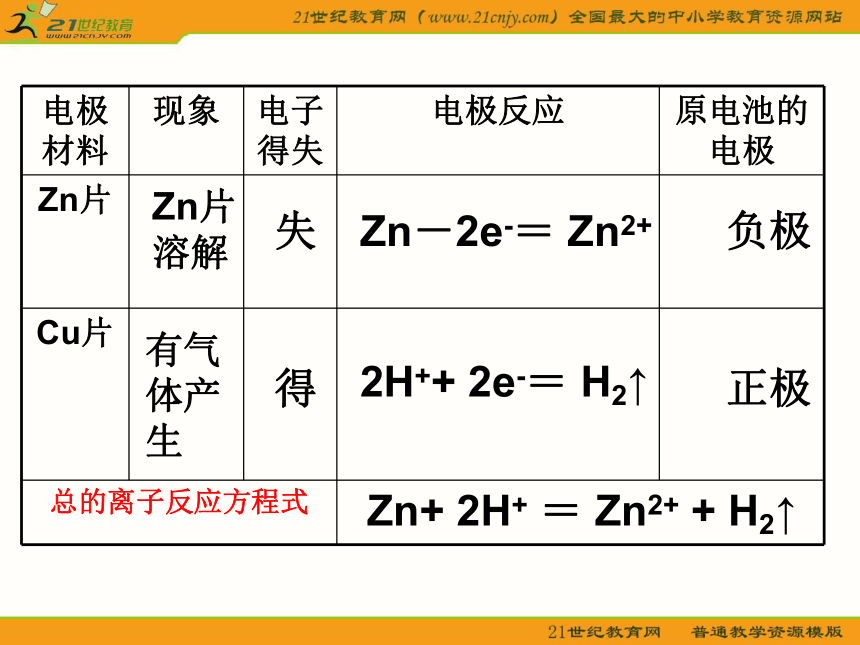
Cu片上有气泡产生失得Zn-2e-= Zn2+2H++ 2e-= H2↑负极正极Zn+ 2H+ = Zn2+ + H2↑有气体产生Zn片溶解一、原电池
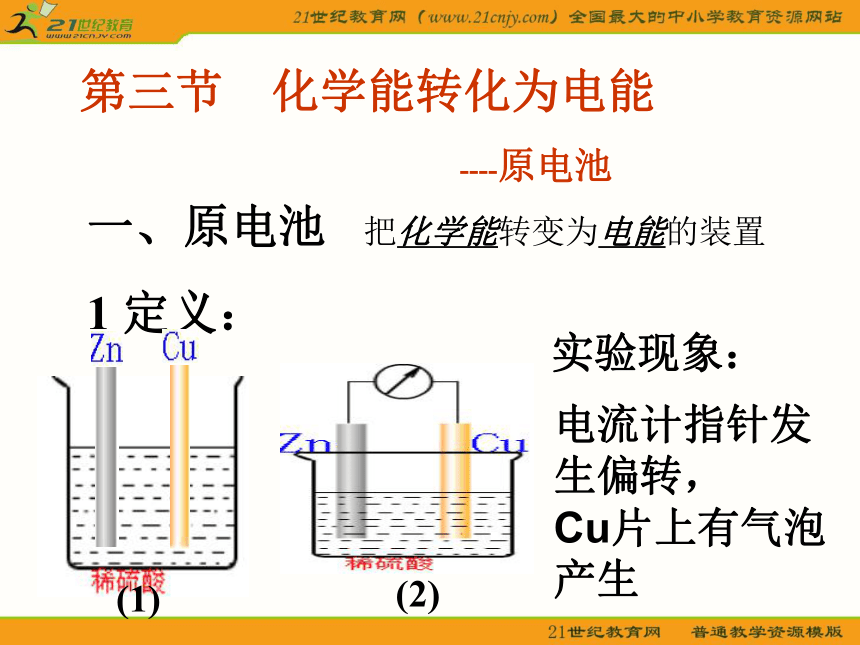
1 定义: 把化学能转变为电能的装置第三节 化学能转化为电能
----原电池 实验现象: 电流计指针发生偏转,
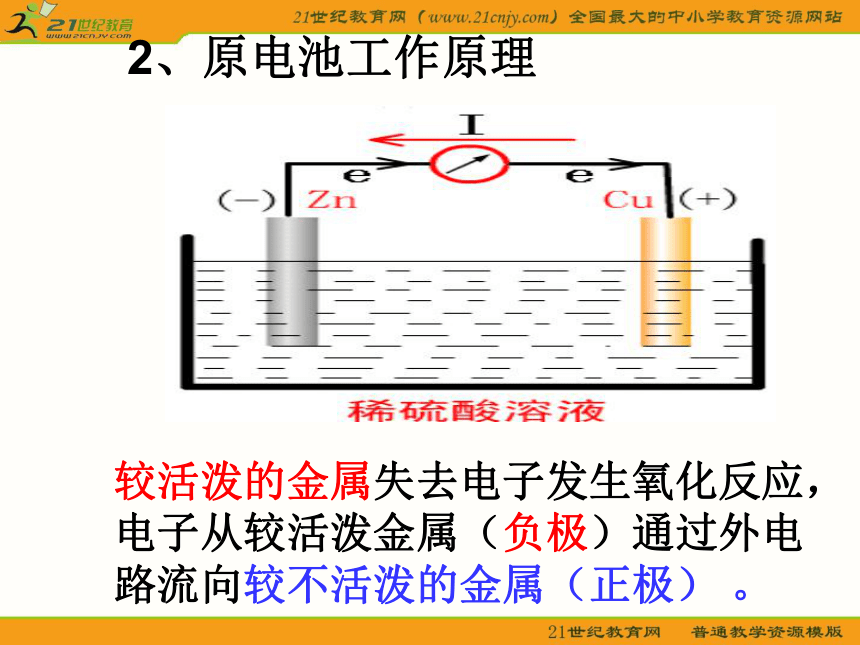
Cu片上有气泡产生(1)(2)2、原电池工作原理较活泼的金属失去电子发生氧化反应,电子从较活泼金属(负极)通过外电
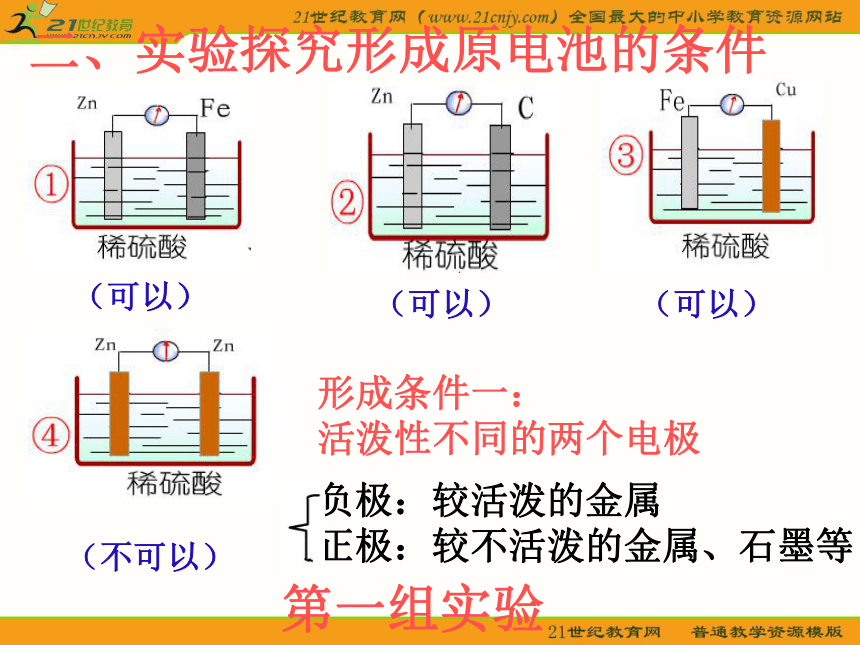
路流向较不活泼的金属(正极) 。二、实验探究形成原电池的条件(可以)(可以)(可以)(不可以)形成条件一:
活泼性不同的两个电极负极:较活泼的金属
正极:较不活泼的金属、石墨等第一组实验(可以)(不可以)形成条件二:电极需插进电解质溶液中
第二组实验实验探究形成原电池的条件第三组实验实验探究形成原电池的条件形成条件三:必须形成闭合回路(不可以)图中所示装置属于原电池的是( ).
是原电池的判断电极并写出电极反应和总反应方程式.C D EE思考:请将氧化还原反应 Zn + Cu2+ = Cu + Zn2+Zn比Zn不活泼的金属或石墨 CuSO4 、CuCl2等设计成一个原电池。负极:
正极:
电解质溶液: 此电池的优点:
能产生持续、稳定的电流。小结:组成原电池的条件有2、两种活泼性不同的金属(或一种是非金属导体)作电极
电3、两电极均插入电解质溶液中
两4、两极相连形成闭合电路1、前提是发生氧化还原反应三、常见的化学电源干电池(NH4Cl糊状物为电解质)
负极(锌筒):Zn-2e—=Zn2+,
正极(石墨)2NH4++2MnO2 + 2e-=2NH3↑+Mn2O3+H2O
总反应:Zn+2NH4++2MnO2= Zn2++2NH3↑+Mn2O3+H2O银锌电池(电解质为KOH)
负极:Zn+2OH--2e-=Zn(OH)2
(或Zn+2OH--2e- =ZnO+H2O)
正极:Ag2O+H2O+2e-=2Ag+2OH-
总反应:Zn+Ag2O+H2O=Zn(OH)2+2Ag
(或 Zn+Ag2O=ZnO+2Ag)讨论:钢铁的腐蚀钢铁在潮湿的空气中更容易腐蚀原因:空气中溶解CO2的水分
酸性增强(形成电解质溶液)Fe和C构成原电池的两极Fe:负极C:正极四、金属的腐蚀和防护金属的防护影响金属腐蚀的因素包括:
金属的 和 。本性介质金属越活泼越容易被腐蚀金属合金中活泼的金属易腐蚀例如:钢铁腐蚀介质对金属腐蚀影响很大:金属在潮湿的空气中、接触腐蚀性
气体或电解质溶液,都容易被腐蚀如何防止金属的腐蚀?常用的金属防腐方法:1、刷油漆2、在金属表面包一层塑料3、选用油脂4、在金属表面镀一层耐腐蚀金属5、连接一种更活泼的金属
--------原电池实验现象:锌片上有气泡产生
而铜片上没有实验现象:电流计指针发生偏转,
Cu片上有气泡产生失得Zn-2e-= Zn2+2H++ 2e-= H2↑负极正极Zn+ 2H+ = Zn2+ + H2↑有气体产生Zn片溶解一、原电池
1 定义: 把化学能转变为电能的装置第三节 化学能转化为电能
----原电池 实验现象: 电流计指针发生偏转,
Cu片上有气泡产生(1)(2)2、原电池工作原理较活泼的金属失去电子发生氧化反应,电子从较活泼金属(负极)通过外电
路流向较不活泼的金属(正极) 。二、实验探究形成原电池的条件(可以)(可以)(可以)(不可以)形成条件一:
活泼性不同的两个电极负极:较活泼的金属
正极:较不活泼的金属、石墨等第一组实验(可以)(不可以)形成条件二:电极需插进电解质溶液中
第二组实验实验探究形成原电池的条件第三组实验实验探究形成原电池的条件形成条件三:必须形成闭合回路(不可以)图中所示装置属于原电池的是( ).
是原电池的判断电极并写出电极反应和总反应方程式.C D EE思考:请将氧化还原反应 Zn + Cu2+ = Cu + Zn2+Zn比Zn不活泼的金属或石墨 CuSO4 、CuCl2等设计成一个原电池。负极:
正极:
电解质溶液: 此电池的优点:
能产生持续、稳定的电流。小结:组成原电池的条件有2、两种活泼性不同的金属(或一种是非金属导体)作电极
电3、两电极均插入电解质溶液中
两4、两极相连形成闭合电路1、前提是发生氧化还原反应三、常见的化学电源干电池(NH4Cl糊状物为电解质)
负极(锌筒):Zn-2e—=Zn2+,
正极(石墨)2NH4++2MnO2 + 2e-=2NH3↑+Mn2O3+H2O
总反应:Zn+2NH4++2MnO2= Zn2++2NH3↑+Mn2O3+H2O银锌电池(电解质为KOH)
负极:Zn+2OH--2e-=Zn(OH)2
(或Zn+2OH--2e- =ZnO+H2O)
正极:Ag2O+H2O+2e-=2Ag+2OH-
总反应:Zn+Ag2O+H2O=Zn(OH)2+2Ag
(或 Zn+Ag2O=ZnO+2Ag)讨论:钢铁的腐蚀钢铁在潮湿的空气中更容易腐蚀原因:空气中溶解CO2的水分
酸性增强(形成电解质溶液)Fe和C构成原电池的两极Fe:负极C:正极四、金属的腐蚀和防护金属的防护影响金属腐蚀的因素包括:
金属的 和 。本性介质金属越活泼越容易被腐蚀金属合金中活泼的金属易腐蚀例如:钢铁腐蚀介质对金属腐蚀影响很大:金属在潮湿的空气中、接触腐蚀性
气体或电解质溶液,都容易被腐蚀如何防止金属的腐蚀?常用的金属防腐方法:1、刷油漆2、在金属表面包一层塑料3、选用油脂4、在金属表面镀一层耐腐蚀金属5、连接一种更活泼的金属
