苏教版选修四专题一第一单元 化学反应中的热效应(练习)
文档属性
| 名称 | 苏教版选修四专题一第一单元 化学反应中的热效应(练习) |

|
|
| 格式 | zip | ||
| 文件大小 | 31.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-17 00:00:00 | ||
图片预览


文档简介
《化学反应中的热效应》
一、选择题
1. 今有如下三个热化学方程式:
H2(g)+1/2O2(g)=H2O(g);ΔH=aKJ·mol-1,
H2(g)+1/2O2(g)=H2O(l);ΔH== bkJ·mol-1,
2H2(g)+O2(g)=2H2O(l);ΔH== ckJ·mol-1,
关于它们的下列表述正确的是
A.它们都是吸热反应 B.a、b和c均为正值
C.a== b D.2b== c
2. 在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g);△H =-566kJ CH4(g) + 2O2(g) = CO2(g) + 2H2O(l);△H =-890kJ
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
A.2912kJ B.2953kJ C.3236kJ D.3867kJ
3. 关于热化学方程式:2H2(g)+02(g)=2H20(1), H=-571.6 kJ·mol-1,下列有关叙述不正确的是
A.2mol H2完全燃烧生成液态水时放出571.6 kJ的热
B.1mol H2完全燃烧生成液态水时放出285.8kJ的热
C.2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D.上述热化学方程式可表示为H2(g)+ O2(g)=H20(1), H=-285.8 kJ·mol-1
4. 同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是
A.2A ( l ) + B ( l ) = 2C (g ) △H1
B.2A ( g ) + B ( g ) = 2C (g ) △H2
C.2A ( g ) + B ( g ) = 2C ( l ) △H3
D.2A ( l ) + B ( l ) = 2C ( l ) △H4
5. 下列有关热化学方程式的叙述正确的是
A. 已知2H2(g)+O2(g) = 2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ
B. 已知4P(红磷,s)= P4(白磷,s);△H>0,则白磷比红磷稳定
C. 含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+1/2H2SO4(aq)= 1/2Na2SO4(aq)+H2O(l);△H=-57.4kJ/mol
D. 己知C(s)+ O2(g)= CO2(g);△H1 C(s)+1/2 O2(g)= CO(g);△H2 则△H1>△H2
6. 下列属于热化学方程式的是
A.C + O2 CO2
B.H2 + CuO H2O + Cu -Q
C.H2(气) + Cl2(气) === 2HCl + Q
D.C(固) + O2(气) === CO2(气) + 393.5kJ
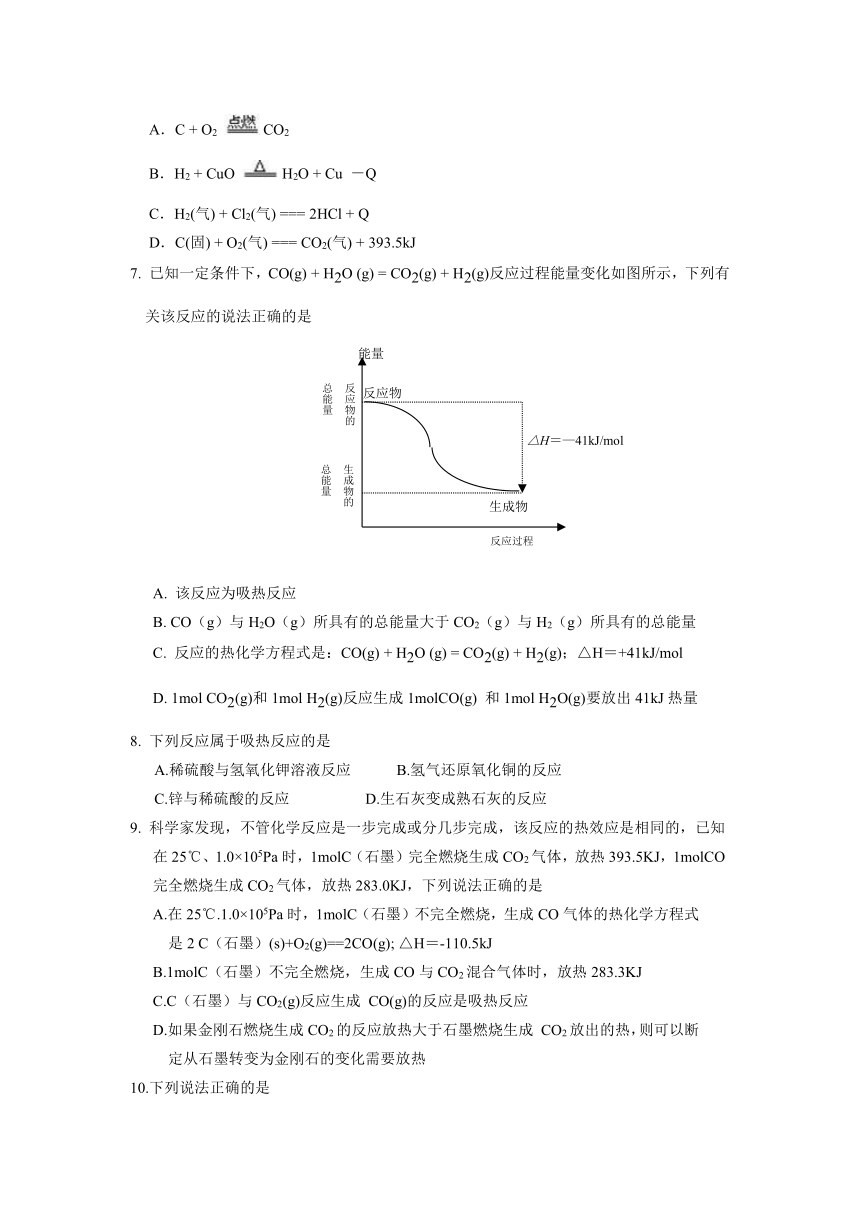
7. 已知一定条件下,CO(g) + H2O (g) = CO2(g) + H2(g)反应过程能量变化如图所示,下列有关该反应的说法正确的是
A. 该反应为吸热反应
B. CO(g)与H2O(g)所具有的总能量大于CO2(g)与H2(g)所具有的总能量
C. 反应的热化学方程式是:CO(g) + H2O (g) = CO2(g) + H2(g);△H=+41kJ/mol
D. 1mol CO2(g)和1mol H2(g)反应生成1molCO(g) 和1mol H2O(g)要放出41kJ热量
8. 下列反应属于吸热反应的是
A.稀硫酸与氢氧化钾溶液反应 B.氢气还原氧化铜的反应
C.锌与稀硫酸的反应 D.生石灰变成熟石灰的反应
9. 科学家发现,不管化学反应是一步完成或分几步完成,该反应的热效应是相同的,已知在25℃、1.0×105Pa时,1molC(石墨)完全燃烧生成CO2气体,放热393.5KJ,1molCO完全燃烧生成CO2气体,放热283.0KJ,下列说法正确的是
A.在25℃.1.0×105Pa时,1molC(石墨)不完全燃烧,生成CO气体的热化学方程式是2 C(石墨)(s)+O2(g)==2CO(g); △H=-110.5kJ
B.1molC(石墨)不完全燃烧,生成CO与CO2混合气体时,放热283.3KJ
C.C(石墨)与CO2(g)反应生成 CO(g)的反应是吸热反应
D.如果金刚石燃烧生成CO2的反应放热大于石墨燃烧生成 CO2放出的热,则可以断定从石墨转变为金刚石的变化需要放热
10.下列说法正确的是
A. 若反应X + Y = M是放热反应,该反应一定不用加热。
B. 需要加热方能发生的反应一定是吸热反应。
C. CO2与CaO化合是放热反应,则CaCO3分解是吸热反应。
D. 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热。
11.已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
12.已知方程式2H2(g)+O2(g)=2H2O(l) △H1=–571.6KJ·mol-1,则关于方程式
2H2O(l) =2H2(g)+O2(g) △H2=?的说法正确的是
A. 方程式中化学计量数表示分子数
B. 该反应△H2大于零
C. 该反应的△H2=-571.6kJ·mol-1
D. 该反应可表示36g水分解时的热效应
13.25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量。下列表示该反应的热化学方程式中正确的是
CH4O(l)+3/2O2(g) = CO2(g)+2H2O(l) △H=-725.8kJ/mol
2CH4O(l)+3O2(g)= 2CO2(g)+4H2O(l) △H=+1451.6kJ/mol
2CH4O+O2 = 2CO2+4H2O(l) △H=-22.68kJ/mol
CH4O(l)+3/2O2(g) = CO2(g)+2H2O(g) △H=-725.8kJ/mol
14.在36 g 碳不完全燃烧所得气体中,CO占体积,CO2占体积。且有:
C(s) + O2(g) = CO(g) ;△H = -110.5 kJ/mol , CO(g) + O2(g) = CO2(g) ;△H = -283 kJ/mol
与这些碳完全燃烧相比,损失的热量是
A.172.5 kJ B. 1149 kJ
C.283kJ D. 517.5 kJ
15.已知:①1 mol H2 分子中化学键断裂时需要吸收 436kJ 的能量
②1 mol Cl2 分子中化学键断裂时需要吸收 243kJ 的能量
③由H原子和Cl原子形成1mol HCl分子时释放 431kJ 的能量
则下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g) + Cl2(g) = 2HCl(g)
B.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H = 183kJ/mol
C.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H =-183kJ/mol
D.氢气和氯气反应生成 1 mol 氯化氢气体,反应的△H =-183kJ/mol
二、填空题
16. 已知:在298K、100kPa时,
①C(s,石墨)+O2(g) = CO2(g) △H1 = -400 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) △H2 = -570 kJ·mol-1;
③2C2H2(g)+5O2(g) = 4CO2(g)+ 2H2O(l) △H3 = -2600 kJ·mol-1;
(1)写出298K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式 。
(2)现有一定量的乙炔在足量氧气中完全燃烧,放出热量650 kJ。将反应后的二氧化碳气体缓缓通入到含有0.5 mol Ca (OH)2的澄清石灰水中充分反应。
将反应后的物质分为a、b、c三等份,分别进行下列实验,回答相应问题:
①在a中加入少量的氢氧化钠溶液,写出反应的离子方程式 。
②加热b,发生反应的离子方程式 。
③在c中加入适量的FeCl3溶液,观察到的实验现象是 。
17.(1)右图是等质量的Na2CO3、NaHCO3粉末分别与足量的盐发生反应时的情景,产生CO2气体的体积较多的试管中加入的固体试剂是________,当反应结束时,A、B两试管中消耗的盐酸的质量之比为__________。
实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)
(a) (b)
(2)若Na2CO3 (aq) + HCl(aq) == NaHCO3(aq) + NaCl(aq) + Q1 ,
NaHCO3(aq) + HCl(aq) == NaCl(aq) + H2CO3(aq) + Q2 ,
H2CO3(aq) == H2O(l) + CO2(g) – Q3
注:aq- 表示溶液中、 l- 表示液体、 g- 表示气体
试根据上述两组实验现象分别可得出的与Q1、Q2、Q3有关的不等式为:
_____________、________________。
18.已知:金刚石、石墨的热化学方程式:
C(s,金刚石)+O2(g) =CO2(g) H = -395.4 kJ/mol
C(s,石墨)+O2(g) =CO2(g) H = -393.5 kJ/mol
则石墨转化为金刚石的反应热 H= ,两物质中 较为稳定 。
答案
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
D B C A C D B B C C A B A C C
二、填空题
16.(1)C(s,石墨)+H2(g) = C2H2(g) △H = -215 kJ·mol-1 (2分)
(2)①Ca2+ + HCO+ OH- = CaCO3↓+H2O(2分)
②Ca2+ + 2HCO CaCO3↓+H2O+ CO2↑(2分)
③产生红褐色沉淀,产生无色气体。(2分)
17. (1)NaHCO3 53:84 b a (2)Q1>Q2 Q3>0
18.+1.9 kJ/mol;石墨
能量
反应物
生成物
反应过程
△H=—41kJ/mol
反应物的
总能量
生成物的
总能量
一、选择题
1. 今有如下三个热化学方程式:
H2(g)+1/2O2(g)=H2O(g);ΔH=aKJ·mol-1,
H2(g)+1/2O2(g)=H2O(l);ΔH== bkJ·mol-1,
2H2(g)+O2(g)=2H2O(l);ΔH== ckJ·mol-1,
关于它们的下列表述正确的是
A.它们都是吸热反应 B.a、b和c均为正值
C.a== b D.2b== c
2. 在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g);△H =-566kJ CH4(g) + 2O2(g) = CO2(g) + 2H2O(l);△H =-890kJ
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
A.2912kJ B.2953kJ C.3236kJ D.3867kJ
3. 关于热化学方程式:2H2(g)+02(g)=2H20(1), H=-571.6 kJ·mol-1,下列有关叙述不正确的是
A.2mol H2完全燃烧生成液态水时放出571.6 kJ的热
B.1mol H2完全燃烧生成液态水时放出285.8kJ的热
C.2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D.上述热化学方程式可表示为H2(g)+ O2(g)=H20(1), H=-285.8 kJ·mol-1
4. 同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是
A.2A ( l ) + B ( l ) = 2C (g ) △H1
B.2A ( g ) + B ( g ) = 2C (g ) △H2
C.2A ( g ) + B ( g ) = 2C ( l ) △H3
D.2A ( l ) + B ( l ) = 2C ( l ) △H4
5. 下列有关热化学方程式的叙述正确的是
A. 已知2H2(g)+O2(g) = 2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ
B. 已知4P(红磷,s)= P4(白磷,s);△H>0,则白磷比红磷稳定
C. 含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+1/2H2SO4(aq)= 1/2Na2SO4(aq)+H2O(l);△H=-57.4kJ/mol
D. 己知C(s)+ O2(g)= CO2(g);△H1 C(s)+1/2 O2(g)= CO(g);△H2 则△H1>△H2
6. 下列属于热化学方程式的是
A.C + O2 CO2
B.H2 + CuO H2O + Cu -Q
C.H2(气) + Cl2(气) === 2HCl + Q
D.C(固) + O2(气) === CO2(气) + 393.5kJ
7. 已知一定条件下,CO(g) + H2O (g) = CO2(g) + H2(g)反应过程能量变化如图所示,下列有关该反应的说法正确的是
A. 该反应为吸热反应
B. CO(g)与H2O(g)所具有的总能量大于CO2(g)与H2(g)所具有的总能量
C. 反应的热化学方程式是:CO(g) + H2O (g) = CO2(g) + H2(g);△H=+41kJ/mol
D. 1mol CO2(g)和1mol H2(g)反应生成1molCO(g) 和1mol H2O(g)要放出41kJ热量
8. 下列反应属于吸热反应的是
A.稀硫酸与氢氧化钾溶液反应 B.氢气还原氧化铜的反应
C.锌与稀硫酸的反应 D.生石灰变成熟石灰的反应
9. 科学家发现,不管化学反应是一步完成或分几步完成,该反应的热效应是相同的,已知在25℃、1.0×105Pa时,1molC(石墨)完全燃烧生成CO2气体,放热393.5KJ,1molCO完全燃烧生成CO2气体,放热283.0KJ,下列说法正确的是
A.在25℃.1.0×105Pa时,1molC(石墨)不完全燃烧,生成CO气体的热化学方程式是2 C(石墨)(s)+O2(g)==2CO(g); △H=-110.5kJ
B.1molC(石墨)不完全燃烧,生成CO与CO2混合气体时,放热283.3KJ
C.C(石墨)与CO2(g)反应生成 CO(g)的反应是吸热反应
D.如果金刚石燃烧生成CO2的反应放热大于石墨燃烧生成 CO2放出的热,则可以断定从石墨转变为金刚石的变化需要放热
10.下列说法正确的是
A. 若反应X + Y = M是放热反应,该反应一定不用加热。
B. 需要加热方能发生的反应一定是吸热反应。
C. CO2与CaO化合是放热反应,则CaCO3分解是吸热反应。
D. 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热。
11.已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
12.已知方程式2H2(g)+O2(g)=2H2O(l) △H1=–571.6KJ·mol-1,则关于方程式
2H2O(l) =2H2(g)+O2(g) △H2=?的说法正确的是
A. 方程式中化学计量数表示分子数
B. 该反应△H2大于零
C. 该反应的△H2=-571.6kJ·mol-1
D. 该反应可表示36g水分解时的热效应
13.25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量。下列表示该反应的热化学方程式中正确的是
CH4O(l)+3/2O2(g) = CO2(g)+2H2O(l) △H=-725.8kJ/mol
2CH4O(l)+3O2(g)= 2CO2(g)+4H2O(l) △H=+1451.6kJ/mol
2CH4O+O2 = 2CO2+4H2O(l) △H=-22.68kJ/mol
CH4O(l)+3/2O2(g) = CO2(g)+2H2O(g) △H=-725.8kJ/mol
14.在36 g 碳不完全燃烧所得气体中,CO占体积,CO2占体积。且有:
C(s) + O2(g) = CO(g) ;△H = -110.5 kJ/mol , CO(g) + O2(g) = CO2(g) ;△H = -283 kJ/mol
与这些碳完全燃烧相比,损失的热量是
A.172.5 kJ B. 1149 kJ
C.283kJ D. 517.5 kJ
15.已知:①1 mol H2 分子中化学键断裂时需要吸收 436kJ 的能量
②1 mol Cl2 分子中化学键断裂时需要吸收 243kJ 的能量
③由H原子和Cl原子形成1mol HCl分子时释放 431kJ 的能量
则下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g) + Cl2(g) = 2HCl(g)
B.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H = 183kJ/mol
C.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H =-183kJ/mol
D.氢气和氯气反应生成 1 mol 氯化氢气体,反应的△H =-183kJ/mol
二、填空题
16. 已知:在298K、100kPa时,
①C(s,石墨)+O2(g) = CO2(g) △H1 = -400 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) △H2 = -570 kJ·mol-1;
③2C2H2(g)+5O2(g) = 4CO2(g)+ 2H2O(l) △H3 = -2600 kJ·mol-1;
(1)写出298K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式 。
(2)现有一定量的乙炔在足量氧气中完全燃烧,放出热量650 kJ。将反应后的二氧化碳气体缓缓通入到含有0.5 mol Ca (OH)2的澄清石灰水中充分反应。
将反应后的物质分为a、b、c三等份,分别进行下列实验,回答相应问题:
①在a中加入少量的氢氧化钠溶液,写出反应的离子方程式 。
②加热b,发生反应的离子方程式 。
③在c中加入适量的FeCl3溶液,观察到的实验现象是 。
17.(1)右图是等质量的Na2CO3、NaHCO3粉末分别与足量的盐发生反应时的情景,产生CO2气体的体积较多的试管中加入的固体试剂是________,当反应结束时,A、B两试管中消耗的盐酸的质量之比为__________。
实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)
(a) (b)
(2)若Na2CO3 (aq) + HCl(aq) == NaHCO3(aq) + NaCl(aq) + Q1 ,
NaHCO3(aq) + HCl(aq) == NaCl(aq) + H2CO3(aq) + Q2 ,
H2CO3(aq) == H2O(l) + CO2(g) – Q3
注:aq- 表示溶液中、 l- 表示液体、 g- 表示气体
试根据上述两组实验现象分别可得出的与Q1、Q2、Q3有关的不等式为:
_____________、________________。
18.已知:金刚石、石墨的热化学方程式:
C(s,金刚石)+O2(g) =CO2(g) H = -395.4 kJ/mol
C(s,石墨)+O2(g) =CO2(g) H = -393.5 kJ/mol
则石墨转化为金刚石的反应热 H= ,两物质中 较为稳定 。
答案
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
D B C A C D B B C C A B A C C
二、填空题
16.(1)C(s,石墨)+H2(g) = C2H2(g) △H = -215 kJ·mol-1 (2分)
(2)①Ca2+ + HCO+ OH- = CaCO3↓+H2O(2分)
②Ca2+ + 2HCO CaCO3↓+H2O+ CO2↑(2分)
③产生红褐色沉淀,产生无色气体。(2分)
17. (1)NaHCO3 53:84 b a (2)Q1>Q2 Q3>0
18.+1.9 kJ/mol;石墨
能量
反应物
生成物
反应过程
△H=—41kJ/mol
反应物的
总能量
生成物的
总能量
