第二节 化学计量在实验中的应用(一)
文档属性
| 名称 | 第二节 化学计量在实验中的应用(一) |  | |
| 格式 | rar | ||
| 文件大小 | 27.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-09-21 21:30:00 | ||
图片预览



文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
课题:第二节 化学计量在实验中的应用(一) ------物质的量和摩尔质量 授课班级
课 时 1
教学目的 知识与技能 1、认识摩尔是物质的是的基本单位,了解物质的量与微观粒子之间的关系,了解 摩尔质量的概念,了解提出摩尔这一概念的重要性和必要性,懂得阿伏加德罗常数的涵义2、了解物质的量、摩尔质量、物质的质量之间的关系,能用于进行简单的化学计算。
过程与方法 1、初步培养学生演绎推理、归纳推理、逻辑推理和运用化学知识进行计算的能力2、通过物质的量这一联系微观粒子与宏观质量的物理量的学习,引导学生以化学的眼光、从微观的角度地认识丰富多彩的物质世界,认识到宏观和微观的相互转化是研究化学的科学方法之一。
情感态度价值观 1、通过对概念的透彻理解,培养学生严谨、认真的学习态度,体会定量研究的方法对研究和学习化学的重要作用。
重 点 物质的量及单位;摩尔质量的概念和有关摩尔质量的计算
难 点 物质的量及单位------摩尔
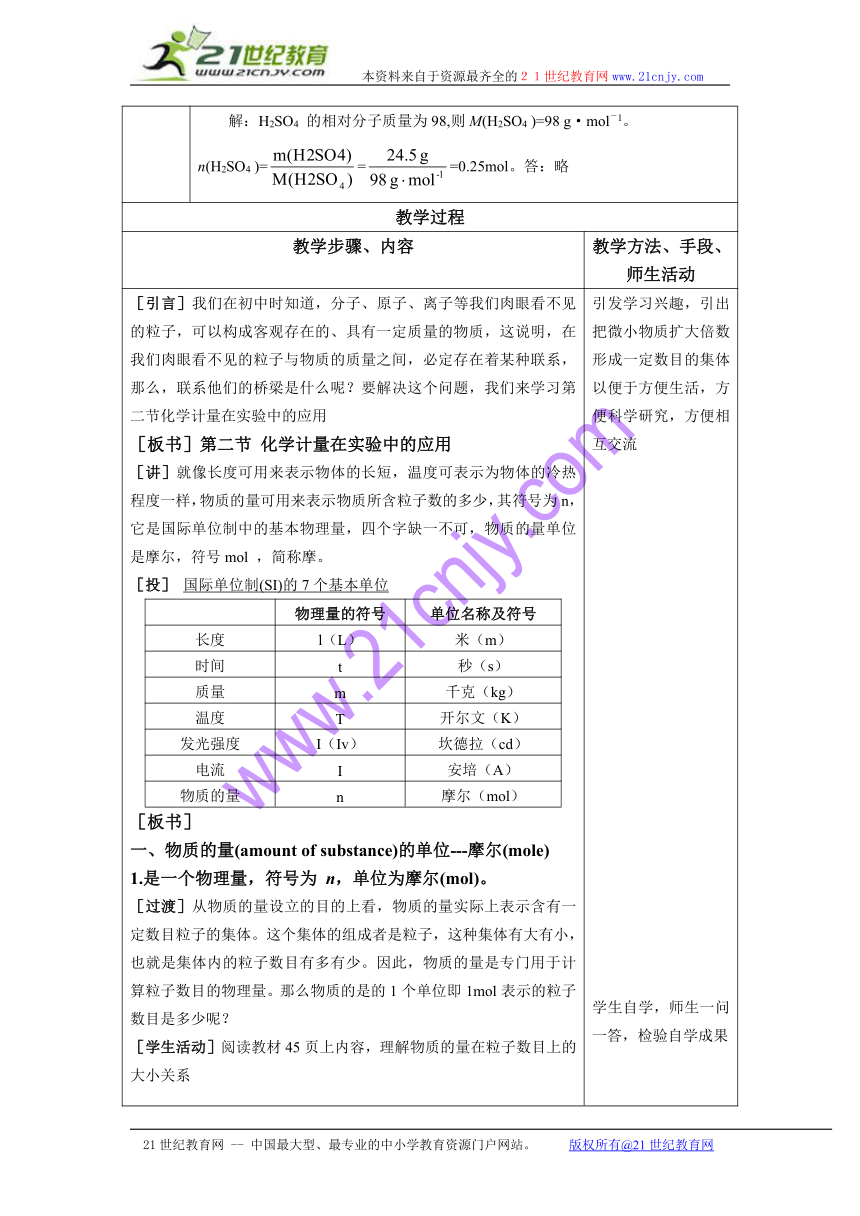
知识结构与板书设计 第二节 化学计量在实验中的应用一、物质的量(amount of substance)的单位---摩尔(mole)1.是一个物理量,符号为 n,单位为摩尔(mol)。2、阿伏加德罗常数:表示1mol任何粒子的粒子数,符号为NA,单位为mol-1,数值约为6.02*1023 mol-13、注意:使用mol时,必须指明粒子的种类,可以是分子、原子、离子、电子等。4.N、NA与n的关系: A1=1 mol任何粒子或物质的质量是以克为单位,在数值上就等于该粒子的相对原子(分子、离子)质量。5、摩尔质量:(1)定义:单位物质的量的物质所具有的质量,符号为M(2)、公式:M= 单位 g·mol-16、有关摩尔质量的相关计算例1:24.5 g H2SO4 的物质的量是_________解:H2SO4 的相对分子质量为98,则M(H2SO4 )=98 g·mol-1。n(H2SO4 )===0.25mol。答:略
教学过程
教学步骤、内容 教学方法、手段、师生活动
[引言]我们在初中时知道,分子、原子、离子等我们肉眼看不见的粒子,可以构成客观存在的、具有一定质量的物质,这说明,在我们肉眼看不见的粒子与物质的质量之间,必定存在着某种联系,那么,联系他们的桥梁是什么呢?要解决这个问题,我们来学习第二节化学计量在实验中的应用[板书]第二节 化学计量在实验中的应用[讲]就像长度可用来表示物体的长短,温度可表示为物体的冷热程度一样,物质的量可用来表示物质所含粒子数的多少,其符号为n,它是国际单位制中的基本物理量,四个字缺一不可,物质的量单位是摩尔,符号mol ,简称摩。[投] 国际单位制(SI)的7个基本单位物理量的符号单位名称及符号长度l(L)米(m)时间t秒(s)质量m千克(kg)温度T开尔文(K)发光强度I(Iv)坎德拉(cd)电流I安培(A)物质的量n摩尔(mol)[板书]一、物质的量(amount of substance)的单位---摩尔(mole)1.是一个物理量,符号为 n,单位为摩尔(mol)。[过渡]从物质的量设立的目的上看,物质的量实际上表示含有一定数目粒子的集体。这个集体的组成者是粒子,这种集体有大有小,也就是集体内的粒子数目有多有少。因此,物质的量是专门用于计算粒子数目的物理量。那么物质的是的1个单位即1mol表示的粒子数目是多少呢?[学生活动]阅读教材45页上内容,理解物质的量在粒子数目上的大小关系[问]1mol粒子的数目大约是多少?(约为6.02*1023个)[问]6.02*1023这个数值是以什么为依据得出的?(是以0.012kg12C中所含碳原子数为依据得出来的)[问]12C原子特指什么结构的碳原子?(12C指原子核内有6个质子和6个中子的碳原子)[师]大家回答得很好。由此,我们可以得出以下结论: 1mol任何粒子的数目是0.012kg12C中所含的碳原子数目约为6.02*1023个[讲]1mol任何粒子的数目也叫阿伏加德罗常数。阿伏加德罗是意大利物理学家。因他对6.02*1023这个数据的测得有着很大的贡献,故用他的名字来表示1mol任何粒子的粒子数,以示纪念。化学上,我们用NA来表示阿伏加德罗常数,其单位mol-1,它表示1mol任何粒子的粒子数,其数值近似6.02*1023个等于。[板书]2、阿伏加德罗常数:表示1mol任何粒子的粒子数,符号为NA,单位为mol-1,数值约为6.02*1023 mol-1[师]下面请同学们点击试题,看看平常计算中是如何应用阿伏加德罗常数的。[点击试题]填空1. 1 mol H2所含氢气分子的个数 。2. 2 mol氢分子含 个氢原子。3. 1 mol SO42―是 个硫酸根离子。[讲]物质的量只限制了所含粒子个数的多少,并没限制粒子的种类,所以使用mol 时应注明所指粒子是哪种?[板书]3、注意:使用mol时,必须指明粒子的种类,可以是分子、原子、离子、电子等。[点击试题]判断正误,说明理由。A. 1 mol氢 B. 1 molCO2 √C. 1 mol小米 × 小米不是微观粒子[讲]请大家根据摩尔相关知识,进行如下计算。[例题]根据摩尔的有关知识,进行计算。1. 1.204×1024个H,合多少 mol (2 mol)2. 5 mol的O2中有多少个氧气分子 (3.01*1024)3. N个水分子的物质的量是多少 (已知,阿伏加德罗常数为NA)[讲]由以上练习,我们得出粒子总个数N、阿伏加德罗常数NA、物质的量n三者之间的关系为:[板书]4.N、NA与n的关系: [讲]摩尔是一个巨大数量粒子集合体,可以是整数,也可以是小数,例如可以有0.5 mol O2,0.01 mol H2SO4等,但分子、原子等具体的粒子,只能是整数,就不能说0.5个或0.01个。下面请大家做随堂练习3[点击试题]1.0.5 mol水中含有 个水分子。2.2 mol水中含有 个水分子, 个氢原子。3.1 mol H2SO4中含有 个H2SO4分子, 个硫酸根离子。4.1 mol HCl溶于水,水中存在的溶质粒子是什么 它们的物质的量各是多少 5.1个水分子中有 个电子,1 mol H2O中呢 [过]前面我们学习了物质的量,知道它是一个基本物理量,单位为摩尔,它表示含有一定数目的粒子集体。那么,1 mol粒子的数目是以什么为标准得出来的?其数目约为多少?(是以0.012 kg 12C中所含碳原子数目为标准得来的;其数目约为6.02×1023)[问]我们初中所学某种原子的相对原子质量也是以碳-12原子为标准得出来的,它是怎样定义的?(以碳-12原子的质量的1/12作为标准,其他原子的质量跟它比较所得的数值,就是这种原子的相对原子质量)[师]很好!请大家推导思考题1[思考]假如一原子的质量为m1,碳-12原子的质量为mC,则该原子的相对原子质量A1怎样表示?请大家用代数式表示出来。[副板]A1=[师]大家表示的都很正确。若另一种原子的质量为m2,则它的相对原子质量A2又该怎样表示,请大家口答。(A2=。)[问]A1比A2与m1与m2的关系是什么呢?请大家推导。( A1∶A2=m1∶m2)[师]很正确!这也就是说:原子的质量比=原子相对原子质量比。[师]下面让我们导出下列关系:微观粒子 一个C原子 一个O原子 一个Fe原子 1 mol C原子 1 mol O原子 1 mol Fe原子宏观质量 0.012 kg=12 g x g y g相对原子质量 12 16 56[师]由刚才我们对原子相对原子质量的深入理解知道:原子的质量比=原子的相对原子质量比。∴1 mol任何原子的质量比,就等于它们的相对原子质量比。请大家根据此结论,计算出x值和y值。[结果]x=16 y=56[问]1 mol钠原子的质量是多少 1 mol氢原子的质量呢?(1 mol钠原子的质量是23 g,1 mol氢原子的质量是1 g)[问]由此可得出什么结论?(1 mol任何原子的质量,在数值上都等于它们的相对原子质量)[问]单位呢?( 克!)[问]1 mol分子的质量,与它的相对分子质量有什么关系?为什么?(因为分子都是由原子构成的,而分子的相对分子质量等于构成它的原子的相对原子质量的总和。1 mol任何原子的质量在数值上等于它的相对原子质量,单位为克,则1 mol任何分子的质量就应该在数值上等于它的相对分子质量,单位为克)[师]很正确!那么,对于粒子中的离子来讲,又将怎样呢?请大家阅读课本12页最后一段后回答。(对于离子来说,由于电子的质量很小,当原子得到或失去电子变成离子时,电子的质量可略去不计,因此,1 mol离子的质量在数值上就等于该离子的式量,单位为克)[师]回答得很好,综合以上分析,我们可得出以下结论:[副板]1 mol任何粒子或物质的质量是以克为单位,在数值上就等于该粒子的相对原子(分子、离子)质量。[师]请大家做以下练习:[点击试题]1 mol H2O的质量是 。1 mol NaCl的质量是 。1 mol Na+的质量是 。1 mol S的质量是 。[师]化学上,我们把1 mol物质所具有的质量叫摩尔质量。[板书]5、摩尔质量:(1)定义:单位物质的量的物质所具有的质量,符号为M[师]也就是说,物质的摩尔质量是该物质的质量与该物质的物质的量之比[板书](2)、公式:M= 单位 g·mol-1[讲]依据此式,我们可以把物质的质量与构成物质的粒子集体---- 物质的量联系起来,请大家口答下列空[点击试题]1.Na的摩尔质量 。2.NaCl的摩尔质量 。3. SO摩尔质量 。[师]大家在解答有关摩尔质量的问题时,一定要注意单位!下面,让我们根据摩尔质量的为进行计算。注意解题格式。[板书]6、有关摩尔质量的相关计算例1:24.5 g H2SO4 的物质的量是_________解:H2SO4 的相对分子质量为98,则M(H2SO4 )=98 g·mol-1。n(H2SO4 )===0.25mol。答:略[点击试题]1。5 mol Na2CO3 的质量是多少?[小结]从本节课的学习中我们知道:1 mol不同的物质中,构成它们的粒子的数目虽然相同,但由于不同粒子的质量一般不同,故1 mol不同物质的质量一般也不相同,以克为单位时,其数值就等于构成该物质的粒子的相对原子(或分子)质量。在进行有关摩尔质量的计算时,一定要注意单位和解题格式。[自我评价]1. 1.5 mol H2SO4的质量是 。其中含有 mol O, mol H,其质量分别为 和 。2. 0.01 mol某物质的质量为1.08 g,此物质的摩尔质量为 。3.下列说法正确的是( )A.71 g氯相当于2 mol氯B.每摩尔物质中含有6.02×1023个原子C.阿伏加德罗常数为12 g 12C所含的碳原子数D.1 mol KClO3中含有3 mol氧元素4.如果1 g水中含有m个氢原子,则阿伏加德罗常数是( )A. B.9m C.2m D.18m5下列说法正确的是( )A.氮原子的质量就是氮的相对原子质量B.氢氧化钠的摩尔质量是40 gC.1 mol H2SO4中含有1 mol H2D.氩气的摩尔质量在数值上等于它的相对原子质量6、0.8g 某物质含有3.01*1022个分子,该物质的式量约为( ) A、8 B、16 C、64 D、160课后作业 1、71g Na2SO4 中含有Na+和SO42-物质的量各是__________________2、 19.6g H2SO4 中氧元素的质量_________________3、 含有1.5*1022个分子,其质量为2。7g 求分子质量4、多少克H2SO4 所含的分子数与3.6克10%盐酸所含溶质的分子数相等5、 0.2 mol KClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子数相等。 引发学习兴趣,引出把微小物质扩大倍数形成一定数目的集体以便于方便生活,方便科学研究,方便相互交流学生自学,师生一问一答,检验自学成果进行化学史的教育,培养学生科学态度 6.02*1023个 2.408*1024 6.02*1023 A、 × 没有指出是分子、原子或离子B. √C. × 小米不是微观粒子1. (2 mol)2. (3.01*1024)引导学生自我总结公式 3.01*1023 1.204*1024 ; 2.408*1024 6.02*1023; 6.02*1023 H+ 、Cl― 各1 mol 10; 6.02*1024学生推导,教师巡视并指导教师引发思考,学生展开讨论,一步步得出结论,有利于学生对概念的深入理解和推理,归纳能力的培养学生讨论学生阅读,18g 58.5g 23g 32g 23 g·mol-1 58.5 g·mol-1 96 g·mol-1 53 g147g ;6;3 ;96g ;3g 108g/mol CBDB1、1 mol ;0.5 mol 2、12.8 g3、1084、0.98克5、11.1克
教学回顾:
扩大6.02×1023倍
扩大6.0×1023倍
扩大6.02×1023倍
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
课题:第二节 化学计量在实验中的应用(一) ------物质的量和摩尔质量 授课班级
课 时 1
教学目的 知识与技能 1、认识摩尔是物质的是的基本单位,了解物质的量与微观粒子之间的关系,了解 摩尔质量的概念,了解提出摩尔这一概念的重要性和必要性,懂得阿伏加德罗常数的涵义2、了解物质的量、摩尔质量、物质的质量之间的关系,能用于进行简单的化学计算。
过程与方法 1、初步培养学生演绎推理、归纳推理、逻辑推理和运用化学知识进行计算的能力2、通过物质的量这一联系微观粒子与宏观质量的物理量的学习,引导学生以化学的眼光、从微观的角度地认识丰富多彩的物质世界,认识到宏观和微观的相互转化是研究化学的科学方法之一。
情感态度价值观 1、通过对概念的透彻理解,培养学生严谨、认真的学习态度,体会定量研究的方法对研究和学习化学的重要作用。
重 点 物质的量及单位;摩尔质量的概念和有关摩尔质量的计算
难 点 物质的量及单位------摩尔
知识结构与板书设计 第二节 化学计量在实验中的应用一、物质的量(amount of substance)的单位---摩尔(mole)1.是一个物理量,符号为 n,单位为摩尔(mol)。2、阿伏加德罗常数:表示1mol任何粒子的粒子数,符号为NA,单位为mol-1,数值约为6.02*1023 mol-13、注意:使用mol时,必须指明粒子的种类,可以是分子、原子、离子、电子等。4.N、NA与n的关系: A1=1 mol任何粒子或物质的质量是以克为单位,在数值上就等于该粒子的相对原子(分子、离子)质量。5、摩尔质量:(1)定义:单位物质的量的物质所具有的质量,符号为M(2)、公式:M= 单位 g·mol-16、有关摩尔质量的相关计算例1:24.5 g H2SO4 的物质的量是_________解:H2SO4 的相对分子质量为98,则M(H2SO4 )=98 g·mol-1。n(H2SO4 )===0.25mol。答:略
教学过程
教学步骤、内容 教学方法、手段、师生活动
[引言]我们在初中时知道,分子、原子、离子等我们肉眼看不见的粒子,可以构成客观存在的、具有一定质量的物质,这说明,在我们肉眼看不见的粒子与物质的质量之间,必定存在着某种联系,那么,联系他们的桥梁是什么呢?要解决这个问题,我们来学习第二节化学计量在实验中的应用[板书]第二节 化学计量在实验中的应用[讲]就像长度可用来表示物体的长短,温度可表示为物体的冷热程度一样,物质的量可用来表示物质所含粒子数的多少,其符号为n,它是国际单位制中的基本物理量,四个字缺一不可,物质的量单位是摩尔,符号mol ,简称摩。[投] 国际单位制(SI)的7个基本单位物理量的符号单位名称及符号长度l(L)米(m)时间t秒(s)质量m千克(kg)温度T开尔文(K)发光强度I(Iv)坎德拉(cd)电流I安培(A)物质的量n摩尔(mol)[板书]一、物质的量(amount of substance)的单位---摩尔(mole)1.是一个物理量,符号为 n,单位为摩尔(mol)。[过渡]从物质的量设立的目的上看,物质的量实际上表示含有一定数目粒子的集体。这个集体的组成者是粒子,这种集体有大有小,也就是集体内的粒子数目有多有少。因此,物质的量是专门用于计算粒子数目的物理量。那么物质的是的1个单位即1mol表示的粒子数目是多少呢?[学生活动]阅读教材45页上内容,理解物质的量在粒子数目上的大小关系[问]1mol粒子的数目大约是多少?(约为6.02*1023个)[问]6.02*1023这个数值是以什么为依据得出的?(是以0.012kg12C中所含碳原子数为依据得出来的)[问]12C原子特指什么结构的碳原子?(12C指原子核内有6个质子和6个中子的碳原子)[师]大家回答得很好。由此,我们可以得出以下结论: 1mol任何粒子的数目是0.012kg12C中所含的碳原子数目约为6.02*1023个[讲]1mol任何粒子的数目也叫阿伏加德罗常数。阿伏加德罗是意大利物理学家。因他对6.02*1023这个数据的测得有着很大的贡献,故用他的名字来表示1mol任何粒子的粒子数,以示纪念。化学上,我们用NA来表示阿伏加德罗常数,其单位mol-1,它表示1mol任何粒子的粒子数,其数值近似6.02*1023个等于。[板书]2、阿伏加德罗常数:表示1mol任何粒子的粒子数,符号为NA,单位为mol-1,数值约为6.02*1023 mol-1[师]下面请同学们点击试题,看看平常计算中是如何应用阿伏加德罗常数的。[点击试题]填空1. 1 mol H2所含氢气分子的个数 。2. 2 mol氢分子含 个氢原子。3. 1 mol SO42―是 个硫酸根离子。[讲]物质的量只限制了所含粒子个数的多少,并没限制粒子的种类,所以使用mol 时应注明所指粒子是哪种?[板书]3、注意:使用mol时,必须指明粒子的种类,可以是分子、原子、离子、电子等。[点击试题]判断正误,说明理由。A. 1 mol氢 B. 1 molCO2 √C. 1 mol小米 × 小米不是微观粒子[讲]请大家根据摩尔相关知识,进行如下计算。[例题]根据摩尔的有关知识,进行计算。1. 1.204×1024个H,合多少 mol (2 mol)2. 5 mol的O2中有多少个氧气分子 (3.01*1024)3. N个水分子的物质的量是多少 (已知,阿伏加德罗常数为NA)[讲]由以上练习,我们得出粒子总个数N、阿伏加德罗常数NA、物质的量n三者之间的关系为:[板书]4.N、NA与n的关系: [讲]摩尔是一个巨大数量粒子集合体,可以是整数,也可以是小数,例如可以有0.5 mol O2,0.01 mol H2SO4等,但分子、原子等具体的粒子,只能是整数,就不能说0.5个或0.01个。下面请大家做随堂练习3[点击试题]1.0.5 mol水中含有 个水分子。2.2 mol水中含有 个水分子, 个氢原子。3.1 mol H2SO4中含有 个H2SO4分子, 个硫酸根离子。4.1 mol HCl溶于水,水中存在的溶质粒子是什么 它们的物质的量各是多少 5.1个水分子中有 个电子,1 mol H2O中呢 [过]前面我们学习了物质的量,知道它是一个基本物理量,单位为摩尔,它表示含有一定数目的粒子集体。那么,1 mol粒子的数目是以什么为标准得出来的?其数目约为多少?(是以0.012 kg 12C中所含碳原子数目为标准得来的;其数目约为6.02×1023)[问]我们初中所学某种原子的相对原子质量也是以碳-12原子为标准得出来的,它是怎样定义的?(以碳-12原子的质量的1/12作为标准,其他原子的质量跟它比较所得的数值,就是这种原子的相对原子质量)[师]很好!请大家推导思考题1[思考]假如一原子的质量为m1,碳-12原子的质量为mC,则该原子的相对原子质量A1怎样表示?请大家用代数式表示出来。[副板]A1=[师]大家表示的都很正确。若另一种原子的质量为m2,则它的相对原子质量A2又该怎样表示,请大家口答。(A2=。)[问]A1比A2与m1与m2的关系是什么呢?请大家推导。( A1∶A2=m1∶m2)[师]很正确!这也就是说:原子的质量比=原子相对原子质量比。[师]下面让我们导出下列关系:微观粒子 一个C原子 一个O原子 一个Fe原子 1 mol C原子 1 mol O原子 1 mol Fe原子宏观质量 0.012 kg=12 g x g y g相对原子质量 12 16 56[师]由刚才我们对原子相对原子质量的深入理解知道:原子的质量比=原子的相对原子质量比。∴1 mol任何原子的质量比,就等于它们的相对原子质量比。请大家根据此结论,计算出x值和y值。[结果]x=16 y=56[问]1 mol钠原子的质量是多少 1 mol氢原子的质量呢?(1 mol钠原子的质量是23 g,1 mol氢原子的质量是1 g)[问]由此可得出什么结论?(1 mol任何原子的质量,在数值上都等于它们的相对原子质量)[问]单位呢?( 克!)[问]1 mol分子的质量,与它的相对分子质量有什么关系?为什么?(因为分子都是由原子构成的,而分子的相对分子质量等于构成它的原子的相对原子质量的总和。1 mol任何原子的质量在数值上等于它的相对原子质量,单位为克,则1 mol任何分子的质量就应该在数值上等于它的相对分子质量,单位为克)[师]很正确!那么,对于粒子中的离子来讲,又将怎样呢?请大家阅读课本12页最后一段后回答。(对于离子来说,由于电子的质量很小,当原子得到或失去电子变成离子时,电子的质量可略去不计,因此,1 mol离子的质量在数值上就等于该离子的式量,单位为克)[师]回答得很好,综合以上分析,我们可得出以下结论:[副板]1 mol任何粒子或物质的质量是以克为单位,在数值上就等于该粒子的相对原子(分子、离子)质量。[师]请大家做以下练习:[点击试题]1 mol H2O的质量是 。1 mol NaCl的质量是 。1 mol Na+的质量是 。1 mol S的质量是 。[师]化学上,我们把1 mol物质所具有的质量叫摩尔质量。[板书]5、摩尔质量:(1)定义:单位物质的量的物质所具有的质量,符号为M[师]也就是说,物质的摩尔质量是该物质的质量与该物质的物质的量之比[板书](2)、公式:M= 单位 g·mol-1[讲]依据此式,我们可以把物质的质量与构成物质的粒子集体---- 物质的量联系起来,请大家口答下列空[点击试题]1.Na的摩尔质量 。2.NaCl的摩尔质量 。3. SO摩尔质量 。[师]大家在解答有关摩尔质量的问题时,一定要注意单位!下面,让我们根据摩尔质量的为进行计算。注意解题格式。[板书]6、有关摩尔质量的相关计算例1:24.5 g H2SO4 的物质的量是_________解:H2SO4 的相对分子质量为98,则M(H2SO4 )=98 g·mol-1。n(H2SO4 )===0.25mol。答:略[点击试题]1。5 mol Na2CO3 的质量是多少?[小结]从本节课的学习中我们知道:1 mol不同的物质中,构成它们的粒子的数目虽然相同,但由于不同粒子的质量一般不同,故1 mol不同物质的质量一般也不相同,以克为单位时,其数值就等于构成该物质的粒子的相对原子(或分子)质量。在进行有关摩尔质量的计算时,一定要注意单位和解题格式。[自我评价]1. 1.5 mol H2SO4的质量是 。其中含有 mol O, mol H,其质量分别为 和 。2. 0.01 mol某物质的质量为1.08 g,此物质的摩尔质量为 。3.下列说法正确的是( )A.71 g氯相当于2 mol氯B.每摩尔物质中含有6.02×1023个原子C.阿伏加德罗常数为12 g 12C所含的碳原子数D.1 mol KClO3中含有3 mol氧元素4.如果1 g水中含有m个氢原子,则阿伏加德罗常数是( )A. B.9m C.2m D.18m5下列说法正确的是( )A.氮原子的质量就是氮的相对原子质量B.氢氧化钠的摩尔质量是40 gC.1 mol H2SO4中含有1 mol H2D.氩气的摩尔质量在数值上等于它的相对原子质量6、0.8g 某物质含有3.01*1022个分子,该物质的式量约为( ) A、8 B、16 C、64 D、160课后作业 1、71g Na2SO4 中含有Na+和SO42-物质的量各是__________________2、 19.6g H2SO4 中氧元素的质量_________________3、 含有1.5*1022个分子,其质量为2。7g 求分子质量4、多少克H2SO4 所含的分子数与3.6克10%盐酸所含溶质的分子数相等5、 0.2 mol KClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子数相等。 引发学习兴趣,引出把微小物质扩大倍数形成一定数目的集体以便于方便生活,方便科学研究,方便相互交流学生自学,师生一问一答,检验自学成果进行化学史的教育,培养学生科学态度 6.02*1023个 2.408*1024 6.02*1023 A、 × 没有指出是分子、原子或离子B. √C. × 小米不是微观粒子1. (2 mol)2. (3.01*1024)引导学生自我总结公式 3.01*1023 1.204*1024 ; 2.408*1024 6.02*1023; 6.02*1023 H+ 、Cl― 各1 mol 10; 6.02*1024学生推导,教师巡视并指导教师引发思考,学生展开讨论,一步步得出结论,有利于学生对概念的深入理解和推理,归纳能力的培养学生讨论学生阅读,18g 58.5g 23g 32g 23 g·mol-1 58.5 g·mol-1 96 g·mol-1 53 g147g ;6;3 ;96g ;3g 108g/mol CBDB1、1 mol ;0.5 mol 2、12.8 g3、1084、0.98克5、11.1克
教学回顾:
扩大6.02×1023倍
扩大6.0×1023倍
扩大6.02×1023倍
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
