物质的分离与提纯
图片预览







文档简介
课件28张PPT。物质的分离与提纯 日常生活中,我们所接触的各种各样的物质,大多数都是混合物,而化学研究、工业生产中经常要对混合物进行分离和提纯,如:石油的分馏、自来水的净化处理等。 ——混合物的分离和提纯分离和提纯有什么不同?分离:是通过适当的方法,把混合物中的几种物质分开,每一组分都要保留下来,并恢复到原状态,得到比较纯的物质。提纯:指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去。 我们在初中科学里也学过一些简单的实验方法,可用于混合物的分离和提纯,请同学们回忆一下,你了解哪些分离、提纯的方法?过滤、结晶等【问题】过滤注意点:
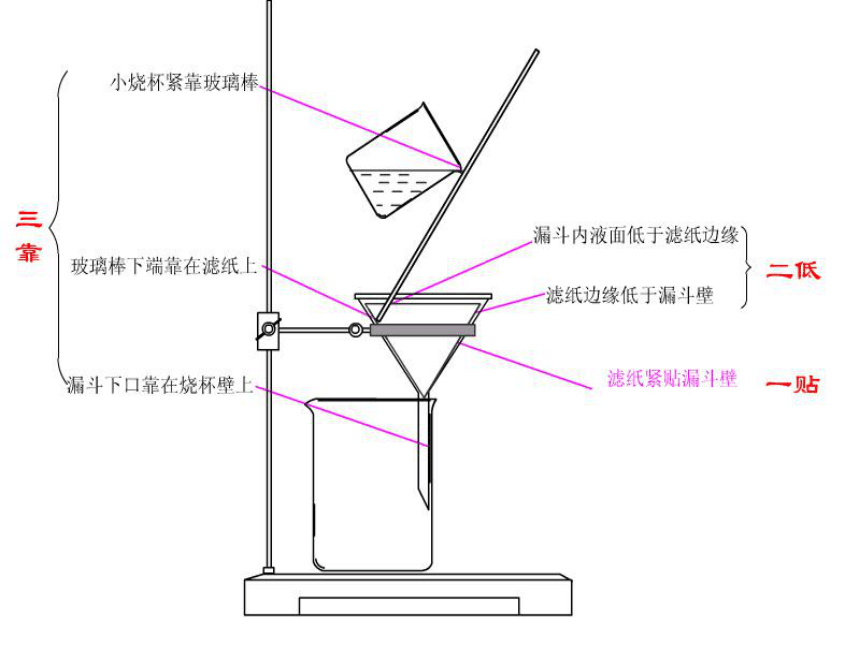
“一贴二低三靠”
通常用来分离液体和不溶的固体。1.蒸发结晶注意事项:a、蒸发皿中的溶液不超过容积的2/3;
b、加热时要不断搅拌,以免溶液溅出;
c、当析出大量晶体时就应熄灭酒精灯,利用余热蒸发至干。结晶2.冷却结晶 适用于溶解度不同的固体混合物的分离。【交流和讨论1】 已知Mg(OH)2难溶于水,BaSO4既难溶于水,又难溶于酸,BaCO3难溶于水,但可溶于盐酸。现有含Na2SO4、MgCl2和泥沙等杂质的粗食盐,请你设计实验方案,用粗食盐提纯氯化钠。思考:1.该实验的目的是什么?
2.怎样才能实现这个目的?
3.用什么试剂来除杂?
4.所加试剂的量有什么要求?
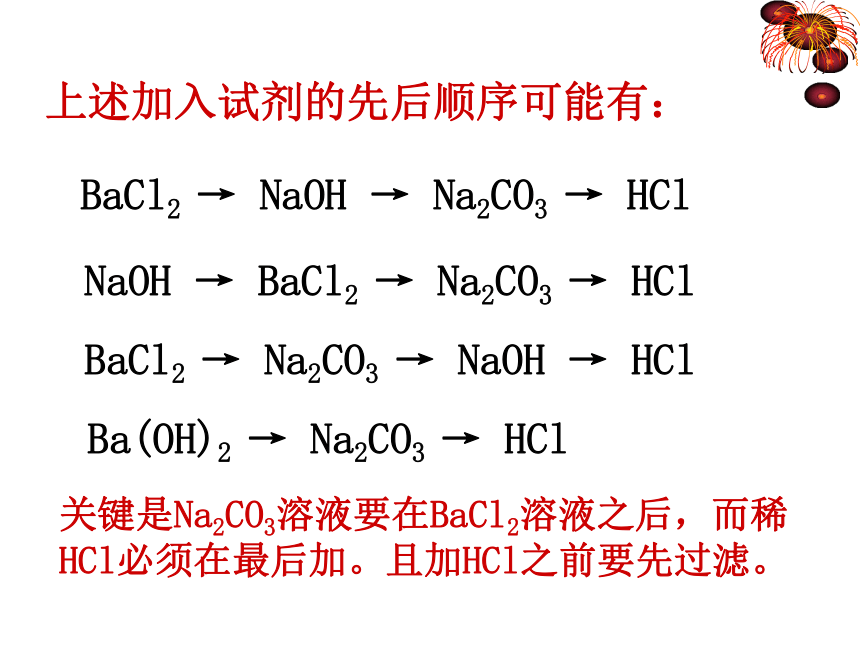
5.所加试剂的顺序又如何呢? (得到纯净的氯化钠)(先除去其中的杂质)(BaCl2、NaOH、Na2CO3、HCl)(必须过量)上述加入试剂的先后顺序可能有:BaCl2 → NaOH → Na2CO3 → HCl关键是Na2CO3溶液要在BaCl2溶液之后,而稀HCl必须在最后加。且加HCl之前要先过滤。NaOH → BaCl2 → Na2CO3 → HClBaCl2 → Na2CO3 → NaOH → HCl Ba(OH)2 → Na2CO3 → HCl【交流和讨论1】 已知氢氧化镁难溶于水,硫酸钡既难溶于水,又难溶于酸,碳酸钡难溶于水,但可溶于盐酸。现有含硫酸钠、氯化镁和泥沙等杂质的粗食盐,请你设计实验方案,用粗食盐提纯氯化钠。思考:
6.加入试剂发生的反应方程式? 1、将粗食盐加水溶解并过滤。(溶解、过滤)2、向(1)所得滤液加入过量BaCl2溶液到沉淀不再 增加为止,静置沉降。(除SO42-)3、继续加入过量Na2CO3溶液,直至沉淀不再生成为止,静置沉降。(除Ba2+)4、再加入过量的NaOH溶液,直至沉淀不再生成,静置沉降。(除Mg2+)5、将(4)所得混合物过滤,往滤液中加入稍过量的稀HCl至不再产生气泡。(除OH-、CO32-)6、将(5)所得溶液加热蒸发结晶。(除HCl、得NaCl)实验方案:溶解 →过滤 → BaCl2(过量) → Na0H(过量)
→ Na2CO3(过量) → 过滤 → 盐酸(过量) →
蒸发结晶也可以用下列方式来表示: 1、除杂时所加试剂必须过量;
2、过量的试剂也必须除去;
3、分离和提纯的方法要求最佳。物质的分离和提纯中须注意:实验室里用不纯的氯酸钾
(少量的硫酸钾与碳酸钾)
和二氧化锰制取氧气,请
问如何提取完全反应后剩
余物质中的氯化钾?
设计一个实验方案。方案思路:
溶解 → 过滤 → BaCl2(过量) → K2CO3(过量) → 过滤 → HCl(过量) → 蒸发结晶练习:【交流和讨论2】 现有氯化钾和硝酸钾的固体混合物50g,其中KCl的质量分数为10%,请设计实验方案提纯硝酸钾。 设计思路:KCl、KNO3混合物KCl、KNO3溶液KNO3(S)、KCl+ KNO3溶液KNO3(S)加热溶解降温结晶过滤设计方案:将混合物溶于适量水中加热溶解(水大约30 mL),自然冷却结晶,过滤得KNO3晶体。【观察和思考】实验步骤:在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1mlCCl4,振荡、静置。现象:溴水呈橙色。加CCl4后溶液分层,上层几乎无色,下层呈橙红色。萃取 利用物质在互不相溶的溶剂中溶解度的不同,将物质从一种溶剂转移到另一溶剂中,从而进行分离的方法称为萃取。萃取剂要求:
1.两种溶剂要互不相容
2.溶质在萃取剂中的溶解度比在原溶剂中的溶解度大的多
3.溶质、溶剂之间不能反应。▲操作注意:
1.充分振荡,充分静止,然后分液;
2.分液时保持漏斗内与大气压一致;下层溶液下口出,上层溶液上口出。
萃取之后一般通过分液的方法将互不相溶的液体分离。蒸馏 利用互溶液体混合物中各组分沸点不同(通常沸点需相差30℃以上)进行分离提纯的操作。其过程是:将液态物质加热至沸点,使之汽化,然后将蒸气重新冷凝为液体的操作过程成为蒸馏。蒸馏实验示意图注意点:①实验前在蒸馏烧瓶中先加入几粒沸石(或碎瓷片)—防止液体暴沸③冷凝水的方向: ——利用各组分沸点不同,将液态混合物
分离和提纯的方法蒸馏投放沸石或瓷片温度计水银球处于支管口处水,下入上出操作注意:
1、先通水,再加热
2、刚开始收集到的馏分
应弃去
3、全程严格控制好温度用蒸馏原理进行多种混合液体的分离,叫分馏 溶液体积不超过烧瓶体积1/2实验室蒸馏石油汽油60℃ ~150 ℃
煤油150℃ ~300 ℃常压分馏、减压分馏工业分馏石油.MPG拓展视野【课堂小结】物质的分离、提纯注意:不同的分离方法都有一定的适用范围,要根据不同混合物的性质选择合适的方法进行分离,且有时需要多种方法配合使用。同时在分离和提纯时也要满足基本原则:不增、不减、易分、复原。固体与液体不互溶的混合物粗盐的提纯混合物中各成分在溶剂中溶解度不同,包括蒸发溶剂结晶和降温结晶分离NaCl和KNO3的混合物 ①难挥发的固体杂质在液体中形成的混合物
②互溶液体沸点有明显差异蒸馏水、石油的分馏两种互不混溶的液体混合物 CCl4和水的分离溶质在互不相溶的溶剂里溶解度不同利用CCl4从溴水中萃取溴 练习: 用于分离或提纯物质的已学方法有:
A.萃取 B.分液 C.过滤
D.加热分解 E.蒸发 F.蒸馏
下列各组混合物的分离或提纯应选用上述哪种方法最合
适?(把选用方法的标号填入括号内)
(1)除去Ca(OH)2溶液中悬浮的Ca(OH)2 颗粒( )
(2)把饱和食盐水中的食盐提取出来( )
(3)除去酒精中溶解的微量食盐( )
(4)把溴水中的溴提取出来 ( )
(5)用自来水制取医用蒸馏水 ( )
(6)除去氧化钙中的碳酸钙 ( )
(7)分离柴油和水的混合物 ( )BDACEFF酒精和水的混合物如何分离?先加生石灰(CaO)除去水,
再过滤,将滤液蒸馏
“一贴二低三靠”
通常用来分离液体和不溶的固体。1.蒸发结晶注意事项:a、蒸发皿中的溶液不超过容积的2/3;
b、加热时要不断搅拌,以免溶液溅出;
c、当析出大量晶体时就应熄灭酒精灯,利用余热蒸发至干。结晶2.冷却结晶 适用于溶解度不同的固体混合物的分离。【交流和讨论1】 已知Mg(OH)2难溶于水,BaSO4既难溶于水,又难溶于酸,BaCO3难溶于水,但可溶于盐酸。现有含Na2SO4、MgCl2和泥沙等杂质的粗食盐,请你设计实验方案,用粗食盐提纯氯化钠。思考:1.该实验的目的是什么?
2.怎样才能实现这个目的?
3.用什么试剂来除杂?
4.所加试剂的量有什么要求?
5.所加试剂的顺序又如何呢? (得到纯净的氯化钠)(先除去其中的杂质)(BaCl2、NaOH、Na2CO3、HCl)(必须过量)上述加入试剂的先后顺序可能有:BaCl2 → NaOH → Na2CO3 → HCl关键是Na2CO3溶液要在BaCl2溶液之后,而稀HCl必须在最后加。且加HCl之前要先过滤。NaOH → BaCl2 → Na2CO3 → HClBaCl2 → Na2CO3 → NaOH → HCl Ba(OH)2 → Na2CO3 → HCl【交流和讨论1】 已知氢氧化镁难溶于水,硫酸钡既难溶于水,又难溶于酸,碳酸钡难溶于水,但可溶于盐酸。现有含硫酸钠、氯化镁和泥沙等杂质的粗食盐,请你设计实验方案,用粗食盐提纯氯化钠。思考:
6.加入试剂发生的反应方程式? 1、将粗食盐加水溶解并过滤。(溶解、过滤)2、向(1)所得滤液加入过量BaCl2溶液到沉淀不再 增加为止,静置沉降。(除SO42-)3、继续加入过量Na2CO3溶液,直至沉淀不再生成为止,静置沉降。(除Ba2+)4、再加入过量的NaOH溶液,直至沉淀不再生成,静置沉降。(除Mg2+)5、将(4)所得混合物过滤,往滤液中加入稍过量的稀HCl至不再产生气泡。(除OH-、CO32-)6、将(5)所得溶液加热蒸发结晶。(除HCl、得NaCl)实验方案:溶解 →过滤 → BaCl2(过量) → Na0H(过量)
→ Na2CO3(过量) → 过滤 → 盐酸(过量) →
蒸发结晶也可以用下列方式来表示: 1、除杂时所加试剂必须过量;
2、过量的试剂也必须除去;
3、分离和提纯的方法要求最佳。物质的分离和提纯中须注意:实验室里用不纯的氯酸钾
(少量的硫酸钾与碳酸钾)
和二氧化锰制取氧气,请
问如何提取完全反应后剩
余物质中的氯化钾?
设计一个实验方案。方案思路:
溶解 → 过滤 → BaCl2(过量) → K2CO3(过量) → 过滤 → HCl(过量) → 蒸发结晶练习:【交流和讨论2】 现有氯化钾和硝酸钾的固体混合物50g,其中KCl的质量分数为10%,请设计实验方案提纯硝酸钾。 设计思路:KCl、KNO3混合物KCl、KNO3溶液KNO3(S)、KCl+ KNO3溶液KNO3(S)加热溶解降温结晶过滤设计方案:将混合物溶于适量水中加热溶解(水大约30 mL),自然冷却结晶,过滤得KNO3晶体。【观察和思考】实验步骤:在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1mlCCl4,振荡、静置。现象:溴水呈橙色。加CCl4后溶液分层,上层几乎无色,下层呈橙红色。萃取 利用物质在互不相溶的溶剂中溶解度的不同,将物质从一种溶剂转移到另一溶剂中,从而进行分离的方法称为萃取。萃取剂要求:
1.两种溶剂要互不相容
2.溶质在萃取剂中的溶解度比在原溶剂中的溶解度大的多
3.溶质、溶剂之间不能反应。▲操作注意:
1.充分振荡,充分静止,然后分液;
2.分液时保持漏斗内与大气压一致;下层溶液下口出,上层溶液上口出。
萃取之后一般通过分液的方法将互不相溶的液体分离。蒸馏 利用互溶液体混合物中各组分沸点不同(通常沸点需相差30℃以上)进行分离提纯的操作。其过程是:将液态物质加热至沸点,使之汽化,然后将蒸气重新冷凝为液体的操作过程成为蒸馏。蒸馏实验示意图注意点:①实验前在蒸馏烧瓶中先加入几粒沸石(或碎瓷片)—防止液体暴沸③冷凝水的方向: ——利用各组分沸点不同,将液态混合物
分离和提纯的方法蒸馏投放沸石或瓷片温度计水银球处于支管口处水,下入上出操作注意:
1、先通水,再加热
2、刚开始收集到的馏分
应弃去
3、全程严格控制好温度用蒸馏原理进行多种混合液体的分离,叫分馏 溶液体积不超过烧瓶体积1/2实验室蒸馏石油汽油60℃ ~150 ℃
煤油150℃ ~300 ℃常压分馏、减压分馏工业分馏石油.MPG拓展视野【课堂小结】物质的分离、提纯注意:不同的分离方法都有一定的适用范围,要根据不同混合物的性质选择合适的方法进行分离,且有时需要多种方法配合使用。同时在分离和提纯时也要满足基本原则:不增、不减、易分、复原。固体与液体不互溶的混合物粗盐的提纯混合物中各成分在溶剂中溶解度不同,包括蒸发溶剂结晶和降温结晶分离NaCl和KNO3的混合物 ①难挥发的固体杂质在液体中形成的混合物
②互溶液体沸点有明显差异蒸馏水、石油的分馏两种互不混溶的液体混合物 CCl4和水的分离溶质在互不相溶的溶剂里溶解度不同利用CCl4从溴水中萃取溴 练习: 用于分离或提纯物质的已学方法有:
A.萃取 B.分液 C.过滤
D.加热分解 E.蒸发 F.蒸馏
下列各组混合物的分离或提纯应选用上述哪种方法最合
适?(把选用方法的标号填入括号内)
(1)除去Ca(OH)2溶液中悬浮的Ca(OH)2 颗粒( )
(2)把饱和食盐水中的食盐提取出来( )
(3)除去酒精中溶解的微量食盐( )
(4)把溴水中的溴提取出来 ( )
(5)用自来水制取医用蒸馏水 ( )
(6)除去氧化钙中的碳酸钙 ( )
(7)分离柴油和水的混合物 ( )BDACEFF酒精和水的混合物如何分离?先加生石灰(CaO)除去水,
再过滤,将滤液蒸馏
