物质的量浓度
图片预览








文档简介
课件21张PPT。溶液的配制及分析 知识目标:
1、掌握容量瓶的使用方法,初步学会配制一定物质 的量浓度溶液的方法和技能
能力目标:
2、培养学生的观察能力、发现问题和解决问题的能力,语言表达能力和归纳总结能力
情感目标:
3、重视实验态度,培养学生严谨、求实的科学作风
教学重难点:
一定物质的量浓度的溶液的配制方法已知 100mL 0.100mol/L的Na2CO3溶液?n(Na2CO3)=c(Na2CO3) ×V= 0.100mol/×0.100L=0.0100mol
m(Na2CO3)=M(Na2CO3)×n(Na2CO3)=106g/mol×0.0100mol
=1.06g溶液的体积(V)=100mL1.你从中可以得到哪些信息?2.在1.06g Na2CO3中加入100mL的水是否可以得到100mL的溶液的呢?3.怎样才能使最终所得溶液的体积为100mL呢?向 你 讨 教线构造:细颈、梨形、平底的玻璃瓶 2.特点:瓶上标有温度,容积,瓶颈上有一道刻度线 容积容 量 瓶 3.注意事项:①溶解、反应不能在容量瓶中进行②溶液恢复至室温后才能转移到容量瓶
③容量瓶只有一个刻度线,只能配制体积与容量瓶容积相同的溶液 实验室要配制 100mL 0.100 mol/L Na2CO3溶液,结合课本24页,请讨论与思考:
①如何进行配制?
②需要用那些仪器及药品?
活动与探究1.计算2.称量3.溶解4.转移5.定容6.摇匀天平、药匙烧杯、玻璃棒容量瓶(100mL)、烧杯、玻璃棒
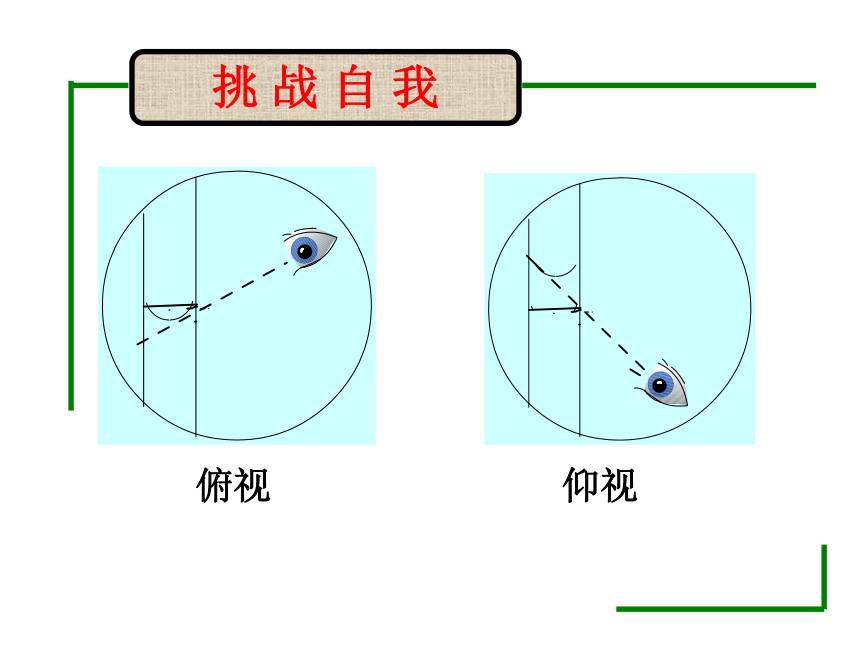
胶头滴管转移视频.定容检漏1.未用蒸馏水洗涤烧杯和玻璃棒(偏低)2.未冷却就转移(偏高)3.定容时水加多了,超过刻度线(偏低)交流与讨论挑 战 自 我俯视仰视1、准确配制一定物质的量浓度的NaOH溶液,下面实验操作中正确的是( )
A、称量时,将NaOH固体直接放在天平的托盘上面称量。
B、将称量好NaOH的固体放入容量瓶中,再加少量水溶解。
C、在烧杯中溶解NaOH固体立即注入容量瓶中。
D、将烧杯中已冷却的NaOH溶液注入未经干燥的容量瓶中。
D问题解决2、某实验中共需要480mL0.5mol/L NaCl的溶液,有一学生准备在实验室中进行配制。他开出的实验用品清单为:蒸馏水、烧杯、天平、玻璃棒。请你分析该同学还缺少的主要仪器 .
实验中应该准确称量 gNaCl。 药匙、500mL容量瓶、胶头滴管14.6
问题解决 1、容量瓶的使用
2、配制一定物质的量浓度的溶液的步骤
3、配制过程中的常见错误分析小
结步骤注意作
业 1、p26练习与实践4
2、同步训练习题
1.是否立即将烧杯里的溶液转移到容量瓶里呢?(冷却后再转移)2.怎样转移呢?(用玻璃棒引流)转移时应该注意哪些呢?(两靠一不靠)3.怎样使溶质全部转移到容量瓶?(洗涤烧杯及玻璃棒2-3次,并将洗涤液转 移到容量瓶)
返回两靠话说“转移”引流操作两靠一不靠返回检 漏 方 法①加水→倒立→观察
② 瓶塞旋转180o →倒立→观察
⑤使用前要检查是否漏水①溶解、反应不能在容量瓶中进行②溶液恢复至室温后才能转移入容量瓶④转移溶液时要用玻棒进行引流③容量瓶只有一个刻度线,不能随意配 制任意体积的溶液整理与 归纳使用容量瓶时应注意的问题:返回整理与 归纳配制的步骤:
计算→称量→溶解→转移→定容→摇匀返回谢谢!再见!
1、掌握容量瓶的使用方法,初步学会配制一定物质 的量浓度溶液的方法和技能
能力目标:
2、培养学生的观察能力、发现问题和解决问题的能力,语言表达能力和归纳总结能力
情感目标:
3、重视实验态度,培养学生严谨、求实的科学作风
教学重难点:
一定物质的量浓度的溶液的配制方法已知 100mL 0.100mol/L的Na2CO3溶液?n(Na2CO3)=c(Na2CO3) ×V= 0.100mol/×0.100L=0.0100mol
m(Na2CO3)=M(Na2CO3)×n(Na2CO3)=106g/mol×0.0100mol
=1.06g溶液的体积(V)=100mL1.你从中可以得到哪些信息?2.在1.06g Na2CO3中加入100mL的水是否可以得到100mL的溶液的呢?3.怎样才能使最终所得溶液的体积为100mL呢?向 你 讨 教线构造:细颈、梨形、平底的玻璃瓶 2.特点:瓶上标有温度,容积,瓶颈上有一道刻度线 容积容 量 瓶 3.注意事项:①溶解、反应不能在容量瓶中进行②溶液恢复至室温后才能转移到容量瓶
③容量瓶只有一个刻度线,只能配制体积与容量瓶容积相同的溶液 实验室要配制 100mL 0.100 mol/L Na2CO3溶液,结合课本24页,请讨论与思考:
①如何进行配制?
②需要用那些仪器及药品?
活动与探究1.计算2.称量3.溶解4.转移5.定容6.摇匀天平、药匙烧杯、玻璃棒容量瓶(100mL)、烧杯、玻璃棒
胶头滴管转移视频.定容检漏1.未用蒸馏水洗涤烧杯和玻璃棒(偏低)2.未冷却就转移(偏高)3.定容时水加多了,超过刻度线(偏低)交流与讨论挑 战 自 我俯视仰视1、准确配制一定物质的量浓度的NaOH溶液,下面实验操作中正确的是( )
A、称量时,将NaOH固体直接放在天平的托盘上面称量。
B、将称量好NaOH的固体放入容量瓶中,再加少量水溶解。
C、在烧杯中溶解NaOH固体立即注入容量瓶中。
D、将烧杯中已冷却的NaOH溶液注入未经干燥的容量瓶中。
D问题解决2、某实验中共需要480mL0.5mol/L NaCl的溶液,有一学生准备在实验室中进行配制。他开出的实验用品清单为:蒸馏水、烧杯、天平、玻璃棒。请你分析该同学还缺少的主要仪器 .
实验中应该准确称量 gNaCl。 药匙、500mL容量瓶、胶头滴管14.6
问题解决 1、容量瓶的使用
2、配制一定物质的量浓度的溶液的步骤
3、配制过程中的常见错误分析小
结步骤注意作
业 1、p26练习与实践4
2、同步训练习题
1.是否立即将烧杯里的溶液转移到容量瓶里呢?(冷却后再转移)2.怎样转移呢?(用玻璃棒引流)转移时应该注意哪些呢?(两靠一不靠)3.怎样使溶质全部转移到容量瓶?(洗涤烧杯及玻璃棒2-3次,并将洗涤液转 移到容量瓶)
返回两靠话说“转移”引流操作两靠一不靠返回检 漏 方 法①加水→倒立→观察
② 瓶塞旋转180o →倒立→观察
⑤使用前要检查是否漏水①溶解、反应不能在容量瓶中进行②溶液恢复至室温后才能转移入容量瓶④转移溶液时要用玻棒进行引流③容量瓶只有一个刻度线,不能随意配 制任意体积的溶液整理与 归纳使用容量瓶时应注意的问题:返回整理与 归纳配制的步骤:
计算→称量→溶解→转移→定容→摇匀返回谢谢!再见!
