物质的分散系
图片预览







文档简介
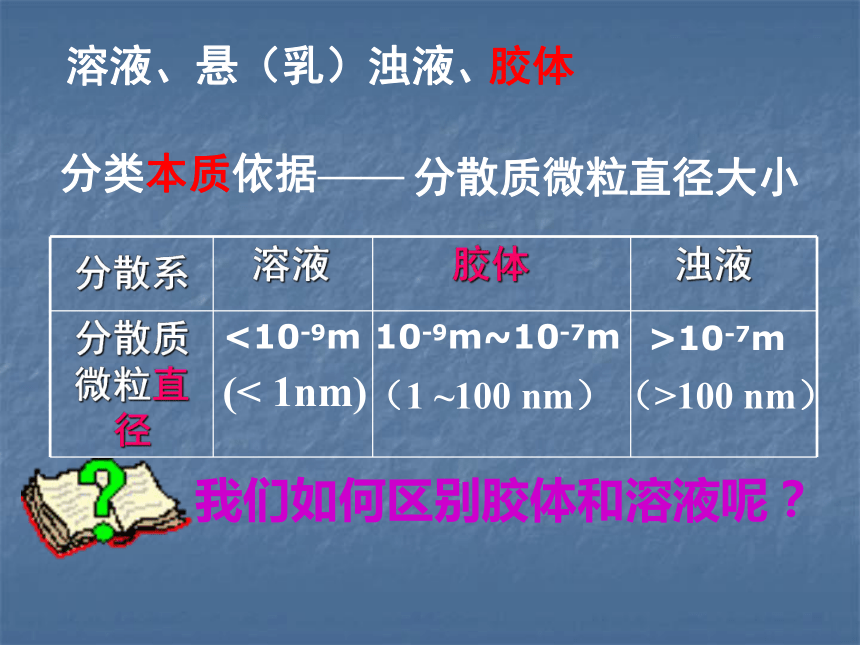
课件26张PPT。物质的分散系高一化学组什么叫分散系,分散质、分散剂?自主学习一、分散系 把一种(或几种)物质分散在另一种物质中所得到的混合物分散质:分散成微粒的物质分散剂:微粒分散在其中的物质溶液、悬(乳)浊液、分类本质依据——<10-9m(< 1nm) 10-9m~10-7m(1 ~100 nm) >10-7m(>100 nm) 我们如何区别胶体和溶液呢?溶液浊液胶体
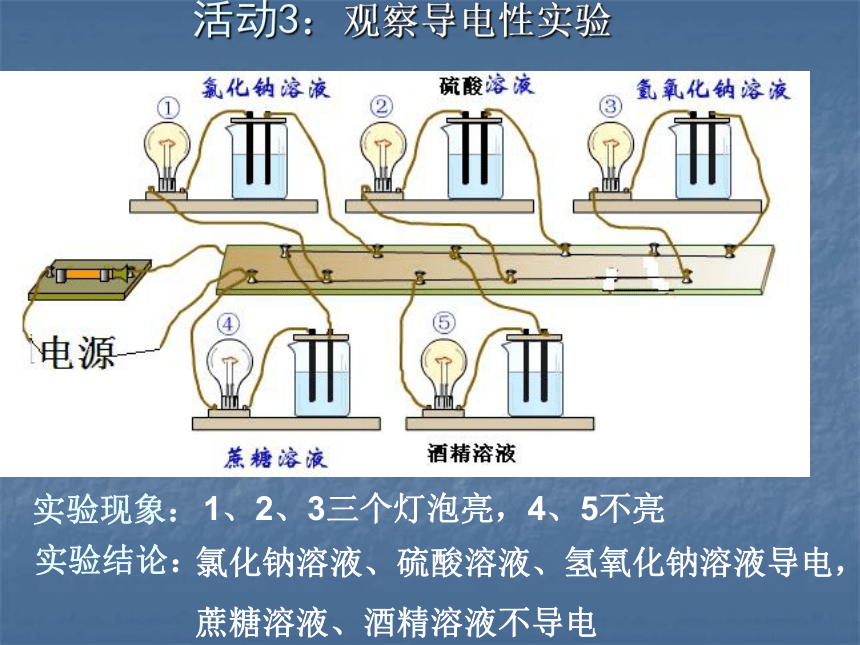
胶体 分散质微粒直径大小 将盛有CuSO4溶液和Fe(OH)3胶体的烧杯置于暗处,分别用激光手电筒照射烧杯中的液体,在与光束垂直的方向进行观察,并记录实验现象。活动与探究1盛氢氧化铁胶体的烧杯中有一条光亮的通路,硫酸铜溶液中没有胶体具有 丁达尔效应实验报告单活动与探索二、胶体1、丁达尔效应——区别胶体和溶液2、具有吸附性 ——用于净水丁达尔效应:当光束通过胶体时,在垂直于光线的方向可以看到一条光亮的通路,该现象称为丁达尔效应活动3:观察导电性实验实验结论:实验现象:1、2、3三个灯泡亮,4、5不亮氯化钠溶液、硫酸溶液、氢氧化钠溶液导电,
蔗糖溶液、酒精溶液不导电氯化钠溶解的微观过程蔗糖溶解的微观过程三、 电解质与非电解质——以分子存在,不能电离出离子——能电离出离子电离:电解质在水溶液或熔融状态下产生自由移动的离子的过程 (酸、碱、盐、某些金属化合物) (蔗糖、酒精、许多有机 物)
三、 电解质与非电解质——以分子存在,不能电离出离子——(或)自身能电离出离子 (酸、碱、盐、某些金属化合物) (蔗糖、酒精、许多有机 物)
问题解决讨论二:判断物质是否是电解质的依据是什么?判断1: BaSO4难溶于水,水溶液不导电,所以BaSO4
是非电解质。判断2:KNO3水溶液能导电,它的水溶液是电解质。讨论一:Na2O溶于水能导电,能否说明它是电解质。CO2溶于水能导电,它是电解质吗?判断3:NaCl晶体不能导电,它不是电解质。分散系
溶液胶体浊液化合物电解质非电解质(混合物)分散质微粒直径丁达尔效应吸附性(能否电离)小结:书本作业:
P16 1、6、7实践作业:
(1)查阅资料,找出日常生活中接触到的胶体。
(2)配制鸡蛋清溶液,并观察其丁达尔现象。2、胶体的最本质的特征是( )
A、丁达尔效应 B、具有吸附性
C、分散质粒子的直径在1nm~100nm之间1、在物质分类中,前者包括后者的是( )
A、氧化物、化合物 B、化合物、电解质
C、溶液、胶体 D、溶液、分散系
BCTest timeTest time
3、请写出以下化合物的电离方程式:
1)Ba(OH)2=
2)MgCl2 =
3)Al2(SO4)3 =
4、判断下列物质中不属于电解质的是( )
A.NaOH B.盐酸
C.硝酸钠 D.三氧化硫5、判断下列物质中属于非电解质的是( )
A.NaOH B.盐酸
C.硝酸钠 D.三氧化硫BDD敬请指导!房间里的丁达尔效应自然界的丁达尔现象往盛有浑浊水的烧杯中加一滴管Fe(OH)3胶体,搅拌后静置片刻,与原混合液比较液体的澄清程度并记录。活动与探究2加入氢氧化铁胶体的烧杯中溶液变澄清,在烧杯底部出现沉淀,另一个烧杯仍然浑浊胶体具有丁达尔效应胶体具有较强的吸附性,能吸附溶液中悬浮的颗粒实验报告单活动与探索盛氢氧化铁胶体的烧杯中有一条光亮的通路,硫酸铜溶液中没有胶体有什么用??? 胶体的作用 胶体能够使水中的悬浮的固体颗粒凝聚而沉降下来,具有凝聚作用,因此,氢氧化铁胶体可以用来净水。
日常生活中我们常用来净水的是KAl(SO4)2·12H2O(十二水硫酸铝钾),俗称明矾,溶于水会形成Al(OH)3胶体, Al(OH)3具有很好的凝聚作用,是一种良好的净水剂。利用了胶体的吸附性。阅读P15的资料卡电离方程式 表示电解质在溶液中或熔融状态下电离成能够自由移动的离子的式子。H2SO4
NaCl
NaOH
电离产生金属阳离子或铵根离子和酸根离子的化合物——盐电离产生的阳离子全部是H+的化合物——酸电离产生的阴离子全部是OH-的化合物——碱H2SO4 = 2H+ + SO42-
NaCl = Na+ + Cl–
NaOH = Na+ + OH-
胶体 分散质微粒直径大小 将盛有CuSO4溶液和Fe(OH)3胶体的烧杯置于暗处,分别用激光手电筒照射烧杯中的液体,在与光束垂直的方向进行观察,并记录实验现象。活动与探究1盛氢氧化铁胶体的烧杯中有一条光亮的通路,硫酸铜溶液中没有胶体具有 丁达尔效应实验报告单活动与探索二、胶体1、丁达尔效应——区别胶体和溶液2、具有吸附性 ——用于净水丁达尔效应:当光束通过胶体时,在垂直于光线的方向可以看到一条光亮的通路,该现象称为丁达尔效应活动3:观察导电性实验实验结论:实验现象:1、2、3三个灯泡亮,4、5不亮氯化钠溶液、硫酸溶液、氢氧化钠溶液导电,
蔗糖溶液、酒精溶液不导电氯化钠溶解的微观过程蔗糖溶解的微观过程三、 电解质与非电解质——以分子存在,不能电离出离子——能电离出离子电离:电解质在水溶液或熔融状态下产生自由移动的离子的过程 (酸、碱、盐、某些金属化合物) (蔗糖、酒精、许多有机 物)
三、 电解质与非电解质——以分子存在,不能电离出离子——(或)自身能电离出离子 (酸、碱、盐、某些金属化合物) (蔗糖、酒精、许多有机 物)
问题解决讨论二:判断物质是否是电解质的依据是什么?判断1: BaSO4难溶于水,水溶液不导电,所以BaSO4
是非电解质。判断2:KNO3水溶液能导电,它的水溶液是电解质。讨论一:Na2O溶于水能导电,能否说明它是电解质。CO2溶于水能导电,它是电解质吗?判断3:NaCl晶体不能导电,它不是电解质。分散系
溶液胶体浊液化合物电解质非电解质(混合物)分散质微粒直径丁达尔效应吸附性(能否电离)小结:书本作业:
P16 1、6、7实践作业:
(1)查阅资料,找出日常生活中接触到的胶体。
(2)配制鸡蛋清溶液,并观察其丁达尔现象。2、胶体的最本质的特征是( )
A、丁达尔效应 B、具有吸附性
C、分散质粒子的直径在1nm~100nm之间1、在物质分类中,前者包括后者的是( )
A、氧化物、化合物 B、化合物、电解质
C、溶液、胶体 D、溶液、分散系
BCTest timeTest time
3、请写出以下化合物的电离方程式:
1)Ba(OH)2=
2)MgCl2 =
3)Al2(SO4)3 =
4、判断下列物质中不属于电解质的是( )
A.NaOH B.盐酸
C.硝酸钠 D.三氧化硫5、判断下列物质中属于非电解质的是( )
A.NaOH B.盐酸
C.硝酸钠 D.三氧化硫BDD敬请指导!房间里的丁达尔效应自然界的丁达尔现象往盛有浑浊水的烧杯中加一滴管Fe(OH)3胶体,搅拌后静置片刻,与原混合液比较液体的澄清程度并记录。活动与探究2加入氢氧化铁胶体的烧杯中溶液变澄清,在烧杯底部出现沉淀,另一个烧杯仍然浑浊胶体具有丁达尔效应胶体具有较强的吸附性,能吸附溶液中悬浮的颗粒实验报告单活动与探索盛氢氧化铁胶体的烧杯中有一条光亮的通路,硫酸铜溶液中没有胶体有什么用??? 胶体的作用 胶体能够使水中的悬浮的固体颗粒凝聚而沉降下来,具有凝聚作用,因此,氢氧化铁胶体可以用来净水。
日常生活中我们常用来净水的是KAl(SO4)2·12H2O(十二水硫酸铝钾),俗称明矾,溶于水会形成Al(OH)3胶体, Al(OH)3具有很好的凝聚作用,是一种良好的净水剂。利用了胶体的吸附性。阅读P15的资料卡电离方程式 表示电解质在溶液中或熔融状态下电离成能够自由移动的离子的式子。H2SO4
NaCl
NaOH
电离产生金属阳离子或铵根离子和酸根离子的化合物——盐电离产生的阳离子全部是H+的化合物——酸电离产生的阴离子全部是OH-的化合物——碱H2SO4 = 2H+ + SO42-
NaCl = Na+ + Cl–
NaOH = Na+ + OH-
