必修1. 3 .1化学中常用的物理量—物质的量 第一课时
文档属性
| 名称 | 必修1. 3 .1化学中常用的物理量—物质的量 第一课时 |

|
|
| 格式 | rar | ||
| 文件大小 | 492.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-10-17 00:00:00 | ||
图片预览







文档简介
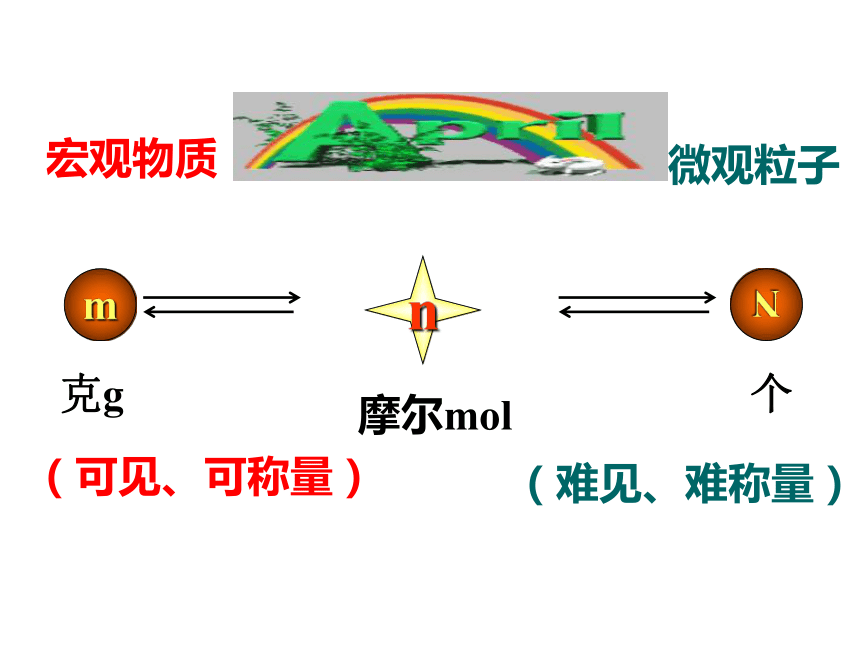
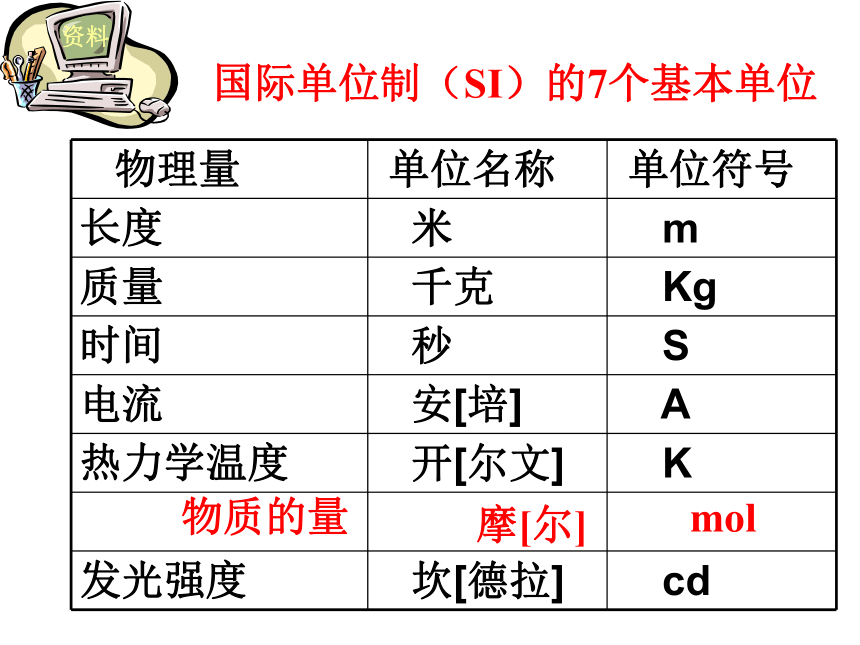
课件25张PPT。第一课时物质的量及其单位—摩尔 水是大家非常熟悉的物质,它是由水分子构成的。一滴水(约0.05mL)大约含有17万亿亿个水分子。如果一个个地去数,即使分秒不停,一个人一生也无法完成这项任务。那么怎样才能既科学又方便地知道一定量的水中含有多少个水分子呢?n(难见、难称量)微观粒子宏观物质(可见、可称量)个克g摩尔mol资料国际单位制(SI)的7个基本单位物质的量摩[尔]mol注意:物质的量是一个专用名词,不能拆开理解,也不能增减字. ?[思考]已知:一个碳原子的质量为 1.993 × 10-23kg
求: 0.012kg 12C中所含的碳原子数?解:碳原子数=0.012kg1.993 × 10-23kg ≈ 6.02×1023 0.012Kg12C中所含C原子数1mol任何微粒的粒子数阿伏加德罗 常数的值= 6.02×1023=近似为二、阿伏加德罗常数的含义1摩尔(mol)(1)使用“mol”单位时,应用化学式指明粒子的种类。如0.5molNa+、2molH2、1molCa。(2)以mol为单位计量的对象只能是微观粒子,而不是宏观物质。如可以说1molH2O、0.5mole-;但不可以说1mol人、2mol树等注意:实例:日常生活中我们常用一个词”打”,一打代表12宏
观
上1打啤酒-----12瓶1打袜子-----12双
1打信封-----12个微
观
上1摩O-----1摩O2-----
1摩OH-----6.02×1023O原子6.02×1023O2分子6.02×1023OH-离子------24只-----2×6.02×1023O原子
朗读下列表示,找出其中关键词 1mol 12C含有6.02×1023个12C
1mol H2O含有6.02×1023个H2O
1mol NO3-含有6.02×1023个NO3-
1mol e-含有6.02×1023个e-1 mol任何微粒含有对应微粒数目都相等,且都等于6.02×1023个错:1mol任何物质都含有6.02×1023 个原子正:1mol任何原子都含有6.02×1023 个原子BBBD4 3. 物质的量(n)、阿伏加德罗常数(NA)、粒子数(N)之间的关系为:物质的量=粒子数阿伏加德罗常数n=NNA N=n×NA由于NA是常数,N2N1n1n2 =例题11 mol H2O 中含有多少摩尔氢原子?多少摩尔氧原子?共有多少摩尔的原子? 关系式 : H2O ~ 2H ~ O~ 3原子 微粒数 1个 2 个 1个 3个扩大NA 倍 NA 2NA NA 3NA物质的量 1mol 2mol 1mol 3mol练习1Na2CO3- 2Na+- CO32-- C - 3O
1个 2个 1个 1个 3个 1mol 2mol 1mol 1mol 3mol NA个 2 NA个 NA个 NA个 3 NA个练习2H3PO4- 3H - P - 4O
1个 3个 1个 4个 1mol 3mol 1mol 4mol NA个 3 NA个 NA个 4 NA个在0.5molO2中含有的电子数目是多少?
解:O2的电子数为N(e- )= n(O)×8×NA = 4.816 × 1024 答: 0.5molO2的电子数为4.816 × 1024个。[例题2]=0.5 mol×2×8×6.02×1023mol-1练习3 CH4- C - 4H -质子数-电子数
1个 1个 4个 1mol 1mol 4mol 10mol 10mol NH3- N - 3H -质子数-电子数
1个 1个 3个 1mol 1mol 3mol 10mol 10mol10个 10个10个 10个练习4 NH4+- N - 4H -质子数-电子数
1个 1个 4个 1mol 1mol 4mol 11mol 10mol OH-- O - H -质子数-电子数 1mol 1mol 1mol 9mol 10mol11个 10个4.物质的量与化学方程式计量数的关系 关系式 : 2H2+O2 = 2 H2O 微粒数 2个 1 个 2个 扩大NA 倍 2NA NA 2NA物质的量 2mol 1mol 2mol 结论:化学方程式前系数比=各物质的物质的量之比n(难见、难称量)微观粒子宏观物质(可见、可称量)物质的量个克g摩尔mol阿伏加德罗常数NA=6.02×1023mol-物质的量是联系微观与宏观的桥梁意义生平简介
意大利化学家1776年8月9日生于都灵市一个律师家庭,1856年7月9日卒于都灵市。1792年进都灵大学法律系学习,取得法学博士学位后,曾开业当律师。1800年弃法从理,十分勤奋,1820年被聘任都灵大学理科教授。自 18年被选为都灵科学院院士后,还担任过意大利教育委员和度量衡学会会长.
阿伏加德罗阿伏伽德罗的贡献与成就 阿伏伽德罗分子学说:
(1)许多气体分子是由两个原子组成的,如氧气、氮气,它们决非是单原子的。(2)在同温、同压下,同体积的气体有同数个分子。
同温同压下同体积气体有同数个分子数,这已成为阿伏加德罗定律。
1摩尔物质所含的分子数为6.02×1023,被命名为阿佛加德罗常数。它是自然科学中的基本常数之一。
求: 0.012kg 12C中所含的碳原子数?解:碳原子数=0.012kg1.993 × 10-23kg ≈ 6.02×1023 0.012Kg12C中所含C原子数1mol任何微粒的粒子数阿伏加德罗 常数的值= 6.02×1023=近似为二、阿伏加德罗常数的含义1摩尔(mol)(1)使用“mol”单位时,应用化学式指明粒子的种类。如0.5molNa+、2molH2、1molCa。(2)以mol为单位计量的对象只能是微观粒子,而不是宏观物质。如可以说1molH2O、0.5mole-;但不可以说1mol人、2mol树等注意:实例:日常生活中我们常用一个词”打”,一打代表12宏
观
上1打啤酒-----12瓶1打袜子-----12双
1打信封-----12个微
观
上1摩O-----1摩O2-----
1摩OH-----6.02×1023O原子6.02×1023O2分子6.02×1023OH-离子------24只-----2×6.02×1023O原子
朗读下列表示,找出其中关键词 1mol 12C含有6.02×1023个12C
1mol H2O含有6.02×1023个H2O
1mol NO3-含有6.02×1023个NO3-
1mol e-含有6.02×1023个e-1 mol任何微粒含有对应微粒数目都相等,且都等于6.02×1023个错:1mol任何物质都含有6.02×1023 个原子正:1mol任何原子都含有6.02×1023 个原子BBBD4 3. 物质的量(n)、阿伏加德罗常数(NA)、粒子数(N)之间的关系为:物质的量=粒子数阿伏加德罗常数n=NNA N=n×NA由于NA是常数,N2N1n1n2 =例题11 mol H2O 中含有多少摩尔氢原子?多少摩尔氧原子?共有多少摩尔的原子? 关系式 : H2O ~ 2H ~ O~ 3原子 微粒数 1个 2 个 1个 3个扩大NA 倍 NA 2NA NA 3NA物质的量 1mol 2mol 1mol 3mol练习1Na2CO3- 2Na+- CO32-- C - 3O
1个 2个 1个 1个 3个 1mol 2mol 1mol 1mol 3mol NA个 2 NA个 NA个 NA个 3 NA个练习2H3PO4- 3H - P - 4O
1个 3个 1个 4个 1mol 3mol 1mol 4mol NA个 3 NA个 NA个 4 NA个在0.5molO2中含有的电子数目是多少?
解:O2的电子数为N(e- )= n(O)×8×NA = 4.816 × 1024 答: 0.5molO2的电子数为4.816 × 1024个。[例题2]=0.5 mol×2×8×6.02×1023mol-1练习3 CH4- C - 4H -质子数-电子数
1个 1个 4个 1mol 1mol 4mol 10mol 10mol NH3- N - 3H -质子数-电子数
1个 1个 3个 1mol 1mol 3mol 10mol 10mol10个 10个10个 10个练习4 NH4+- N - 4H -质子数-电子数
1个 1个 4个 1mol 1mol 4mol 11mol 10mol OH-- O - H -质子数-电子数 1mol 1mol 1mol 9mol 10mol11个 10个4.物质的量与化学方程式计量数的关系 关系式 : 2H2+O2 = 2 H2O 微粒数 2个 1 个 2个 扩大NA 倍 2NA NA 2NA物质的量 2mol 1mol 2mol 结论:化学方程式前系数比=各物质的物质的量之比n(难见、难称量)微观粒子宏观物质(可见、可称量)物质的量个克g摩尔mol阿伏加德罗常数NA=6.02×1023mol-物质的量是联系微观与宏观的桥梁意义生平简介
意大利化学家1776年8月9日生于都灵市一个律师家庭,1856年7月9日卒于都灵市。1792年进都灵大学法律系学习,取得法学博士学位后,曾开业当律师。1800年弃法从理,十分勤奋,1820年被聘任都灵大学理科教授。自 18年被选为都灵科学院院士后,还担任过意大利教育委员和度量衡学会会长.
阿伏加德罗阿伏伽德罗的贡献与成就 阿伏伽德罗分子学说:
(1)许多气体分子是由两个原子组成的,如氧气、氮气,它们决非是单原子的。(2)在同温、同压下,同体积的气体有同数个分子。
同温同压下同体积气体有同数个分子数,这已成为阿伏加德罗定律。
1摩尔物质所含的分子数为6.02×1023,被命名为阿佛加德罗常数。它是自然科学中的基本常数之一。
