海水晒盐第1课时
图片预览






文档简介
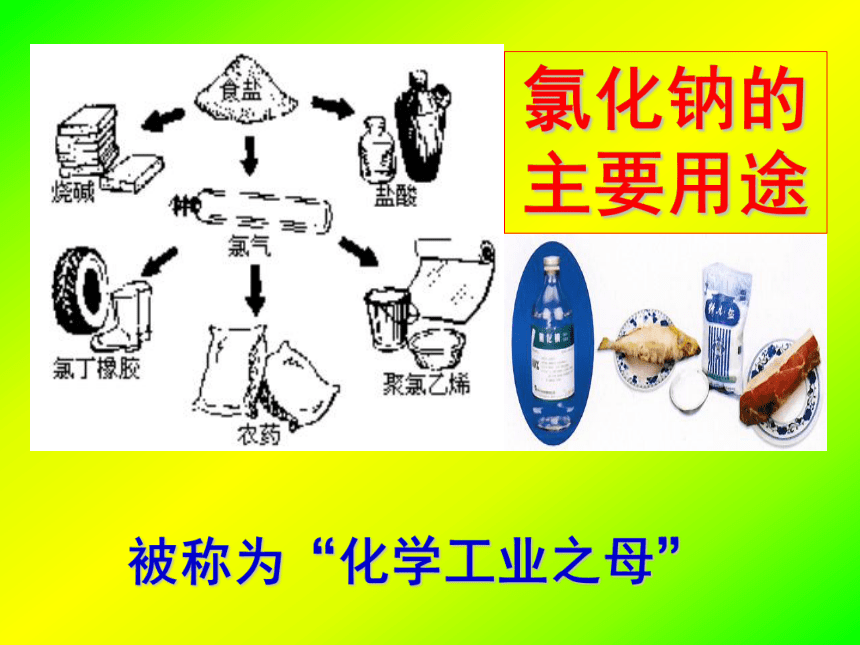
课件19张PPT。播放《闪闪的红星》潘冬子送盐片段交流:从影片中,你得到了哪些化学信息?氯化钠的主要用途 被称为“化学工业之母”鲁教版九年级化学第二单元海水“晒盐”淄川实验中学 王立群知识与技能:
1、知道蒸发结晶是海水晒盐的基本原理;知道蒸发结晶是结晶的一种途径。、
2、理解“饱和溶液”、“不饱和溶液”的概念,会判断溶液是否饱和。
3、理解饱和溶液与不饱和溶液的转化条件。
过程与方法:通过探索实验,培养学生观察能力和分析推理能力。
情感态度:通过学生分组实验,培养从现象到本质的认识事物的科学方法。 教学目标:
教学重点:
1、“饱和溶液”、“不饱和溶液”的概念。
2、海水晒盐的基本原理-蒸发结晶的理解
教学难点:
饱和溶液与不饱和溶液的转化条件。(1)用NaCl和KNO3做溶解实验,探究 “在一定量的水中,食盐能否无限溶解”?
(2)学生说实验现象,引出饱和溶液和不饱和溶液的定义。
探究一:固体在水中能否无限制地溶解?探究二:如何判断一种溶液是饱和溶液?(1)一般地,只要看在一定温度下,是否有不能继续溶解的剩余物质存在.
(2)在一定温度下,溶质从溶液里析出后的剩余溶液,一定是饱和溶液。
(3)往溶液中加入该物质,看是否溶解1、要想让刚才的饱和溶液中剩余的固体溶解,你们有什么好主意?
2、如何把不饱和溶液转化为饱和溶液?
探究三:饱和溶液和不饱和的相互转化
饱和溶液 不饱和溶液升温 加溶剂降温 加溶质 蒸发溶剂饱和溶液:在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液,就是该溶质的饱和溶液。
不饱和溶液:在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液,就是该溶质的不饱和溶液。完善概念:探究四:提取海水中的食盐(1)海水是饱和溶液还是不饱和溶液,如何检验?
(2)实验:提取海水中的食盐?小组交流:你对 “海水晒盐”的了解。结晶:固体物质从它的饱和溶液中以晶体的形式析出的过程叫做结晶。思考:结晶可以用什么方法?冰糖硫酸铜晶体明矾晶体古代盐民在海边煮盐思考交流:(1)“盐田法”晒盐与你制得的食盐的方法有什么不同?成分上有什么区别?
(2)你认为哪些自然条件有利于海水“晒盐”?课外延伸:(1)母液直接排掉,好吗?
(2)怎样对母液进一步加工,如何利用呢?谈收获:
本节课你学会了什么新知识,还有什么疑惑的地方?巩固应用:1.在一定温度下,某物质的饱和溶液一定是( )
A、浓溶液 B、稀溶液 C、不能继续溶解该物质的溶液 D、还能继续溶解该物质的溶液
2.对于多数固体溶质的不饱和溶液,要使之成为饱和溶液,可采用的方法有( )
①降低温度;②升高温度;③加同种溶质;④加溶剂;⑤恒温蒸发溶剂。
A.①③⑤ B.②③④ C.①②③ D.②③⑤
3.向一杯接近饱和的KN03溶液中,逐渐加入KN03晶体,下图符合溶液中溶质的质量变化规律的是( )
作业:小论文《我理想中的“晒盐”场》再 见敬 谢 指 导!
1、知道蒸发结晶是海水晒盐的基本原理;知道蒸发结晶是结晶的一种途径。、
2、理解“饱和溶液”、“不饱和溶液”的概念,会判断溶液是否饱和。
3、理解饱和溶液与不饱和溶液的转化条件。
过程与方法:通过探索实验,培养学生观察能力和分析推理能力。
情感态度:通过学生分组实验,培养从现象到本质的认识事物的科学方法。 教学目标:
教学重点:
1、“饱和溶液”、“不饱和溶液”的概念。
2、海水晒盐的基本原理-蒸发结晶的理解
教学难点:
饱和溶液与不饱和溶液的转化条件。(1)用NaCl和KNO3做溶解实验,探究 “在一定量的水中,食盐能否无限溶解”?
(2)学生说实验现象,引出饱和溶液和不饱和溶液的定义。
探究一:固体在水中能否无限制地溶解?探究二:如何判断一种溶液是饱和溶液?(1)一般地,只要看在一定温度下,是否有不能继续溶解的剩余物质存在.
(2)在一定温度下,溶质从溶液里析出后的剩余溶液,一定是饱和溶液。
(3)往溶液中加入该物质,看是否溶解1、要想让刚才的饱和溶液中剩余的固体溶解,你们有什么好主意?
2、如何把不饱和溶液转化为饱和溶液?
探究三:饱和溶液和不饱和的相互转化
饱和溶液 不饱和溶液升温 加溶剂降温 加溶质 蒸发溶剂饱和溶液:在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液,就是该溶质的饱和溶液。
不饱和溶液:在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液,就是该溶质的不饱和溶液。完善概念:探究四:提取海水中的食盐(1)海水是饱和溶液还是不饱和溶液,如何检验?
(2)实验:提取海水中的食盐?小组交流:你对 “海水晒盐”的了解。结晶:固体物质从它的饱和溶液中以晶体的形式析出的过程叫做结晶。思考:结晶可以用什么方法?冰糖硫酸铜晶体明矾晶体古代盐民在海边煮盐思考交流:(1)“盐田法”晒盐与你制得的食盐的方法有什么不同?成分上有什么区别?
(2)你认为哪些自然条件有利于海水“晒盐”?课外延伸:(1)母液直接排掉,好吗?
(2)怎样对母液进一步加工,如何利用呢?谈收获:
本节课你学会了什么新知识,还有什么疑惑的地方?巩固应用:1.在一定温度下,某物质的饱和溶液一定是( )
A、浓溶液 B、稀溶液 C、不能继续溶解该物质的溶液 D、还能继续溶解该物质的溶液
2.对于多数固体溶质的不饱和溶液,要使之成为饱和溶液,可采用的方法有( )
①降低温度;②升高温度;③加同种溶质;④加溶剂;⑤恒温蒸发溶剂。
A.①③⑤ B.②③④ C.①②③ D.②③⑤
3.向一杯接近饱和的KN03溶液中,逐渐加入KN03晶体,下图符合溶液中溶质的质量变化规律的是( )
作业:小论文《我理想中的“晒盐”场》再 见敬 谢 指 导!
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
