质量守恒定律
图片预览







文档简介
课件48张PPT。质量守恒定律参加化学反应的各物质的质量总和
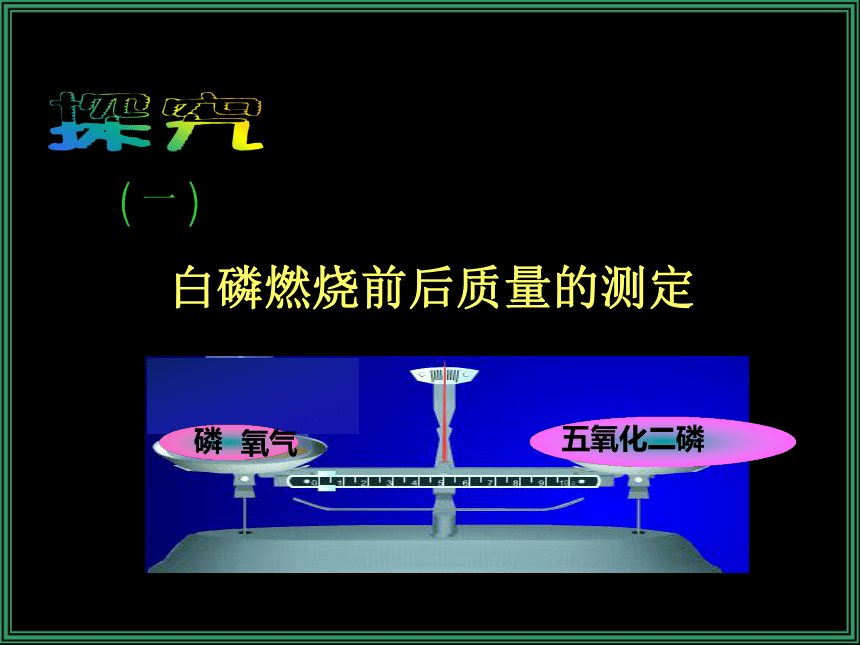
反应后生成的各物质的质量总和你的猜想呢?小明小林白磷燃烧前后质量的测定氧气实验现象 白磷燃烧,放出大量白烟;
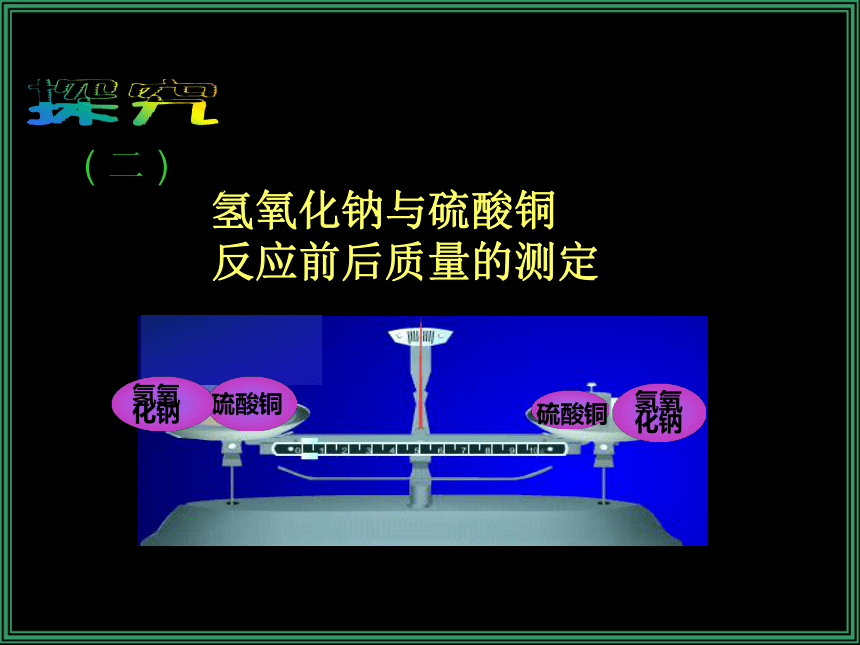
气球先胀大后缩小氢氧化钠与硫酸铜
反应前后质量的测定实验现象溶液由蓝色变为浅绿色
铁钉表面析出一层红色物质实验结论参加化学反应的各物质的质量总和
反应后生成的各物质的质量总和
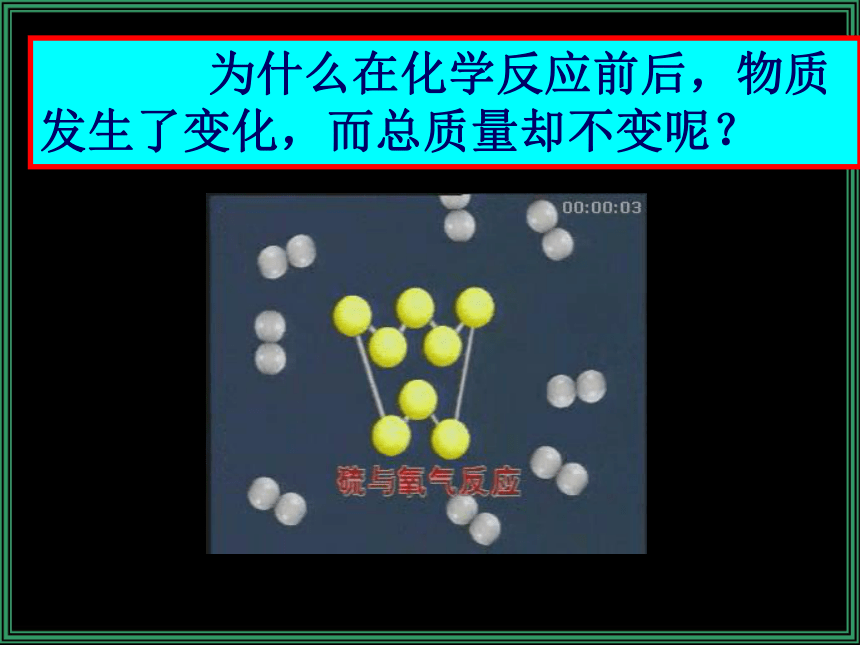
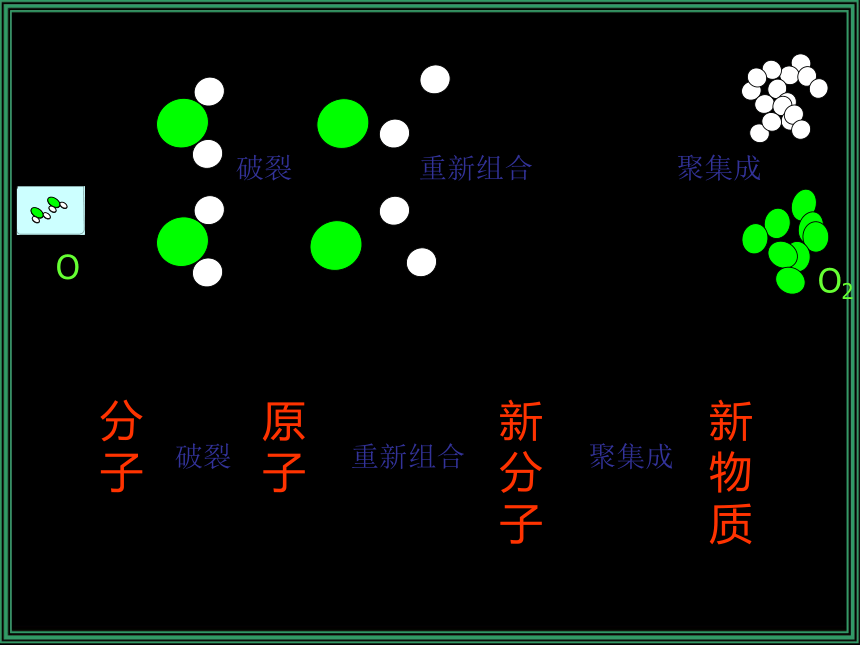
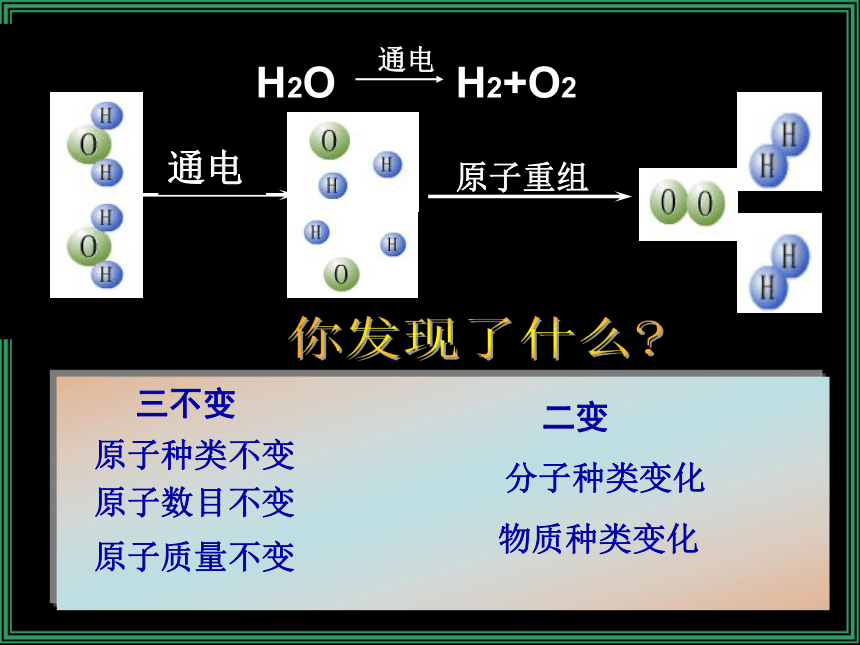
?=一、质量守恒定律(见书P57) 参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。适用范围:化学变化。 为什么在化学反应前后,物质发生了变化,而总质量却不变呢? 分 子原 子新物质新分子H2O2H2O4个2个6个4个2个6个 三不变分子种类变化
原子种类不变原子数目不变原子质量不变 二变物质种类变化
你发现了什么?原子数目原子质量原子种类元素质量元素种类物质的种类分子的种类可能
改变分子数目物质的总质量二、质量守恒的原因:元 素不 变。(宏 观)种类 质量 物质总质量②原子数目没有增减①原子种类没有改变③原子质量没有变化 ①进行有关的计算②解释现象注意点 ①化学反应
③重点词语
②一切化学变化都遵循
原理运用小结小结3、在A+B→C+D的反应中,5克A和
一定的B恰好完全反应,生成3克C
和10克D,则B的质量是( )
(A)18克 (B)7克 (C)8克 (D)6克
C⑷参加化学反应的各物质的质量总和,等于
反应后生成的各物质的质量总和。( )⑶在化学反应中,对有气体生成的反应,反
应前后的原子种类不一定相同。 ( )⑵参加化学反应的各物质的分子个数与反应
后各生成物的分子个数相等。 ( )
⑴反应前各物质的质量总和,一定等于反应
后生成的各物质的质量总和。 ( )×××√判断题1、现有一反应A+B→C+D,有10gA和5gB反应,反应结束后还剩余3gA,B无剩余,生成4g的C,则生成D的质量为 。 2、根据质量守恒定律,2L氢气和1L氧气反应能生成3L水,这句话对吗? 8g不对 3.化学反应前后:①物质的化学性质 ② 原子的种类 ③元素的种类 ④分子的数目 ⑤反应物质量总和与生成物质量总和. 其中一定不发生变化的是 ( )
A. ①②③④⑤ B. ①②③⑤
C. ②③⑤ D. ①③④ C4.下列叙述符合质量守恒定律的是 ( )
A.5g酒精与5g水混合得到10g酒精溶液
B.2g氢气与18g 氧气反应生成20g水
C.高锰酸钾加热分解后,试管内固体药品
减少的质量等于生成氧气的质量
D.水蒸发成水蒸气的质量等于水的质量C方案三碳酸钠+盐酸→氯化钠+水+二氧化碳质量减少想一想氢氧化钙+二氧化碳→碳酸钙+水质量增加再想想铁丝燃烧木材的燃烧用质量守恒定律解释 蜡烛燃烧后什么
也没有留下,难道物
质从世上消失了吗?
思考蜡烛燃烧时生成了水和二氧化碳,
根据质量守恒定律,参加反应的
蜡烛和氧气的质量总和一定等于
生成的水蒸气和二氧化碳的质量
由于水蒸气和二氧化碳以气体形式逸出,所以蜡烛质量变小讨论质量守恒定律时,各状态的物质均要讨论 蜡烛在空气中燃烧后,生成二氧化碳和水,试推断蜡烛中一定含有_____元素,可能含有___元素。三、质量守恒的应用
1、推断物质的组成元素碳 氢氧“水变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?廣而告之中世纪,我国乃至世界上普遍流行着一种炼丹术,一些巫师,术士们认为可以用硫磺(S),硝酸钾(KNO3),木炭(C)等物质通过一定的方法炼出金(AU)来,达到点石成金的效果,这种说法对吗?为什么? 环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式为:I2O5 + 5CO =I2 + 5X,根据生成X的多少,可以判断CO的含量,则X的化学式为 。 CO22、推断物质的化学式练习我国新一代气象卫星风云三号于2008年5月27日成功发射,运载火箭的主要燃料是,用R表示,化学方程式为R﹢2N2O4=3N2﹢4H2O﹢2CO2则偏三甲肼的化学式是
A C2H8N2 B N2H4 C CH 4 D C6H7N再见
请同学们完成作业本及方指中的相应作业化学方程式怎样用一个式子来表示化学反应呢?氢气 +氧气 → 水该式子确实能表示反应物、生成物及反应条件;但书写不方便、国际上也不通用且不能体现质量守恒定律。点燃思考:如:氢气在氧气中燃烧生成水化学方程式用化学式来表示化学反应的式子。
化学方程式包含哪些意义?表示反应在什么条件下进行表示各物质之间原子和分子的个数比表示什么物质参加反应,结果生成了什么物质表示反应物、生成物各物质间的质量比讨论:化学方程式的意义1宏观意义:
表示反应物,生成物和反应条件
表示碳和氧气发生反应,生成二氧化碳
表示反应在点燃条件下进行
2微观意义:
表示参加反应的各物质间的粒子数量关系 即粒子个数比
粒子个数比即化学式前面的化学计量数之比
表示反应物碳原子,氧分子和生成物二氧化碳分子的粒子个数比为1:1:1
3质量意义: 表示各物质之间的质量关系,即各物质之间的质量比
质量比=相对分子质量与化学计量数乘积之比
化学方程式的涵义4P + 5O2 2P2O5
4×31 5×32 2×142 点燃1、表示磷和氧气参加反应,结果生成五氧化二磷。3、表示反应物中磷原子、氧分子和生成物中五 氧化二磷分子的个数比为4∶5∶2。4、表示每124份质量的磷与160份质量的氧气反应 生成284份质量的五氧化二磷。 质量比为 31∶40∶712、表示反应在点燃条件下进行你能说!化学方程式的读法:1宏观读法: 碳和氧气在点燃条件下反应生成二氧化碳
2微观读法:
每一个碳原子和一个氧气分子在点燃条件下反应生成一个二氧化碳分子
3质量读法:
每12份质量碳和32份质量氧气在点燃条件下反应生成 44份质量二氧化碳
:考考你 化学方程式2H2+O2 2H2O表示
A 氢气加氧气等于水
B 氢气跟氧气混合可生成水
C 在点燃条件下,每4份质量的氢气与32份质量的氧气反应生成36份的水
D 2分子氢气与1分子氧气反应,生成2分子水
C点燃 4Al+3O2 2Al2O3反应中铝,氧气,三氧化二铝的质量比是
A 27:32:102
B 27:16:43
C 4:3:2
D 9:8:17
D点燃化学方程式:用化学式来表示化学反应的式子。遵循原则: 1、以客观事实为依据 2、遵守质量守恒定律(反应前后原子数目相等) 试一试:
看看谁最先写出氢气在氧气中燃烧生成水
化学方程式?
1、根据实验事实写出反应物和生成物的化学式P + O2 —— P2O54P + 5O2 —— 2P2O54P + 5O2 ==== 2P2O5点燃 2、配平化学方程式(使反应前后各原子数目相 等) 3、注明:反应条件(点燃、加热“△”、高温、通 电、催化剂)、生成物状态(气体↑或沉淀↓)化学方程式书写步骤(以磷在氧气中燃烧为例) 4. 改横线为等号加热:对物质的升温,常用 符号代替点燃:达到可燃物的着火点高温:达到一定的温度(>600℃)只有在反应物中没有气体参加生成物中的气体才能用气体符号在溶液中只有在反应物中没有固体参加生成物中的固体才能用沉淀符号催化剂(具体名称)4指出下列化学方程式的错误之处
C + O2 ==== CO2
KClO3 ====== KCl + O2
H2O ===== H2 + O
3Fe +2 O2 ==== Fe3O4
Mg + O2 ==== MgO2
点燃通电加热燃烧MnO2点燃你能解决这些问题吗?最小公倍数法首先找出其中出现次数较多,且原子个数相差较多的原子作为配平起点,求出其最小公倍数,再由最小公倍数确定相关化学式的化学计量数,配平化学方程式
Fe + O2 —— Fe3O4
Mg + O2 —— MgO
H2O —— H2 + O2你能配平吗?P99练习练习:配平下列化学方程式并注明反应发生的条件:
反应后生成的各物质的质量总和你的猜想呢?小明小林白磷燃烧前后质量的测定氧气实验现象 白磷燃烧,放出大量白烟;
气球先胀大后缩小氢氧化钠与硫酸铜
反应前后质量的测定实验现象溶液由蓝色变为浅绿色
铁钉表面析出一层红色物质实验结论参加化学反应的各物质的质量总和
反应后生成的各物质的质量总和
?=一、质量守恒定律(见书P57) 参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。适用范围:化学变化。 为什么在化学反应前后,物质发生了变化,而总质量却不变呢? 分 子原 子新物质新分子H2O2H2O4个2个6个4个2个6个 三不变分子种类变化
原子种类不变原子数目不变原子质量不变 二变物质种类变化
你发现了什么?原子数目原子质量原子种类元素质量元素种类物质的种类分子的种类可能
改变分子数目物质的总质量二、质量守恒的原因:元 素不 变。(宏 观)种类 质量 物质总质量②原子数目没有增减①原子种类没有改变③原子质量没有变化 ①进行有关的计算②解释现象注意点 ①化学反应
③重点词语
②一切化学变化都遵循
原理运用小结小结3、在A+B→C+D的反应中,5克A和
一定的B恰好完全反应,生成3克C
和10克D,则B的质量是( )
(A)18克 (B)7克 (C)8克 (D)6克
C⑷参加化学反应的各物质的质量总和,等于
反应后生成的各物质的质量总和。( )⑶在化学反应中,对有气体生成的反应,反
应前后的原子种类不一定相同。 ( )⑵参加化学反应的各物质的分子个数与反应
后各生成物的分子个数相等。 ( )
⑴反应前各物质的质量总和,一定等于反应
后生成的各物质的质量总和。 ( )×××√判断题1、现有一反应A+B→C+D,有10gA和5gB反应,反应结束后还剩余3gA,B无剩余,生成4g的C,则生成D的质量为 。 2、根据质量守恒定律,2L氢气和1L氧气反应能生成3L水,这句话对吗? 8g不对 3.化学反应前后:①物质的化学性质 ② 原子的种类 ③元素的种类 ④分子的数目 ⑤反应物质量总和与生成物质量总和. 其中一定不发生变化的是 ( )
A. ①②③④⑤ B. ①②③⑤
C. ②③⑤ D. ①③④ C4.下列叙述符合质量守恒定律的是 ( )
A.5g酒精与5g水混合得到10g酒精溶液
B.2g氢气与18g 氧气反应生成20g水
C.高锰酸钾加热分解后,试管内固体药品
减少的质量等于生成氧气的质量
D.水蒸发成水蒸气的质量等于水的质量C方案三碳酸钠+盐酸→氯化钠+水+二氧化碳质量减少想一想氢氧化钙+二氧化碳→碳酸钙+水质量增加再想想铁丝燃烧木材的燃烧用质量守恒定律解释 蜡烛燃烧后什么
也没有留下,难道物
质从世上消失了吗?
思考蜡烛燃烧时生成了水和二氧化碳,
根据质量守恒定律,参加反应的
蜡烛和氧气的质量总和一定等于
生成的水蒸气和二氧化碳的质量
由于水蒸气和二氧化碳以气体形式逸出,所以蜡烛质量变小讨论质量守恒定律时,各状态的物质均要讨论 蜡烛在空气中燃烧后,生成二氧化碳和水,试推断蜡烛中一定含有_____元素,可能含有___元素。三、质量守恒的应用
1、推断物质的组成元素碳 氢氧“水变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?廣而告之中世纪,我国乃至世界上普遍流行着一种炼丹术,一些巫师,术士们认为可以用硫磺(S),硝酸钾(KNO3),木炭(C)等物质通过一定的方法炼出金(AU)来,达到点石成金的效果,这种说法对吗?为什么? 环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式为:I2O5 + 5CO =I2 + 5X,根据生成X的多少,可以判断CO的含量,则X的化学式为 。 CO22、推断物质的化学式练习我国新一代气象卫星风云三号于2008年5月27日成功发射,运载火箭的主要燃料是,用R表示,化学方程式为R﹢2N2O4=3N2﹢4H2O﹢2CO2则偏三甲肼的化学式是
A C2H8N2 B N2H4 C CH 4 D C6H7N再见
请同学们完成作业本及方指中的相应作业化学方程式怎样用一个式子来表示化学反应呢?氢气 +氧气 → 水该式子确实能表示反应物、生成物及反应条件;但书写不方便、国际上也不通用且不能体现质量守恒定律。点燃思考:如:氢气在氧气中燃烧生成水化学方程式用化学式来表示化学反应的式子。
化学方程式包含哪些意义?表示反应在什么条件下进行表示各物质之间原子和分子的个数比表示什么物质参加反应,结果生成了什么物质表示反应物、生成物各物质间的质量比讨论:化学方程式的意义1宏观意义:
表示反应物,生成物和反应条件
表示碳和氧气发生反应,生成二氧化碳
表示反应在点燃条件下进行
2微观意义:
表示参加反应的各物质间的粒子数量关系 即粒子个数比
粒子个数比即化学式前面的化学计量数之比
表示反应物碳原子,氧分子和生成物二氧化碳分子的粒子个数比为1:1:1
3质量意义: 表示各物质之间的质量关系,即各物质之间的质量比
质量比=相对分子质量与化学计量数乘积之比
化学方程式的涵义4P + 5O2 2P2O5
4×31 5×32 2×142 点燃1、表示磷和氧气参加反应,结果生成五氧化二磷。3、表示反应物中磷原子、氧分子和生成物中五 氧化二磷分子的个数比为4∶5∶2。4、表示每124份质量的磷与160份质量的氧气反应 生成284份质量的五氧化二磷。 质量比为 31∶40∶712、表示反应在点燃条件下进行你能说!化学方程式的读法:1宏观读法: 碳和氧气在点燃条件下反应生成二氧化碳
2微观读法:
每一个碳原子和一个氧气分子在点燃条件下反应生成一个二氧化碳分子
3质量读法:
每12份质量碳和32份质量氧气在点燃条件下反应生成 44份质量二氧化碳
:考考你 化学方程式2H2+O2 2H2O表示
A 氢气加氧气等于水
B 氢气跟氧气混合可生成水
C 在点燃条件下,每4份质量的氢气与32份质量的氧气反应生成36份的水
D 2分子氢气与1分子氧气反应,生成2分子水
C点燃 4Al+3O2 2Al2O3反应中铝,氧气,三氧化二铝的质量比是
A 27:32:102
B 27:16:43
C 4:3:2
D 9:8:17
D点燃化学方程式:用化学式来表示化学反应的式子。遵循原则: 1、以客观事实为依据 2、遵守质量守恒定律(反应前后原子数目相等) 试一试:
看看谁最先写出氢气在氧气中燃烧生成水
化学方程式?
1、根据实验事实写出反应物和生成物的化学式P + O2 —— P2O54P + 5O2 —— 2P2O54P + 5O2 ==== 2P2O5点燃 2、配平化学方程式(使反应前后各原子数目相 等) 3、注明:反应条件(点燃、加热“△”、高温、通 电、催化剂)、生成物状态(气体↑或沉淀↓)化学方程式书写步骤(以磷在氧气中燃烧为例) 4. 改横线为等号加热:对物质的升温,常用 符号代替点燃:达到可燃物的着火点高温:达到一定的温度(>600℃)只有在反应物中没有气体参加生成物中的气体才能用气体符号在溶液中只有在反应物中没有固体参加生成物中的固体才能用沉淀符号催化剂(具体名称)4指出下列化学方程式的错误之处
C + O2 ==== CO2
KClO3 ====== KCl + O2
H2O ===== H2 + O
3Fe +2 O2 ==== Fe3O4
Mg + O2 ==== MgO2
点燃通电加热燃烧MnO2点燃你能解决这些问题吗?最小公倍数法首先找出其中出现次数较多,且原子个数相差较多的原子作为配平起点,求出其最小公倍数,再由最小公倍数确定相关化学式的化学计量数,配平化学方程式
Fe + O2 —— Fe3O4
Mg + O2 —— MgO
H2O —— H2 + O2你能配平吗?P99练习练习:配平下列化学方程式并注明反应发生的条件:
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
