高中化学人教版选修四第二章之影响反应速率的因素课件
文档属性
| 名称 | 高中化学人教版选修四第二章之影响反应速率的因素课件 |

|
|
| 格式 | rar | ||
| 文件大小 | 253.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-11-07 00:00:00 | ||
图片预览







文档简介
课件20张PPT。影响反应速率的因素复习提问:
1.什么叫反应速率?
化学反应进行的快慢程度
2.用什么物理量的变化来描述化学反应速率?
单位时间反应物或生成物物质的量浓度的减少或增加来描述化学反应速率
3.反应速率的单位是什么?
mol/l·h mol/l·min mol/l·s
练习 反应4NH3+5O2=4NO+6H2O 在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率Vx为( )
A.VNO =0. 12mol/(L.min)
B.VH2O=0.18mol/(L.min)
C.VNO=0.002mol/(L.s)
D.VO2=0.0025mol/(L.s)ABCD 影响反应速率的因素(2)外因:(1)内因(主要因素) :参加反应物质的性质 反应物分子中的化学键断裂、生成物分子中的化学键形成过程
——旧键断裂,新键生成——化学反应的本质:①浓度:②压强:③温度:④催化剂:
⑤其他因素:光、颗粒大小、溶剂等。如果分子间能够发生化学反应:
1、反应物分子必须相互碰撞;
2、分子必须具有一定的能量
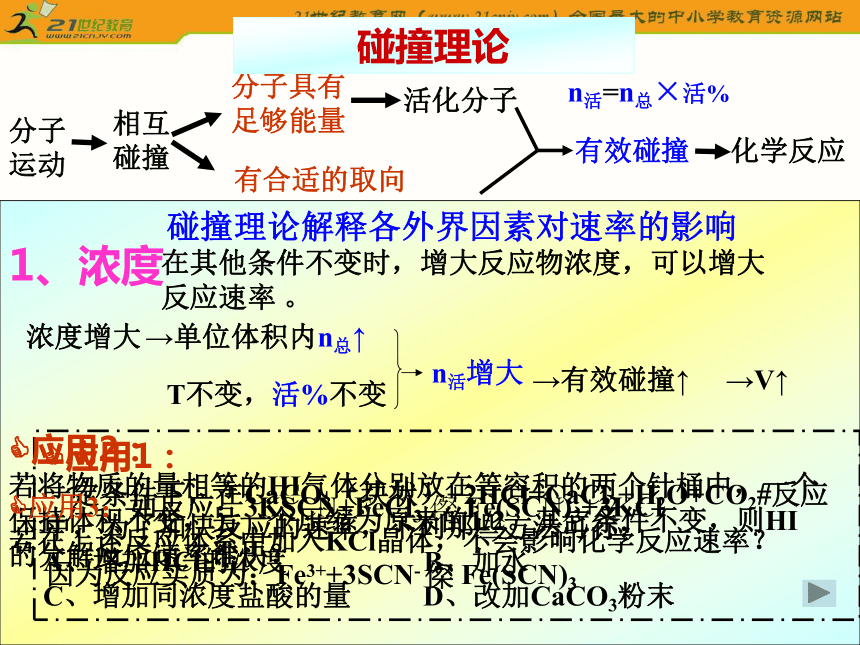
3、活化分子碰撞时,必须有合适的取向反应速率理论本质分子
运动分子具有
足够能量有合适的取向 碰撞理论 1、浓度n活=n总×活%浓度增大→单位体积内n总↑T不变,活%不变→有效碰撞↑→V↑?应用1:
一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2?反应中,为了加快反应的速率,下列那些方法可行:
A、增加HCl的浓度 B、加水
C、增加同浓度盐酸的量 D、改加CaCO3粉末 ?应用2:
若将物质的量相等的HI气体分别放在等容积的两个针桶中,一个保持体积不变,另一个压缩为原来的1/2。其它条件不变,则HI的分解反应速率谁快?
在其他条件不变时,增大反应物浓度,可以增大反应速率 。?应用3:如反应:3KSCN+FeCl3 ? Fe(SCN)3+3KCl
若在上述反应体系中加入KCl晶体,不会影响化学反应速率?因为反应实质为:Fe3++3SCN- ? Fe(SCN)3如果分子间能够发生化学反应:
1、反应物分子必须相互碰撞;
2、分子必须具有一定的能量
3、活化分子碰撞时,必须有合适的取向2、压强压强增大 → 体积减小
其他条件不变→V↑ 压强对于反应速率的影响是通过对浓度的影响实现的
P增大→C成比例增大,P减小→C成比例减小
发散思考:压强对于任意化学反应的速率都有影响吗?压强只对于有气体参加的反应的速率有影响(紧扣对C的影响)其他条件不变,增大压强,气体体积缩小,浓度增大,反应速率加快。 例2、在N2+3H2 ? 2NH3中,当其他外界条件不变时:
?减小体系压强,该反应的速率怎么变?
?在反应中保持体系容积不变,充入N2 ,反应的速率怎么变?
在反应中保持体系容积不变,充入He,反应的速率怎么变?
在反应中保持体系压强不变,充入He,反应的速率怎么变?压强对反应速率的影响例3、对于反应N2+O2=2NO在密闭容器中进行,下列条件哪些不能加快该反应的化学反应速率( )
A、缩小体积使压强增大
B、体积不变充入 N2 使压强增大
C、体积不变充入 O2使压强增大
D、使体积增大到原来的2倍
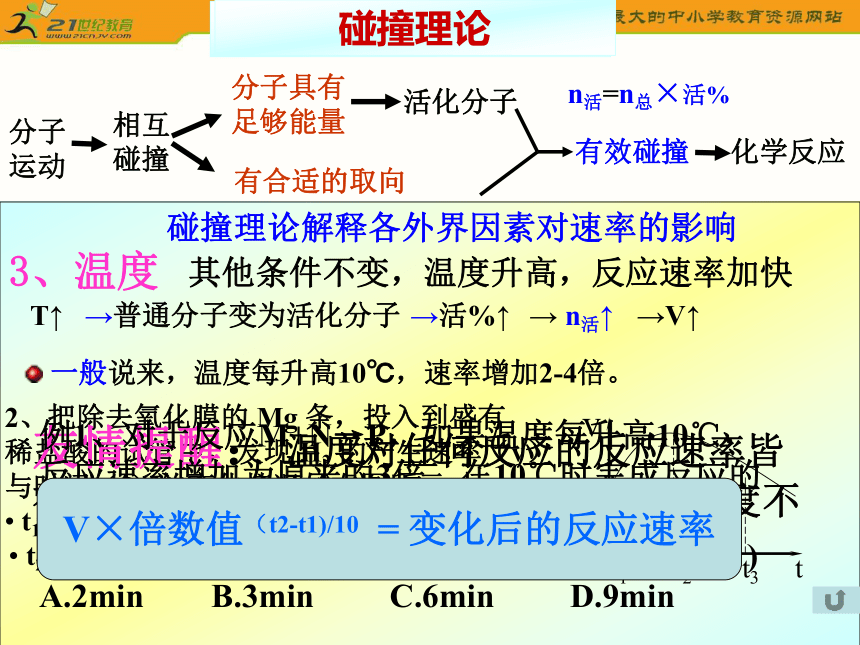
E、体积不变充入氦气使压强增大压强对反应速率的影响DE 一般说来,温度每升高10℃,速率增加2-4倍。T↑→普通分子变为活化分子→活%↑→ n活↑→V↑3、温度其他条件不变,温度升高,反应速率加快友情提醒: 温度对任何反应的反应速率皆有影响,但对于吸热或放热反应影响的程度不同,对吸热反应影响程度较大。
V×倍数值(t2-t1)/10 = 变化后的反应速率正催化剂→降低反应的活化能→V↑4、催化剂——改变反应的途径→活%↑
n总不变钻隧道友情提醒:
?使用催化剂同等程度的增大(减慢)、正逆反应速率,从而改变反应到达平衡所需时间。
?没特别指明一般指正催化剂
?催化剂只能催化可能发生的反应,对不发生的反应无作用
?催化剂一定的具有选择性 解释:
“对可逆反应而言,催化剂既能催化正反应又能催化逆反应”
试利用如图原理加以解释? 取2g干燥Al粉和3g碘粉小心混匀,分四堆,往混合物上分别加0.5g水、1g胆矾、1g无水CuSO4。
首先加水那堆冒火花,发生剧烈反应;
其次是加胆矾的;
最难反应的是加无水CuSO4的那堆。
1)铝和碘反应的方程式:__________________
2)铝和碘反应还可以看到___________________
3)三堆混合物发生反应的先后顺序说明_______催化剂对反应速率的影响小结:影响化学反应速率的因素内因:物质本身的性质
外因:见表。对反应速率的 影响:一般是:
催化剂>温度>浓度。 增大反应物的浓度使反应速率加快的主要原因( )
对于气体参与体系增大压强使反应速率加快的主要原因是( )
升高温度使反应速率加快的主要原因是( )
使用催化剂使反应速率加快的主要原因是( )
A、活化分子百分数不变,但提高单位体积内活化分子的总数
B、 增大分子的运动速率而使有效碰撞增加
C、 升高反应物分子的能量,使活化分子的百分数增加
D、降低反应所需的能量,使活化分子百分数增加AAC D外在条件对反应速率的影响——综合——理论分析类1、将一定浓度的盐酸倒入碳酸钙中,若作如下改变的情况,其中能使最初的化学反应速率增大的是 ( )
A、盐酸的浓度不变,而使盐酸的用量一倍
B、盐酸的浓度增大一倍,而使盐酸的用量减少到原来的一半
C、盐酸的浓度和用量都不变,增加碳酸钙的量
D、盐酸和碳酸钙不变,增大压强一倍
E、加入CaCl2溶液
F、加入CaCl2固体
G、将CaCO3用CaCO3粉末代替BG2、硫代硫酸钠( Na2S2O3)与稀硫酸发生如下反应:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O外在条件对反应速率的影响——综合——实践应用类 下列四种情况中最早出现浑浊的是: ( )
(1)10℃时0.1 mol /L Na2S2O3和0.1 mol /L H2SO4各 5 mL
(2)10℃时0.1 mol /L Na2S2O3和0.1 mol /L H2SO4 各5 mL,加水10mL
(3) 20℃ 时0.1 mol /L Na2S2O3和0.1 mol /L H2SO4各 5 mL
(4) 20℃ 时0.2mol /L Na2S2O3和0.1 mol /L H2SO4各5 mL,加水10 mLC没合适的取向没足够的能量足够的能量
合适的取向类比法:借鉴投篮——获得灵感 +有关“活化分子” 定义:
——具有一定的能量,在碰撞过程中足以令旧化学键断裂,而发生反应(即发生“有效碰撞”)的分子称为活化分子。
特点:
——有比反应物分子平均动能高的能量
图形表示——“爬山坡”
单位体积内活化分子数越多,反应速率越快 解析:本题是一道化学与数学、物理学科间知识渗透试题,它主要考查学生“将化学问题抽象成数学问题,利用数学工具通过计算和推理解决化学问题”的能力。因每升高10℃反应速率增加为原来3倍,如升高的温度为△t,则反应速率增加为原来的3 倍,反应由10℃升至40℃,反应速率增加为原来的3 =33倍,完成反应的10%所需时间为54min/33=2min。 设10℃时反应速度为v,则由题意40℃时反应速率为27v,故 v×54min=27v·t t=2min再见
1.什么叫反应速率?
化学反应进行的快慢程度
2.用什么物理量的变化来描述化学反应速率?
单位时间反应物或生成物物质的量浓度的减少或增加来描述化学反应速率
3.反应速率的单位是什么?
mol/l·h mol/l·min mol/l·s
练习 反应4NH3+5O2=4NO+6H2O 在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率Vx为( )
A.VNO =0. 12mol/(L.min)
B.VH2O=0.18mol/(L.min)
C.VNO=0.002mol/(L.s)
D.VO2=0.0025mol/(L.s)ABCD 影响反应速率的因素(2)外因:(1)内因(主要因素) :参加反应物质的性质 反应物分子中的化学键断裂、生成物分子中的化学键形成过程
——旧键断裂,新键生成——化学反应的本质:①浓度:②压强:③温度:④催化剂:
⑤其他因素:光、颗粒大小、溶剂等。如果分子间能够发生化学反应:
1、反应物分子必须相互碰撞;
2、分子必须具有一定的能量
3、活化分子碰撞时,必须有合适的取向反应速率理论本质分子
运动分子具有
足够能量有合适的取向 碰撞理论 1、浓度n活=n总×活%浓度增大→单位体积内n总↑T不变,活%不变→有效碰撞↑→V↑?应用1:
一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2?反应中,为了加快反应的速率,下列那些方法可行:
A、增加HCl的浓度 B、加水
C、增加同浓度盐酸的量 D、改加CaCO3粉末 ?应用2:
若将物质的量相等的HI气体分别放在等容积的两个针桶中,一个保持体积不变,另一个压缩为原来的1/2。其它条件不变,则HI的分解反应速率谁快?
在其他条件不变时,增大反应物浓度,可以增大反应速率 。?应用3:如反应:3KSCN+FeCl3 ? Fe(SCN)3+3KCl
若在上述反应体系中加入KCl晶体,不会影响化学反应速率?因为反应实质为:Fe3++3SCN- ? Fe(SCN)3如果分子间能够发生化学反应:
1、反应物分子必须相互碰撞;
2、分子必须具有一定的能量
3、活化分子碰撞时,必须有合适的取向2、压强压强增大 → 体积减小
其他条件不变→V↑ 压强对于反应速率的影响是通过对浓度的影响实现的
P增大→C成比例增大,P减小→C成比例减小
发散思考:压强对于任意化学反应的速率都有影响吗?压强只对于有气体参加的反应的速率有影响(紧扣对C的影响)其他条件不变,增大压强,气体体积缩小,浓度增大,反应速率加快。 例2、在N2+3H2 ? 2NH3中,当其他外界条件不变时:
?减小体系压强,该反应的速率怎么变?
?在反应中保持体系容积不变,充入N2 ,反应的速率怎么变?
在反应中保持体系容积不变,充入He,反应的速率怎么变?
在反应中保持体系压强不变,充入He,反应的速率怎么变?压强对反应速率的影响例3、对于反应N2+O2=2NO在密闭容器中进行,下列条件哪些不能加快该反应的化学反应速率( )
A、缩小体积使压强增大
B、体积不变充入 N2 使压强增大
C、体积不变充入 O2使压强增大
D、使体积增大到原来的2倍
E、体积不变充入氦气使压强增大压强对反应速率的影响DE 一般说来,温度每升高10℃,速率增加2-4倍。T↑→普通分子变为活化分子→活%↑→ n活↑→V↑3、温度其他条件不变,温度升高,反应速率加快友情提醒: 温度对任何反应的反应速率皆有影响,但对于吸热或放热反应影响的程度不同,对吸热反应影响程度较大。
V×倍数值(t2-t1)/10 = 变化后的反应速率正催化剂→降低反应的活化能→V↑4、催化剂——改变反应的途径→活%↑
n总不变钻隧道友情提醒:
?使用催化剂同等程度的增大(减慢)、正逆反应速率,从而改变反应到达平衡所需时间。
?没特别指明一般指正催化剂
?催化剂只能催化可能发生的反应,对不发生的反应无作用
?催化剂一定的具有选择性 解释:
“对可逆反应而言,催化剂既能催化正反应又能催化逆反应”
试利用如图原理加以解释? 取2g干燥Al粉和3g碘粉小心混匀,分四堆,往混合物上分别加0.5g水、1g胆矾、1g无水CuSO4。
首先加水那堆冒火花,发生剧烈反应;
其次是加胆矾的;
最难反应的是加无水CuSO4的那堆。
1)铝和碘反应的方程式:__________________
2)铝和碘反应还可以看到___________________
3)三堆混合物发生反应的先后顺序说明_______催化剂对反应速率的影响小结:影响化学反应速率的因素内因:物质本身的性质
外因:见表。对反应速率的 影响:一般是:
催化剂>温度>浓度。 增大反应物的浓度使反应速率加快的主要原因( )
对于气体参与体系增大压强使反应速率加快的主要原因是( )
升高温度使反应速率加快的主要原因是( )
使用催化剂使反应速率加快的主要原因是( )
A、活化分子百分数不变,但提高单位体积内活化分子的总数
B、 增大分子的运动速率而使有效碰撞增加
C、 升高反应物分子的能量,使活化分子的百分数增加
D、降低反应所需的能量,使活化分子百分数增加AAC D外在条件对反应速率的影响——综合——理论分析类1、将一定浓度的盐酸倒入碳酸钙中,若作如下改变的情况,其中能使最初的化学反应速率增大的是 ( )
A、盐酸的浓度不变,而使盐酸的用量一倍
B、盐酸的浓度增大一倍,而使盐酸的用量减少到原来的一半
C、盐酸的浓度和用量都不变,增加碳酸钙的量
D、盐酸和碳酸钙不变,增大压强一倍
E、加入CaCl2溶液
F、加入CaCl2固体
G、将CaCO3用CaCO3粉末代替BG2、硫代硫酸钠( Na2S2O3)与稀硫酸发生如下反应:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O外在条件对反应速率的影响——综合——实践应用类 下列四种情况中最早出现浑浊的是: ( )
(1)10℃时0.1 mol /L Na2S2O3和0.1 mol /L H2SO4各 5 mL
(2)10℃时0.1 mol /L Na2S2O3和0.1 mol /L H2SO4 各5 mL,加水10mL
(3) 20℃ 时0.1 mol /L Na2S2O3和0.1 mol /L H2SO4各 5 mL
(4) 20℃ 时0.2mol /L Na2S2O3和0.1 mol /L H2SO4各5 mL,加水10 mLC没合适的取向没足够的能量足够的能量
合适的取向类比法:借鉴投篮——获得灵感 +有关“活化分子” 定义:
——具有一定的能量,在碰撞过程中足以令旧化学键断裂,而发生反应(即发生“有效碰撞”)的分子称为活化分子。
特点:
——有比反应物分子平均动能高的能量
图形表示——“爬山坡”
单位体积内活化分子数越多,反应速率越快 解析:本题是一道化学与数学、物理学科间知识渗透试题,它主要考查学生“将化学问题抽象成数学问题,利用数学工具通过计算和推理解决化学问题”的能力。因每升高10℃反应速率增加为原来3倍,如升高的温度为△t,则反应速率增加为原来的3 倍,反应由10℃升至40℃,反应速率增加为原来的3 =33倍,完成反应的10%所需时间为54min/33=2min。 设10℃时反应速度为v,则由题意40℃时反应速率为27v,故 v×54min=27v·t t=2min再见
