必修1化学第三章单元测试:金属及其化合物1
文档属性
| 名称 | 必修1化学第三章单元测试:金属及其化合物1 |

|
|
| 格式 | rar | ||
| 文件大小 | 67.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-11-07 00:00:00 | ||
图片预览


文档简介
第三章 金属及其化合物
1. 一块金属钠投入过量的AlCl3溶液中,生成物是( )
A.H2 、NaOH B. H2、Al(OH)3
C. H2 、NaCl 、NaAlO2 D. H2 、NaCl 、Al(OH)3
2. 下列物质中,可用于治疗胃酸过多的是 ( )
A. 碳酸钠 B. 氢氧化铝 C. 氧化钙 D. 碳酸钙
3. 既与稀HCl反应,又与NaOH溶液反应的是 ( )
A. Mg B. Al C. Fe D. Cu
4. 下面有关Na2CO3 与NaHCO3的叙述错误的是 ( )
A.Na2CO3遇少量酸可转化为NaHCO3
B.在水中的溶解度Na2CO3比NaHCO3大
C.与同浓度的硫酸反应时,Na2CO3比NaHCO3剧烈
D.NaHCO3能与NaOH反应,而Na2CO3不能
5. 只能用焰色反应实验区分的是( )
A. NaCl和Na2CO3 B. KCl和NaCl
C. KCl和K2CO3 D.钠和钾
6. 为了检验某FeCl2溶液是否变质,可向溶液中加入( )
A.NaOH溶液 B.铁片 C.KSCN溶液 D.石蕊溶液
7. 某溶液中加入铝粉,有H2放出,在该溶液中一定能大量共存的离子组是( )
A.K+、Mg2+、Cl-、SO42- B.Na+、NH4+、SO42-、HCO3-
C.Na+、Ba2+、NO3-、Cl- D.K+、Na+、NO3-、AlO2-
8. Mg、Al、Fe三种金属分别跟同浓度、同体积的稀盐酸反应时,放出的氢气质量相等,则下列说法中正确的是( )
A.三种金属的物质的量相等
B.三种金属均过量
C.三种金属的质量相等
D.参加反应的三种金属的质量比为12:9:28
9. 只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液, 这种试剂是( )
A.Ba(OH)2 B.H2SO4 C.NaOH D.AgNO3
10. 下列离子方程式书写正确的是( )
A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓ C. 三氯化铁溶液中加入铁粉
D. FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
11. 除去下列物质中的少量杂质:
(1)Na2CO3固体中的NaHCO3,方法是 ,反应方程式: 。
(2)Na2CO3溶液中的NaHCO3,方法是 ,反应方程式: 。
12. 有4种钠的化合物,W、X、Y、Z,根据下列反应式判断W、X、Y、Z的化学式WX+CO2+H2O ;Z+CO2X+O2 ;Z+H2OY+O2↑;X+Ca(OH)2Y+CaCO3↓。
W为 ,X为 ,Y为 ,Z为 。
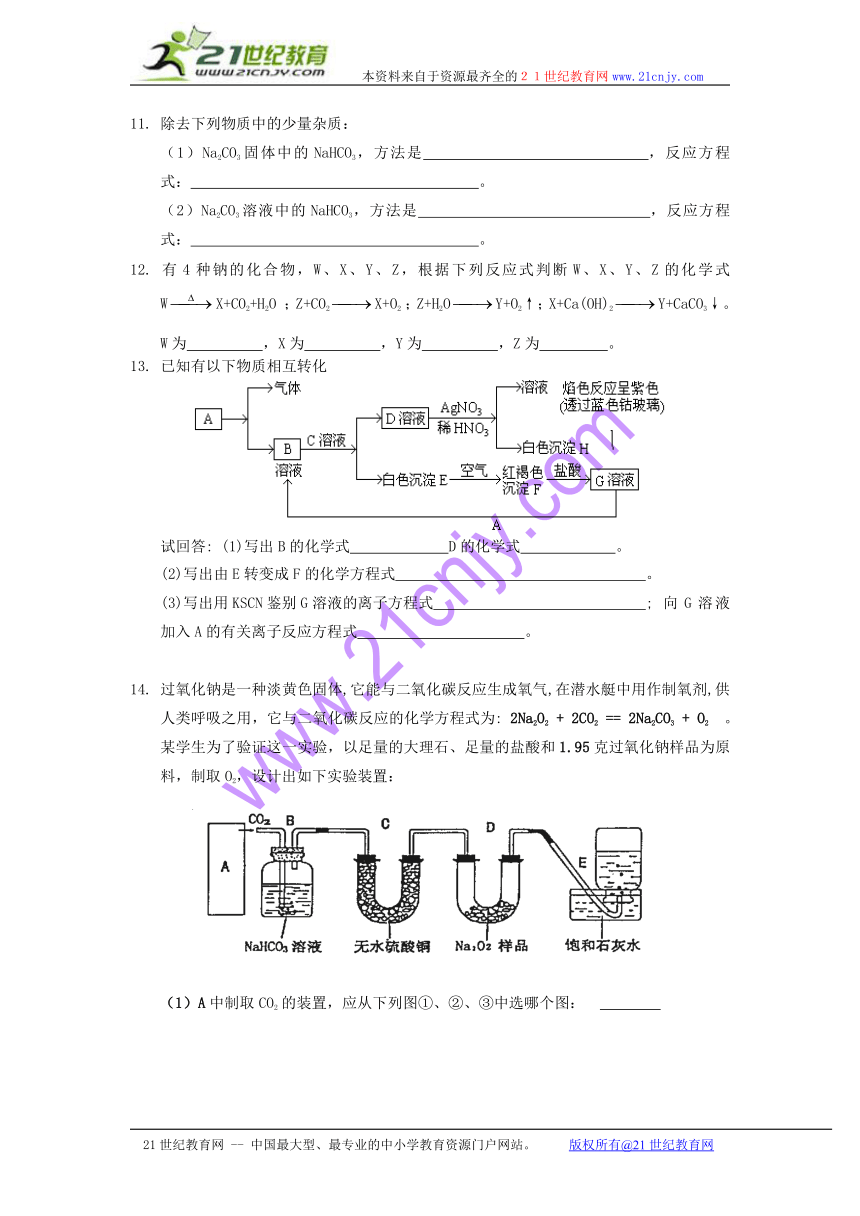
13. 已知有以下物质相互转化
试回答: (1)写出B的化学式 D的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出用KSCN鉴别G溶液的离子方程式 ; 向G溶液加入A的有关离子反应方程式 。
14. 过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用,它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 == 2Na2CO3 + O2 。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95克过氧化钠样品为原料,制取O2,设计出如下实验装置:
(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图:
B装置的作用是 ,C装置内可能出现的现象是 。为了检验E中收集到的气体,在取出集气瓶后,用 的木条伸入集气瓶内,木条会出现 。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因: 。
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
。
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值 (答大或小),相差约 mL(取整数值,所用数据均在标准状况下测定),这是由于_______________________________________________________________________。
(5)你认为上述A---E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项: 。(用甲、乙、丙、丁回答)
15. 加热10.0g碳酸钠和碳酸氢钠的混合物至质量不变化,剩余固体的质量为8.45g,求混合物中碳酸钠的质量分数。
参考答案
1.D 2.B 3.B 4.C 5.B 6.C 7.C 8.BD 9.C 10.D
11.(1)加热 2NaHCO3 === Na2CO3+ CO2↑+H2O
(2)加入NaOH溶液 NaHCO3+、NaOH === Na2CO3+ H2O
12.NaHCO3 Na2CO3 NaOH Na2O2
13.(1)FeCl2 KCl (2)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)Fe3++SCN-=Fe(SCN)2+ 2Fe3++Fe=3Fe2+
14.(1)图2 吸收A装置中产生的酸雾 变蓝 带火的木条 复燃
(2) D中有部分CO2未参加反应流入E中生成沉淀
(3)E中石灰水的白色浑浊明显增加,瓶内液面的下降接近停止
(4)小 30 因样品中含有不与CO2反应生成气体的杂质
(5)乙
15.58%
21世纪教育网
1. 一块金属钠投入过量的AlCl3溶液中,生成物是( )
A.H2 、NaOH B. H2、Al(OH)3
C. H2 、NaCl 、NaAlO2 D. H2 、NaCl 、Al(OH)3
2. 下列物质中,可用于治疗胃酸过多的是 ( )
A. 碳酸钠 B. 氢氧化铝 C. 氧化钙 D. 碳酸钙
3. 既与稀HCl反应,又与NaOH溶液反应的是 ( )
A. Mg B. Al C. Fe D. Cu
4. 下面有关Na2CO3 与NaHCO3的叙述错误的是 ( )
A.Na2CO3遇少量酸可转化为NaHCO3
B.在水中的溶解度Na2CO3比NaHCO3大
C.与同浓度的硫酸反应时,Na2CO3比NaHCO3剧烈
D.NaHCO3能与NaOH反应,而Na2CO3不能
5. 只能用焰色反应实验区分的是( )
A. NaCl和Na2CO3 B. KCl和NaCl
C. KCl和K2CO3 D.钠和钾
6. 为了检验某FeCl2溶液是否变质,可向溶液中加入( )
A.NaOH溶液 B.铁片 C.KSCN溶液 D.石蕊溶液
7. 某溶液中加入铝粉,有H2放出,在该溶液中一定能大量共存的离子组是( )
A.K+、Mg2+、Cl-、SO42- B.Na+、NH4+、SO42-、HCO3-
C.Na+、Ba2+、NO3-、Cl- D.K+、Na+、NO3-、AlO2-
8. Mg、Al、Fe三种金属分别跟同浓度、同体积的稀盐酸反应时,放出的氢气质量相等,则下列说法中正确的是( )
A.三种金属的物质的量相等
B.三种金属均过量
C.三种金属的质量相等
D.参加反应的三种金属的质量比为12:9:28
9. 只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液, 这种试剂是( )
A.Ba(OH)2 B.H2SO4 C.NaOH D.AgNO3
10. 下列离子方程式书写正确的是( )
A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓ C. 三氯化铁溶液中加入铁粉
D. FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
11. 除去下列物质中的少量杂质:
(1)Na2CO3固体中的NaHCO3,方法是 ,反应方程式: 。
(2)Na2CO3溶液中的NaHCO3,方法是 ,反应方程式: 。
12. 有4种钠的化合物,W、X、Y、Z,根据下列反应式判断W、X、Y、Z的化学式WX+CO2+H2O ;Z+CO2X+O2 ;Z+H2OY+O2↑;X+Ca(OH)2Y+CaCO3↓。
W为 ,X为 ,Y为 ,Z为 。
13. 已知有以下物质相互转化
试回答: (1)写出B的化学式 D的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出用KSCN鉴别G溶液的离子方程式 ; 向G溶液加入A的有关离子反应方程式 。
14. 过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用,它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 == 2Na2CO3 + O2 。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95克过氧化钠样品为原料,制取O2,设计出如下实验装置:
(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图:
B装置的作用是 ,C装置内可能出现的现象是 。为了检验E中收集到的气体,在取出集气瓶后,用 的木条伸入集气瓶内,木条会出现 。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因: 。
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
。
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值 (答大或小),相差约 mL(取整数值,所用数据均在标准状况下测定),这是由于_______________________________________________________________________。
(5)你认为上述A---E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项: 。(用甲、乙、丙、丁回答)
15. 加热10.0g碳酸钠和碳酸氢钠的混合物至质量不变化,剩余固体的质量为8.45g,求混合物中碳酸钠的质量分数。
参考答案
1.D 2.B 3.B 4.C 5.B 6.C 7.C 8.BD 9.C 10.D
11.(1)加热 2NaHCO3 === Na2CO3+ CO2↑+H2O
(2)加入NaOH溶液 NaHCO3+、NaOH === Na2CO3+ H2O
12.NaHCO3 Na2CO3 NaOH Na2O2
13.(1)FeCl2 KCl (2)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)Fe3++SCN-=Fe(SCN)2+ 2Fe3++Fe=3Fe2+
14.(1)图2 吸收A装置中产生的酸雾 变蓝 带火的木条 复燃
(2) D中有部分CO2未参加反应流入E中生成沉淀
(3)E中石灰水的白色浑浊明显增加,瓶内液面的下降接近停止
(4)小 30 因样品中含有不与CO2反应生成气体的杂质
(5)乙
15.58%
21世纪教育网
