溴和碘的提取
图片预览






文档简介
课件28张PPT。溴和碘的提取一、分析教材
本节内容选自苏教版化学必修1专题2:“从海水中获得的化学物质”,以自然资源十分丰富的海洋作为研究对象,引出海洋中总储量较多的化学物质的提取、性质和应用。
“溴、碘的提取”是第一单元“氯、溴、碘及其化合物”部分的内容,它在对氯气的性质和生产原理学习的基础上,以类比的方式进一步探究溴、碘的性质及从海水(或海带)中提取溴、碘的原理和方法,本节内容不仅复习巩固了上一节“氧化还原反应”的知识,同时以实验探究的方式学习元素及其化合物,为下一单元“钠及其化合物”的学习提供方法指导。另外,溴碘及其化合物知识与前面所学的氯的知识相结合,让学生形成卤素性质相似性和递变性变化规律的认知,为必修2学习元素周期律知识打下坚实的基础。二、学情分析在本节课之前,学生已经学习了“氯气的生产原理和性质”以及“氧化还原反应”的有关知识,对以实验探究的方式学习元素及其化合物有了初步的认知,学生也对碘及其化合物在生产和生活中的应用有一定的了解。但提取溴、碘的反应原理以及氯、溴、碘之间的相互置换对于学生是陌生的知识,这也是本节课教学的重难点。为此,我将引导学生类比应用氯气和氧化还原反应的知识,以实验探究、合作学习的方式,突破这一教学重难点。三、教学目标1、了解从海水中提取溴、碘的过程,认识溴、碘及其化合物的性质和用途。
2、通过实验探究,掌握提取溴、碘的反应原理以及氯、溴、碘氧化性递变规律。
3、体验实验、观察、类比和归纳等方法在学习元素及其化合物中的作用。
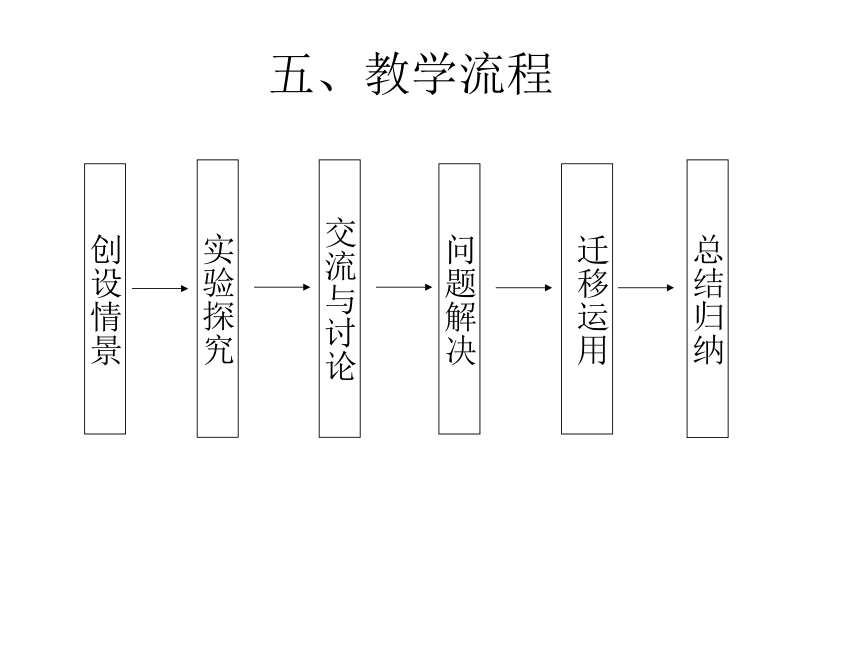
4、通过海水提取溴、碘的学习,能够建立一种生活和生产实际中物质制备和提取的一般过程和方法,感受海洋资源的丰富及合理开发海洋资源的意义。四、教法分析 为实现上述教学目标,我将主要采用实验探究、交流讨论、问题解决相融合的教学方法。在教学中,我将让学生多次分组进行实验探究,使学生进一步了解实验探究的过程和一般方法。同时使学生在交流合作中取长补短,培养主体性和合作竞争意识。 五、教学流程
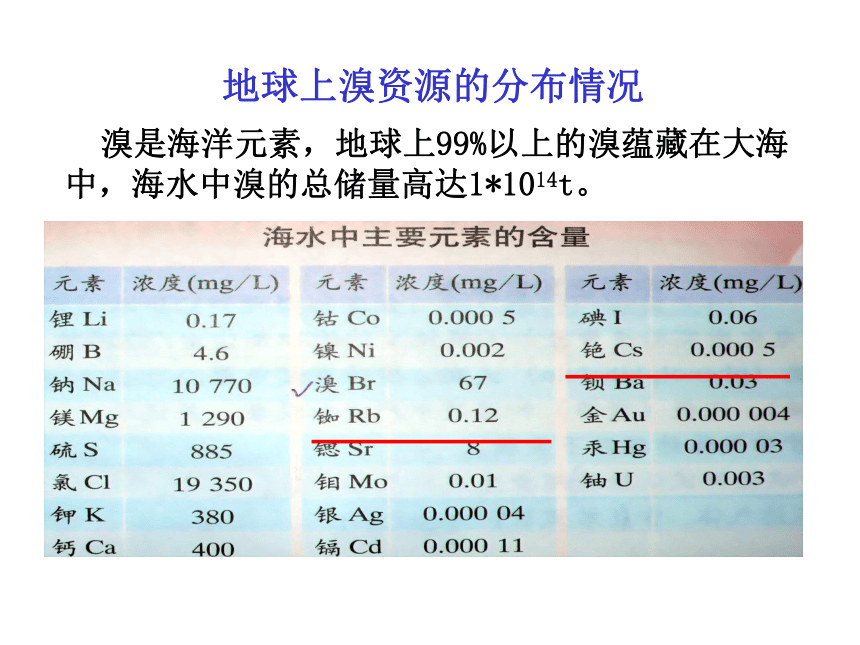
溴对人类发展的作用主要用作制取溴化物,并用于医药、农药、染料、香料、摄影材料、灭火剂、选矿、冶金、鞣革、净水等部门用作普通分析试剂和有机合成剂。地球上溴资源的分布情况 溴是海洋元素,地球上99%以上的溴蕴藏在大海中,海水中溴的总储量高达1*1014t。
碘是一种人体必需的微量元素,有“智力元素”之称 ,能促进人体能量代谢,维持生理功能,促进大脑发育 ……溴(Br2)、碘(I2)的性质溴单质常温下,深红棕色、密度比水大的液体,易挥发。
碘单质是紫黑色的固体,易升华,遇淀粉变蓝。
溴和碘在水中的溶解度都很小,但易溶于酒精、四氯化碳等有机溶剂。海水中溴的提取流程从海带中碘的提取流程加热升华海洋中的溴、碘是以什么形态存在的,能否直接分离?
如何把碘由化合态变为游离态,加入什么物质可以实现这个转化?
提取溴、碘的反应原理是什么?思考(1)组实验探究(2)组实验探究(3)组实验探究展示结果:(1)组展示结果:(2)组展示结果:(3)组无色→橙黄色.加入CCl4,上层变浅,下层变橙红色;加入苯,上层变橙红色,下层变浅;加入酒精后不分层无色→棕黄色.加入CCl4上层变浅,下层变紫红色;加入苯,上层变紫红色,下层变浅;加入酒精后不分层
无色→棕黄色.加入CCl4上层变浅,下层变紫红色;加入苯,上层变紫红色,下层变浅;加入酒精后不分层
有溴单质生成有碘单质生成有碘单质生成Cl2 + 2KBr = 2KCl + Br2Cl2 + 2KI = 2KCl + I2Br2 + 2KI = 2KBr + I20 -1 -1 0氧化性: Cl2> Br2> I2还原性: Cl-< Br-< I-交流与讨论如何鉴别Cl-,Br-,I-? ①先加氯水,再加CCl4萃取,看颜色,溴橙红碘紫红氯不变 。②加硝酸酸化的硝酸银,沉淀颜色不同。AgCl白色,AgBr淡黄色,AgI黄色。工业提取Br2:
提取粗盐后的母液→通入Cl2→鼓入热空气→挥发Br2蒸气→冷凝得液溴
工业提取I2:
海带粉碎→加水浸泡→通入Cl2→过滤→蒸发→升华→冷凝I2蒸气得晶体交流与讨论 得到的单质溴、碘如何从海水中提取出来呢? 是萃取的吗?演示实验:溴的挥发、碘的升华碘缺乏症是目前已知的导致人类智力障碍的主要原因。为解决这一全国性问题,我国已经开始实施“智力工程”。
你知道采取了哪些措施吗?
沧州各县市是否属于碘缺乏区?交流与讨论[随堂测试]1、将溴水和下列试剂混合振荡,静置后下层为橙色的是( )
A.酒精 B.苯
C.四氯化碳 D.汽油
2、碘缺乏症是目前已知的导致人类智力障碍的主要原因。为解决这一全国性问题,我国已经开始实施“智力工程”。最经济可行的措施是( )
A.食盐加碘(盐) B.面包加碘(盐) C.大量食用海带 D.注射含碘药剂 CA3、向含有KBr和KI的混合溶液里通入足量的氯气,充分反应后将溶液蒸干,并将剩余的残渣灼烧,最终留下残渣的成分是( )
A.KCl、KBr
B. KCl 、I2
C. Br2、 I2
D. KClD板书设计一、溴、碘的物理性质 二、氯溴碘之间的置换反应氧化性: Cl2> Br2> I2还原性: Cl-< Br-< I-三、工业上溴、碘的提取 四、卤素离子的检验
“溴、碘的提取”是第一单元“氯、溴、碘及其化合物”部分的内容,它在对氯气的性质和生产原理学习的基础上,以类比的方式进一步探究溴、碘的性质及从海水(或海带)中提取溴、碘的原理和方法,本节内容不仅复习巩固了上一节“氧化还原反应”的知识,同时以实验探究的方式学习元素及其化合物,为下一单元“钠及其化合物”的学习提供方法指导。另外,溴碘及其化合物知识与前面所学的氯的知识相结合,让学生形成卤素性质相似性和递变性变化规律的认知,为必修2学习元素周期律知识打下坚实的基础。二、学情分析在本节课之前,学生已经学习了“氯气的生产原理和性质”以及“氧化还原反应”的有关知识,对以实验探究的方式学习元素及其化合物有了初步的认知,学生也对碘及其化合物在生产和生活中的应用有一定的了解。但提取溴、碘的反应原理以及氯、溴、碘之间的相互置换对于学生是陌生的知识,这也是本节课教学的重难点。为此,我将引导学生类比应用氯气和氧化还原反应的知识,以实验探究、合作学习的方式,突破这一教学重难点。三、教学目标1、了解从海水中提取溴、碘的过程,认识溴、碘及其化合物的性质和用途。
2、通过实验探究,掌握提取溴、碘的反应原理以及氯、溴、碘氧化性递变规律。
3、体验实验、观察、类比和归纳等方法在学习元素及其化合物中的作用。
4、通过海水提取溴、碘的学习,能够建立一种生活和生产实际中物质制备和提取的一般过程和方法,感受海洋资源的丰富及合理开发海洋资源的意义。四、教法分析 为实现上述教学目标,我将主要采用实验探究、交流讨论、问题解决相融合的教学方法。在教学中,我将让学生多次分组进行实验探究,使学生进一步了解实验探究的过程和一般方法。同时使学生在交流合作中取长补短,培养主体性和合作竞争意识。 五、教学流程
溴对人类发展的作用主要用作制取溴化物,并用于医药、农药、染料、香料、摄影材料、灭火剂、选矿、冶金、鞣革、净水等部门用作普通分析试剂和有机合成剂。地球上溴资源的分布情况 溴是海洋元素,地球上99%以上的溴蕴藏在大海中,海水中溴的总储量高达1*1014t。
碘是一种人体必需的微量元素,有“智力元素”之称 ,能促进人体能量代谢,维持生理功能,促进大脑发育 ……溴(Br2)、碘(I2)的性质溴单质常温下,深红棕色、密度比水大的液体,易挥发。
碘单质是紫黑色的固体,易升华,遇淀粉变蓝。
溴和碘在水中的溶解度都很小,但易溶于酒精、四氯化碳等有机溶剂。海水中溴的提取流程从海带中碘的提取流程加热升华海洋中的溴、碘是以什么形态存在的,能否直接分离?
如何把碘由化合态变为游离态,加入什么物质可以实现这个转化?
提取溴、碘的反应原理是什么?思考(1)组实验探究(2)组实验探究(3)组实验探究展示结果:(1)组展示结果:(2)组展示结果:(3)组无色→橙黄色.加入CCl4,上层变浅,下层变橙红色;加入苯,上层变橙红色,下层变浅;加入酒精后不分层无色→棕黄色.加入CCl4上层变浅,下层变紫红色;加入苯,上层变紫红色,下层变浅;加入酒精后不分层
无色→棕黄色.加入CCl4上层变浅,下层变紫红色;加入苯,上层变紫红色,下层变浅;加入酒精后不分层
有溴单质生成有碘单质生成有碘单质生成Cl2 + 2KBr = 2KCl + Br2Cl2 + 2KI = 2KCl + I2Br2 + 2KI = 2KBr + I20 -1 -1 0氧化性: Cl2> Br2> I2还原性: Cl-< Br-< I-交流与讨论如何鉴别Cl-,Br-,I-? ①先加氯水,再加CCl4萃取,看颜色,溴橙红碘紫红氯不变 。②加硝酸酸化的硝酸银,沉淀颜色不同。AgCl白色,AgBr淡黄色,AgI黄色。工业提取Br2:
提取粗盐后的母液→通入Cl2→鼓入热空气→挥发Br2蒸气→冷凝得液溴
工业提取I2:
海带粉碎→加水浸泡→通入Cl2→过滤→蒸发→升华→冷凝I2蒸气得晶体交流与讨论 得到的单质溴、碘如何从海水中提取出来呢? 是萃取的吗?演示实验:溴的挥发、碘的升华碘缺乏症是目前已知的导致人类智力障碍的主要原因。为解决这一全国性问题,我国已经开始实施“智力工程”。
你知道采取了哪些措施吗?
沧州各县市是否属于碘缺乏区?交流与讨论[随堂测试]1、将溴水和下列试剂混合振荡,静置后下层为橙色的是( )
A.酒精 B.苯
C.四氯化碳 D.汽油
2、碘缺乏症是目前已知的导致人类智力障碍的主要原因。为解决这一全国性问题,我国已经开始实施“智力工程”。最经济可行的措施是( )
A.食盐加碘(盐) B.面包加碘(盐) C.大量食用海带 D.注射含碘药剂 CA3、向含有KBr和KI的混合溶液里通入足量的氯气,充分反应后将溶液蒸干,并将剩余的残渣灼烧,最终留下残渣的成分是( )
A.KCl、KBr
B. KCl 、I2
C. Br2、 I2
D. KClD板书设计一、溴、碘的物理性质 二、氯溴碘之间的置换反应氧化性: Cl2> Br2> I2还原性: Cl-< Br-< I-三、工业上溴、碘的提取 四、卤素离子的检验
