金属的化学性质
图片预览

文档简介
《金属的化学性质》教学设计
连云港市海宁中学
张 妮 妮
课题2金属的化学性质
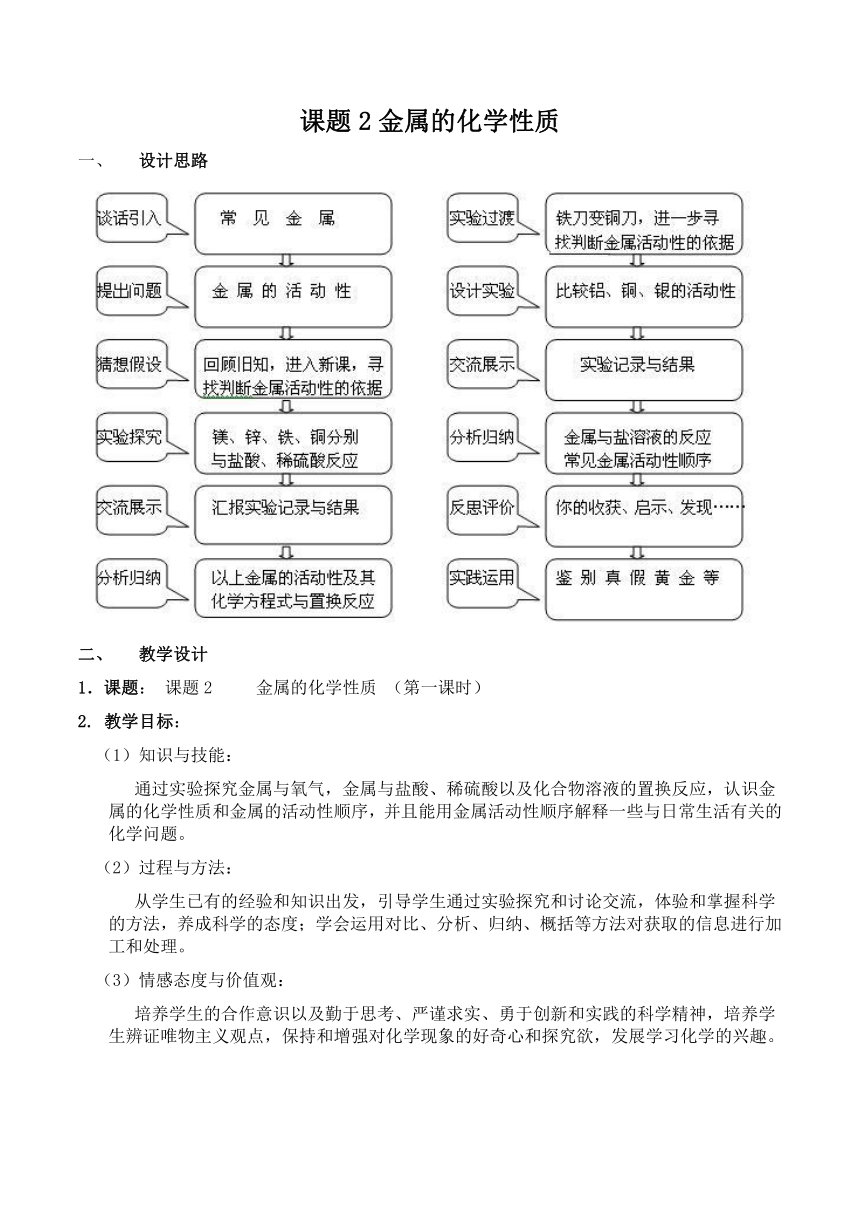
1、 设计思路
2、 教学设计
1.课题: 课题2 金属的化学性质 (第一课时)
2. 教学目标:
(1)知识与技能:
通过实验探究金属与氧气,金属与盐酸、稀硫酸以及化合物溶液的置换反应,认识金属的化学性质和金属的活动性顺序,并且能用金属活动性顺序解释一些与日常生活有关的化学问题。
(2)过程与方法:
从学生已有的经验和知识出发,引导学生通过实验探究和讨论交流,体验和掌握科学的方法,养成科学的态度;学会运用对比、分析、归纳、概括等方法对获取的信息进行加工和处理。
(3)情感态度与价值观:
培养学生的合作意识以及勤于思考、严谨求实、勇于创新和实践的科学精神,培养学生辨证唯物主义观点,保持和增强对化学现象的好奇心和探究欲,发展学习化学的兴趣。
3.教学重点、难点:
重点:金属活动性顺序。
难点:对金属活动性顺序的初步探究及利用金属活动性顺序对置换反应的判断。
4.教学方法:小组合作法、实验探究法。以活动元教学设计方法进行设计。
5.教学准备:仪器药品、 铁片、铜片、铝片、铁丝、铜丝、铝丝、酒精灯、火柴、砂纸、稀盐酸、稀硫酸、硫酸铜溶液等
6. 教学过程:
引入:物质的结构决定性质,性质决定用途。我们知道有些金属可以和氧气发生反应,回忆哪些金属可以和氧气发生化学反应吗? 提出问题, 回忆已有的知识得出:铁、镁、铜等 引发学生思考、回忆
提问:这些金属和氧气发生反应需要什么条件? 小组讨论、汇报 考察学生对问题的归纳能力
引导:大家拿出盒子中的镁条、铝片观察。用砂纸打磨,观察,比较颜色、光泽的变化。想一想是谁让镁条、铝片穿上外衣的?说明什么? 氧气。镁、铝在常温的条件下就可以和氧气发生化学反应。 培养学生的观察能力
俗语“真金不怕火炼”说明什么? 熔点高,但金的表面没有发生变化,说明金即使在高温的条件下也不与氧气发生反应。 化学知识密切联系实际生活
以上的实验事实说明什么? 不同的金属与氧气发生反应的条件不同。与氧气反应的条件不同说明金属的化学活动性不同。 培养认知结构
结论:镁、铝比较活泼;铁、铜次之;金最不活泼。
[投影]资料:金属可以与酸反应放出氢气,而且,不同的金属放出氢气的速率不同。 设计(金属与盐酸或硫酸的实验)、展示、预测实验现象。探究四种金属与盐酸、硫酸反应的实验。展示本组实验现象及成果。 考察学生的设计问题、实验探究的能力
[师-生]总结:镁、锌、铁能与盐酸、硫酸反应生成氢气,铜不能与盐酸、硫酸反应。并且镁与盐酸、硫酸反应最剧烈。锌次之,铁与盐酸、硫酸反应较为缓和。
所以我们可以得出镁、锌、铁、铜的金属活动性顺序为(幻灯片)。 书写有关化学方程式 训练基本的化学用语
引出置换反应的概念,即一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。
如果我们把H加到四种金属之间,你会把它加到哪儿 讨论,发表意见,得出结论。 培养学生的发散思维能力
我们在学习质量守恒的时候,我们把铁丝浸入硫酸铜溶液中,看到什么现象,发生了什么反应?反应得化学方程式是什么? 回答 ,写出反应方程式。 回忆已有知识、引入新知识,为下面的实验做铺垫
那么铜能否与硫酸亚铁反应,生成铁? 学生思考 反向思维,使知识构建更合理
[实验]铜与硫酸亚铁反应。 观察、描述、得出结论
铁比铜活泼,铁能把铜从硫酸铜溶液中反应出来,而铜不能反应出铁,说明什么? 如果一种金属能把另一种金属从它的溶液中反应出来,那么第一种金属就比第二种金属活泼。 培养学生将描述性知识转化为结论性知识
下面请大家只利用盒子里的溶液和金属设计实验自行实验判断铝、铜、银的金属活动性顺序。 活动与探究:实验并填表。汇报实验结果,展示。 将结论性的知识用实验探究的方法加以验证
[师-生]总结:从以上的实验可以得出铝、铜、银的金属活动性顺序为: (幻灯片:三种金属的活动性)
金属活动性顺序表可以给我们一些什么信息? 讨论,交流后汇报1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。2、在金属活动性顺序里,位于氢前面的金属能置换出盐酸、硫酸中的氢。3、在金属活动性顺序里,位于前面的金属能把位于后面的金属从他们的化合物溶液中置换出来。 将本节课的知识更加合理化,培养学生的严谨的科学态度。
7. 板书设计:
课题2 金属的化学性质
一、 金属的化学性质
1、金属与氧气的反应
金属+氧气→金属氧化物
金属的活动性:Mg>Al>Fe,Cu>Au
2、金属与酸的反应
Mg+2HCl==MgCl2+H2↑ Zn+2HCl==ZnCl+H2↑
Fe+2HCl==FeCl2+H2↑ Mg+H2SO4==MgSO4+H2↑
Zn+H2SO4==ZnSO4+H2↑ Fe+H2SO4==FeSO4+H2↑
金属+酸→金属化合物+氢气
金属的活动性:Mg>Zn>Fe>Cu
置换反应:A+BC→AC+B
3、金属与金属化合物溶液反应
金属+金属化合物→新金属化合物+新金属
2Al+3CuSO4=Al(SO4)3+3Cu
Cu+2AgNO3=Cu(NO3)2+2Ag
金属的活动性:Al>Cu>Ag
二、金属的活动性顺序
8、课后拓展——设计、观察与思考:
铁在常温下几乎不与氧气反应,但在潮湿的空气中却易与空气中氧气反应而生锈。现有洁净无锈的铁钉、试管、食醋、食盐水、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙。试设计实验比较铁钉在不同环境中的锈蚀速度,以供我们在后面课题的学习中进行交流
9.教学反思:
教材的内容组织符合物质的认知规律,对物质的认识由感性认识上升到理性认识。课堂教学设计遵循学生的认知规律,突出活动中重点知识的掌握及难点突破,以学生活动为主体,教师及时讲解、点评、总结,使教学过程更加合理,有效。
连云港市海宁中学
张 妮 妮
课题2金属的化学性质
1、 设计思路
2、 教学设计
1.课题: 课题2 金属的化学性质 (第一课时)
2. 教学目标:
(1)知识与技能:
通过实验探究金属与氧气,金属与盐酸、稀硫酸以及化合物溶液的置换反应,认识金属的化学性质和金属的活动性顺序,并且能用金属活动性顺序解释一些与日常生活有关的化学问题。
(2)过程与方法:
从学生已有的经验和知识出发,引导学生通过实验探究和讨论交流,体验和掌握科学的方法,养成科学的态度;学会运用对比、分析、归纳、概括等方法对获取的信息进行加工和处理。
(3)情感态度与价值观:
培养学生的合作意识以及勤于思考、严谨求实、勇于创新和实践的科学精神,培养学生辨证唯物主义观点,保持和增强对化学现象的好奇心和探究欲,发展学习化学的兴趣。
3.教学重点、难点:
重点:金属活动性顺序。
难点:对金属活动性顺序的初步探究及利用金属活动性顺序对置换反应的判断。
4.教学方法:小组合作法、实验探究法。以活动元教学设计方法进行设计。
5.教学准备:仪器药品、 铁片、铜片、铝片、铁丝、铜丝、铝丝、酒精灯、火柴、砂纸、稀盐酸、稀硫酸、硫酸铜溶液等
6. 教学过程:
引入:物质的结构决定性质,性质决定用途。我们知道有些金属可以和氧气发生反应,回忆哪些金属可以和氧气发生化学反应吗? 提出问题, 回忆已有的知识得出:铁、镁、铜等 引发学生思考、回忆
提问:这些金属和氧气发生反应需要什么条件? 小组讨论、汇报 考察学生对问题的归纳能力
引导:大家拿出盒子中的镁条、铝片观察。用砂纸打磨,观察,比较颜色、光泽的变化。想一想是谁让镁条、铝片穿上外衣的?说明什么? 氧气。镁、铝在常温的条件下就可以和氧气发生化学反应。 培养学生的观察能力
俗语“真金不怕火炼”说明什么? 熔点高,但金的表面没有发生变化,说明金即使在高温的条件下也不与氧气发生反应。 化学知识密切联系实际生活
以上的实验事实说明什么? 不同的金属与氧气发生反应的条件不同。与氧气反应的条件不同说明金属的化学活动性不同。 培养认知结构
结论:镁、铝比较活泼;铁、铜次之;金最不活泼。
[投影]资料:金属可以与酸反应放出氢气,而且,不同的金属放出氢气的速率不同。 设计(金属与盐酸或硫酸的实验)、展示、预测实验现象。探究四种金属与盐酸、硫酸反应的实验。展示本组实验现象及成果。 考察学生的设计问题、实验探究的能力
[师-生]总结:镁、锌、铁能与盐酸、硫酸反应生成氢气,铜不能与盐酸、硫酸反应。并且镁与盐酸、硫酸反应最剧烈。锌次之,铁与盐酸、硫酸反应较为缓和。
所以我们可以得出镁、锌、铁、铜的金属活动性顺序为(幻灯片)。 书写有关化学方程式 训练基本的化学用语
引出置换反应的概念,即一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。
如果我们把H加到四种金属之间,你会把它加到哪儿 讨论,发表意见,得出结论。 培养学生的发散思维能力
我们在学习质量守恒的时候,我们把铁丝浸入硫酸铜溶液中,看到什么现象,发生了什么反应?反应得化学方程式是什么? 回答 ,写出反应方程式。 回忆已有知识、引入新知识,为下面的实验做铺垫
那么铜能否与硫酸亚铁反应,生成铁? 学生思考 反向思维,使知识构建更合理
[实验]铜与硫酸亚铁反应。 观察、描述、得出结论
铁比铜活泼,铁能把铜从硫酸铜溶液中反应出来,而铜不能反应出铁,说明什么? 如果一种金属能把另一种金属从它的溶液中反应出来,那么第一种金属就比第二种金属活泼。 培养学生将描述性知识转化为结论性知识
下面请大家只利用盒子里的溶液和金属设计实验自行实验判断铝、铜、银的金属活动性顺序。 活动与探究:实验并填表。汇报实验结果,展示。 将结论性的知识用实验探究的方法加以验证
[师-生]总结:从以上的实验可以得出铝、铜、银的金属活动性顺序为: (幻灯片:三种金属的活动性)
金属活动性顺序表可以给我们一些什么信息? 讨论,交流后汇报1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。2、在金属活动性顺序里,位于氢前面的金属能置换出盐酸、硫酸中的氢。3、在金属活动性顺序里,位于前面的金属能把位于后面的金属从他们的化合物溶液中置换出来。 将本节课的知识更加合理化,培养学生的严谨的科学态度。
7. 板书设计:
课题2 金属的化学性质
一、 金属的化学性质
1、金属与氧气的反应
金属+氧气→金属氧化物
金属的活动性:Mg>Al>Fe,Cu>Au
2、金属与酸的反应
Mg+2HCl==MgCl2+H2↑ Zn+2HCl==ZnCl+H2↑
Fe+2HCl==FeCl2+H2↑ Mg+H2SO4==MgSO4+H2↑
Zn+H2SO4==ZnSO4+H2↑ Fe+H2SO4==FeSO4+H2↑
金属+酸→金属化合物+氢气
金属的活动性:Mg>Zn>Fe>Cu
置换反应:A+BC→AC+B
3、金属与金属化合物溶液反应
金属+金属化合物→新金属化合物+新金属
2Al+3CuSO4=Al(SO4)3+3Cu
Cu+2AgNO3=Cu(NO3)2+2Ag
金属的活动性:Al>Cu>Ag
二、金属的活动性顺序
8、课后拓展——设计、观察与思考:
铁在常温下几乎不与氧气反应,但在潮湿的空气中却易与空气中氧气反应而生锈。现有洁净无锈的铁钉、试管、食醋、食盐水、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙。试设计实验比较铁钉在不同环境中的锈蚀速度,以供我们在后面课题的学习中进行交流
9.教学反思:
教材的内容组织符合物质的认知规律,对物质的认识由感性认识上升到理性认识。课堂教学设计遵循学生的认知规律,突出活动中重点知识的掌握及难点突破,以学生活动为主体,教师及时讲解、点评、总结,使教学过程更加合理,有效。
同课章节目录
