2010年山东省高中化学优质课评选课件:2.2 第1课时《电解质及其电离》
文档属性
| 名称 | 2010年山东省高中化学优质课评选课件:2.2 第1课时《电解质及其电离》 |

|
|
| 格式 | rar | ||
| 文件大小 | 520.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-11-26 00:00:00 | ||
图片预览




文档简介
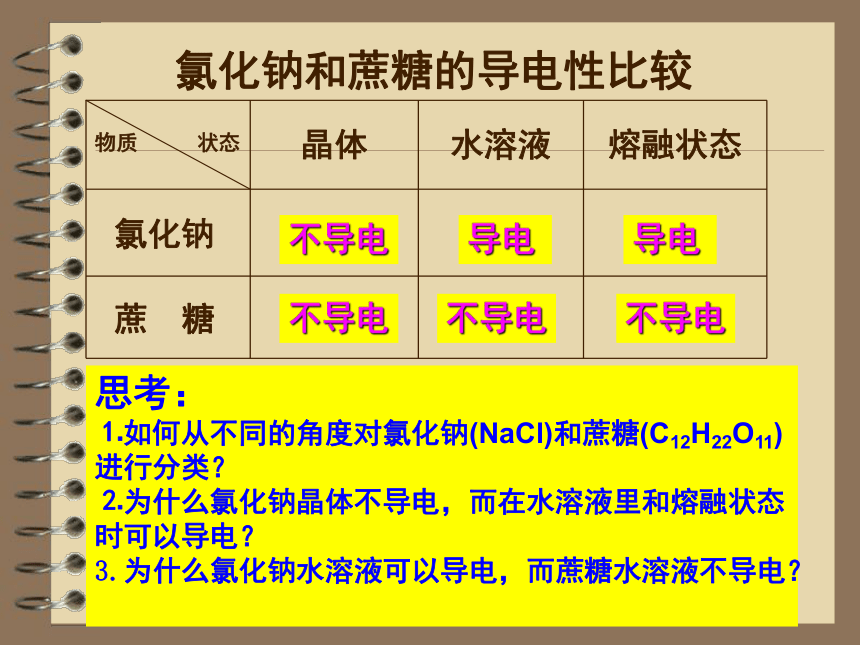
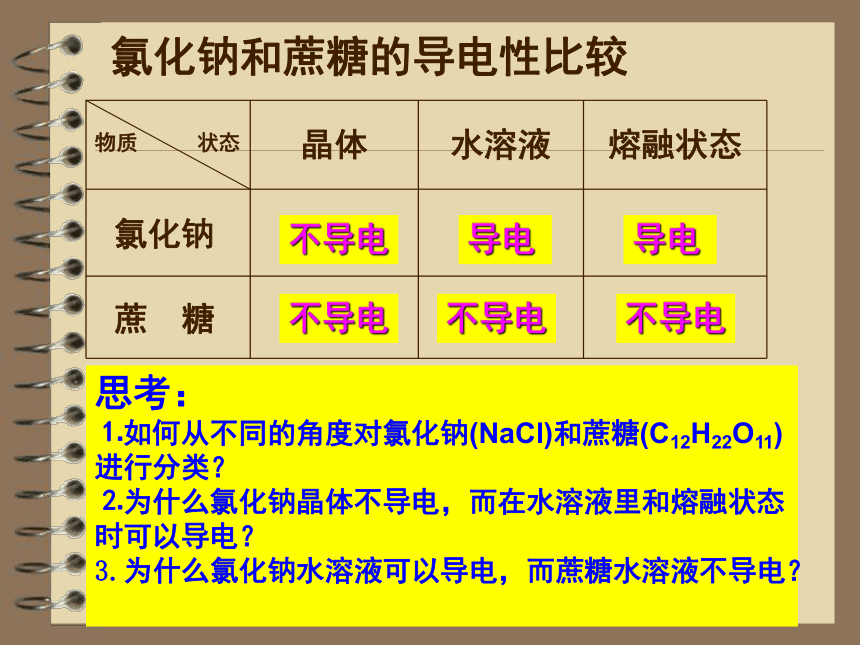
课件18张PPT。第二节 电解质(第一课时)电解质及其电离菏泽市巨野县第一中学 梁劲松氯化钠和蔗糖的导电性比较不导电不导电导电不导电导电不导电思考:
⒈如何从不同的角度对氯化钠(NaCl)和蔗糖(C12H22O11)进行分类?
⒉为什么氯化钠晶体不导电,而在水溶液里和熔融状态时可以导电?
3.为什么氯化钠水溶液可以导电,而蔗糖水溶液不导电?一、电解质及其电离⒈电解质和非电解质
电解质非电解质在水溶液里和熔融状态下都不能导电的化合物。在水溶液里或熔融状态下能够导电的化合物。 下列物质属于电解质的是( )①石墨 ②液态氯化氢 ③氢氧化钠溶液
④ 无水酒精 ⑤硝酸钾晶体 ⑥蔗糖溶液
⑦熔融的氢氧化钠 ⑧盐酸【交流·研讨】氯化钠和蔗糖的导电性比较不导电不导电导电不导电导电不导电思考:
⒈如何从不同的角度对氯化钠(NaCl)和蔗糖(C12H22O11)进行分类?
⒉为什么氯化钠晶体不导电,而在水溶液里和熔融状态时可以导电?
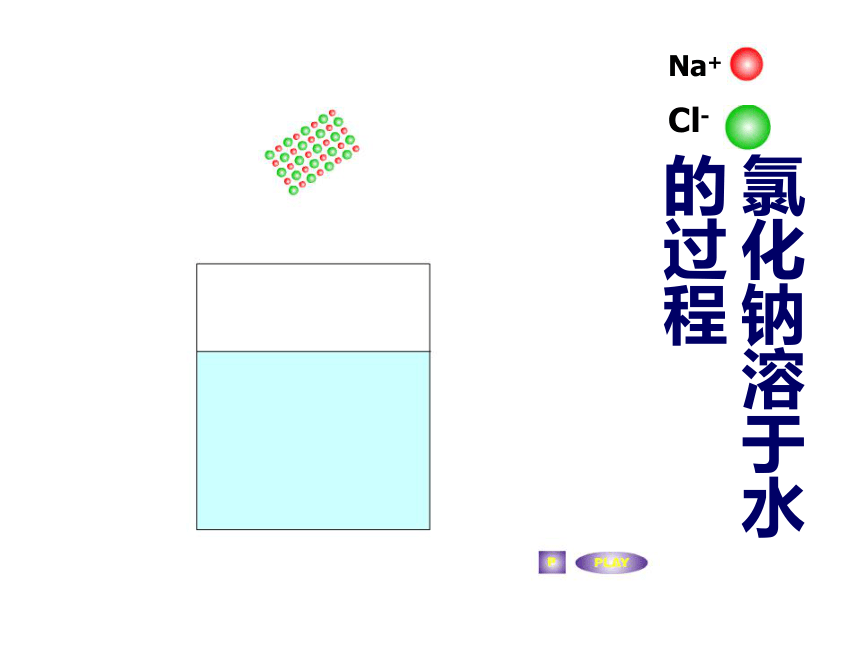
3.为什么氯化钠水溶液可以导电,而蔗糖水溶液不导电?氯化钠溶于水的过程Na+Cl-⒉电解质的电离⑴概念 像氯化钠这样溶解于水或受热熔化时,离解成自由移动的离子的过程称为电离。实验证明:
酸在溶于水时可以发生电离,碱和盐
在溶于水或受热熔化时可以发生电离。下列物质属于电解质的是( ) 能导电的是( )①石墨 ②液态氯化氢 ③氢氧化钠溶液
④ 无水酒精 ⑤硝酸钾晶体 ⑥蔗糖溶液
⑦熔融的氢氧化钠 ⑧盐酸【交流·研讨】氯化钠和蔗糖的导电性比较不导电不导电导电不导电导电不导电思考:
⒈如何从不同的角度对氯化钠(NaCl)和蔗糖(C12H22O11)进行分类?
⒉为什么氯化钠晶体不导电,而在水溶液里和熔融状态时可以导电?
3.为什么氯化钠水溶液可以导电,而蔗糖水溶液不导电?⑵电离方程式① HCl = H+ + Cl-
② Ca(OH)2 = Ca2+ + 2OH-
③ NaCl = Na+ + Cl-【方法导引】书写电离方程式注意事项1、方程式左边是电解质的化学式,右边
是电离产生的离子符号。
2、电解质溶液是呈电中性的,电离产生
的阳离子所带正电荷总数等于阴离子所带
负电荷总数。
3、电离前后原子数目和种类不变。
4、电离产生的阴阳离子数目用阿拉伯数字
2、3等表示。⑴ 硝酸、硫酸 :
⑵ 氢氧化钾、氢氧化钡:
⑶ 硫酸铜、氯化铜:请分别书写下列各组物质的电离方程式, 并进一步从电离的角度认识酸、碱、盐。⑶ 酸、碱、盐①酸②碱③盐电离时,能生成金属阳离子(或铵根离子)
和酸根阴离子的化合物。电离时,生成的阴离子全部是OH-的化合物。电离时,生成的阳离子全部是H+的化合物。【问题与思考】已知NaHSO4在水溶液中发生如下电离:
NaHSO4 = Na+ + H+ + SO42- ,
则NaHSO4属于酸、碱、盐中的哪一种?NaHSO4属于盐,因为其电离时产生了
金属阳离子Na+ 和酸根离子SO42-。
【问题解决】溶液由溶质、溶剂两部分组成,溶质
(化合物)在水溶液里是以什么状态
存在的?分子还是离子? 电解质:在水溶液里以离子形式存在
非电解质:在水溶液里以分子形式存在?⒈通过本节课的学习,你学习了哪些知识?
⒉在学习过程中,你还领悟了哪些方法?
⒈完成学案上的形成性检测。
⒉预习电解质(第2课时)—— “电解质
在水溶液中的反应” 。
⒊查阅资料,写一篇小论文《生命与电解质》
作业 谢谢各位专家同仁莅临指导
巨野县第一中学
⒈如何从不同的角度对氯化钠(NaCl)和蔗糖(C12H22O11)进行分类?
⒉为什么氯化钠晶体不导电,而在水溶液里和熔融状态时可以导电?
3.为什么氯化钠水溶液可以导电,而蔗糖水溶液不导电?一、电解质及其电离⒈电解质和非电解质
电解质非电解质在水溶液里和熔融状态下都不能导电的化合物。在水溶液里或熔融状态下能够导电的化合物。 下列物质属于电解质的是( )①石墨 ②液态氯化氢 ③氢氧化钠溶液
④ 无水酒精 ⑤硝酸钾晶体 ⑥蔗糖溶液
⑦熔融的氢氧化钠 ⑧盐酸【交流·研讨】氯化钠和蔗糖的导电性比较不导电不导电导电不导电导电不导电思考:
⒈如何从不同的角度对氯化钠(NaCl)和蔗糖(C12H22O11)进行分类?
⒉为什么氯化钠晶体不导电,而在水溶液里和熔融状态时可以导电?
3.为什么氯化钠水溶液可以导电,而蔗糖水溶液不导电?氯化钠溶于水的过程Na+Cl-⒉电解质的电离⑴概念 像氯化钠这样溶解于水或受热熔化时,离解成自由移动的离子的过程称为电离。实验证明:
酸在溶于水时可以发生电离,碱和盐
在溶于水或受热熔化时可以发生电离。下列物质属于电解质的是( ) 能导电的是( )①石墨 ②液态氯化氢 ③氢氧化钠溶液
④ 无水酒精 ⑤硝酸钾晶体 ⑥蔗糖溶液
⑦熔融的氢氧化钠 ⑧盐酸【交流·研讨】氯化钠和蔗糖的导电性比较不导电不导电导电不导电导电不导电思考:
⒈如何从不同的角度对氯化钠(NaCl)和蔗糖(C12H22O11)进行分类?
⒉为什么氯化钠晶体不导电,而在水溶液里和熔融状态时可以导电?
3.为什么氯化钠水溶液可以导电,而蔗糖水溶液不导电?⑵电离方程式① HCl = H+ + Cl-
② Ca(OH)2 = Ca2+ + 2OH-
③ NaCl = Na+ + Cl-【方法导引】书写电离方程式注意事项1、方程式左边是电解质的化学式,右边
是电离产生的离子符号。
2、电解质溶液是呈电中性的,电离产生
的阳离子所带正电荷总数等于阴离子所带
负电荷总数。
3、电离前后原子数目和种类不变。
4、电离产生的阴阳离子数目用阿拉伯数字
2、3等表示。⑴ 硝酸、硫酸 :
⑵ 氢氧化钾、氢氧化钡:
⑶ 硫酸铜、氯化铜:请分别书写下列各组物质的电离方程式, 并进一步从电离的角度认识酸、碱、盐。⑶ 酸、碱、盐①酸②碱③盐电离时,能生成金属阳离子(或铵根离子)
和酸根阴离子的化合物。电离时,生成的阴离子全部是OH-的化合物。电离时,生成的阳离子全部是H+的化合物。【问题与思考】已知NaHSO4在水溶液中发生如下电离:
NaHSO4 = Na+ + H+ + SO42- ,
则NaHSO4属于酸、碱、盐中的哪一种?NaHSO4属于盐,因为其电离时产生了
金属阳离子Na+ 和酸根离子SO42-。
【问题解决】溶液由溶质、溶剂两部分组成,溶质
(化合物)在水溶液里是以什么状态
存在的?分子还是离子? 电解质:在水溶液里以离子形式存在
非电解质:在水溶液里以分子形式存在?⒈通过本节课的学习,你学习了哪些知识?
⒉在学习过程中,你还领悟了哪些方法?
⒈完成学案上的形成性检测。
⒉预习电解质(第2课时)—— “电解质
在水溶液中的反应” 。
⒊查阅资料,写一篇小论文《生命与电解质》
作业 谢谢各位专家同仁莅临指导
巨野县第一中学
