高中化学苏教版必修二专题1 微观结构与物质的多样性第三单元从微观结构看物质的多样性ppt(30张)
文档属性
| 名称 | 高中化学苏教版必修二专题1 微观结构与物质的多样性第三单元从微观结构看物质的多样性ppt(30张) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-01-02 00:00:00 | ||
图片预览








文档简介
C60(足球烯)
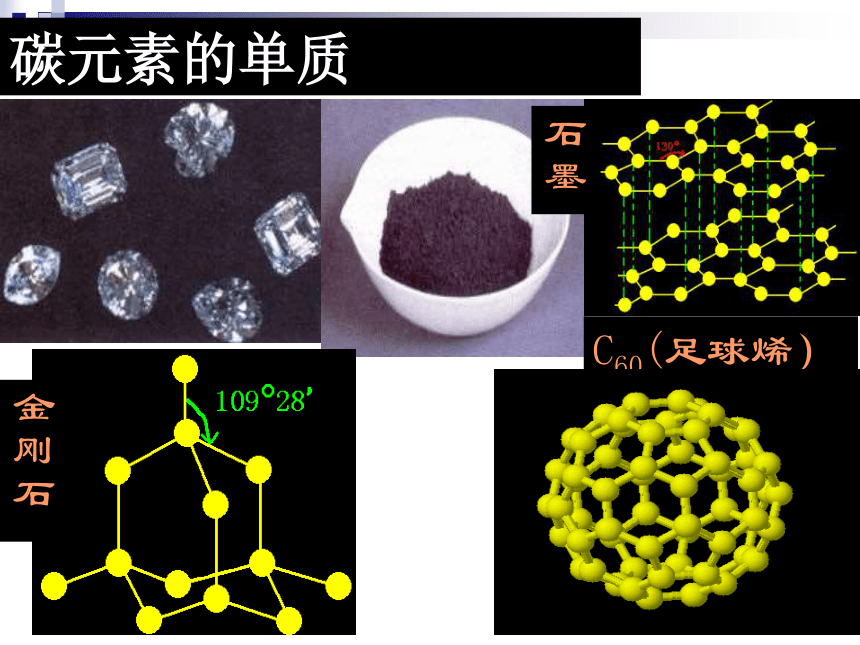
碳元素的单质
金刚石是正四面体空间网状结构,原子间的作用力很强
石墨是层状结构,层间分子间作用力弱,所以层与层间易滑动
金刚石和石墨物理性质的差异,主要是由于碳原子排列结构的不同引起的
其中C60是60个碳原子形成的封闭笼状分子,形似足球,故称之为“足球烯”)
富勒烯:固态碳的第三种结构形式,三维空心球状结构。(包括C60、C70和纳米碳管等)
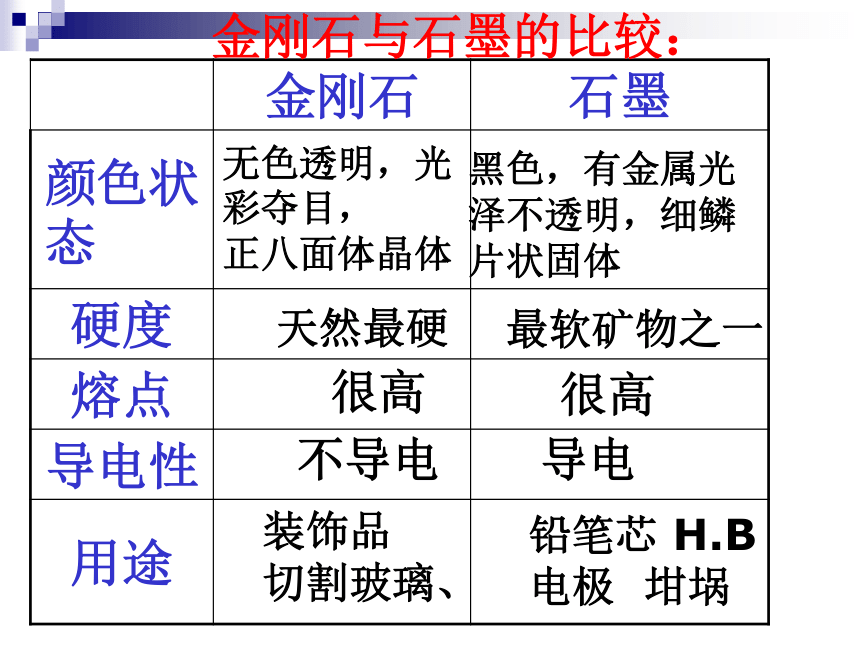
无色透明,光彩夺目,
正八面体晶体
黑色,有金属光
泽不透明,细鳞
片状固体
天然最硬
最软矿物之一
很高
很高
导电
不导电
装饰品
切割玻璃、
铅笔芯 H.B
电极 坩埚
金刚石与石墨的比较:
金刚石 石墨
颜色状态
硬度
熔点
导电性
用途
同素异形体:同一种元
素形成的不同单质 。
强调:(1)同种元素
(2)不同单质
(组成或结构不同)
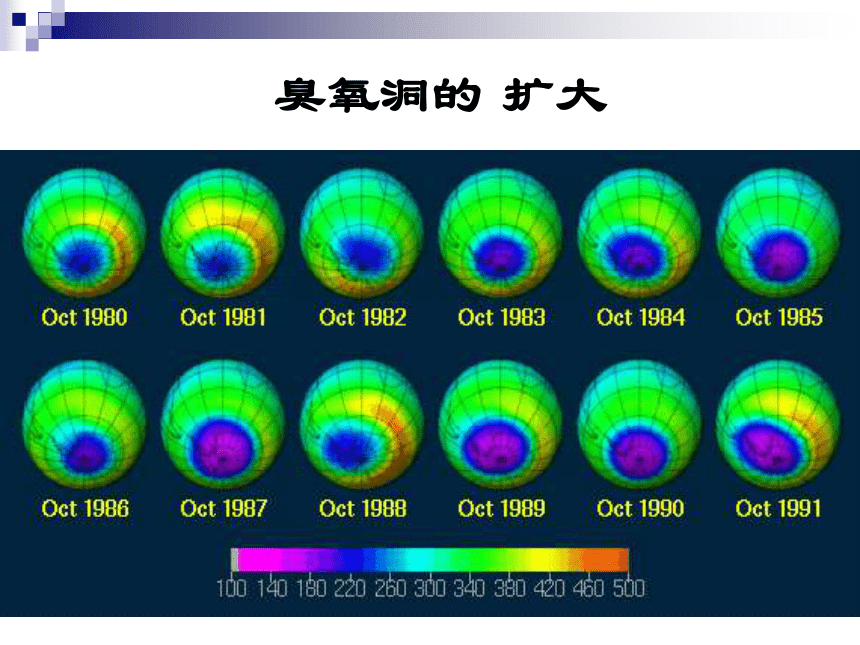
臭氧与氧气的性质对比
3O2 == 2O3
放电
臭氧洞的 扩大
白色或浅黄色蜡状固体,剧毒。不溶于水,易于二硫化碳,着火点是40OC,熔点44OC,隔绝空气260OC得红磷.
白磷:
暗红色粉末,无毒,不溶于水也不溶于二硫化碳,着火点246OC、416OC升华(隔绝空气)气体骤冷后得白磷。
红磷:
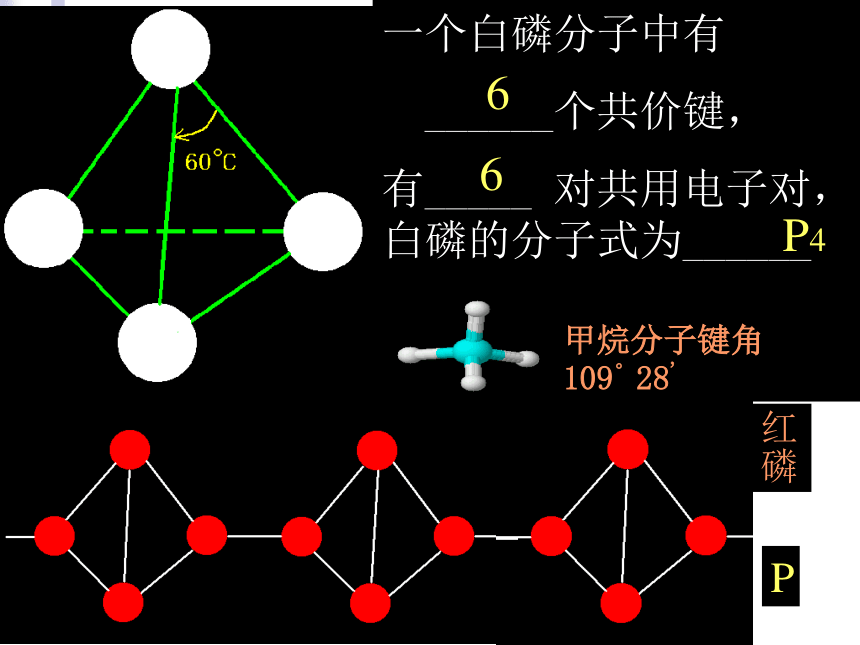
一个白磷分子中有
______个共价键,
有_____ 对共用电子对,白磷的分子式为______
6
6
P4
红磷
P
甲烷分子键角109°28'
KClO3、MnO2、 S
红磷、Sb2S3
判断下面哪些是同素异形体( ),哪些是同位素( )
A.红磷、白磷
B.水、重水
C.16O、17O、18O
D.金刚石、石墨
比较:正丁烷与异丁烷
4
4
10
10
直链
支链
C4H10
C4H10
正丁烷 异丁烷
球棍模型
碳原子数目
氢原子数目
碳链的形式
分子式
化合物具有相同的分子式,但具有不同结构的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
2、同分异构体
同分异构现象
有下列各组物质: A、 6C与6C
B、金刚石与石墨 C、乙醇与二甲醚
D、
(1)互为同位素的是________
(2)互为同素异形体的是________
(3)互为同分异构体的是______
(4)互为同一物质的是________
12
13
A
B
CD
E
不同类型的晶体
一、离子晶体
定义:
实例:
食盐、
氯化铯
物理性质:
形成离子晶体的物质:
像氯化钠、氯化铯这样离子间通过
离子键结合而成的晶体叫做离子晶体。
具有较高的熔沸点,在熔融状态或水溶液
中能导电,有些离子晶体溶于水,有些难溶于水
KOH 、 CuSO4、
NH4Cl 、 CaO、等离子化合物
下一页
返回
二、分子晶体
分子晶体:
分子晶体的物理性质:
定义:
实例:如干冰、冰等共价化合物
形成分子晶体的物质:
熔、沸点低,硬度小,在水
中的溶解度存在很大的差异。
H2、Cl2、He 、HCl 、H2O、CO2等
分子间通过分子间作用力相
结合的晶体,叫做分子晶体。
讨论:
2、 CO2和SiO2的一些物理性质如下表所示,通过比较判断SiO2晶体是否属于分子晶体。
熔 点 沸 点
干 冰(CO2) -56.2℃ -78.4℃
SiO2 1723℃ 2230℃
1比较碘晶体与溴晶体 冰与硫化氢晶体
的熔点,并解析原因。
干冰晶体结构示意
每个二氧化碳分子周围有12CO2
二氧化硅晶体
三、原子晶体
定义:
实例:
原子晶体的物理性质:
如二氧化硅晶体、
金刚石
常见的原子晶体:
熔沸点很高,硬度很大,难溶于水,
一般不导电。
金刚石、金刚砂(SiC)、
晶体硅、石英(SiO2)
这种相邻原子通过共价键结合而形成
空间网状结构的晶体,叫做原子晶体。
Si
o
共价键
返回
109?28?
共价键
返回
四、金属晶体
1、概念:通过金属离子与自由电子之间的较强的相互作用形成的晶体。
2、实例:金属单质都是金属晶体。
3、共同的物理性质:导电性、导热性、延展性 。在金属晶体中,金属阳离子半径越小,电荷数越大,金属键越强,该金属的熔点越高。
4、结构特点:
(1)在晶体中,不存在单个分子
(2)金属阳离子被自由电子所包围
晶型的变化(以第三周期为例)
金属晶体
原子
晶体
分子晶体
离子晶体
原子
晶体
分子晶体
单质 Na Mg Al Si P S8 Cl2 Ar
熔点℃ 97.8 651 660 1410 44 112.8 -101 -189.2
沸点℃ 989.8 1107 2467 2355 280 444.6 -34.6 -185.7
晶型
氧化物 Na2O MgO Al2O3 SiO2 P2O5 SO3 Cl2O7
熔点℃ 920 2820 2027 1700 24 16.9 -91.5
晶型
液晶是一种介于晶体和液体之间的中间态物质。液晶兼有液体和晶体的某些特点,表现出一些独特的性质,通常只有那些分子较大、分子形状呈长形或碟形的物质,才易形成液晶态。液晶应用十分广泛。
碳元素的单质
金刚石是正四面体空间网状结构,原子间的作用力很强
石墨是层状结构,层间分子间作用力弱,所以层与层间易滑动
金刚石和石墨物理性质的差异,主要是由于碳原子排列结构的不同引起的
其中C60是60个碳原子形成的封闭笼状分子,形似足球,故称之为“足球烯”)
富勒烯:固态碳的第三种结构形式,三维空心球状结构。(包括C60、C70和纳米碳管等)
无色透明,光彩夺目,
正八面体晶体
黑色,有金属光
泽不透明,细鳞
片状固体
天然最硬
最软矿物之一
很高
很高
导电
不导电
装饰品
切割玻璃、
铅笔芯 H.B
电极 坩埚
金刚石与石墨的比较:
金刚石 石墨
颜色状态
硬度
熔点
导电性
用途
同素异形体:同一种元
素形成的不同单质 。
强调:(1)同种元素
(2)不同单质
(组成或结构不同)
臭氧与氧气的性质对比
3O2 == 2O3
放电
臭氧洞的 扩大
白色或浅黄色蜡状固体,剧毒。不溶于水,易于二硫化碳,着火点是40OC,熔点44OC,隔绝空气260OC得红磷.
白磷:
暗红色粉末,无毒,不溶于水也不溶于二硫化碳,着火点246OC、416OC升华(隔绝空气)气体骤冷后得白磷。
红磷:
一个白磷分子中有
______个共价键,
有_____ 对共用电子对,白磷的分子式为______
6
6
P4
红磷
P
甲烷分子键角109°28'
KClO3、MnO2、 S
红磷、Sb2S3
判断下面哪些是同素异形体( ),哪些是同位素( )
A.红磷、白磷
B.水、重水
C.16O、17O、18O
D.金刚石、石墨
比较:正丁烷与异丁烷
4
4
10
10
直链
支链
C4H10
C4H10
正丁烷 异丁烷
球棍模型
碳原子数目
氢原子数目
碳链的形式
分子式
化合物具有相同的分子式,但具有不同结构的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
2、同分异构体
同分异构现象
有下列各组物质: A、 6C与6C
B、金刚石与石墨 C、乙醇与二甲醚
D、
(1)互为同位素的是________
(2)互为同素异形体的是________
(3)互为同分异构体的是______
(4)互为同一物质的是________
12
13
A
B
CD
E
不同类型的晶体
一、离子晶体
定义:
实例:
食盐、
氯化铯
物理性质:
形成离子晶体的物质:
像氯化钠、氯化铯这样离子间通过
离子键结合而成的晶体叫做离子晶体。
具有较高的熔沸点,在熔融状态或水溶液
中能导电,有些离子晶体溶于水,有些难溶于水
KOH 、 CuSO4、
NH4Cl 、 CaO、等离子化合物
下一页
返回
二、分子晶体
分子晶体:
分子晶体的物理性质:
定义:
实例:如干冰、冰等共价化合物
形成分子晶体的物质:
熔、沸点低,硬度小,在水
中的溶解度存在很大的差异。
H2、Cl2、He 、HCl 、H2O、CO2等
分子间通过分子间作用力相
结合的晶体,叫做分子晶体。
讨论:
2、 CO2和SiO2的一些物理性质如下表所示,通过比较判断SiO2晶体是否属于分子晶体。
熔 点 沸 点
干 冰(CO2) -56.2℃ -78.4℃
SiO2 1723℃ 2230℃
1比较碘晶体与溴晶体 冰与硫化氢晶体
的熔点,并解析原因。
干冰晶体结构示意
每个二氧化碳分子周围有12CO2
二氧化硅晶体
三、原子晶体
定义:
实例:
原子晶体的物理性质:
如二氧化硅晶体、
金刚石
常见的原子晶体:
熔沸点很高,硬度很大,难溶于水,
一般不导电。
金刚石、金刚砂(SiC)、
晶体硅、石英(SiO2)
这种相邻原子通过共价键结合而形成
空间网状结构的晶体,叫做原子晶体。
Si
o
共价键
返回
109?28?
共价键
返回
四、金属晶体
1、概念:通过金属离子与自由电子之间的较强的相互作用形成的晶体。
2、实例:金属单质都是金属晶体。
3、共同的物理性质:导电性、导热性、延展性 。在金属晶体中,金属阳离子半径越小,电荷数越大,金属键越强,该金属的熔点越高。
4、结构特点:
(1)在晶体中,不存在单个分子
(2)金属阳离子被自由电子所包围
晶型的变化(以第三周期为例)
金属晶体
原子
晶体
分子晶体
离子晶体
原子
晶体
分子晶体
单质 Na Mg Al Si P S8 Cl2 Ar
熔点℃ 97.8 651 660 1410 44 112.8 -101 -189.2
沸点℃ 989.8 1107 2467 2355 280 444.6 -34.6 -185.7
晶型
氧化物 Na2O MgO Al2O3 SiO2 P2O5 SO3 Cl2O7
熔点℃ 920 2820 2027 1700 24 16.9 -91.5
晶型
液晶是一种介于晶体和液体之间的中间态物质。液晶兼有液体和晶体的某些特点,表现出一些独特的性质,通常只有那些分子较大、分子形状呈长形或碟形的物质,才易形成液晶态。液晶应用十分广泛。
