二氧化硫的性质和作用
图片预览











文档简介
课件30张PPT。
化学必修一
专题四
含硫化合物的性质和应用之二氧化硫的性质和作用制作人:张微微说课内容说教材(说教材的作用地位,说教学目标,说教学重难点)
说教法
说学法
说教学过程
说教学反馈
说板书设计
说教材.在教材中的地位和作用
它是高中教材详细讲述氧化性,还原性于一身的酸性氧化物。它是在学生学习了氯,溴,碘,硅,纳,镁,铝,铁,铜及其化合物的基础上进一步认识的一种重要的非金属元素。同时,学生在初三已初步了解了酸雨与二氧化硫的联系。本节课是在此基础上进一步认识二氧化硫的其它重要性质和作用.使学生系统的形成元素化合物的知识网络.二.说教学目标
1.知识技能目标
了解酸雨的成因,危害和防治措施. 了解二氧化硫的物理性质.
掌握二氧化硫的化学性质.
2.过程与方法目标
使用”问题为索引,学生为主体”的学习方法.使学生初步学会从实验推导化学性质的学习方法,培养学生的观察分析能力.3.情感态度与价值观目标
通过认识酸雨的危害和防治措施培养学生的环保意识,使学生形成与大自然友好相处的正确认识.
通过做实验让学生领略实验学习乐趣,培养学生实事求是的科学态度,体验个人及学科价值.
三.说教学重难点
重点:二氧化硫的化学性质.
难点:二氧化硫的漂白性质.
酸雨的成因
实验现象的分析和归纳说教法 学情分析:经过半个多学期的学习和初高中的衔接磨合,高一学生已经具备学习元素化合物知识的基础,初步掌握某些基本实验技能,思维活跃,对化学有着浓厚的兴趣,特采取以下方法:
1,情境激趣法:运用多媒体,创设问题情境,调动学生内在的学习动力,促使学生在意境中主动探究科学的奥妙.
2,实验促学法:通过老师的演示,学生的协助,让学生观察分析实验现象,掌握其中化学性质.
3,讨论总结法:通过讨论分析,最终总结二氧化硫的有关化学性质.
说学法我们的学生素质比较高,有强烈求知欲,思维能力渐趋成熟.但也有思维方面的劣势,他们习惯演绎式的教学方法,但是学生经过前面几个专题的学习,对采用探究法研究化学已有一定的基础,同时,对二氧化硫与酸雨的联系也有一定的了解.在活动中学生相互交流,相互讨论,相互评价,成为课堂的主体.说教学程序 (一)被冠以”空中死神””空中杀手”称号的物质是谁.设置疑问,导入新课.同时用多媒体展示二氧化硫造成全球性污染的有关录像.
(二)让学生观察一小瓶矿泉水瓶中的二氧化硫,描述物理性质.强调闻气味的正确方法.
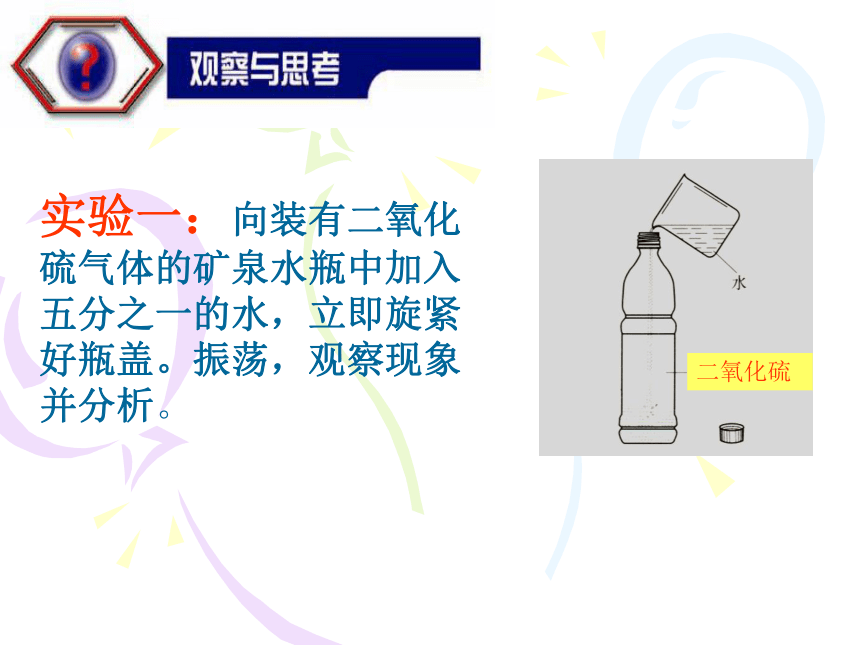
(三)由老师演示,学生协助完成课本”观察与思考”栏目中的实验【实验一】用充满80mL二氧化硫的针筒吸入10mL蒸馏水,用橡皮塞堵住针筒的前端,振荡,观察针筒内气体体积的变化.然后用pH试纸测定二氧化硫水溶液的pH.【实验二】想试管中加入5mL二氧化硫水溶液,滴加品红溶液,振荡,然后加热试管,观察加热前后溶液颜色的变化.【实验三】向另一支试管中加入5mL二氧化硫水溶液,滴加氯化钡溶液,再滴加0.5mL3%的过氧化氢溶液,振荡,放置片刻后滴加稀盐酸,观察实验现象.实验现象:矿泉水瓶 瘪了。实验结论: SO2易溶于水现象分析:由于SO2易溶液于水,使瓶内压强减小,大气压把矿泉水瓶压扁了。 实验过程: 用玻璃棒沾取SO2水溶液于PH试纸测该溶液的PH值。类比CO2与水的反应。实验现象:溶液PH值<7 实验结论: SO2溶于水,实质上有部分与水发生了化学反应且生成了酸。SO2+H20 H2SO3(亚硫酸)实验二:
1.滴管中吸有品红溶液1~2mL
2.试管装满气体,气球胀大了
3.压挤滴管,品红溶液滴下,振荡试管,观察现象.
4.加热试管底部,观察溶液颜色的变化.
实验现象: 滴入品色溶液时,气球瘪了,品红溶液褪色了; 加热后,气球又胀大了,品红溶液又恢复红色了。 实验结论: SO2具有漂白性(可逆性)用SO2漂白过的新旧报纸 等物质量的SO2和Cl2同时通入品红溶液,漂白效果是否增强?
思考: 从二氧化硫中硫的化合价 分析,SO2是否具有还原性?实验三 :
SO2水溶液中滴加几滴BaCl2溶液,再加入1~2mLH2O2 水溶液,观察现象实验现象:开始时产生少量白色沉淀,加入H2O2后白色沉淀增多。为什么会出现这种现象?请同学们大胆的猜测,并试着写出方程式 实验结论:
SO2具有还原性
2H2SO3+ O2 = 2H2SO4
SO2 + H2O2 = H2SO4
H2SO4 +BaCl2 = BaSO4↓ + 2HCl(四).通过幻灯片图示,介绍硫酸型酸雨的形成原因,引导学生书写化学方程式.
最后,请学生欣赏迈克尔.杰克逊的经典之作”地球之歌”.通过震撼人心的画面,声嘶力竭的呼吁,让学生真切的体会到地球面临的严峻考验和全球环保的重要性,让我们一起来拯救地球.说教学反馈由老师引导,学生书写方程式的形式完成课堂小结.
老师当堂出一些题目让学生做,达到巩固知识的目的.
老师布置课后作业.1、下列关于SO2的说法中错误的是( )
A. SO2是一种无色,有刺激性气味的
有毒气体
B. SO2能使紫色的石蕊变红色
C. SO2只有还原性
D. SO2能与CaO反应生成CaSO3C2.下列物质做干燥剂可干燥SO2的是( )
A.生石灰(固体CaO)
B.NaOH固体
C.碱石灰(固体CaO和NaOH的混合物)
D.浓硫酸D 3、下列气体之中,能污染大气,但可以被碱溶液吸收的是( )
A、CO B、Cl2
C、SO2 D、N2B C4、在下列变化中,不属于化学变化的
是( )
A、SO2使品红溶液褪色
B、氯水使有色布条褪色
C、活性炭使红墨水褪色
D、O3使某些染料褪色
C布置作业:
1、练习:课本P95 1、3
2、书面作业:课本P95 5、6
3、调查研究:
上网查资料:了解酸雨的形成原因、危害和防治方法。
说板书设计二氧化硫的性质
物理性质:无色,有刺激性气味,易溶于水的气体。
化学性质:
1)氧化性:SO2+H2S=3S+2H2O
2)还原性:2SO2+O2=2SO3
3)漂白性:使品红溶液褪色。
酸雨的来源:化石燃料燃烧,含硫矿石的冶炼和硫酸,磷肥,纸浆生产的工业废气。
危害——形成酸雨(Ph<5.6)SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4
2SO2+O2=2SO3 SO3+H2O=H2SO4
防治——净化和回收
Thank you for your attention
专题四
含硫化合物的性质和应用之二氧化硫的性质和作用制作人:张微微说课内容说教材(说教材的作用地位,说教学目标,说教学重难点)
说教法
说学法
说教学过程
说教学反馈
说板书设计
说教材.在教材中的地位和作用
它是高中教材详细讲述氧化性,还原性于一身的酸性氧化物。它是在学生学习了氯,溴,碘,硅,纳,镁,铝,铁,铜及其化合物的基础上进一步认识的一种重要的非金属元素。同时,学生在初三已初步了解了酸雨与二氧化硫的联系。本节课是在此基础上进一步认识二氧化硫的其它重要性质和作用.使学生系统的形成元素化合物的知识网络.二.说教学目标
1.知识技能目标
了解酸雨的成因,危害和防治措施. 了解二氧化硫的物理性质.
掌握二氧化硫的化学性质.
2.过程与方法目标
使用”问题为索引,学生为主体”的学习方法.使学生初步学会从实验推导化学性质的学习方法,培养学生的观察分析能力.3.情感态度与价值观目标
通过认识酸雨的危害和防治措施培养学生的环保意识,使学生形成与大自然友好相处的正确认识.
通过做实验让学生领略实验学习乐趣,培养学生实事求是的科学态度,体验个人及学科价值.
三.说教学重难点
重点:二氧化硫的化学性质.
难点:二氧化硫的漂白性质.
酸雨的成因
实验现象的分析和归纳说教法 学情分析:经过半个多学期的学习和初高中的衔接磨合,高一学生已经具备学习元素化合物知识的基础,初步掌握某些基本实验技能,思维活跃,对化学有着浓厚的兴趣,特采取以下方法:
1,情境激趣法:运用多媒体,创设问题情境,调动学生内在的学习动力,促使学生在意境中主动探究科学的奥妙.
2,实验促学法:通过老师的演示,学生的协助,让学生观察分析实验现象,掌握其中化学性质.
3,讨论总结法:通过讨论分析,最终总结二氧化硫的有关化学性质.
说学法我们的学生素质比较高,有强烈求知欲,思维能力渐趋成熟.但也有思维方面的劣势,他们习惯演绎式的教学方法,但是学生经过前面几个专题的学习,对采用探究法研究化学已有一定的基础,同时,对二氧化硫与酸雨的联系也有一定的了解.在活动中学生相互交流,相互讨论,相互评价,成为课堂的主体.说教学程序 (一)被冠以”空中死神””空中杀手”称号的物质是谁.设置疑问,导入新课.同时用多媒体展示二氧化硫造成全球性污染的有关录像.
(二)让学生观察一小瓶矿泉水瓶中的二氧化硫,描述物理性质.强调闻气味的正确方法.
(三)由老师演示,学生协助完成课本”观察与思考”栏目中的实验【实验一】用充满80mL二氧化硫的针筒吸入10mL蒸馏水,用橡皮塞堵住针筒的前端,振荡,观察针筒内气体体积的变化.然后用pH试纸测定二氧化硫水溶液的pH.【实验二】想试管中加入5mL二氧化硫水溶液,滴加品红溶液,振荡,然后加热试管,观察加热前后溶液颜色的变化.【实验三】向另一支试管中加入5mL二氧化硫水溶液,滴加氯化钡溶液,再滴加0.5mL3%的过氧化氢溶液,振荡,放置片刻后滴加稀盐酸,观察实验现象.实验现象:矿泉水瓶 瘪了。实验结论: SO2易溶于水现象分析:由于SO2易溶液于水,使瓶内压强减小,大气压把矿泉水瓶压扁了。 实验过程: 用玻璃棒沾取SO2水溶液于PH试纸测该溶液的PH值。类比CO2与水的反应。实验现象:溶液PH值<7 实验结论: SO2溶于水,实质上有部分与水发生了化学反应且生成了酸。SO2+H20 H2SO3(亚硫酸)实验二:
1.滴管中吸有品红溶液1~2mL
2.试管装满气体,气球胀大了
3.压挤滴管,品红溶液滴下,振荡试管,观察现象.
4.加热试管底部,观察溶液颜色的变化.
实验现象: 滴入品色溶液时,气球瘪了,品红溶液褪色了; 加热后,气球又胀大了,品红溶液又恢复红色了。 实验结论: SO2具有漂白性(可逆性)用SO2漂白过的新旧报纸 等物质量的SO2和Cl2同时通入品红溶液,漂白效果是否增强?
思考: 从二氧化硫中硫的化合价 分析,SO2是否具有还原性?实验三 :
SO2水溶液中滴加几滴BaCl2溶液,再加入1~2mLH2O2 水溶液,观察现象实验现象:开始时产生少量白色沉淀,加入H2O2后白色沉淀增多。为什么会出现这种现象?请同学们大胆的猜测,并试着写出方程式 实验结论:
SO2具有还原性
2H2SO3+ O2 = 2H2SO4
SO2 + H2O2 = H2SO4
H2SO4 +BaCl2 = BaSO4↓ + 2HCl(四).通过幻灯片图示,介绍硫酸型酸雨的形成原因,引导学生书写化学方程式.
最后,请学生欣赏迈克尔.杰克逊的经典之作”地球之歌”.通过震撼人心的画面,声嘶力竭的呼吁,让学生真切的体会到地球面临的严峻考验和全球环保的重要性,让我们一起来拯救地球.说教学反馈由老师引导,学生书写方程式的形式完成课堂小结.
老师当堂出一些题目让学生做,达到巩固知识的目的.
老师布置课后作业.1、下列关于SO2的说法中错误的是( )
A. SO2是一种无色,有刺激性气味的
有毒气体
B. SO2能使紫色的石蕊变红色
C. SO2只有还原性
D. SO2能与CaO反应生成CaSO3C2.下列物质做干燥剂可干燥SO2的是( )
A.生石灰(固体CaO)
B.NaOH固体
C.碱石灰(固体CaO和NaOH的混合物)
D.浓硫酸D 3、下列气体之中,能污染大气,但可以被碱溶液吸收的是( )
A、CO B、Cl2
C、SO2 D、N2B C4、在下列变化中,不属于化学变化的
是( )
A、SO2使品红溶液褪色
B、氯水使有色布条褪色
C、活性炭使红墨水褪色
D、O3使某些染料褪色
C布置作业:
1、练习:课本P95 1、3
2、书面作业:课本P95 5、6
3、调查研究:
上网查资料:了解酸雨的形成原因、危害和防治方法。
说板书设计二氧化硫的性质
物理性质:无色,有刺激性气味,易溶于水的气体。
化学性质:
1)氧化性:SO2+H2S=3S+2H2O
2)还原性:2SO2+O2=2SO3
3)漂白性:使品红溶液褪色。
酸雨的来源:化石燃料燃烧,含硫矿石的冶炼和硫酸,磷肥,纸浆生产的工业废气。
危害——形成酸雨(Ph<5.6)SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4
2SO2+O2=2SO3 SO3+H2O=H2SO4
防治——净化和回收
Thank you for your attention
