化学(苏教版选修3):《原子核外电子运动》(2)课件
文档属性
| 名称 | 化学(苏教版选修3):《原子核外电子运动》(2)课件 |
|
|
| 格式 | rar | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-01-19 00:00:00 | ||
图片预览







文档简介
课件36张PPT。核外电子的运动特征原子核外电子的运动1.原子是由哪些基本微粒构成的?
2.构成原子的各种微粒是否带有电荷?为什么原子是电中性的?
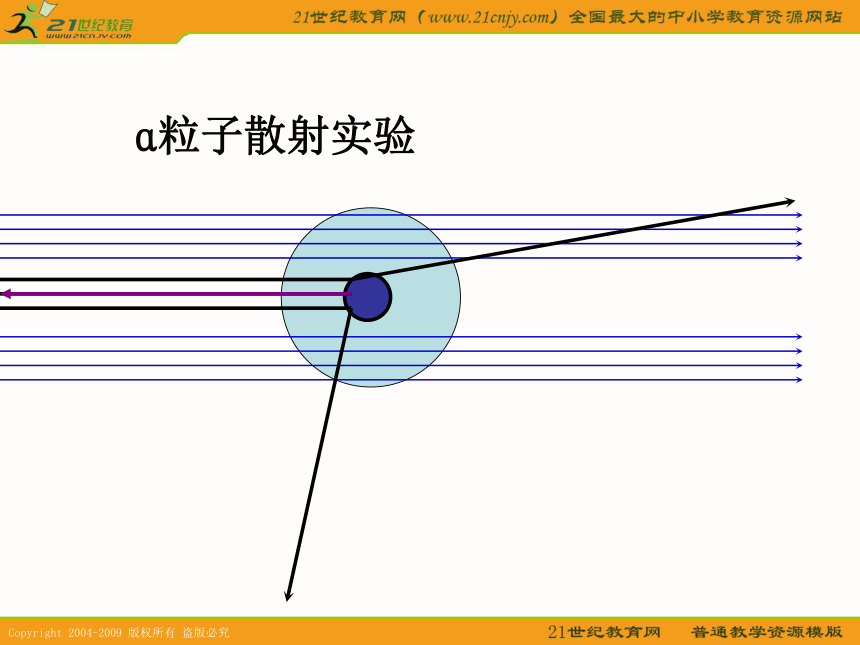
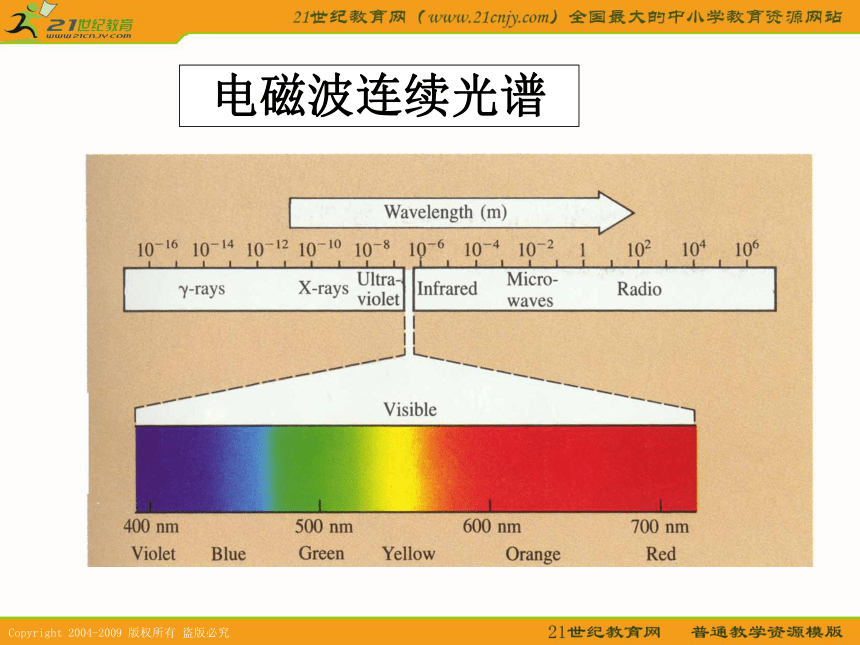
3.构成原子的各种微粒在数量上有什么规律?这些微粒的体积和质量有什么特点?你知道吗?1. 道尔顿原子模型 19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体,在化学反应中保持本性不变。一、原子结构的认识历史课堂求知互动2. 汤姆生原子模型 1897年,英国科学家汤姆生发现了电子。提出了“葡萄干面包式”模型。认为原子是可以再分的。3. 卢瑟福原子模型 1911年,英国物理学家卢瑟褔通过α粒子散射实验提出带核的原子结构模型。认为原子是由带正电荷的原子核和带负电核外电子构成。卢瑟福认为原子质量主要集中在原子核上,电子在原子核外空间高速运动。卢瑟福——原子之父α粒子散射实验连续光谱(自然界)连续光谱(实验室)电磁波连续光谱经典电磁理论不能解释氢原子光谱: 经典电磁理论:
电子绕核作高速圆周运动,
发出连续电磁波→ 连续光谱,
电子能量↓ → 坠入原子核→原子湮灭
事实:
氢原子光谱是线状(而不是连续光谱);
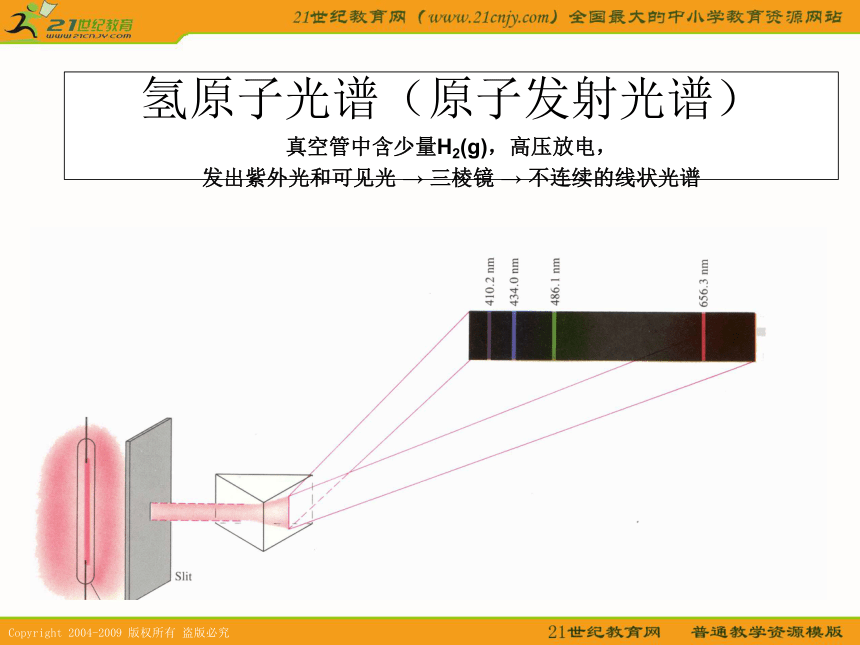
原子没有湮灭。氢原子光谱(原子发射光谱) 真空管中含少量H2(g),高压放电, 发出紫外光和可见光 → 三棱镜 → 不连续的线状光谱4.波尔原子模型 1913年,丹麦物理学家玻尔把普朗克的相关理论与卢瑟福的原子模型相结合,较好地解释了氢原子光谱,提出新的原子结构模型。
原子能级连续光谱和原子发射光谱(线状光谱)比较 波尔原子模型局限性 1. 只限于解释氢原子或类氢离子(单电子体系)的光谱,不能解释多电子原子的光谱。 2. 人为地允许某些物理量(电子运动的轨道角动量和电子能量)“量子化”,以修正经典力学(牛顿力学)。5. 电子云模型原子核外电子的运动状态(原子轨道)二、原子核外电子的排布相关知识链接原子核外电子的运动特征(电子云)原子核外电子的排布规律
1S电子在原子核外出现的概率分布图讨论:原子核外电子运动有哪些特征?人们按照图示的方法制作电子云的轮廓图常把电子出现的概率约为
90%的空间圈出来1.电子层1S 2SPZ d 轨道角度分布图(剖面图) S的原子轨道是________形的,电子层序数越大,原子轨道的________。2.原子轨道 P的原子轨道是________形的,每个P轨道有_______个轨道,它们互相垂直,分别以_____、______、_______为符号。P原子轨道的平均半径也随电子层序数增大而_____。 问题1:完成下面表格问题2: KLMNOP1s2s2p3s3p3d4s4p4d4f核 外 电 子 填 充 顺 序 图轨道能量顺序71.最低能量原理──电子在原子轨道上的排布,要尽可能使电子的能量最低。2.泡利不相容原理──每个原子轨道最多只能容纳两个电子,且自旋方向必须相反。原子核外电子排布的三大原理3.洪特规则──电子在等价轨道(能量相同的轨道)上排布时,总是尽可能分占不同的轨道,且自旋方向相同。这种排布,电子的能量最低。能级图针对训练写出下列元素原子结构示意图、电子排布式及其简化形式、外围电子排布式、电子轨道表示式: 根据洪特规则,人们总结出,当同一亚层轨道半充满、全充满以及全空时,是比较稳定的。洪特规则特例:全充满半充满全空本课总结:知识体系
2.构成原子的各种微粒是否带有电荷?为什么原子是电中性的?
3.构成原子的各种微粒在数量上有什么规律?这些微粒的体积和质量有什么特点?你知道吗?1. 道尔顿原子模型 19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体,在化学反应中保持本性不变。一、原子结构的认识历史课堂求知互动2. 汤姆生原子模型 1897年,英国科学家汤姆生发现了电子。提出了“葡萄干面包式”模型。认为原子是可以再分的。3. 卢瑟福原子模型 1911年,英国物理学家卢瑟褔通过α粒子散射实验提出带核的原子结构模型。认为原子是由带正电荷的原子核和带负电核外电子构成。卢瑟福认为原子质量主要集中在原子核上,电子在原子核外空间高速运动。卢瑟福——原子之父α粒子散射实验连续光谱(自然界)连续光谱(实验室)电磁波连续光谱经典电磁理论不能解释氢原子光谱: 经典电磁理论:
电子绕核作高速圆周运动,
发出连续电磁波→ 连续光谱,
电子能量↓ → 坠入原子核→原子湮灭
事实:
氢原子光谱是线状(而不是连续光谱);
原子没有湮灭。氢原子光谱(原子发射光谱) 真空管中含少量H2(g),高压放电, 发出紫外光和可见光 → 三棱镜 → 不连续的线状光谱4.波尔原子模型 1913年,丹麦物理学家玻尔把普朗克的相关理论与卢瑟福的原子模型相结合,较好地解释了氢原子光谱,提出新的原子结构模型。
原子能级连续光谱和原子发射光谱(线状光谱)比较 波尔原子模型局限性 1. 只限于解释氢原子或类氢离子(单电子体系)的光谱,不能解释多电子原子的光谱。 2. 人为地允许某些物理量(电子运动的轨道角动量和电子能量)“量子化”,以修正经典力学(牛顿力学)。5. 电子云模型原子核外电子的运动状态(原子轨道)二、原子核外电子的排布相关知识链接原子核外电子的运动特征(电子云)原子核外电子的排布规律
1S电子在原子核外出现的概率分布图讨论:原子核外电子运动有哪些特征?人们按照图示的方法制作电子云的轮廓图常把电子出现的概率约为
90%的空间圈出来1.电子层1S 2SPZ d 轨道角度分布图(剖面图) S的原子轨道是________形的,电子层序数越大,原子轨道的________。2.原子轨道 P的原子轨道是________形的,每个P轨道有_______个轨道,它们互相垂直,分别以_____、______、_______为符号。P原子轨道的平均半径也随电子层序数增大而_____。 问题1:完成下面表格问题2: KLMNOP1s2s2p3s3p3d4s4p4d4f核 外 电 子 填 充 顺 序 图轨道能量顺序71.最低能量原理──电子在原子轨道上的排布,要尽可能使电子的能量最低。2.泡利不相容原理──每个原子轨道最多只能容纳两个电子,且自旋方向必须相反。原子核外电子排布的三大原理3.洪特规则──电子在等价轨道(能量相同的轨道)上排布时,总是尽可能分占不同的轨道,且自旋方向相同。这种排布,电子的能量最低。能级图针对训练写出下列元素原子结构示意图、电子排布式及其简化形式、外围电子排布式、电子轨道表示式: 根据洪特规则,人们总结出,当同一亚层轨道半充满、全充满以及全空时,是比较稳定的。洪特规则特例:全充满半充满全空本课总结:知识体系
