第五单元 化学与社会发展
图片预览


文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
第五单元 化学与社会发展
第一节 化学与能源开发
一、基础练习:
1、化学电池是一种将___________直接转化为___________的装置。一节1号电池烂在地里,能使1 m2的土壤永久失去利用价值;一粒纽扣电池能使600 t水受污染,相当于一个人一生的水饮用量。废旧电池的乱扔乱放,会导致___________________。应该采取的措施有___________________。
2、氢能源的优点:__________________、___________________、____________________。
3、下列说法是否正确?正确的,在( )中打“√”,错误的,在( )中打“×”。
(1)太阳能、风能、地热能、波浪能和氢能等都是待开发利用的新能源( )
(2)化石燃料是一种永不枯竭的再生能源( ) (3)随意丢弃废旧电池会造成环境污染( )
(4)化学电源(池)是一种将化学能直接转化为电能的装置( )
(5)氢能是一种热值高、不会污染环境的理想“绿色能源”( )
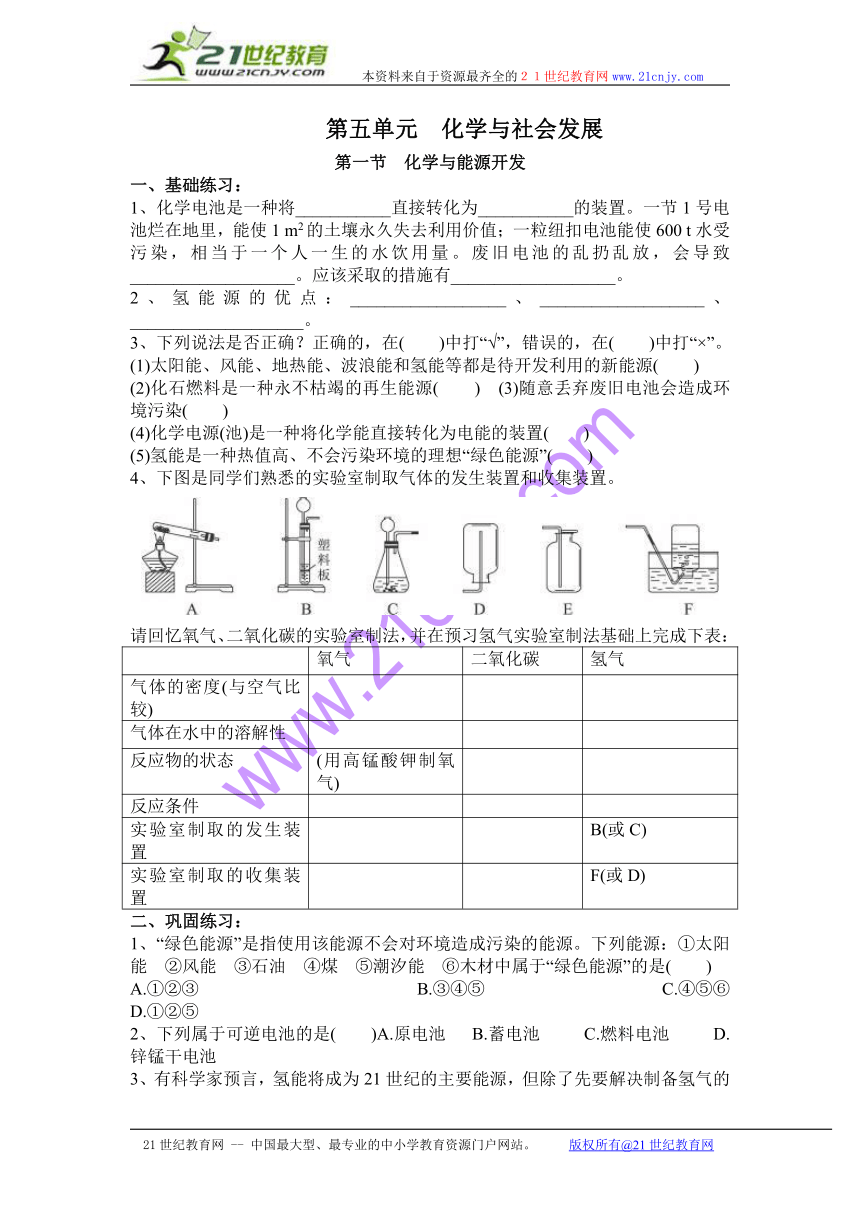
4、下图是同学们熟悉的实验室制取气体的发生装置和收集装置。
请回忆氧气、二氧化碳的实验室制法,并在预习氢气实验室制法基础上完成下表:
氧气 二氧化碳 氢气
气体的密度(与空气比较)
气体在水中的溶解性
反应物的状态 (用高锰酸钾制氧气)
反应条件
实验室制取的发生装置 B(或C)
实验室制取的收集装置 F(或D)
二、巩固练习:
1、“绿色能源”是指使用该能源不会对环境造成污染的能源。下列能源:①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材中属于“绿色能源”的是( )
A.①②③ B.③④⑤ C.④⑤⑥ D.①②⑤
2、下列属于可逆电池的是( )A.原电池 B.蓄电池 C.燃料电池 D.锌锰干电池
3、有科学家预言,氢能将成为21世纪的主要能源,但除了先要解决制备氢气的能源消耗问题之外,还必须解决的问题是( )
A.原料受到限制 B.造成环境污染 C.储存和运输不便 D.氢气燃烧放出的热量少
4、铅蓄电池是一种化学电源,它的正负极是分别浸在稀硫酸中的铜和二氧化铜,充电和放电时发生如下反应:Pb+PbO2+2H2SO4 2PbSO4+2H2O。放电过程中将__________能转变成___________能;充电过程则是将___________能转变成___________能。
5、按照“西气东输”计划,2003年底天然气进入南京。南京35万户管道煤气用户3年内全部用上天然气。
(1)煤气的主要成分CO燃烧的化学方程式为_________________________________;天然气的主要成分CH4燃烧的化学方程式为_________________________________。
(2)实验证明,在同温同压下,相同体积的任何气体中含有的分子数相同。则在同温同压下,相同体积的CO和CH4分别充分燃烧,消耗氧气较多的是___________。
(3)燃气灶由灶体、进燃气管、进空气管、电子开关等部件组成。目前的管道煤气用户改用天然气,必须对燃气灶加以改造。如果进燃气管的直径不变,改造后的燃气灶与原来的相比,进空气管的直径应___________(填“增大”或“减小”)。
6、目前,化石燃料是人类生产、生活中使用的主要能源。随着全球能源需求量的增长,化石燃料等不可再生能源将日趋枯竭。世界各国人民的节能意识也日趋增强(右图是我国的节能标志),科学家也正在开发新能源,研制节能产品,提高化学能的转化效率等方面积极努力地探索着。请你完成下列各题:
(1)有待继续开发、利用的能源有:______________________。
(2)用化学方程式表示出两个由化学能转化为热能的例子:
①________________________________;②_________________________________。
(3)生产、生活中存在着化学能和电能的相互转化,请你分别各举一例。
①由化学能转化为电能:________________________________;
②由电能转化为化学能:___________________________________。
(4)氢气具有热值高,且____________________的特点,因此被认为是最清洁的燃料。
7、有一乡村中学由于条件所限,仅有一大一小两种试管和稀硫酸,甲、乙两个学生找来铝制牙膏皮,各自设计了一种装置(如右图所示),制取并收集一试管氢气。
(1)哪个学生设计的装置较合适?___________,另一个学生装置设计的不合理原因是_______ __________________。
(2)用较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是_______________________________________。
(3)还可以用哪些物品代替废牙膏皮和稀硫酸完成实验?_____________________________。
三、提高训练
1、下列气体在空气中点燃前必须检查其纯度的是( )
A.H2 B.CO C.沼气 D.都必须要
2、煤矿井下禁止吸烟,以防点燃坑道内的可燃性气体而引起爆炸,这种可燃性的气体主要是( )A.氨气 B.甲烷 C.氢气 D.液化石油气
3、手机中使用的锂(Li)电池是新型的高能电池,某种锂电池的总反应可表示为Li+MnO2====LiMnO2。此反应中锂元素的化合价变化为0→+1,下列对锰元素的化合价变化判断正确的是( )
A.+4→+3 B.+2→+3 C.0→+2 C.-4→-2
4、 6月5日是“世界环境日”。我国的环保主题是“人人参与,创建绿色家园”。下列有关能源的开发和利用不符合该主题的是( )
A.氢能是理想的新型能源,它具有资源丰富、燃烧放热多、产物不污染环境等优点
B.为减少空气污染,应提倡使用乙醇汽油 C.开发和利用太阳能、水能、风能等能源
D.煤、石油、天然气等化石燃料为不可再生能源,应禁止使用
5、2003年4月,我国登山运动员再次登上世界屋脊——珠穆朗玛峰。登山运动员登山时所带的能源是氢化钙(CaH2),它能与水剧烈反应生成氢气和氢氧化钙,该反应的化学方程式为:________________________。
当登山运动员需要热量时,将上述反应中生成的氢气点燃,该过程中实现了能量转化,即___________能转化为___________能。
6、推广使用含10%乙醇的汽油,目的是开发石油替代资源,改善汽车尾气排放。常温下乙醇是一种能溶于水和汽油的液体,能在空气中燃烧。制取乙醇的方法是将淀粉水解生成葡萄糖(化学式为C6H12O6),葡萄糖在酶的作用下发生分解反应转化为乙醇(化学式为C2H5OH)和二氧化碳。另查资料知,纸张等含纤维素的物质也可水解生成葡萄糖。请根据上述信息完成下列问题:(1)总结乙醇的有关知识:
乙醇的物理性质:_______________________________________________________,
乙醇的化学性质(用化学方程式表示):______________________________________。
(2)写出葡萄糖转化为乙醇的化学方程式:_____ _____________________________。
7、供选择的仪器装置如下图所示(图中A—G为装置代号,①—⑧为仪器的接口符号)。供选择的药品有:金属钠、铜片、锌粒、炭粉、硝酸、稀硫酸。
完成下列问题:
(1)写出B装置中的仪器名称:甲___________,乙___________,丙___________。
(2)实验室制取氢气时,常选用的药品是___________和___________;发生反应的化学方程式为________________________________________。
(3)若一个学生选用盐酸为原料之一,则制得的氢气中会含有少量盐酸的酸雾,如让氢气通过装置(写装置代号)___________,酸雾即可除去,化学反应方程式为________________________;制取和收集的装置是(写装置代号)___________和___________。
(4)请正确连接氢气的制取、除酸雾和收集氢气的装置(写接口符号)___________接___________,___________接___________。
8、用如右图所示的装置制取氢气,在多孔塑料板上放锌粒,稀H2SO4由A中加入,若打开弹簧夹,酸液由A中流下与锌粒接触即发生反应,产生的氢气由支管导出,试完成下列问题:(1)仪器A的名称是_________。
(2)检查此装置的气密性时,关闭弹簧夹,从仪器A处注入适量的___________形成液封后,若看到仪器A内___________,则表明装置气密性良好。
(3)若关闭弹簧夹,容器内继续反应产生的氢气会使容器内___________,将酸液压回仪器A中,使酸液与锌粒___________,反应即自行停止。
(4)若氢气发生装置气密性良好,该同学用排水法收集一试管氢气,经检验不纯,你认为可能的原因是___________________________________。
(5)若在塑料隔板上放小块大理石,A中放稀HCl,___________(填“能”或“否”)用弹簧夹控制CO2的发生和停止。
9、有下列实验:用砂纸擦除铜片和锌片表面的氧化膜,再用导线将铜片和锌片连接到电流计的正、负极上,然后把锌片和铜片一起插入盛有CuSO4溶液的烧杯中(如右图所示)。试完成下列问题:
(1)可以观察到的现象有:①锌片逐渐溶解;②铜片上析出铜;③溶液蓝色逐渐变浅;
④电流表_______________________。
(2)实验中发生的能量变化形式是由___________能变为___________能,发生这种能量变化的化学方程式是_____________________________________。
10、从2001年起,我国积极推广乙醇汽油,它是由汽油和乙醇按一定比例混合而成。
(1)汽油主要含有碳、氢两种元素,它燃烧的主要产物是___________和_________。由于汽油中还含有少量硫、氮等元素,在燃烧过程中会产生少量二氧化硫及氮的氧化物等。
(2)粮食中的淀粉经过发酵可以得到乙醇。绿色植物通过_________把二氧化碳和水转化为淀粉,同时释放出___________。
(3)使用乙醇汽油的优点有哪些?(至少写出两点) , 。
第二节 化学与材料研制
一、基础练习
1、棉花、羊毛、蚕丝等属于( )
A.合成材料 B.天然纤维 C.复合材料 D.无机非金属材料
2、下列常见的材料中,属于金属材料的是( )
A.青铜 B.玻璃钢 C.陶瓷 D.聚乙烯塑料
3、常见的材料有金属材料、无机非金属材料、合成材料、复合材料四大类。请根据生活经验按下列要求各举两例:
(1)金属材料:____________、___________。(2)无机非金属材料:_____________、___________。
(3)合成材料:____________、___________。(4)复合材料:__________________、___________。
注意:金属材料指金属单质及其合金;无机非金属材料主要包括水泥、陶瓷、玻璃、光导纤维;合成材料主要指塑料、合成纤维、合成橡胶;复合材料是两种或两种以上材料组合而成的新型材料。
二、巩固练习:
1、在日常生活中,我们经常要用到以下物质,其中属于有机合成材料的是( )
A.棉花 B.塑料 C.羊毛 D.天然橡胶
2、日常生活中常见的下列物质,属于合成材料的是( )
A.毛皮 B.毛料西服 C.尼龙绳 D.天然橡胶
3、下列塑料产品中有热固性的是( )
A.防水手套 B.插座外壳 C.雨衣 D.浴帽
4、随着人们生活水平的提高,人类对材料的品种与性能的要求越来越高,对材料的认识也越来越科学。下列叙述中正确的是( )
A.塑料不属于合成有机高分子材料 B.棉线和羊毛都属于合成纤维
C.大部分塑料在自然环境中很难腐烂 D.橡胶在通常情况下不易燃烧
5、生产下列金属制品,各自利用了该金属的什么性质?
(1)铝壶、铁锅:_________。(2)铝制、铜制导线:__________。(3)铝合金门窗:_________。
6、下列说法是否正确?正确的,在( )中打“√”,错误的,在( )中打“×”。
(1)使用金属材料时,要特别注意防止金属锈蚀,以延长其使用寿命( )
(2)合成材料一般包括塑料、合成橡胶、合成纤维( ) (3)陶瓷材料是一种复合材料( )
(4)聚氯乙烯是一种常见塑料,它无毒可用于包装食品( )
(5)“白色污染”是由废弃难降解的塑料制品造成的( )
7、商场出售的服装都挂有面料成分及洗涤说明的标签,右图为某服装的标签。试完成下列问题:(1)面料中的天然纤维是__________,合成纤维是_ _____。
(2)检验其主要成分为丝的简单方法是_______________________。
(3)你认为洗涤时应注意的事项是__________________________。
三、提高训练
1、下列物质所用的高分子材料,你认为具有热固性的是( )
A.塑料凉鞋 B.自行车内胎 C.电线外面的塑料护套 D.电视机外壳
2、下列材料中,能使海水淡化的高分子材料是( )
A.生物高分子材料 B.高分子分离膜 C.液晶高分子材料 D.复合材料
3、时装店里琳琅满目的服装布料中,属于合成材料的是( )
A.羊绒 B.棉布 C.涤纶 D.真丝绸
4、发展绿色食品,避免“白色污染”是保护环境、提高人类生存质量的主要措施,产生“白色污染”的是( )A.工业上的“三废” B.白色废弃物 C.空气污染物 D.塑料
5、塑料制品应用范围最广的是( )
A.建筑 B.包装 C.家具 D.交通
6、手放在一块被火烧烤的板上仍安然无恙,则制造这块板的材料和性质是( )
A.无机材料 透气 B.特殊钢板 耐高温 C.纳米碳板 溶点高 D.某种有机高分子材料 绝热
7、 2010年5月21日南宁市南国明珠歌剧院因电器线路短路火引燃了舞台上的可燃物酿成火灾。下列材料属于易燃物的是( )A.大理石 B.合成纤维 C.瓷砖 D.不锈钢
8、制造普通玻璃的原料是纯碱、石灰石、石英,反应原理是碳酸钠、碳酸钙在高温下分别跟石英反应生成硅酸盐(CaSiO3)。写出这两个反应的化学方程式。
; 。
9、不同的材料具有不同的性能,将下列材料具有的性能用短线连起来:
材料种类 相应的性能
①钢化玻璃 A.耐高温、耐腐蚀、强度大、抗震裂
②光导纤维 B.耐腐蚀、摩擦系数小
③聚四氟乙烯(塑料王) C.透光性能好、有折光性和色散性
④普通塑料 D.透明、高强度
⑤玻璃钢 E.质轻、易加工成型、不导电、不传热、抗腐蚀
10、有机合成材料的出现是材料发展史上的一次重大突破。人们常说的三大合成材料是指:___________、___________、___________。
11、有机高分子化合物的___________比较大,简称有机高分子。链状结构的高分子材料具有___________性,而多数网状结构的高分子材料一经加工成型就不会受热熔化,因而具有___________性。
12、我省宜春某麻纺厂生产的“XX牌”服饰以其美观大方、舒适,为消费者所喜爱。该品牌衬衫的面料成分为“75%苎麻,25%棉”,请问:
(1)该衬衫的纤维种类属于__________(填“天然纤维”或“合成纤维”)。
(2)要检验某服装是否用涤纶制成的该品牌衬衫的假冒产品,简便的方法是:______________。
13、 右图是费俊龙和聂海胜在“神舟”六号飞船中的照片,请你从化学的视角对“神六”飞船的有关信息进行思考并完成下列问题:
(1)航天员在太空中每人每天大约需要0.9 kg氧气、2.5 L水、0.6 kg食物,排出1.0 kg二氧化碳、1.8 kg水蒸气等。上述物质中,属于单质的是___________,属于化合物的是___________,属于混合物的是___________。
(2)“神六”飞船的外壳是用金属、玻璃、工程塑料等材料制成的。其中属于有机合成材料的是_________________________________。
(3)为了处理人体排出的CO2,飞船上采用了与氢氧化钠化学性质相似的氢氧化锂(LiOH)作为吸收剂。LiOH中锂元素的化合价是___________,飞船上LiOH吸收CO2的化学方程式是:_________________________________。
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
第五单元 化学与社会发展
第一节 化学与能源开发
一、基础练习:
1、化学电池是一种将___________直接转化为___________的装置。一节1号电池烂在地里,能使1 m2的土壤永久失去利用价值;一粒纽扣电池能使600 t水受污染,相当于一个人一生的水饮用量。废旧电池的乱扔乱放,会导致___________________。应该采取的措施有___________________。
2、氢能源的优点:__________________、___________________、____________________。
3、下列说法是否正确?正确的,在( )中打“√”,错误的,在( )中打“×”。
(1)太阳能、风能、地热能、波浪能和氢能等都是待开发利用的新能源( )
(2)化石燃料是一种永不枯竭的再生能源( ) (3)随意丢弃废旧电池会造成环境污染( )
(4)化学电源(池)是一种将化学能直接转化为电能的装置( )
(5)氢能是一种热值高、不会污染环境的理想“绿色能源”( )
4、下图是同学们熟悉的实验室制取气体的发生装置和收集装置。
请回忆氧气、二氧化碳的实验室制法,并在预习氢气实验室制法基础上完成下表:
氧气 二氧化碳 氢气
气体的密度(与空气比较)
气体在水中的溶解性
反应物的状态 (用高锰酸钾制氧气)
反应条件
实验室制取的发生装置 B(或C)
实验室制取的收集装置 F(或D)
二、巩固练习:
1、“绿色能源”是指使用该能源不会对环境造成污染的能源。下列能源:①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材中属于“绿色能源”的是( )
A.①②③ B.③④⑤ C.④⑤⑥ D.①②⑤
2、下列属于可逆电池的是( )A.原电池 B.蓄电池 C.燃料电池 D.锌锰干电池
3、有科学家预言,氢能将成为21世纪的主要能源,但除了先要解决制备氢气的能源消耗问题之外,还必须解决的问题是( )
A.原料受到限制 B.造成环境污染 C.储存和运输不便 D.氢气燃烧放出的热量少
4、铅蓄电池是一种化学电源,它的正负极是分别浸在稀硫酸中的铜和二氧化铜,充电和放电时发生如下反应:Pb+PbO2+2H2SO4 2PbSO4+2H2O。放电过程中将__________能转变成___________能;充电过程则是将___________能转变成___________能。
5、按照“西气东输”计划,2003年底天然气进入南京。南京35万户管道煤气用户3年内全部用上天然气。
(1)煤气的主要成分CO燃烧的化学方程式为_________________________________;天然气的主要成分CH4燃烧的化学方程式为_________________________________。
(2)实验证明,在同温同压下,相同体积的任何气体中含有的分子数相同。则在同温同压下,相同体积的CO和CH4分别充分燃烧,消耗氧气较多的是___________。
(3)燃气灶由灶体、进燃气管、进空气管、电子开关等部件组成。目前的管道煤气用户改用天然气,必须对燃气灶加以改造。如果进燃气管的直径不变,改造后的燃气灶与原来的相比,进空气管的直径应___________(填“增大”或“减小”)。
6、目前,化石燃料是人类生产、生活中使用的主要能源。随着全球能源需求量的增长,化石燃料等不可再生能源将日趋枯竭。世界各国人民的节能意识也日趋增强(右图是我国的节能标志),科学家也正在开发新能源,研制节能产品,提高化学能的转化效率等方面积极努力地探索着。请你完成下列各题:
(1)有待继续开发、利用的能源有:______________________。
(2)用化学方程式表示出两个由化学能转化为热能的例子:
①________________________________;②_________________________________。
(3)生产、生活中存在着化学能和电能的相互转化,请你分别各举一例。
①由化学能转化为电能:________________________________;
②由电能转化为化学能:___________________________________。
(4)氢气具有热值高,且____________________的特点,因此被认为是最清洁的燃料。
7、有一乡村中学由于条件所限,仅有一大一小两种试管和稀硫酸,甲、乙两个学生找来铝制牙膏皮,各自设计了一种装置(如右图所示),制取并收集一试管氢气。
(1)哪个学生设计的装置较合适?___________,另一个学生装置设计的不合理原因是_______ __________________。
(2)用较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是_______________________________________。
(3)还可以用哪些物品代替废牙膏皮和稀硫酸完成实验?_____________________________。
三、提高训练
1、下列气体在空气中点燃前必须检查其纯度的是( )
A.H2 B.CO C.沼气 D.都必须要
2、煤矿井下禁止吸烟,以防点燃坑道内的可燃性气体而引起爆炸,这种可燃性的气体主要是( )A.氨气 B.甲烷 C.氢气 D.液化石油气
3、手机中使用的锂(Li)电池是新型的高能电池,某种锂电池的总反应可表示为Li+MnO2====LiMnO2。此反应中锂元素的化合价变化为0→+1,下列对锰元素的化合价变化判断正确的是( )
A.+4→+3 B.+2→+3 C.0→+2 C.-4→-2
4、 6月5日是“世界环境日”。我国的环保主题是“人人参与,创建绿色家园”。下列有关能源的开发和利用不符合该主题的是( )
A.氢能是理想的新型能源,它具有资源丰富、燃烧放热多、产物不污染环境等优点
B.为减少空气污染,应提倡使用乙醇汽油 C.开发和利用太阳能、水能、风能等能源
D.煤、石油、天然气等化石燃料为不可再生能源,应禁止使用
5、2003年4月,我国登山运动员再次登上世界屋脊——珠穆朗玛峰。登山运动员登山时所带的能源是氢化钙(CaH2),它能与水剧烈反应生成氢气和氢氧化钙,该反应的化学方程式为:________________________。
当登山运动员需要热量时,将上述反应中生成的氢气点燃,该过程中实现了能量转化,即___________能转化为___________能。
6、推广使用含10%乙醇的汽油,目的是开发石油替代资源,改善汽车尾气排放。常温下乙醇是一种能溶于水和汽油的液体,能在空气中燃烧。制取乙醇的方法是将淀粉水解生成葡萄糖(化学式为C6H12O6),葡萄糖在酶的作用下发生分解反应转化为乙醇(化学式为C2H5OH)和二氧化碳。另查资料知,纸张等含纤维素的物质也可水解生成葡萄糖。请根据上述信息完成下列问题:(1)总结乙醇的有关知识:
乙醇的物理性质:_______________________________________________________,
乙醇的化学性质(用化学方程式表示):______________________________________。
(2)写出葡萄糖转化为乙醇的化学方程式:_____ _____________________________。
7、供选择的仪器装置如下图所示(图中A—G为装置代号,①—⑧为仪器的接口符号)。供选择的药品有:金属钠、铜片、锌粒、炭粉、硝酸、稀硫酸。
完成下列问题:
(1)写出B装置中的仪器名称:甲___________,乙___________,丙___________。
(2)实验室制取氢气时,常选用的药品是___________和___________;发生反应的化学方程式为________________________________________。
(3)若一个学生选用盐酸为原料之一,则制得的氢气中会含有少量盐酸的酸雾,如让氢气通过装置(写装置代号)___________,酸雾即可除去,化学反应方程式为________________________;制取和收集的装置是(写装置代号)___________和___________。
(4)请正确连接氢气的制取、除酸雾和收集氢气的装置(写接口符号)___________接___________,___________接___________。
8、用如右图所示的装置制取氢气,在多孔塑料板上放锌粒,稀H2SO4由A中加入,若打开弹簧夹,酸液由A中流下与锌粒接触即发生反应,产生的氢气由支管导出,试完成下列问题:(1)仪器A的名称是_________。
(2)检查此装置的气密性时,关闭弹簧夹,从仪器A处注入适量的___________形成液封后,若看到仪器A内___________,则表明装置气密性良好。
(3)若关闭弹簧夹,容器内继续反应产生的氢气会使容器内___________,将酸液压回仪器A中,使酸液与锌粒___________,反应即自行停止。
(4)若氢气发生装置气密性良好,该同学用排水法收集一试管氢气,经检验不纯,你认为可能的原因是___________________________________。
(5)若在塑料隔板上放小块大理石,A中放稀HCl,___________(填“能”或“否”)用弹簧夹控制CO2的发生和停止。
9、有下列实验:用砂纸擦除铜片和锌片表面的氧化膜,再用导线将铜片和锌片连接到电流计的正、负极上,然后把锌片和铜片一起插入盛有CuSO4溶液的烧杯中(如右图所示)。试完成下列问题:
(1)可以观察到的现象有:①锌片逐渐溶解;②铜片上析出铜;③溶液蓝色逐渐变浅;
④电流表_______________________。
(2)实验中发生的能量变化形式是由___________能变为___________能,发生这种能量变化的化学方程式是_____________________________________。
10、从2001年起,我国积极推广乙醇汽油,它是由汽油和乙醇按一定比例混合而成。
(1)汽油主要含有碳、氢两种元素,它燃烧的主要产物是___________和_________。由于汽油中还含有少量硫、氮等元素,在燃烧过程中会产生少量二氧化硫及氮的氧化物等。
(2)粮食中的淀粉经过发酵可以得到乙醇。绿色植物通过_________把二氧化碳和水转化为淀粉,同时释放出___________。
(3)使用乙醇汽油的优点有哪些?(至少写出两点) , 。
第二节 化学与材料研制
一、基础练习
1、棉花、羊毛、蚕丝等属于( )
A.合成材料 B.天然纤维 C.复合材料 D.无机非金属材料
2、下列常见的材料中,属于金属材料的是( )
A.青铜 B.玻璃钢 C.陶瓷 D.聚乙烯塑料
3、常见的材料有金属材料、无机非金属材料、合成材料、复合材料四大类。请根据生活经验按下列要求各举两例:
(1)金属材料:____________、___________。(2)无机非金属材料:_____________、___________。
(3)合成材料:____________、___________。(4)复合材料:__________________、___________。
注意:金属材料指金属单质及其合金;无机非金属材料主要包括水泥、陶瓷、玻璃、光导纤维;合成材料主要指塑料、合成纤维、合成橡胶;复合材料是两种或两种以上材料组合而成的新型材料。
二、巩固练习:
1、在日常生活中,我们经常要用到以下物质,其中属于有机合成材料的是( )
A.棉花 B.塑料 C.羊毛 D.天然橡胶
2、日常生活中常见的下列物质,属于合成材料的是( )
A.毛皮 B.毛料西服 C.尼龙绳 D.天然橡胶
3、下列塑料产品中有热固性的是( )
A.防水手套 B.插座外壳 C.雨衣 D.浴帽
4、随着人们生活水平的提高,人类对材料的品种与性能的要求越来越高,对材料的认识也越来越科学。下列叙述中正确的是( )
A.塑料不属于合成有机高分子材料 B.棉线和羊毛都属于合成纤维
C.大部分塑料在自然环境中很难腐烂 D.橡胶在通常情况下不易燃烧
5、生产下列金属制品,各自利用了该金属的什么性质?
(1)铝壶、铁锅:_________。(2)铝制、铜制导线:__________。(3)铝合金门窗:_________。
6、下列说法是否正确?正确的,在( )中打“√”,错误的,在( )中打“×”。
(1)使用金属材料时,要特别注意防止金属锈蚀,以延长其使用寿命( )
(2)合成材料一般包括塑料、合成橡胶、合成纤维( ) (3)陶瓷材料是一种复合材料( )
(4)聚氯乙烯是一种常见塑料,它无毒可用于包装食品( )
(5)“白色污染”是由废弃难降解的塑料制品造成的( )
7、商场出售的服装都挂有面料成分及洗涤说明的标签,右图为某服装的标签。试完成下列问题:(1)面料中的天然纤维是__________,合成纤维是_ _____。
(2)检验其主要成分为丝的简单方法是_______________________。
(3)你认为洗涤时应注意的事项是__________________________。
三、提高训练
1、下列物质所用的高分子材料,你认为具有热固性的是( )
A.塑料凉鞋 B.自行车内胎 C.电线外面的塑料护套 D.电视机外壳
2、下列材料中,能使海水淡化的高分子材料是( )
A.生物高分子材料 B.高分子分离膜 C.液晶高分子材料 D.复合材料
3、时装店里琳琅满目的服装布料中,属于合成材料的是( )
A.羊绒 B.棉布 C.涤纶 D.真丝绸
4、发展绿色食品,避免“白色污染”是保护环境、提高人类生存质量的主要措施,产生“白色污染”的是( )A.工业上的“三废” B.白色废弃物 C.空气污染物 D.塑料
5、塑料制品应用范围最广的是( )
A.建筑 B.包装 C.家具 D.交通
6、手放在一块被火烧烤的板上仍安然无恙,则制造这块板的材料和性质是( )
A.无机材料 透气 B.特殊钢板 耐高温 C.纳米碳板 溶点高 D.某种有机高分子材料 绝热
7、 2010年5月21日南宁市南国明珠歌剧院因电器线路短路火引燃了舞台上的可燃物酿成火灾。下列材料属于易燃物的是( )A.大理石 B.合成纤维 C.瓷砖 D.不锈钢
8、制造普通玻璃的原料是纯碱、石灰石、石英,反应原理是碳酸钠、碳酸钙在高温下分别跟石英反应生成硅酸盐(CaSiO3)。写出这两个反应的化学方程式。
; 。
9、不同的材料具有不同的性能,将下列材料具有的性能用短线连起来:
材料种类 相应的性能
①钢化玻璃 A.耐高温、耐腐蚀、强度大、抗震裂
②光导纤维 B.耐腐蚀、摩擦系数小
③聚四氟乙烯(塑料王) C.透光性能好、有折光性和色散性
④普通塑料 D.透明、高强度
⑤玻璃钢 E.质轻、易加工成型、不导电、不传热、抗腐蚀
10、有机合成材料的出现是材料发展史上的一次重大突破。人们常说的三大合成材料是指:___________、___________、___________。
11、有机高分子化合物的___________比较大,简称有机高分子。链状结构的高分子材料具有___________性,而多数网状结构的高分子材料一经加工成型就不会受热熔化,因而具有___________性。
12、我省宜春某麻纺厂生产的“XX牌”服饰以其美观大方、舒适,为消费者所喜爱。该品牌衬衫的面料成分为“75%苎麻,25%棉”,请问:
(1)该衬衫的纤维种类属于__________(填“天然纤维”或“合成纤维”)。
(2)要检验某服装是否用涤纶制成的该品牌衬衫的假冒产品,简便的方法是:______________。
13、 右图是费俊龙和聂海胜在“神舟”六号飞船中的照片,请你从化学的视角对“神六”飞船的有关信息进行思考并完成下列问题:
(1)航天员在太空中每人每天大约需要0.9 kg氧气、2.5 L水、0.6 kg食物,排出1.0 kg二氧化碳、1.8 kg水蒸气等。上述物质中,属于单质的是___________,属于化合物的是___________,属于混合物的是___________。
(2)“神六”飞船的外壳是用金属、玻璃、工程塑料等材料制成的。其中属于有机合成材料的是_________________________________。
(3)为了处理人体排出的CO2,飞船上采用了与氢氧化钠化学性质相似的氢氧化锂(LiOH)作为吸收剂。LiOH中锂元素的化合价是___________,飞船上LiOH吸收CO2的化学方程式是:_________________________________。
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
