哈尔滨平房区2018—2019学年度上学期期末调研测试八年级化学(带答案)
文档属性
| 名称 | 哈尔滨平房区2018—2019学年度上学期期末调研测试八年级化学(带答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-01-11 00:00:00 | ||
图片预览



文档简介
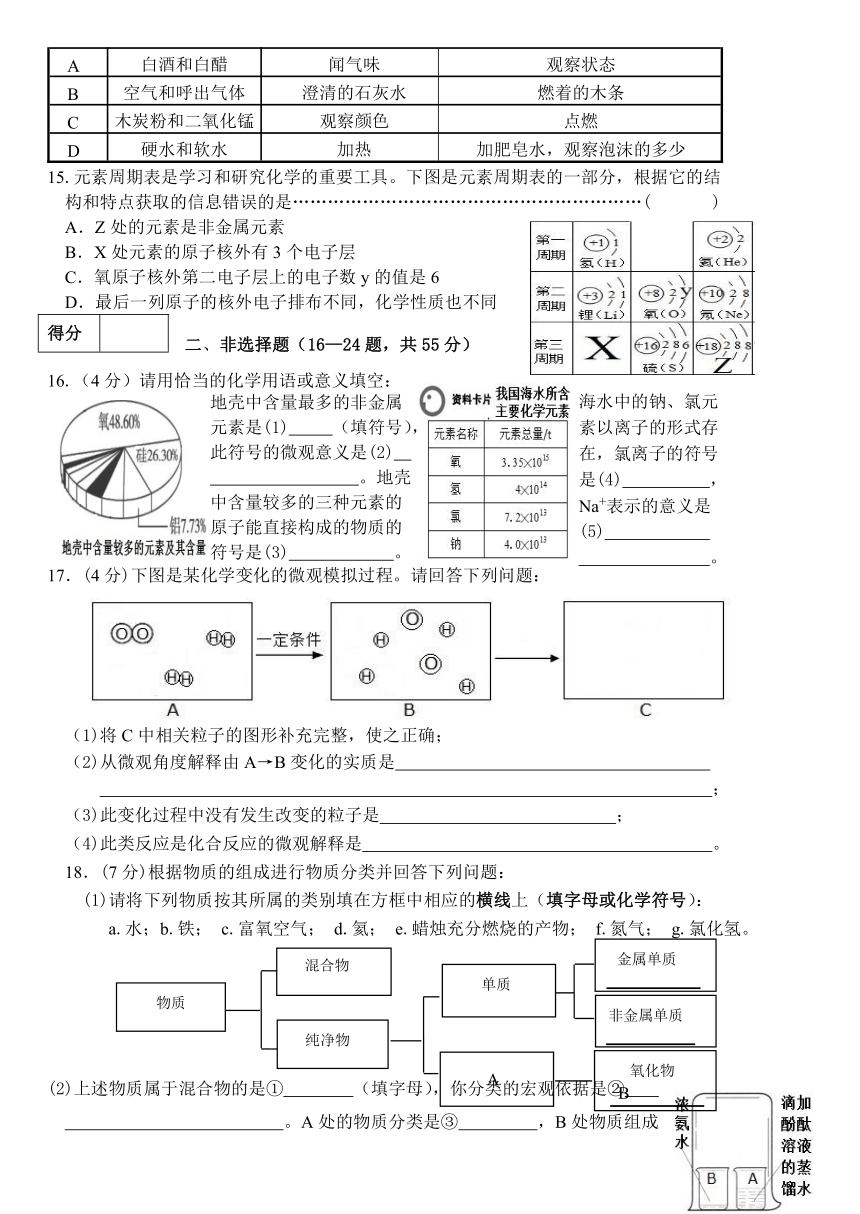
2018—2019学年度上学期期末调研测试
八年级化学
题号 一 二 总 分
得分
得分
一、选择题(1—15题,每题3分,共45分,每小题只有一个正确答案)
1.下列改变我们生活的有关中国“新四大发明”的叙述不能体现化学贡献的是( )
(
D
.通过网络购物,
享受便利生活
) (
C
.利用共享单车出行,减少大气污染
) (
B
.应
用采用石墨烯技术
的手机扫码支付
) (
A
.使用
电力牵引的高铁
优化能源结构
)
2.化学是一门以实验为基础的科学。下列实验操作正确的是……………………( )
(
A
.用滴管取液体
C
.
检查装置的
气密性
B
.
用镊子向试管
中送入固体
D
.
用量筒量取一
定体积的液体
)
3.下列过程中只发生物理变化的是…………………………………………………( )
(
A
.
蜡烛受热熔化并燃烧
B
.氧气变成雪花状固体
C
.食物腐烂变质
D
.
自来水厂投药消毒
)
4.下列物质的用途错误的是…………………………………………………………( )
(
A
.
氧气用于医疗急救
C
.稀有气体作化工原料
B
.乙醇(酒精)作燃料
D
.
灯泡中充氮气以
延长使用寿命
)
5.如果没有空气,将没有生机勃勃的地球。下列关于空气的说法正确的是……( )
A.使用清洁能源,积极植树、种草,可以保护空气
B.空气中的各成分不再保持各自的性质
C.空气中含量最多的化合物是水
D.一氧化碳、二氧化氮和PM2.5等是造成空气污染的有害气体
6.下列实验现象描述正确的是………………………………………………………( )
A.大理石中加入稀盐酸,(白色)固体逐渐减少,固体表面产生二氧化碳气体
B.胆矾中加水再滴加氢氧化钠溶液,蓝色固体减少形成蓝色溶液,再产生蓝色沉淀
C.木炭在氧气中燃烧发出黄白色光,产生大量白烟
D.银白色的铁丝在空气中剧烈燃烧、火星四射,生成黑色固体
7.下列叙述错误的是…………………………………………………………………( )
A.道尔顿创立的分子学说奠定了近代化学的基础
B.实验剩余药品不要随意丢弃,要放入指定的容器内
C.张青莲教授主持测定了锑、锌等几种元素相对原子质量的新值
D.锅炉中使用硬水会使锅炉内结垢,不仅浪费燃料,还易引起管道变形或损坏
8.右图是人类认识原子结构建立的一种模型,通过模型获取的信息错误的是…( )
A.原子是由居于原子中心的原子核与核外电子构成的
(
+
)B.该原子中质子数=核电荷数,均为4
C.该原子结构可表示为 易失去2个电子变成其他原子
D.原子不显电性是因为原子中质子与电子所带电荷的数量相等,电性相反
9.“低碳”,就是较低的二氧化碳排放,可以减缓全球气候变暖。下列有关二氧化碳的叙述正确的是……………………………………………………………………………( )
A.二氧化碳是由碳元素和氧元素组成的单质
B.二氧化碳由碳原子和氧分子构成
C.二氧化碳分子由1个碳原子和2个氧原子构成
D.二氧化碳的化学符号是CO2
10.下列反应的文字表达式及所属的基本反应类型均正确的是 …………………( )
A.铁 + 氧气 点燃 三氧化四铁 化合反应
B.硫 + 氧气 点燃 二氧化硫 氧化反应
C.氯酸钾 氯化钾 + 氧气 分解反应
D.碳酸钙 + 盐酸 氯化钙 + 水 分解反应
11.对下列事实的微观解释正确的是…………………………………………………( )
选项 事 实 解 释
A 焚烧秸秆产生的可吸入颗粒物形成霾 可吸入颗粒物分子不断运动
B 扫描隧道显微镜获得苯分子的图像 苯由离子构成
C 分离液态空气制氧气是物理变化 空气中的各种原子没有发生改变
D 水蒸发为水蒸气,所占体积变大 水分子间的间隔变大
12. “Nature for water(借自然之力,护绿水青山)”,下列有关水的叙述正确的是( )
A.陆地水约占全球水储量的3.5%
B.生活污水实现集中处理和排放,可以节约用水
C.海水淡化目前已成为人类应对淡水短缺的重要途径
D.水体污染,会影响工农业、渔业生产,但不会危害人体健康
13.下列图标是我国“国家节水标志”的是…………………………………………( )
(
A
.
B
.
C
.
D
.
)
14.区分下列各组物质的两种方法都正确的是………………………………………( )
选项 待区分物质 方法一 方法二
A 白酒和白醋 闻气味 观察状态
B 空气和呼出气体 澄清的石灰水 燃着的木条
C 木炭粉和二氧化锰 观察颜色 点燃
D 硬水和软水 加热 加肥皂水,观察泡沫的多少
15.元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分,根据它的结
构和特点获取的信息错误的是……………………………………………………( )
A.Z处的元素是非金属元素
B.X处元素的原子核外有3个电子层
C.氧原子核外第二电子层上的电子数y的值是6
D.最后一列原子的核外电子排布不同,化学性质也不同
得分
二、非选择题(16—24题,共55分)
(
地
壳中含量最多的非金属
元素是
(1)
(填符号)
,
此符号的微观意义是
(2)
。地壳
中含量较多的三种
元素的
原子能直接构成的物质的
符号是
(3)
。
) (
海水中的钠、氯元
素以离子的形式存
在,氯离子的符号
是
(4)
,
Na
+
表示
的意义是
(5)
。
)16.(4分)请用恰当的化学用语或意义填空:
17.(4分)下图是某化学变化的微观模拟过程。请回答下列问题:
(1)将C中相关粒子的图形补充完整,使之正确;
(2)从微观角度解释由A→B变化的实质是
;
(3)此变化过程中没有发生改变的粒子是 ;
(4)此类反应是化合反应的微观解释是 。
18.(7分)根据物质的组成进行物质分类并回答下列问题:
(1)请将下列物质按其所属的类别填在方框中相应的横线上(填字母或化学符号):
(
纯净物
单质
物质
氧化物
金属单质
非金属单质
混合物
)a.水;b.铁; c.富氧空气; d.氦; e.蜡烛充分燃烧的产物; f.氮气; g.氯化氢。
(
B
) (
A
)
(2)上述物质属于混合物的是① (填字母),你分类的宏观依据是②
。A处的物质分类是③ ,B处物质组成上的特点是④ 。
19.(2分)根据探究分子性质的实验回答下列问题:
(1)打开浓氨水的瓶塞,闻到有刺激性气味,说明浓氨有 。
(2)取烧杯A中少量无色溶液置于试管中,向其中滴加浓氨水,观察到
。
(3)继续进行如左图实验,观察到① ,A、B
两烧杯中的物质没有接触却产生与(2)中相同的实验现象,说明② 。
(
A
.
B
.
C
.
)20.(9分)利用学习化学获得的知识和形成的技能解决下列问题。
(1)松花江是哈尔滨的水源地之一,其水样中的不溶性杂质使江水浑浊,可溶性杂质使其具有气味和颜色。为净化母亲河的水样,进行以下活动。利用明矾①
对杂质② ,使其沉降。为除去沉降下来的难溶性杂质,还需进行A操作,实验中出现d烧杯中液体飞溅,滤液滴速慢的现象,可能的原因是③ 。继续将水样通过某种家用净水器,水样变得无色无味,说明净水器中的活性炭不仅可以④ ,还可以⑤
。若要得到“纯水”,还需进行B操作该操作的名称是⑥ 。
(2)用C探究水的组成,关闭电源时观察到a、b管内所得气体的① ,用燃着的木条检验两管中的气体,根据现象可知水通电分解正极得到② ,负极得到③ ,根据④ ,可推断出水的组成。
(
A B
)21.(9分)化学的发展使人类对空气的认识不断更新。
(1)A是拉瓦锡用定量的方法研究空气组成的实验。仿照拉
瓦锡实验的原理,我们用装置B测量空气中氧气的含量。
A中一部分银白色的液态汞加热后变成红色粉末,反应
的表达式是 。
(2)装置B待红磷熄灭并冷却到室温,打开弹簧夹,观察到烧杯中的液面下降,烧杯和导管
中的水进入集气瓶中,①
。因为红磷燃烧消耗② ,
,使集气瓶内③ , ,小于外界大气压,在压
强差的作用下,产生上述现象。进入集气瓶中水的体积即为瓶中④
。据上述现象,可得出的结论是⑤ 。
实验前在玻璃导管中充满水的目的是⑥
。
(3)英国科学家瑞利和拉姆塞发现从空气中取得的氮的密度为1.2572kg/m3;而从氨中取得
的氮的密度为1.2505kg/m3。根据这个细微的差异,他们发现了
密度比氮大的气体氩,对空气的组成做出更准确的判定。两位科
学家因此分获诺贝尔奖。目前,人们已用实验方法精确地测定空
气的成分,请将空气的成分或体积分数填写在统计图的横线上。
22.(8分)参与氧气的实验室制取与性质的实验过程并回答下列问题:
(
A
B C
D
)
(1)C中仪器a的名称是① ;实验室用一种暗紫色的固体药品制氧气的符号表达式为② ;在实验室中,用此药品制取氧气你所选择的发生和收集装置是③ (填字母),实验室用你选择的装置收集氧气的原因是④ 。写出在用上述发生和收集装置制氧气的过程中,能防止仪器b炸裂的一条正确的操作是⑤
。
(2)进行氧气的性质实验如图B,集气瓶内预先留有少量水的作用是①
。硫在空气和氧气中燃烧,产生的不同的现象是②
。这说明氧气的化学性质③ 。
(
A
B
C
D
)23. (4分)右图是初中化学常见的四种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去)。B为常见液体,常温下A、C、D为气态且均为单质,C分别能在A、D中燃烧。用“—”表示两种物质之间可以发生化学反应,用“→”表示一种物质可以转化为另一种物质。请回答下列问题:
(1)在图中写出A、D物质的化学符号;
(2)C在A中燃烧的实验现象是
;
(3)写出B→C的符号表达式 ;
(4)根据所学的化学知识,用“→”将图中的转化关系补充完整。
24.(8分)学习了在过氧化氢分解制氧气的反应中二氧化锰的作用后,石建和秦思发现红
砖粉末(主要含有氧化铁)也会对过氧化氢分解制氧气产生影响。
【提出问题】红砖粉末在过氧化氢分解制氧气的反应中起什么作用呢?
【猜想与假设】石建的猜想:红砖粉末在过氧化氢分解制氧气的反应中不起催化作用;
秦思的猜想:(1) 。
【实验探究】为验证猜想,进行下列实验活动。
实验序号 【实验过程】 【收集证据】 【解释与结论】
I 实验前称量红砖粉末的质量 质量为mg
II 伸入A中的带火星的木条不能复燃 是因为 (2) 。
III 将I称量的红砖粉末放入B中, 观察到C中的(3) 。 用符号表达式解释C的 液体中产生现象的原因是(4) 。 与II对比,证明红砖粉末 (5) 。
IV 待试管C中没有现象时,重新加入过氧化氢溶液,伸入带火星的木条。重复此操作 均观察到与III中相同的实验现象 证明化学反应前后红砖粉末的(6) 。
V 反复实验后,经过相应的操作,再次称量红砖粉末的质量 质量为mg 证明化学反应前后红砖粉末的(7) 。
【总结与反思】综合上述实验结论,可确定(8) 的猜想正确。实验室中用过氧化氢
制氧气时使用二氧化锰而不是红砖粉末,由此你得出的一条结论或提出的一个有探究价值的问题是(9) 。
2018—2019年度上学期期末调研测试八年级化学答案及评分标准说明:化学名词或术语、化学用语错误不得分;文字、符号表达式条件答错或未答扣一
半分;元素符号书写不准确、非化学名词的错别字、漏字等3个扣1分,但不重
复扣分。简答题其他答法,合理可酌情给分。
一、选择题(共45分,每小题3分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
选项 D C B C A B A C D C D A A B D
二、非选择题(16—24题,共55分)(无特殊标识的每空1分)
16.(4分)(1)O(0.5分);(2)氧元素的一个原子;
(3)Si(0.5分)、Al(0.5分);(4)Cl-(0.5分) ;
(5)1个钠离子带1个单位的正电荷或1个带1个单位正电荷的钠离子。
17.(4分)(1)见右图;
(2)在一定条件下,氧分子分解成氧原子,
氢分子分解成氢原子; (3)氢原子和氧原子;
(4)由两种或两种以上的分子发生反应生成一种(新的)
分子(合理即可)。
18.(7分)(1)(3分)每条横线上所填的字母或物质的化学符号1分
(
混合物纯净物
质
单
金属
非
单质
物
氧化
物
质
金属
单质
) (
b
或
Fe
)
(
d
或
He
;
f
或
N
2
)
(
A
)
(
a
或
H
2
O
) (
B
)
(2)(4分)①c、e;
②由两种或两种以上的物质混合而成(合理即可);
③化合物;
④只含一种物质,该物质由氧元素和另一种元素组成(合理即可)。
19.(2分)(1)挥发性(0.5分);(2)(试管中的)无色溶液变红(0.5分);
(3)①A烧杯中的无色溶液变红(0.5分);
②(构成物质的)分子是不断运动的(0.5分)。
20.(9分)(1)(5分)①溶于水后生成的胶状物;②吸附(0.5分);
③漏斗下端管尖没有紧靠烧杯内壁;
④滤去水样中的不溶性物质;
⑤吸附掉一些溶解性的杂质,除去色素和臭味;
⑥蒸馏(0.5分)。
(2)(4分)①体积比约为2:1;②氧气(或O2);
③氢气(或H2);④化学变化前后元素的种类不变。
21.(9分)(1)(1分)Hg+O2 △ HgO或汞+氧气 △ 氧化汞;
(2)(6分)①集气瓶中的液面升高,最终约升高至刻度1处;
②空气中的氧气(0.5分),生成五氧化二磷(或P2O5)固体(0.5分);
③气体减少(0.5分),气压减小(0.5分);
④(红磷所消耗的)空气中氧气的体积;⑤氧气约占空气总体积的1/5;
⑥防止烧杯中的水部分地残留在玻璃导管中,以使测量结果更加准确。
(3)(2分)见右图,每空1分。
22.(8分)(1)(5分)①水槽;
②KMnO4 △ K2MnO4+MnO2+O2;
③A、C;
④氧气不易溶于水(且不与水反应);
⑤实验结束时,先把导管移出水面,然后再熄灭酒精灯或试管口略向下
倾斜或加热试管时,先使酒精灯火焰在试管下方来回移动,让试管均
匀受热,然后对高锰酸钾所在的部位加热或加热时,试管外壁要干燥或加热后的试管不能立即接触冷水或用冷水清洗。 (
A
B
C
D
O
2
Cl
2
)
(2)(3分)①吸收二氧化硫,防止其污染空气;
②在空气中燃烧发出微弱的淡蓝色火焰,在氧气中
燃烧发出蓝紫色火焰;③比较活泼。
23.(4分)(1)A. O2(0.5分);D.Cl2(0.5分);
(2)气体燃烧,产生淡蓝色火焰,放热(若在火
焰上方罩干冷烧杯,烧杯内壁出现小液滴)
(3)H2O H2 + O2;(4)见右图,C→B。
24.(8分)(1)红砖粉末在过氧化氢制氧气的反应中起催化作用(0.5分);
(2)过氧化氢溶液在常温下分解缓慢,放出的氧气很少,不能使带火星的木条复燃;
(3)无色液体中产生气泡,带火星的木条复燃;
(4)H2O 2 H2O + O2 ;
(5)能改变(或加快)过氧化氢溶液的分解速率;
(6)化学性质没有发生变化;
(7)(本身的)质量没有发生变化;
(8)秦思(0.5分);
(9)一个化学反应可以有不同的(或多种)催化剂或某些反应并非只有一种催化剂(或二氧化锰是否比红砖粉末对过氧化氢溶液的催化作用更好?)(合理即可)。
八年级化学
题号 一 二 总 分
得分
得分
一、选择题(1—15题,每题3分,共45分,每小题只有一个正确答案)
1.下列改变我们生活的有关中国“新四大发明”的叙述不能体现化学贡献的是( )
(
D
.通过网络购物,
享受便利生活
) (
C
.利用共享单车出行,减少大气污染
) (
B
.应
用采用石墨烯技术
的手机扫码支付
) (
A
.使用
电力牵引的高铁
优化能源结构
)
2.化学是一门以实验为基础的科学。下列实验操作正确的是……………………( )
(
A
.用滴管取液体
C
.
检查装置的
气密性
B
.
用镊子向试管
中送入固体
D
.
用量筒量取一
定体积的液体
)
3.下列过程中只发生物理变化的是…………………………………………………( )
(
A
.
蜡烛受热熔化并燃烧
B
.氧气变成雪花状固体
C
.食物腐烂变质
D
.
自来水厂投药消毒
)
4.下列物质的用途错误的是…………………………………………………………( )
(
A
.
氧气用于医疗急救
C
.稀有气体作化工原料
B
.乙醇(酒精)作燃料
D
.
灯泡中充氮气以
延长使用寿命
)
5.如果没有空气,将没有生机勃勃的地球。下列关于空气的说法正确的是……( )
A.使用清洁能源,积极植树、种草,可以保护空气
B.空气中的各成分不再保持各自的性质
C.空气中含量最多的化合物是水
D.一氧化碳、二氧化氮和PM2.5等是造成空气污染的有害气体
6.下列实验现象描述正确的是………………………………………………………( )
A.大理石中加入稀盐酸,(白色)固体逐渐减少,固体表面产生二氧化碳气体
B.胆矾中加水再滴加氢氧化钠溶液,蓝色固体减少形成蓝色溶液,再产生蓝色沉淀
C.木炭在氧气中燃烧发出黄白色光,产生大量白烟
D.银白色的铁丝在空气中剧烈燃烧、火星四射,生成黑色固体
7.下列叙述错误的是…………………………………………………………………( )
A.道尔顿创立的分子学说奠定了近代化学的基础
B.实验剩余药品不要随意丢弃,要放入指定的容器内
C.张青莲教授主持测定了锑、锌等几种元素相对原子质量的新值
D.锅炉中使用硬水会使锅炉内结垢,不仅浪费燃料,还易引起管道变形或损坏
8.右图是人类认识原子结构建立的一种模型,通过模型获取的信息错误的是…( )
A.原子是由居于原子中心的原子核与核外电子构成的
(
+
)B.该原子中质子数=核电荷数,均为4
C.该原子结构可表示为 易失去2个电子变成其他原子
D.原子不显电性是因为原子中质子与电子所带电荷的数量相等,电性相反
9.“低碳”,就是较低的二氧化碳排放,可以减缓全球气候变暖。下列有关二氧化碳的叙述正确的是……………………………………………………………………………( )
A.二氧化碳是由碳元素和氧元素组成的单质
B.二氧化碳由碳原子和氧分子构成
C.二氧化碳分子由1个碳原子和2个氧原子构成
D.二氧化碳的化学符号是CO2
10.下列反应的文字表达式及所属的基本反应类型均正确的是 …………………( )
A.铁 + 氧气 点燃 三氧化四铁 化合反应
B.硫 + 氧气 点燃 二氧化硫 氧化反应
C.氯酸钾 氯化钾 + 氧气 分解反应
D.碳酸钙 + 盐酸 氯化钙 + 水 分解反应
11.对下列事实的微观解释正确的是…………………………………………………( )
选项 事 实 解 释
A 焚烧秸秆产生的可吸入颗粒物形成霾 可吸入颗粒物分子不断运动
B 扫描隧道显微镜获得苯分子的图像 苯由离子构成
C 分离液态空气制氧气是物理变化 空气中的各种原子没有发生改变
D 水蒸发为水蒸气,所占体积变大 水分子间的间隔变大
12. “Nature for water(借自然之力,护绿水青山)”,下列有关水的叙述正确的是( )
A.陆地水约占全球水储量的3.5%
B.生活污水实现集中处理和排放,可以节约用水
C.海水淡化目前已成为人类应对淡水短缺的重要途径
D.水体污染,会影响工农业、渔业生产,但不会危害人体健康
13.下列图标是我国“国家节水标志”的是…………………………………………( )
(
A
.
B
.
C
.
D
.
)
14.区分下列各组物质的两种方法都正确的是………………………………………( )
选项 待区分物质 方法一 方法二
A 白酒和白醋 闻气味 观察状态
B 空气和呼出气体 澄清的石灰水 燃着的木条
C 木炭粉和二氧化锰 观察颜色 点燃
D 硬水和软水 加热 加肥皂水,观察泡沫的多少
15.元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分,根据它的结
构和特点获取的信息错误的是……………………………………………………( )
A.Z处的元素是非金属元素
B.X处元素的原子核外有3个电子层
C.氧原子核外第二电子层上的电子数y的值是6
D.最后一列原子的核外电子排布不同,化学性质也不同
得分
二、非选择题(16—24题,共55分)
(
地
壳中含量最多的非金属
元素是
(1)
(填符号)
,
此符号的微观意义是
(2)
。地壳
中含量较多的三种
元素的
原子能直接构成的物质的
符号是
(3)
。
) (
海水中的钠、氯元
素以离子的形式存
在,氯离子的符号
是
(4)
,
Na
+
表示
的意义是
(5)
。
)16.(4分)请用恰当的化学用语或意义填空:
17.(4分)下图是某化学变化的微观模拟过程。请回答下列问题:
(1)将C中相关粒子的图形补充完整,使之正确;
(2)从微观角度解释由A→B变化的实质是
;
(3)此变化过程中没有发生改变的粒子是 ;
(4)此类反应是化合反应的微观解释是 。
18.(7分)根据物质的组成进行物质分类并回答下列问题:
(1)请将下列物质按其所属的类别填在方框中相应的横线上(填字母或化学符号):
(
纯净物
单质
物质
氧化物
金属单质
非金属单质
混合物
)a.水;b.铁; c.富氧空气; d.氦; e.蜡烛充分燃烧的产物; f.氮气; g.氯化氢。
(
B
) (
A
)
(2)上述物质属于混合物的是① (填字母),你分类的宏观依据是②
。A处的物质分类是③ ,B处物质组成上的特点是④ 。
19.(2分)根据探究分子性质的实验回答下列问题:
(1)打开浓氨水的瓶塞,闻到有刺激性气味,说明浓氨有 。
(2)取烧杯A中少量无色溶液置于试管中,向其中滴加浓氨水,观察到
。
(3)继续进行如左图实验,观察到① ,A、B
两烧杯中的物质没有接触却产生与(2)中相同的实验现象,说明② 。
(
A
.
B
.
C
.
)20.(9分)利用学习化学获得的知识和形成的技能解决下列问题。
(1)松花江是哈尔滨的水源地之一,其水样中的不溶性杂质使江水浑浊,可溶性杂质使其具有气味和颜色。为净化母亲河的水样,进行以下活动。利用明矾①
对杂质② ,使其沉降。为除去沉降下来的难溶性杂质,还需进行A操作,实验中出现d烧杯中液体飞溅,滤液滴速慢的现象,可能的原因是③ 。继续将水样通过某种家用净水器,水样变得无色无味,说明净水器中的活性炭不仅可以④ ,还可以⑤
。若要得到“纯水”,还需进行B操作该操作的名称是⑥ 。
(2)用C探究水的组成,关闭电源时观察到a、b管内所得气体的① ,用燃着的木条检验两管中的气体,根据现象可知水通电分解正极得到② ,负极得到③ ,根据④ ,可推断出水的组成。
(
A B
)21.(9分)化学的发展使人类对空气的认识不断更新。
(1)A是拉瓦锡用定量的方法研究空气组成的实验。仿照拉
瓦锡实验的原理,我们用装置B测量空气中氧气的含量。
A中一部分银白色的液态汞加热后变成红色粉末,反应
的表达式是 。
(2)装置B待红磷熄灭并冷却到室温,打开弹簧夹,观察到烧杯中的液面下降,烧杯和导管
中的水进入集气瓶中,①
。因为红磷燃烧消耗② ,
,使集气瓶内③ , ,小于外界大气压,在压
强差的作用下,产生上述现象。进入集气瓶中水的体积即为瓶中④
。据上述现象,可得出的结论是⑤ 。
实验前在玻璃导管中充满水的目的是⑥
。
(3)英国科学家瑞利和拉姆塞发现从空气中取得的氮的密度为1.2572kg/m3;而从氨中取得
的氮的密度为1.2505kg/m3。根据这个细微的差异,他们发现了
密度比氮大的气体氩,对空气的组成做出更准确的判定。两位科
学家因此分获诺贝尔奖。目前,人们已用实验方法精确地测定空
气的成分,请将空气的成分或体积分数填写在统计图的横线上。
22.(8分)参与氧气的实验室制取与性质的实验过程并回答下列问题:
(
A
B C
D
)
(1)C中仪器a的名称是① ;实验室用一种暗紫色的固体药品制氧气的符号表达式为② ;在实验室中,用此药品制取氧气你所选择的发生和收集装置是③ (填字母),实验室用你选择的装置收集氧气的原因是④ 。写出在用上述发生和收集装置制氧气的过程中,能防止仪器b炸裂的一条正确的操作是⑤
。
(2)进行氧气的性质实验如图B,集气瓶内预先留有少量水的作用是①
。硫在空气和氧气中燃烧,产生的不同的现象是②
。这说明氧气的化学性质③ 。
(
A
B
C
D
)23. (4分)右图是初中化学常见的四种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去)。B为常见液体,常温下A、C、D为气态且均为单质,C分别能在A、D中燃烧。用“—”表示两种物质之间可以发生化学反应,用“→”表示一种物质可以转化为另一种物质。请回答下列问题:
(1)在图中写出A、D物质的化学符号;
(2)C在A中燃烧的实验现象是
;
(3)写出B→C的符号表达式 ;
(4)根据所学的化学知识,用“→”将图中的转化关系补充完整。
24.(8分)学习了在过氧化氢分解制氧气的反应中二氧化锰的作用后,石建和秦思发现红
砖粉末(主要含有氧化铁)也会对过氧化氢分解制氧气产生影响。
【提出问题】红砖粉末在过氧化氢分解制氧气的反应中起什么作用呢?
【猜想与假设】石建的猜想:红砖粉末在过氧化氢分解制氧气的反应中不起催化作用;
秦思的猜想:(1) 。
【实验探究】为验证猜想,进行下列实验活动。
实验序号 【实验过程】 【收集证据】 【解释与结论】
I 实验前称量红砖粉末的质量 质量为mg
II 伸入A中的带火星的木条不能复燃 是因为 (2) 。
III 将I称量的红砖粉末放入B中, 观察到C中的(3) 。 用符号表达式解释C的 液体中产生现象的原因是(4) 。 与II对比,证明红砖粉末 (5) 。
IV 待试管C中没有现象时,重新加入过氧化氢溶液,伸入带火星的木条。重复此操作 均观察到与III中相同的实验现象 证明化学反应前后红砖粉末的(6) 。
V 反复实验后,经过相应的操作,再次称量红砖粉末的质量 质量为mg 证明化学反应前后红砖粉末的(7) 。
【总结与反思】综合上述实验结论,可确定(8) 的猜想正确。实验室中用过氧化氢
制氧气时使用二氧化锰而不是红砖粉末,由此你得出的一条结论或提出的一个有探究价值的问题是(9) 。
2018—2019年度上学期期末调研测试八年级化学答案及评分标准说明:化学名词或术语、化学用语错误不得分;文字、符号表达式条件答错或未答扣一
半分;元素符号书写不准确、非化学名词的错别字、漏字等3个扣1分,但不重
复扣分。简答题其他答法,合理可酌情给分。
一、选择题(共45分,每小题3分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
选项 D C B C A B A C D C D A A B D
二、非选择题(16—24题,共55分)(无特殊标识的每空1分)
16.(4分)(1)O(0.5分);(2)氧元素的一个原子;
(3)Si(0.5分)、Al(0.5分);(4)Cl-(0.5分) ;
(5)1个钠离子带1个单位的正电荷或1个带1个单位正电荷的钠离子。
17.(4分)(1)见右图;
(2)在一定条件下,氧分子分解成氧原子,
氢分子分解成氢原子; (3)氢原子和氧原子;
(4)由两种或两种以上的分子发生反应生成一种(新的)
分子(合理即可)。
18.(7分)(1)(3分)每条横线上所填的字母或物质的化学符号1分
(
混合物纯净物
质
单
金属
非
单质
物
氧化
物
质
金属
单质
) (
b
或
Fe
)
(
d
或
He
;
f
或
N
2
)
(
A
)
(
a
或
H
2
O
) (
B
)
(2)(4分)①c、e;
②由两种或两种以上的物质混合而成(合理即可);
③化合物;
④只含一种物质,该物质由氧元素和另一种元素组成(合理即可)。
19.(2分)(1)挥发性(0.5分);(2)(试管中的)无色溶液变红(0.5分);
(3)①A烧杯中的无色溶液变红(0.5分);
②(构成物质的)分子是不断运动的(0.5分)。
20.(9分)(1)(5分)①溶于水后生成的胶状物;②吸附(0.5分);
③漏斗下端管尖没有紧靠烧杯内壁;
④滤去水样中的不溶性物质;
⑤吸附掉一些溶解性的杂质,除去色素和臭味;
⑥蒸馏(0.5分)。
(2)(4分)①体积比约为2:1;②氧气(或O2);
③氢气(或H2);④化学变化前后元素的种类不变。
21.(9分)(1)(1分)Hg+O2 △ HgO或汞+氧气 △ 氧化汞;
(2)(6分)①集气瓶中的液面升高,最终约升高至刻度1处;
②空气中的氧气(0.5分),生成五氧化二磷(或P2O5)固体(0.5分);
③气体减少(0.5分),气压减小(0.5分);
④(红磷所消耗的)空气中氧气的体积;⑤氧气约占空气总体积的1/5;
⑥防止烧杯中的水部分地残留在玻璃导管中,以使测量结果更加准确。
(3)(2分)见右图,每空1分。
22.(8分)(1)(5分)①水槽;
②KMnO4 △ K2MnO4+MnO2+O2;
③A、C;
④氧气不易溶于水(且不与水反应);
⑤实验结束时,先把导管移出水面,然后再熄灭酒精灯或试管口略向下
倾斜或加热试管时,先使酒精灯火焰在试管下方来回移动,让试管均
匀受热,然后对高锰酸钾所在的部位加热或加热时,试管外壁要干燥或加热后的试管不能立即接触冷水或用冷水清洗。 (
A
B
C
D
O
2
Cl
2
)
(2)(3分)①吸收二氧化硫,防止其污染空气;
②在空气中燃烧发出微弱的淡蓝色火焰,在氧气中
燃烧发出蓝紫色火焰;③比较活泼。
23.(4分)(1)A. O2(0.5分);D.Cl2(0.5分);
(2)气体燃烧,产生淡蓝色火焰,放热(若在火
焰上方罩干冷烧杯,烧杯内壁出现小液滴)
(3)H2O H2 + O2;(4)见右图,C→B。
24.(8分)(1)红砖粉末在过氧化氢制氧气的反应中起催化作用(0.5分);
(2)过氧化氢溶液在常温下分解缓慢,放出的氧气很少,不能使带火星的木条复燃;
(3)无色液体中产生气泡,带火星的木条复燃;
(4)H2O 2 H2O + O2 ;
(5)能改变(或加快)过氧化氢溶液的分解速率;
(6)化学性质没有发生变化;
(7)(本身的)质量没有发生变化;
(8)秦思(0.5分);
(9)一个化学反应可以有不同的(或多种)催化剂或某些反应并非只有一种催化剂(或二氧化锰是否比红砖粉末对过氧化氢溶液的催化作用更好?)(合理即可)。
同课章节目录
