原子的构成(1)
图片预览



文档简介
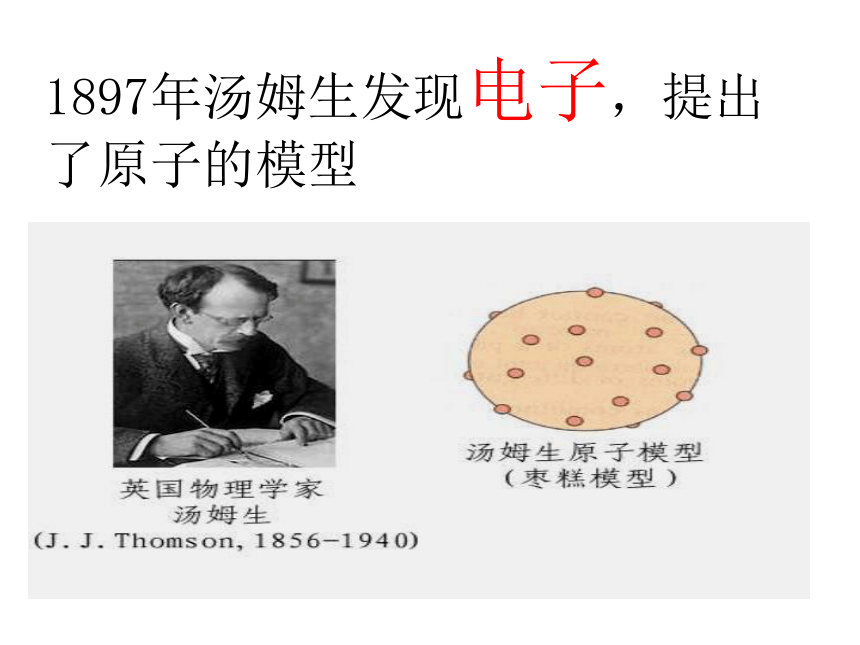
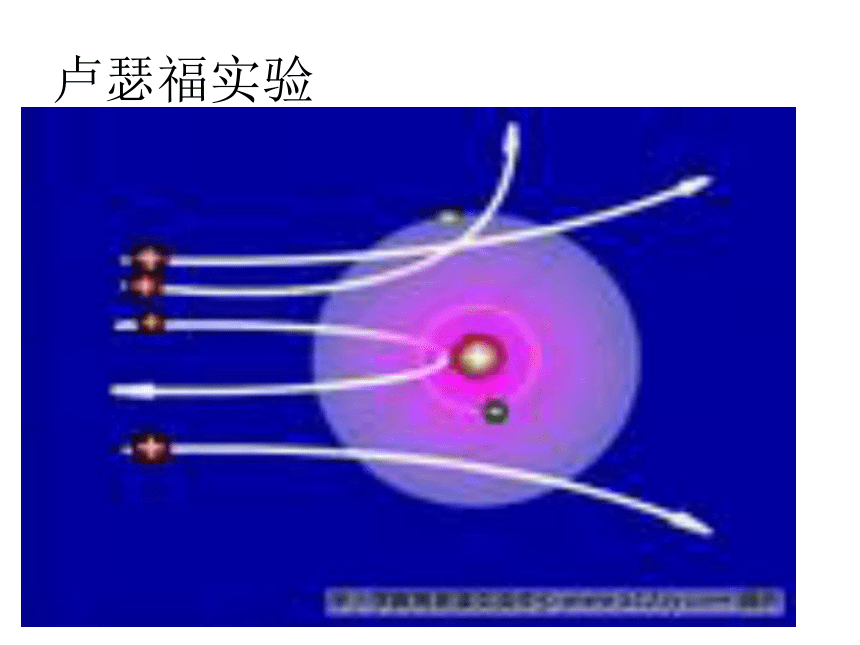
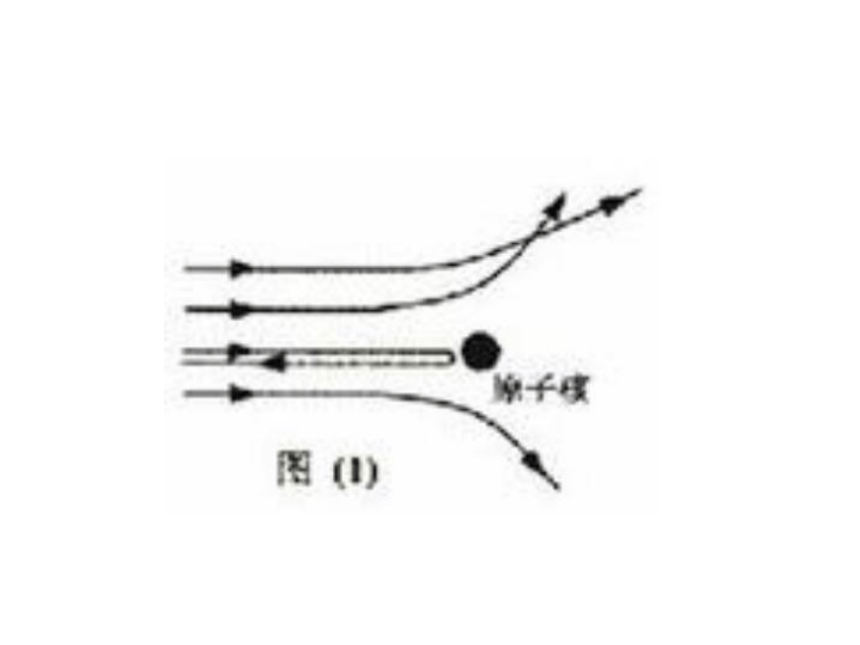
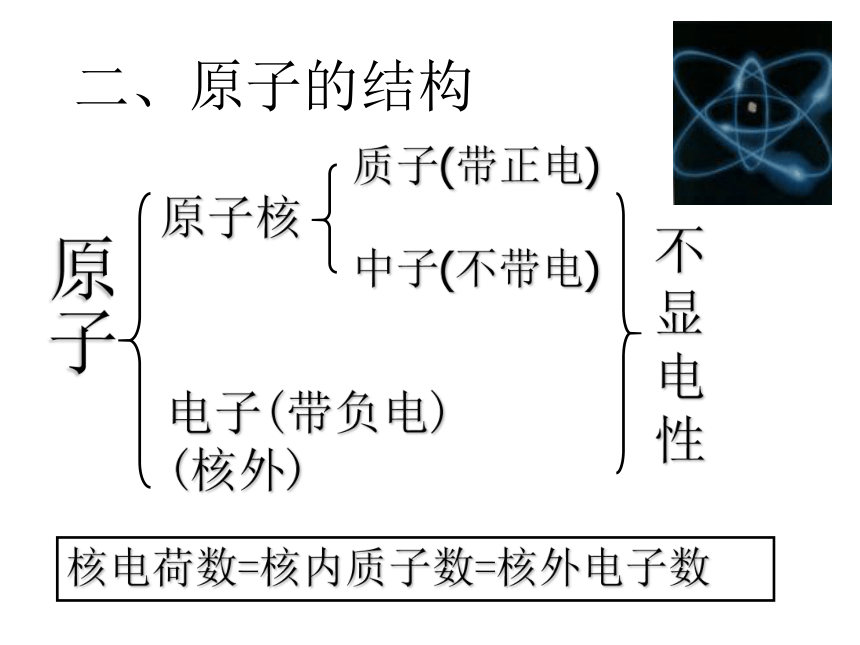
课件16张PPT。第二单元:自然界中的水第三节原子的构成一、原子结构的发现历史2、19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小不可分割的实心球体。1897年汤姆生发现电子,提出了原子的模型卢瑟福实验原子原子核电子(带负电) (核外)质子(带正电)中子(不带电)不显电性核电荷数=核内质子数=核外电子数二、原子的结构1、构成原子的三种粒子的电性、质量如何?
2、原子中有带电的粒子,那么整个原子是否
带电,为什么?
3.原子是如何构成的?
4、原子的质量主要集中在 ?
阅读P45-46页,回答下列问题三.原子中的电子1、电子的分层排布
2、原子结构示意图
3、电子对原子性质的影响
4、离子思考:19世纪英国科学家道尔顿提出了近代原子学说:他认为物质都是由原子构成的,这些原子是微小的不可分割的实心球体;同种原子性质和质量应该相同.上述观点中你认为正确的是:上述观点中你认为不正确的是:1、组成一切原子必不可少的粒子是( )
A、质子 B、质子 电子
C、质子 中子 电子 D、质子 中子B2 、 下列关于原子核的叙述中,正确的是( )。
①通常由中子和电子构成 ②通常由质子和中子构成 ③带负电荷 ④不显电性 ⑤不能再分 ⑥体积比原子小得多 ⑦质量大约相当于原子
A.①⑤ B.②⑦
C.③④ D.②⑥⑦ D3、化学变化中的最小粒子是( )。
A.分子 B.原子
C.质子 D.电子 B 原子失去电子→阳离子(正电荷)
Na+ Mg2+
原子得到电子→阴离子(负电荷)
Cl- S2-
2、原子中有带电的粒子,那么整个原子是否
带电,为什么?
3.原子是如何构成的?
4、原子的质量主要集中在 ?
阅读P45-46页,回答下列问题三.原子中的电子1、电子的分层排布
2、原子结构示意图
3、电子对原子性质的影响
4、离子思考:19世纪英国科学家道尔顿提出了近代原子学说:他认为物质都是由原子构成的,这些原子是微小的不可分割的实心球体;同种原子性质和质量应该相同.上述观点中你认为正确的是:上述观点中你认为不正确的是:1、组成一切原子必不可少的粒子是( )
A、质子 B、质子 电子
C、质子 中子 电子 D、质子 中子B2 、 下列关于原子核的叙述中,正确的是( )。
①通常由中子和电子构成 ②通常由质子和中子构成 ③带负电荷 ④不显电性 ⑤不能再分 ⑥体积比原子小得多 ⑦质量大约相当于原子
A.①⑤ B.②⑦
C.③④ D.②⑥⑦ D3、化学变化中的最小粒子是( )。
A.分子 B.原子
C.质子 D.电子 B 原子失去电子→阳离子(正电荷)
Na+ Mg2+
原子得到电子→阴离子(负电荷)
Cl- S2-
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
