乙醇
图片预览






文档简介
课件26张PPT。第二单元 食品中的有机化合物
∮2-1 乙醇授课人: 郑集高级中学 刘英锋 明月几时有?
把 问青天。
葡萄美 夜光杯,
欲饮琵琶马上催。酒酒 我国灿烂的文化史上记载着许多与酒有关的典故和经典诗句,酒文化源远流长。想一想,你还知道哪些与酒有关诗句?常见的酒中乙醇的含量(用体积分数表示)活动探究一 观察实验台上的无水乙醇试剂,结合生活常识,总结乙醇有哪些物理性质?
(从色、态、味、水溶性、挥发性等方面)一、乙醇的物理性质 无色、透明有特殊香味的液体,俗名酒精。易挥发,沸点78.5℃。
密度比水小,能和水以任意比互溶,能溶解许多无机物和有机物,是一种良好的溶剂。 2、乙醇能萃取溴水中的溴吗?
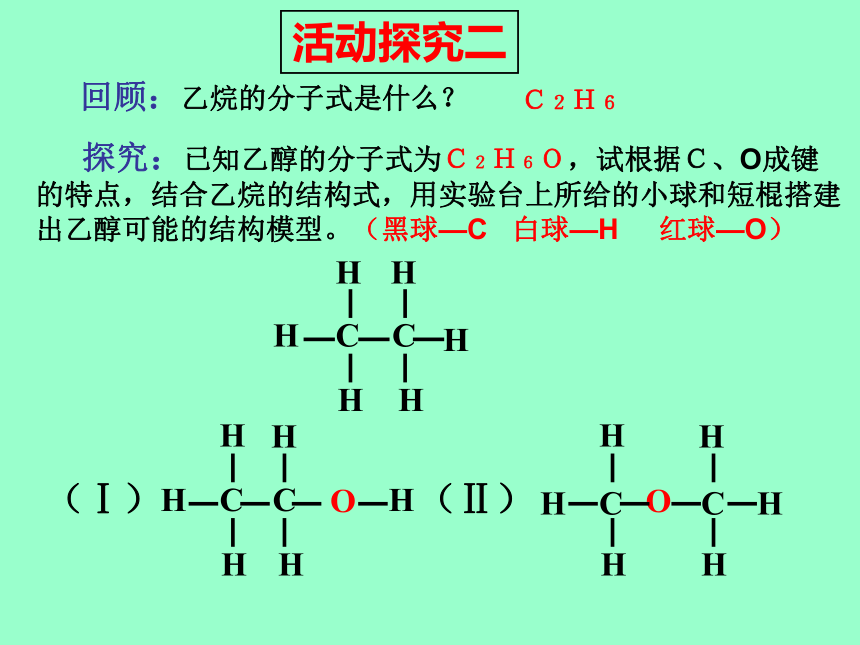
探究:已知乙醇的分子式为C2H6O,试根据C、O成键的特点,结合乙烷的结构式,用实验台上所给的小球和短棍搭建出乙醇可能的结构模型。(黑球—C 白球—H 红球—O)回顾:乙烷的分子式是什么?C2H6活动探究二对比·思考回顾:
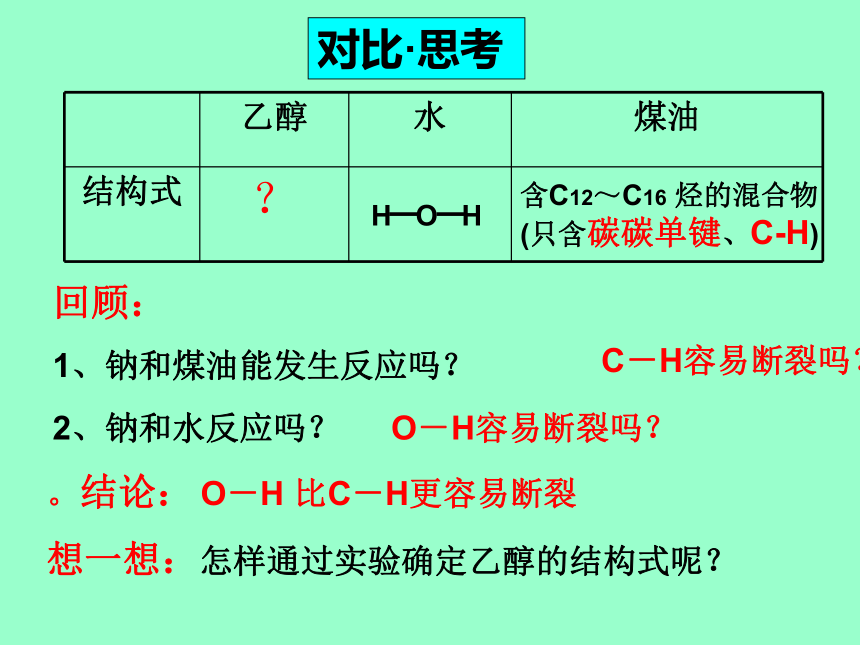
1、钠和煤油能发生反应吗?C-H容易断裂吗?2、钠和水反应吗?O-H容易断裂吗?。结论: O-H 比C-H更容易断裂想一想:怎样通过实验确定乙醇的结构式呢?含C12~C16 烃的混合物 (只含碳碳单键、C-H)浮、熔
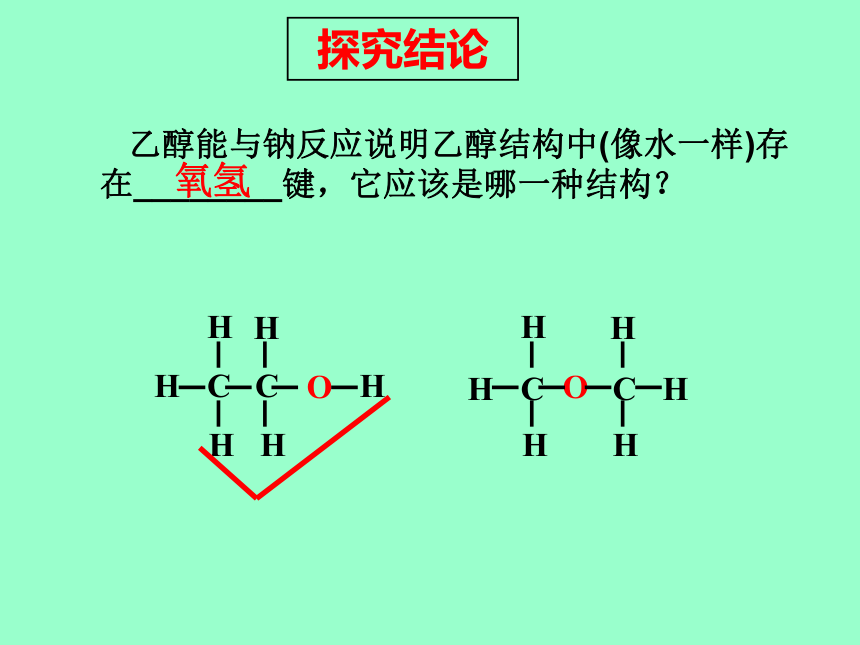
游、响先沉在底部,表面有气泡,后上浮, 响声很小活动探究三思考:钠和乙醇产生的气体是什么?应如何验证?探究结论 乙醇能与钠反应说明乙醇结构中(像水一样)存在________键,它应该是哪一种结构?氧氢二、乙醇的组成和结构球棍模型比例模型分子式:C2H6O 结构式:结构简式:CH3CH2OH
或 C2H5OH两个概念1、官能团:决定有机化合物化学特性的原子或原子团。
如—X(卤原子), —NO2(硝基) —CHO(醛基)
—COOH(羧基)
想一想:你已经学了哪些官能团?2、烃的衍生物:烃分子中的氢原子被其他原子或原子团所取代而来的有机化合物。三、乙醇的化学性质1、与活泼金属钠反应( 反应)2CH3CH2OH + 2Na → 2CH3CH2ONa﹢H2↑
乙醇钠 练习:写出乙醇和K,乙醇和Ca反应的化学方程式。 羟基中氢原子的活泼性:水____乙醇(填“大于”或“小于”),水比乙醇更_____(填“难”或“易”)电离出氢离子.取代(断O—H)大于易三、乙醇的化学性质2、氧化反应⑴燃烧淡蓝色火焰,同时放出大量热。作燃料现象:活动探究四 向小试管中加入约3mL无水乙醇,将铜丝在酒精灯外焰上灼烧至红热,迅速插入乙醇中,反复几次,观察铜丝颜色的变化,再闻试管中液体的气味,感受反应前后的变化。铜丝由亮红色变成黑色铜丝由黑色又变成亮红色,反复几次后,试管口可闻到刺激性气味三、乙醇的化学性质2、氧化反应(2)催化氧化(断O—H和C—H)想一想!结论
催化氧化的条件:
羟基相连的C上至少有一个H
CH3 CH2CH2OH都属于与乙醇同类的烃的衍生物,它们能否发生像乙醇那样的催化氧化反应?如能,请写出它们被氧化的产物。三、乙醇的化学性质2、氧化反应(3)可被强氧化剂氧化(了解) 乙醇可被酸性高锰酸钾溶液或酸性重铬酸钾溶液氧化生成乙酸(CH3COOH)。2K2Cr2O7 + 3C2H5OH +8H2SO4 → 2Cr2(SO4)3 +3CH3COOH
(橙红色) (绿色) +2K2SO4+11H2O身边的化学 有了这个酒精检测仪,只需让饮酒者对着进气孔吹口气,几秒钟就可知道他是否饮酒以及相关的浓度数据,厉害吧!四、乙醇的主要用途四、乙醇的主要用途3、作溶剂4、作燃料—汽车、酒精灯等5、作化工原料 (如工业上用来制乙酸)乙醇二、乙醇的结构一、乙醇的物理性质三、乙醇的化学性质1、与钠反应(取代反应) 2 CH3CH2 —O—H +2Na →2 CH3CH2ONa + H2↑ 2、氧化反应小结(1)燃烧(2)催化氧化(3)可被强氧化剂氧化四、乙醇的主要用途制饮料,作消毒剂,作溶剂,作燃料,作化工原料 。巩固练习①1、假酒中严重超标的是 ( )
A.乙醇 B.乙醛 C.甲醇 D. 醋酸C2、 向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述正确的是 ( )
A.钠块浮在乙醇的上面四处游动 B.发出嘶嘶的声响
C. 钠块熔化成闪亮的小球 D. 钠块表面有气泡冒出DC巩固练习C谢谢乙醇与O2发生催化氧化的机理演示
(请注意观察乙醇中什么键断裂了?)乙醇与钠反应的机理演示:
(请注意观察乙醇中什么键断裂了?)
把 问青天。
葡萄美 夜光杯,
欲饮琵琶马上催。酒酒 我国灿烂的文化史上记载着许多与酒有关的典故和经典诗句,酒文化源远流长。想一想,你还知道哪些与酒有关诗句?常见的酒中乙醇的含量(用体积分数表示)活动探究一 观察实验台上的无水乙醇试剂,结合生活常识,总结乙醇有哪些物理性质?
(从色、态、味、水溶性、挥发性等方面)一、乙醇的物理性质 无色、透明有特殊香味的液体,俗名酒精。易挥发,沸点78.5℃。
密度比水小,能和水以任意比互溶,能溶解许多无机物和有机物,是一种良好的溶剂。 2、乙醇能萃取溴水中的溴吗?
探究:已知乙醇的分子式为C2H6O,试根据C、O成键的特点,结合乙烷的结构式,用实验台上所给的小球和短棍搭建出乙醇可能的结构模型。(黑球—C 白球—H 红球—O)回顾:乙烷的分子式是什么?C2H6活动探究二对比·思考回顾:
1、钠和煤油能发生反应吗?C-H容易断裂吗?2、钠和水反应吗?O-H容易断裂吗?。结论: O-H 比C-H更容易断裂想一想:怎样通过实验确定乙醇的结构式呢?含C12~C16 烃的混合物 (只含碳碳单键、C-H)浮、熔
游、响先沉在底部,表面有气泡,后上浮, 响声很小活动探究三思考:钠和乙醇产生的气体是什么?应如何验证?探究结论 乙醇能与钠反应说明乙醇结构中(像水一样)存在________键,它应该是哪一种结构?氧氢二、乙醇的组成和结构球棍模型比例模型分子式:C2H6O 结构式:结构简式:CH3CH2OH
或 C2H5OH两个概念1、官能团:决定有机化合物化学特性的原子或原子团。
如—X(卤原子), —NO2(硝基) —CHO(醛基)
—COOH(羧基)
想一想:你已经学了哪些官能团?2、烃的衍生物:烃分子中的氢原子被其他原子或原子团所取代而来的有机化合物。三、乙醇的化学性质1、与活泼金属钠反应( 反应)2CH3CH2OH + 2Na → 2CH3CH2ONa﹢H2↑
乙醇钠 练习:写出乙醇和K,乙醇和Ca反应的化学方程式。 羟基中氢原子的活泼性:水____乙醇(填“大于”或“小于”),水比乙醇更_____(填“难”或“易”)电离出氢离子.取代(断O—H)大于易三、乙醇的化学性质2、氧化反应⑴燃烧淡蓝色火焰,同时放出大量热。作燃料现象:活动探究四 向小试管中加入约3mL无水乙醇,将铜丝在酒精灯外焰上灼烧至红热,迅速插入乙醇中,反复几次,观察铜丝颜色的变化,再闻试管中液体的气味,感受反应前后的变化。铜丝由亮红色变成黑色铜丝由黑色又变成亮红色,反复几次后,试管口可闻到刺激性气味三、乙醇的化学性质2、氧化反应(2)催化氧化(断O—H和C—H)想一想!结论
催化氧化的条件:
羟基相连的C上至少有一个H
CH3 CH2CH2OH都属于与乙醇同类的烃的衍生物,它们能否发生像乙醇那样的催化氧化反应?如能,请写出它们被氧化的产物。三、乙醇的化学性质2、氧化反应(3)可被强氧化剂氧化(了解) 乙醇可被酸性高锰酸钾溶液或酸性重铬酸钾溶液氧化生成乙酸(CH3COOH)。2K2Cr2O7 + 3C2H5OH +8H2SO4 → 2Cr2(SO4)3 +3CH3COOH
(橙红色) (绿色) +2K2SO4+11H2O身边的化学 有了这个酒精检测仪,只需让饮酒者对着进气孔吹口气,几秒钟就可知道他是否饮酒以及相关的浓度数据,厉害吧!四、乙醇的主要用途四、乙醇的主要用途3、作溶剂4、作燃料—汽车、酒精灯等5、作化工原料 (如工业上用来制乙酸)乙醇二、乙醇的结构一、乙醇的物理性质三、乙醇的化学性质1、与钠反应(取代反应) 2 CH3CH2 —O—H +2Na →2 CH3CH2ONa + H2↑ 2、氧化反应小结(1)燃烧(2)催化氧化(3)可被强氧化剂氧化四、乙醇的主要用途制饮料,作消毒剂,作溶剂,作燃料,作化工原料 。巩固练习①1、假酒中严重超标的是 ( )
A.乙醇 B.乙醛 C.甲醇 D. 醋酸C2、 向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述正确的是 ( )
A.钠块浮在乙醇的上面四处游动 B.发出嘶嘶的声响
C. 钠块熔化成闪亮的小球 D. 钠块表面有气泡冒出DC巩固练习C谢谢乙醇与O2发生催化氧化的机理演示
(请注意观察乙醇中什么键断裂了?)乙醇与钠反应的机理演示:
(请注意观察乙醇中什么键断裂了?)
