课题3 溶液的浓度 课件
图片预览











文档简介
课件31张PPT。课题3 溶质质量分数(即溶液浓度)学 习 目 标1.知道溶质质量分数的表示方法及其涵义;
2.能进行溶质质量分数的简单计算。
3.知道溶液稀释的关键,能进行简单计算。
4.学会配制一定溶质质量分数溶液的方法与步骤。
5.进一步熟练溶质质量分数的简单计算;
6.能进行溶质质量分数与化学方程式相结合的综合计算。“死海
不死”创设情景人为什么能浮在水面呢?如果人落到水里后,是漂浮在水面上,还是沉在水下呀? 死海的海边有大量食盐析出好帅啊……
思考:1、在这三支试管中溶液的组成是否相同?哪只浓度大?2、你知道那只试管中溶液的浓度最大?你判断的依据? 对于有色溶液,我们可以根据颜色深浅来判断溶液是浓还是浅;但是这种分法比较粗略,不能准确地表明一定量溶液里究竟含有多少溶质不相同【实验9-6】10%20%结论:溶液中溶质的质量分数越大,溶液浓度越大
溶质的质量分数(一般用百分数表示)溶质的质量分数=溶质质量分数=1、定义:是溶质质量和溶液质量之比 。2、公式:溶质质量
溶质+溶剂×100%例1:将3g高锰酸钾加水配成100g溶液(如图1),
求:(1)图1所示溶液中溶质的质量分数?图1解:答:所得溶液的质量分数为3%。= 3%溶液中溶质的质量分数溶液中溶质的质量分数(2)向图1溶液中再加入400g水后,所得溶液(如图2)中溶质的质量分数?图2解:答:所得溶液的质量分数为0.6%。= 0.6%溶液中溶质的质量分数答:所得甘油溶液中溶质的质量分数为80%。 =80%甘油溶液中溶质的质量分数解:(2)冬天,人们常给皮肤抹上一点甘油溶液,使皮肤保持湿润。用400g甘油溶解在100g水中,配制的甘油溶液效果最佳。该甘油溶液的溶质的质量分数是多少?
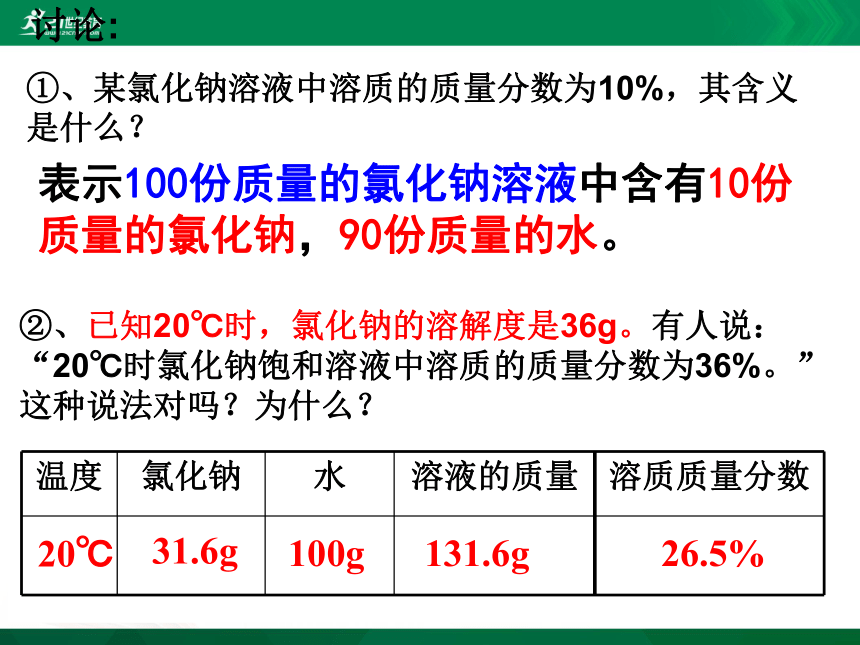
①、某氯化钠溶液中溶质的质量分数为10%,其含义是什么?②、已知20℃时,氯化钠的溶解度是36g。有人说:“20℃时氯化钠饱和溶液中溶质的质量分数为36%。”
这种说法对吗?为什么?表示100份质量的氯化钠溶液中含有10份质量的氯化钠,90份质量的水。讨论: 20℃31.6g100g131.6g26.5%判断下列说法是否正确,并加以改正。
⑴在100克水中溶解30克食盐,溶质质量分数是
30%
⑵从100克10%的食盐溶液里取出10克,其浓度
是10%
⑶将100克10%的食盐溶液和100克10%的食盐溶液混合,混合溶液的浓度是20%
⑷ 20℃时,100克水中最多溶解36克食盐,它的溶解度是36克/100克水,浓度是36%( × )( √ )( × )( × )4.变一变:
【例3】在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?【解】答: 配制150kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。1、在30℃时,将25g硝酸钾固体加入100g水中,充分溶解后,所得溶液的溶质质量分数是多少?随堂练习2、某温度时,蒸干100g氯化钾溶液,得到10g氯化钾,求该溶液中溶质的质量分数。1.计算2.称量(量取)3.溶解要配制50g质量分数为6%的NaCl溶液【实验9-7】m(NaCl)=_____g,m(水)=_____g用玻璃棒搅拌,加快溶解。347实验室里要配制10%的氯化钠溶液150g.
(1)实验步骤有: 、 、 、装瓶并贴好标签。
(2)需要的仪器,除药匙、试剂瓶及标签外,还有 .
(3)需要用氯化钠 g,水 mL。
练一练15135计算称量溶解托盘天平 玻璃棒 烧杯 量筒 滴管练习1、将20克KNO3全部溶于80克水中,所得溶液中溶质的质量分数是____。2、100克30%的NaOH溶液中NaOH的质量是____g.20%303、如右图,要配制 这种葡萄糖注射液, 需要葡萄糖和水各
多少g?葡萄糖注射液
规格:250g
内含:葡萄糖5%2、将80g浓度50%硫酸稀释成20%的稀硫酸,所得溶液体积是多少mL?要加水多少g?(20%的硫酸溶液密度为1.2g/mL)例2:现有98%的浓硫酸,要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需要加水多少克?溶液浓缩或稀释的计算依据:溶液稀释前后,溶质的质量保持不变。讨论此公式只适用于饱和溶液里 已知20℃时,食盐的溶解度为36g。这表明,该饱和溶液的溶质质量分数为36%。这种说法对吗?为什么?练习1、在32℃时,KNO3的溶解度为50g,则所得溶液中的溶质的质量分数为_______。33.3%2、已知某温度下,KCl的溶解度为40g。在该温度下,将25g KCl固体加入到50g水中,充分溶解后,形成的溶液中溶质的质量分数为______。28.6%例3:将13克锌粒放入100g稀硫酸中,恰好完全反应,试求: (1)稀硫酸的溶质的质量分数?
(2)反应后所得溶液中溶质的质量分数?m(反应后溶液)=反应前各物质的总质量 — 气体 — 沉淀(固体杂质)有一块10 g的某合金投入到90g 浓度为40%的硫酸中,产生0.2g氢气,并余下1g不溶性固体,则反应后溶液的质量为___g。1. 150g稀盐酸跟一定质量含少量杂质的石灰石恰好完全反应(杂质不溶解,也不参与反应),生成11g二氧化碳。回答下列问题:
(1)写出稀盐酸跟石灰石反应的化学方程式 。
(2)稀盐酸的溶质质量分数?
(3)反应后溶液中溶质的质量?溶液为多少克?
(4)反应后溶液的溶质质量分数? 2.取出80克稀硫酸放入装有足量锌的启普发生器里,当反应完全后,通过实验测定生成氢气的体积为4.48L(已知在标准状况下,氢气的密度0.089g/L) (1)试计算硫酸溶液的溶质质量分数? (2)将反应后的溶液过滤,蒸发结晶,能得到多少克固体? (3)反应后所得溶液的溶质质量分数是多少?
用锌片与稀硫酸反应制H2 ,每次实验结果记录如下:(1)第2、5次产生的氢气质量是多少?(2)稀硫酸的溶质质量分数为多少?
(3) 10g锌片与100g这种稀硫酸充分反应后,所得溶液的溶质质量分数是多少?20℃时,某NaCl溶液中溶质的质量分数为20%。(1)此时溶液中溶质、溶剂和溶液的质量比为多少?
(2)若将100克此溶液分为二等份,则每一份溶液中溶质的质量分数为多少?
(3)向其中一份中加入10g水,则溶质的质量分数为多少?
(4)向另一份中加入2gNaCl固体全部溶解,则溶液中溶质的质量分数为多少?(5)若从100g此溶液中取出5g溶液,则剩余溶液中溶质的质量分数为多少?
(6)若将其中一份溶液升温到40℃时,溶质的质量分数为多少?(溶剂不蒸发)
(7)若要让100g的此溶液溶质的质量分数减半,则需加水多少克?20℃时,某NaCl溶液中溶质的质量分数为20%。随堂练习有5.6g的铁粉与98g稀硫酸刚好反应.求:
(1)生成氢气的质量是多少? (2)稀硫酸的溶质质量分数?
(3)反应后溶液中溶质的质量?溶液为多少克?
(4)反应后溶液的溶质质量分数? 公式:① 溶质质量分数 =
=② m(液) = m(质) + m(剂)=ρ(液)×V(液) ③溶质质量分数=(此公式只适用于饱和溶液)浓溶液的稀释: [稀释前后,溶质质量不变] ① m(浓)×a%=m(稀)×b% ② m(加水)=m(稀)-m(浓)m(反应后溶液)=反应前各物质的总质量 — 气体 — 沉淀(固体杂质)谢谢21世纪教育网(www.21cnjy.com) 中小学教育资源网站 有大把高质量资料?一线教师?一线教研员?
欢迎加入21世纪教育网教师合作团队!!月薪过万不是梦!!
详情请看:
https://www.21cnjy.com/help/help_extract.php
2.能进行溶质质量分数的简单计算。
3.知道溶液稀释的关键,能进行简单计算。
4.学会配制一定溶质质量分数溶液的方法与步骤。
5.进一步熟练溶质质量分数的简单计算;
6.能进行溶质质量分数与化学方程式相结合的综合计算。“死海
不死”创设情景人为什么能浮在水面呢?如果人落到水里后,是漂浮在水面上,还是沉在水下呀? 死海的海边有大量食盐析出好帅啊……
思考:1、在这三支试管中溶液的组成是否相同?哪只浓度大?2、你知道那只试管中溶液的浓度最大?你判断的依据? 对于有色溶液,我们可以根据颜色深浅来判断溶液是浓还是浅;但是这种分法比较粗略,不能准确地表明一定量溶液里究竟含有多少溶质不相同【实验9-6】10%20%结论:溶液中溶质的质量分数越大,溶液浓度越大
溶质的质量分数(一般用百分数表示)溶质的质量分数=溶质质量分数=1、定义:是溶质质量和溶液质量之比 。2、公式:溶质质量
溶质+溶剂×100%例1:将3g高锰酸钾加水配成100g溶液(如图1),
求:(1)图1所示溶液中溶质的质量分数?图1解:答:所得溶液的质量分数为3%。= 3%溶液中溶质的质量分数溶液中溶质的质量分数(2)向图1溶液中再加入400g水后,所得溶液(如图2)中溶质的质量分数?图2解:答:所得溶液的质量分数为0.6%。= 0.6%溶液中溶质的质量分数答:所得甘油溶液中溶质的质量分数为80%。 =80%甘油溶液中溶质的质量分数解:(2)冬天,人们常给皮肤抹上一点甘油溶液,使皮肤保持湿润。用400g甘油溶解在100g水中,配制的甘油溶液效果最佳。该甘油溶液的溶质的质量分数是多少?
①、某氯化钠溶液中溶质的质量分数为10%,其含义是什么?②、已知20℃时,氯化钠的溶解度是36g。有人说:“20℃时氯化钠饱和溶液中溶质的质量分数为36%。”
这种说法对吗?为什么?表示100份质量的氯化钠溶液中含有10份质量的氯化钠,90份质量的水。讨论: 20℃31.6g100g131.6g26.5%判断下列说法是否正确,并加以改正。
⑴在100克水中溶解30克食盐,溶质质量分数是
30%
⑵从100克10%的食盐溶液里取出10克,其浓度
是10%
⑶将100克10%的食盐溶液和100克10%的食盐溶液混合,混合溶液的浓度是20%
⑷ 20℃时,100克水中最多溶解36克食盐,它的溶解度是36克/100克水,浓度是36%( × )( √ )( × )( × )4.变一变:
【例3】在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?【解】答: 配制150kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。1、在30℃时,将25g硝酸钾固体加入100g水中,充分溶解后,所得溶液的溶质质量分数是多少?随堂练习2、某温度时,蒸干100g氯化钾溶液,得到10g氯化钾,求该溶液中溶质的质量分数。1.计算2.称量(量取)3.溶解要配制50g质量分数为6%的NaCl溶液【实验9-7】m(NaCl)=_____g,m(水)=_____g用玻璃棒搅拌,加快溶解。347实验室里要配制10%的氯化钠溶液150g.
(1)实验步骤有: 、 、 、装瓶并贴好标签。
(2)需要的仪器,除药匙、试剂瓶及标签外,还有 .
(3)需要用氯化钠 g,水 mL。
练一练15135计算称量溶解托盘天平 玻璃棒 烧杯 量筒 滴管练习1、将20克KNO3全部溶于80克水中,所得溶液中溶质的质量分数是____。2、100克30%的NaOH溶液中NaOH的质量是____g.20%303、如右图,要配制 这种葡萄糖注射液, 需要葡萄糖和水各
多少g?葡萄糖注射液
规格:250g
内含:葡萄糖5%2、将80g浓度50%硫酸稀释成20%的稀硫酸,所得溶液体积是多少mL?要加水多少g?(20%的硫酸溶液密度为1.2g/mL)例2:现有98%的浓硫酸,要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需要加水多少克?溶液浓缩或稀释的计算依据:溶液稀释前后,溶质的质量保持不变。讨论此公式只适用于饱和溶液里 已知20℃时,食盐的溶解度为36g。这表明,该饱和溶液的溶质质量分数为36%。这种说法对吗?为什么?练习1、在32℃时,KNO3的溶解度为50g,则所得溶液中的溶质的质量分数为_______。33.3%2、已知某温度下,KCl的溶解度为40g。在该温度下,将25g KCl固体加入到50g水中,充分溶解后,形成的溶液中溶质的质量分数为______。28.6%例3:将13克锌粒放入100g稀硫酸中,恰好完全反应,试求: (1)稀硫酸的溶质的质量分数?
(2)反应后所得溶液中溶质的质量分数?m(反应后溶液)=反应前各物质的总质量 — 气体 — 沉淀(固体杂质)有一块10 g的某合金投入到90g 浓度为40%的硫酸中,产生0.2g氢气,并余下1g不溶性固体,则反应后溶液的质量为___g。1. 150g稀盐酸跟一定质量含少量杂质的石灰石恰好完全反应(杂质不溶解,也不参与反应),生成11g二氧化碳。回答下列问题:
(1)写出稀盐酸跟石灰石反应的化学方程式 。
(2)稀盐酸的溶质质量分数?
(3)反应后溶液中溶质的质量?溶液为多少克?
(4)反应后溶液的溶质质量分数? 2.取出80克稀硫酸放入装有足量锌的启普发生器里,当反应完全后,通过实验测定生成氢气的体积为4.48L(已知在标准状况下,氢气的密度0.089g/L) (1)试计算硫酸溶液的溶质质量分数? (2)将反应后的溶液过滤,蒸发结晶,能得到多少克固体? (3)反应后所得溶液的溶质质量分数是多少?
用锌片与稀硫酸反应制H2 ,每次实验结果记录如下:(1)第2、5次产生的氢气质量是多少?(2)稀硫酸的溶质质量分数为多少?
(3) 10g锌片与100g这种稀硫酸充分反应后,所得溶液的溶质质量分数是多少?20℃时,某NaCl溶液中溶质的质量分数为20%。(1)此时溶液中溶质、溶剂和溶液的质量比为多少?
(2)若将100克此溶液分为二等份,则每一份溶液中溶质的质量分数为多少?
(3)向其中一份中加入10g水,则溶质的质量分数为多少?
(4)向另一份中加入2gNaCl固体全部溶解,则溶液中溶质的质量分数为多少?(5)若从100g此溶液中取出5g溶液,则剩余溶液中溶质的质量分数为多少?
(6)若将其中一份溶液升温到40℃时,溶质的质量分数为多少?(溶剂不蒸发)
(7)若要让100g的此溶液溶质的质量分数减半,则需加水多少克?20℃时,某NaCl溶液中溶质的质量分数为20%。随堂练习有5.6g的铁粉与98g稀硫酸刚好反应.求:
(1)生成氢气的质量是多少? (2)稀硫酸的溶质质量分数?
(3)反应后溶液中溶质的质量?溶液为多少克?
(4)反应后溶液的溶质质量分数? 公式:① 溶质质量分数 =
=② m(液) = m(质) + m(剂)=ρ(液)×V(液) ③溶质质量分数=(此公式只适用于饱和溶液)浓溶液的稀释: [稀释前后,溶质质量不变] ① m(浓)×a%=m(稀)×b% ② m(加水)=m(稀)-m(浓)m(反应后溶液)=反应前各物质的总质量 — 气体 — 沉淀(固体杂质)谢谢21世纪教育网(www.21cnjy.com) 中小学教育资源网站 有大把高质量资料?一线教师?一线教研员?
欢迎加入21世纪教育网教师合作团队!!月薪过万不是梦!!
详情请看:
https://www.21cnjy.com/help/help_extract.php
同课章节目录
