仁爱版初中化学九年级下册专题9《化学与生活》测试题(解析版)
文档属性
| 名称 | 仁爱版初中化学九年级下册专题9《化学与生活》测试题(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 211.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-02-25 00:00:00 | ||
图片预览




文档简介
专题9《化学与生活》测试题
一、单选题(每小题只有一个正确答案)
1.下列气体中,对空气有污染的是( )
A.N2 B.O2 C.CO D.CO2
2.墨烯(C60)是首个发现的二维空间材料,从石墨材料中剥离制得。金刚石、石墨、和C60都是由碳元素组成的单质,下列关于三种碳单质的叙述错误的是( )
A.碳原子的排列方式不同 B.都有优良的导电性
C.在氧气中充分燃烧都能生成二氧化碳 D.将石墨剥离制成石墨烯发生了物理变化
3.下列生活用品由合金材料制成的是( )
A.塑料水杯 B.黄铜挂锁 C.汽车橡胶轮胎 D.“的确良”衬衣
4.为人体活动提供能量的主要营养物质是( )
A.蛋白质 B.维生素 C.糖类 D.油脂
5.架空固体燃料,燃烧就会更旺。架空燃料的实质是( )
A.降低可燃物的着火点 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
6.下列物品中是由有机合成材料制成的是( )
A. B. C. D.
7.区别下列物质,且两种方法均能区别开的是( )
选项 需鉴别物质 方法1 方法2
A 硬水和软水 加稀盐酸,观察 加肥皂水,搅拌观察
B 铝丝和铁丝 看一看颜色 取样,插入稀盐酸中观察
C NH4NO3氮肥和KCl钾肥 加水溶解,触摸烧杯 加熟石灰研磨,闻味
D 蚕丝织品和尼龙织品 触摸纺织品 抽丝灼烧观察
8.关于H2、CO、C三种物质,下列说法正确的是( )
A.都是目前最理想的清洁燃料
B.与金属氧化物发生的反应都生成能使澄清石灰水变浑浊的气体
C.在氧气中燃烧,都产生淡蓝色的火焰
D.与金属氧化物反应后,一定有化合物产生
9.茶叶中含锌、硒、茶氨酸(化学式为C7H14N2O3)等多种成分。茶树适宜在pH为5~6的土壤中生长。下列说法不正确的是( )
A.茶氨酸由碳、氧、氧、氮四种元素组成,一个茶氨酸分子中含有3个氧原子
B.茶树不宜在碱性土壤中生长
C.茶氨酸中碳、氢的质量比为42:7
D.茶叶中的锌、硒指单质,茶氨酸属于有机物
10.新修汀的《环境空气质量标准》增设了PM2.5平均浓度限值,PM2.5是指大气中直径小于或等于2.5微米的做粒物.也称为可人肺颐粒物,主要来源于直接排放的r业污染物和汽车尾气等,是形成雾花天气的最大元凶:下列情况不会引起雾霾天气的是( )
A.就地焚烧桔秆 B.鼓励使用太阳能热水器C.鼓励开私家车出行 D.吸烟
11.下列有关说法: ①CO、CO2、SO2、NO2和O3是污染空气的气体成分。②水占地球表面积3/4,因而水资源取之不尽,用之不竭。③煤、石油、天然气和乙醇汽油都是不可再生资源。④水、蛋白质、糖类等是人体六大营养素之一。⑤在田里焚烧秸秆既浪费了资源,也造成了空气污染,是不可取的。⑥木材是造纸的主要原料之一,节约纸张有利于保护森林。⑦铜有良好的导电性,因而大量用于制作电线。正确的组合是( )
A.①②③④ B.④⑤⑥⑦ C.①④⑤⑦ D.②③⑤⑦
12.材料是时代进步的重要标志.下列有关材料的说法中,错误的是( )
A.废弃塑料会带来“白色污染”
B.电木插座具有热固性,破裂后不能热修补
C.塑料、合成纤维、合金都属于有机合成材料
D.蚕丝、棉花都属于天然纤维
13.健康的生活离不开化学,下列说法正确的是( )
A.油脂是重要的营养物质,可大量摄入油脂
B.淀粉属于糖类,可用于为人体提供能量
C.人体缺锌会引起生长发育缓慢,因此锌元素摄入得越多越好
D.某同学体内缺少维生素,该同学饮食中需适量增加的食物是瘦肉、鸡蛋
14.下列物质的转化在给定条件下能实现的是( )
A.
B.
C.
D.
二、填空题
15.海南烩菜 (配料:粉条、瘦肉、食盐、青菜等)中含有的营养素有________(任写两种)。
16.高纯度的单质硅是信息产业的核心材料,没有硅就没有你喜欢的计算机。请用你学过的知识回答下列问题:
(1)地壳中含有大量的硅元素,它的含量仅次于_______元素。
(2)SiO2是沙子的主要成分,工业上制取粗硅的化学方程式为:SiO2+2CSi+2R,
R的化学式为__________;该化学反应的基本类型是_______________。
(3)硅在O2中燃烧生成SiO2,并放出大量的热,有科学家正研究将硅作为新能源。与化石能源相比较,硅燃烧不排放CO2,因而有助于解决的环境问题是______________。
17.生活中出处处有化学。结合你所学的知识回答下列问题:
(1)如图是一种照明用的台灯.其中标示的各部件中,属于合成材料的是 (填序号)。铜质插头是利用了金属铜的 性。
(2)小明在家烧柴火煮饭,他往灶膛里塞满木柴,结果不仅燃烧不旺,反而产生了很多浓烟,这说明可燃物充分燃烧通常要考虑两点:一是燃烧时有足够的空气;二是燃料与空气要有 。同时小明还发现锅底有一层黑色的物质,该黑色的物质是 。
(3)使用硬水会给生活带来许多麻烦,我们常用 的方法来降低水的硬度。
三、推断题
18.A~F都是初中化学中常见的物质,已知:A是一种固体单质,它的组成元素可形成多种形态不同的单质;C是常用于灭火的气体;D为红色固体单质,它们的转化关系如图所示:
请回答:
(1)物质B的化学式为___________。
(2)反应②的化学方程式为___________。
(3)反应③的化学方程式为____________。
(4)由A的组成元素形成的单质较多,请写出其中的任意两种:________。
19.下图所示,A—D是碳和碳的化合物之间的转化关系。图中“→”表示转化关系。已知D是大理石的主要成分,B、C组成元素相同。
(1)写出A的化学式__________________。
(2)①写出C→B化学方程式______________,②写出D→C化学方程式________________。
四、实验题
20.正确选择实验仪器是实验成功的重要保证,下面是实验室中常见的仪器,请按要求填空。
(1)过滤粗盐水所用到的仪器有_______________________(填序号)。
(2)实验室用锌粒和稀硫酸制取氢气,可选上述仪器中的③与⑧组合成发生装置,该反应的化学方程式为_________________。
(3)利用仪器③与⑦可组合成一个贮气装置,收集氢气(氢气难溶于水、密度小于空气)时,气体应从仪器⑦的________(填“a”或“b”)端通入。
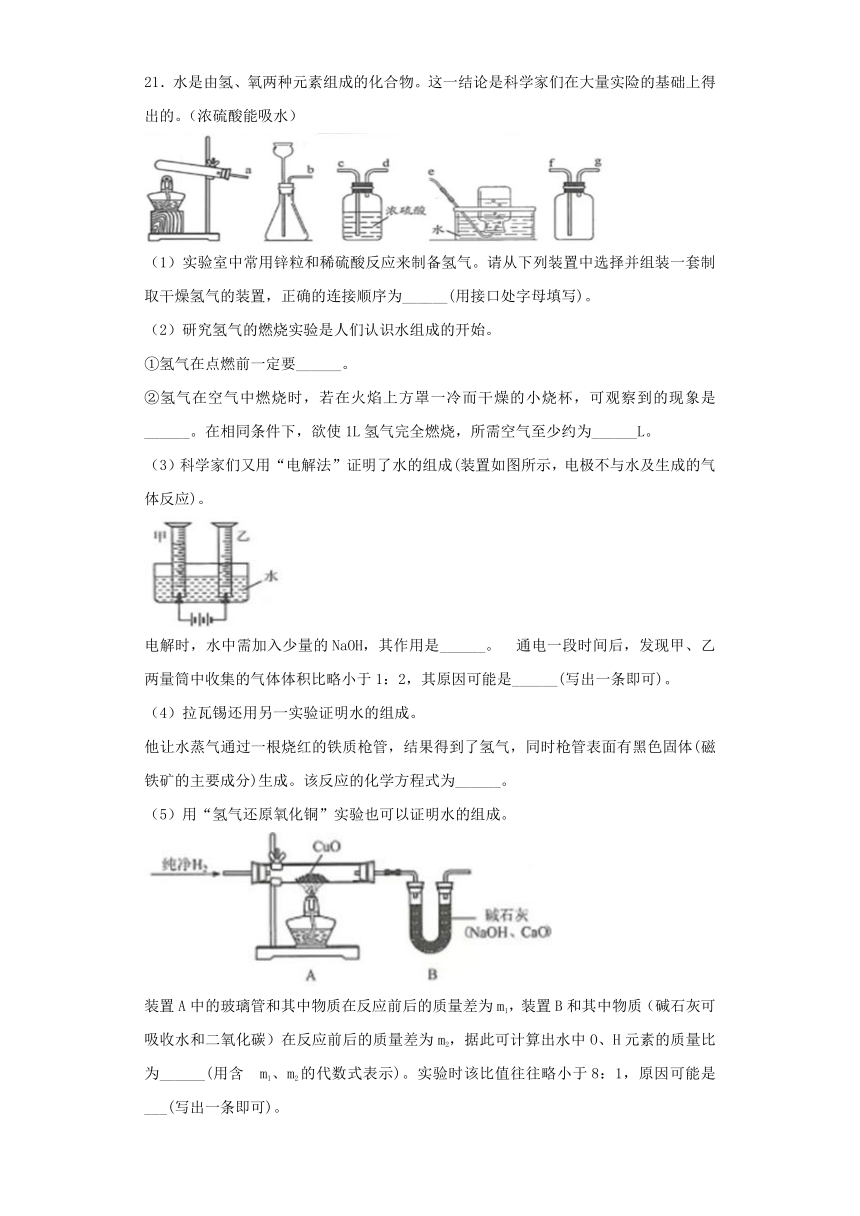
21.水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实险的基础上得出的。(浓硫酸能吸水)
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从下列装置中选择并组装一套制取干燥氢气的装置,正确的连接顺序为______(用接口处字母填写)。
(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要______。
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是______。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为______L。
(3)科学家们又用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体反应)。
电解时,水中需加入少量的NaOH,其作用是______。?通电一段时间后,发现甲、乙两量筒中收集的气体体积比略小于1:2,其原因可能是______(写出一条即可)。
(4)拉瓦锡还用另一实验证明水的组成。
他让水蒸气通过一根烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分)生成。该反应的化学方程式为______。
(5)用“氢气还原氧化铜”实验也可以证明水的组成。
装置A中的玻璃管和其中物质在反应前后的质量差为m1,装置B和其中物质(碱石灰可吸收水和二氧化碳)在反应前后的质量差为m2,据此可计算出水中O、H元素的质量比为______(用含?m1、m2的代数式表示)。实验时该比值往往略小于8:1,原因可能是___(写出一条即可)。
五、计算题
22.某贫血患者共需补充1.4g铁元素,服用的药物中相当于需要硫酸亚铁晶体(FeSO4·7H2O)多少克?
23.在海底和冻土层存在着储量巨大的“天然气水合物”,具有良好开发和应用前景。有科学家开采得到一种天然气水合物样品,取95.6克样品放置在一密闭弃器内,该样品迅速转化为甲烧气体(CH4)和水,将甲烷气体分离并完全燃烧,得到35.2克二氧化碳。求该天然气水合物样品中甲烷的质量分数。(精确到0.1%)
试卷第4页,总6页
参考答案
1.C
【解析】A、氮气为空气的主要成分,无毒,不会造成空气污染,错误;B、氧气无毒,排放在空气中,不会造成空气污染,错误;C、CO有毒,排放在空气中,造成空气污染,正确;D、CO2无毒,排放在空气中,不会造成空气污染,错误。故选C。
点睛:氮气为空气的主要成分,不是污染物,而NO、NO2、CO都有毒,排放在空气中,造成空气污染。
2.B
【解析】
【详解】
A、 金刚石、石墨、和C60都是由碳元素组成的单质,三种碳单质,碳原子的排列方式不同,故A正确;
B、石墨和C60都是优良的导电性,金刚石不能导电,故B错误;
C、金刚石、石墨、和C60都是由碳元素组成,在氧气中完全燃烧都生成二氧化碳,故C正确;
D. 石墨烯是从石墨中剥离出的单层石墨片,石墨烯和石墨是同一种物质,将石墨剥离制成石墨烯发生了物理变化,故D正确。故选B。
3.B
【解析】
试题分析:A、塑料属于合成材料,错误;B、黄铜是合金,属于金属材料,正确;C、合成橡胶属于合成材料,错误;D、的确良属于合成材料,错误。故选B
考点:金属材料与合成材料的区分。
4.C
【解析】人类需要的营养物质有糖类、油脂、蛋白质、维生素、水和无机盐,其中糖类、蛋白质、油脂能够为人体提供能量。其中糖类是人体能量的主要供应者。故选C。
5.D
【解析】分析:促进燃烧的方法是:(1)增大可燃物与氧气的接触面积.(2)增大氧气的浓度.根据实际情况选择促进物质燃烧的方法.
解答:解:使可燃物充分燃烧的条件:一是增大可燃物与氧气的接触面积,二是中的氧气的浓度.一般情况下,增大氧气的浓度较难操作,在空气中燃烧的物质,氧气浓度是一定的,要想燃烧更旺,可增大与氧气的接触面积.“火要空心”就是在燃料中间留一些空气,以增大与氧气的接触面积.故选D
6.A
【解析】
试题分析:A、塑料座椅是用塑料制成的,塑料属于三大合成材料之一,正确;B、青花瓷瓶是用泥土烧制制成的,属于无机非金属材料,错误;C、不锈钢杯是用不锈钢制成的,属于金属材料,错误;D、纯棉衬衫是用纯棉制成的,纯棉属于天然材料,错误。
考点:考查合成材料的使用及其对人和环境的影响的知识。
7.C
【解析】
试题分析:A、硬水和软水都能与稀盐酸反应,但无明显现象,错误;B、铝和铁都是银白色,不能通过观察颜色将二者区分。铝丝和铁丝都能与稀盐酸反应,而产生气泡,但是铝反应快,且得氯化铝溶液是无色的,铁反应慢,得氯化亚铁溶液是浅绿色的,能通过和盐酸反应区分开,错误;C、硝酸铵溶于水溶液温度降低,氯化钾溶于水温度不变;硝酸铵和熟石灰混合研磨因生成氨气产生刺激性气味,氯化钾不能;正确。
D、通过触摸不能区分;灼烧时有烧焦羽毛气味的是蚕丝织品,错误。故选C
考点:物质的鉴别。
8.D
【解析】
根据燃烧产物及现象分析。
解:A、氢气燃烧生成水,无污染,是最理想的清洁燃料,而碳不完全燃烧会生成一氧化碳有毒气体,错误;
B、氢气、CO和C能还原金属氧化物,但氢气还原金属氧化物生成物体是该金属氧化物的金属和水,水不能使澄清石灰水变浑浊,错误;
C、碳在氧气中燃烧时发白光,一氧化碳燃烧发出蓝色火焰,错误;
D、氢气与金属氧化物反应后生成水,碳和一氧化碳与金属氧化物反应后生成二氧化碳,都有化合物生成,正确。
所以本题选D。
9.D
【解析】A、由茶氨酸的化学式可知,茶氨酸是由碳、氢、氧、氮四种元素组成,一个茶氨酸分子中含有3个氧原子,正确;B、茶树适宜在pH为5-6的土壤中生长,适宜在偏酸性土壤中生长,不宜在碱性土壤中生长,正确;C、茶氨酸中碳、氢的质量=12×7:1×14=42:7,正确;D、茶叶中的锌、硒指的是元素,不是单质,茶氨酸是含碳的有机物属于有机物,错误。故选D。
点睛:结合新信息、灵活运用化学式的含义是解题的关键。
10.B
【解析】A、就地焚烧桔秆燃烧后可能有不完全燃烧的产物,会引起雾霾,错误;
B、使用太阳能热水器可以减少化石燃料的燃烧,正确;
C、开私家车可能会因化石燃料的燃烧产生固体小颗粒,造成雾霾,错误;
D、吸烟可能引起雾霾,错误。故选B。
11.B
【解析】根据计入空气污染指数的项目分析;
根据水占地球表面积的多少分析;
根据资源类型分析;
根据六大营养素分析;
⑥根据“绿色化学”分析;
⑦根据铜的性质分析。
解:①计入空气污染指数的项目是:CO、SO2、NO2、O3和可吸入颗粒物。错误;
②水占地球表面积的71%。故错误;③乙醇汽油是可再生资源。故错误;④六大营养素是水、蛋白质、糖类、油脂、无机盐、维生素。正确;⑤在田里焚烧秸秆既浪费了资源,也造成了空气污染,是不可取的。正确;⑥木材是造纸的主要原料之一,节约纸张有利于保护森林。正确;⑦铜有良好的导电性,因而大量用于制作电线。正确。
故本题选B。
12.C
【解析】试题分析:A、废弃塑料会带来“白色污染”,正确;B、电木插座具有热固性,破裂后不能热修补,正确;C、合金属于金属材料,错误;D、蚕丝、棉花都属于天然纤维,正确。
考点:考查合成材料的使用及其对人和环境的影响;有机高分子材料的分类及鉴别方法的知识。
13.B
【解析】A.不可大量摄入油脂,否则会危害人体健康,错误;
B.淀粉属于糖类,可为人体提供能量,正确;
C.锌属于微量元素,摄入过多也会引起别的症症,错误;
D.缺少维生素应多吃水果、蔬菜,错误。
14.D
【解析】A.盐与盐反应时,两种均必须可溶,AgCl不溶于水,无法与碳酸钠反应,故A错误;B.弱酸不能制强酸,则CaCl2溶液中通CO2不可能反应生成碳酸钙沉淀和稀盐酸,故B错误;C.Fe在氧气中燃烧生成黑色的四氧化三铁,故C错误;D.硫酸铜溶液中滴加NaOH制得氢氧化铜悬浊液,加入葡萄糖并加热后生成砖红色沉淀Cu2O,故D正确;答案为D。
15.蛋白质、糖类或淀粉
【解析】
【详解】
粉条中富含有糖类,廋肉中富含有蛋白质,食盐中富含有无机盐,青菜中富含有维生素。
16. 氧 CO 置换反应 温室效应
【解析】(1)地壳中的元素含量由多到少的顺序依次是氧、硅、铝、铁。(2)反应前后各种原子的个数相等,故 R的化学式为CO ,单化化单是置换。(3)二氧化碳是引起温室效应的主要气体。
17.
(1)⑤ 导电
(2)足够大的接触面积 碳
(3)煮沸
【解析】
试题分析:
(1)塑料灯座是用塑料制成的,属于合成材料;故填:⑤;铜质插头是利用了金属铜的导电性,故填:导电;
(2)在烧材煮饭时,引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明物质充分燃烧需要的条件:一是燃烧时要有足够多的空气,二是燃料与空气要有足够大的接触面积;同时小明还发现锅底有一层黑色的物质,该黑色的物质是碳;
(3)使用硬水会给生活带来许多麻烦,我们常用煮沸的方法来降低水的硬度。
考点:合成材料的使用及其对人和环境的影响;硬水与软水;金属的物理性质及用途;完全燃烧与不完全燃烧
18.CuO C+CO22CO Fe2O3+3CO2Fe+3CO2 金刚石、石墨
【解析】
【详解】
C是常用于灭火的气体,则C为二氧化碳,A是一种固体单质,它的组成元素可形成多种形态不同的单质,碳元素可形成不同单质,A可能是碳单质,A同时能够和二氧化碳反应生成能够和氧化铁反应的物质,碳与二氧化碳在高温条件下生成一氧化碳,一氧化碳与氧化铁在高温条件下生成铁和二氧化碳,则E为一氧化碳,F为铁。D为红色固体单质,D是铜,氧化铜在高温条件下生成铜和二氧化碳,则B是氧化铜。代入框图,推断合理。(1)B是氧化铜,化学式为CuO。(2)反应②是二氧化碳与碳高温反应生成一氧化碳,化学方程式为C+CO22CO。(3)反应③是一氧化碳与氧化铁高温反应生成铁和二氧化碳,化学方程式为Fe2O3+3CO2Fe+3CO2。(4)碳元素能组成金刚石、石墨等。
【点睛】
在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
19.C CO2+C2CO CaCO3+2HCl===CaCl2+H2O+CO2↑(或CaCO3CaO+CO2↑)
【解析】
【分析】
A—D是碳和碳的化合物之间的转化关系,则A—D均含有碳元素;D是大理石的主要成分,所以D为碳酸钙;C与D(碳酸钙)可以相互转化,则C为二氧化碳;B、C组成元素相同,则B为一氧化碳;A通过化学反应能生成一氧化碳和二氧化碳,则A为碳。
【详解】
(1)由分析可知,A为碳,其化学式为C,故填C。
(2)①反应C→B是二氧化碳与碳在高温的条件下反应生成一氧化碳,故反应的化学方程式写为:CO2+C2CO;
②反应D→C是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,或碳酸钙在高温条件下分解生成氧化钙和二氧化碳,故反应的化学方程式写为CaCO3+2HCl=CaCl2+H2O+CO2↑或CaCO3CaO+CO2↑。
20. ②④⑥⑨ Zn+H2SO4═ZnSO4+ H2↑ b
【解析】本题考查了过滤的装置,化学方程式的书写,氢气的收集等。
(1)过滤粗盐水所用到的仪器有烧杯、漏斗、玻璃棒、铁架台,故选②④⑥⑨;
(2)锌和稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为Zn+H2SO4═ZnSO4+ H2↑;
(3)氢气难溶于水、密度小于空气。利用仪器③与⑦可组合成一个贮气装置,收集氢气时,气体应从仪器⑦的b端通入。
21.b-c-d-g 验纯 淡蓝色火焰,烧杯内壁出现水雾 2.5 增强水的导电性 相同条件下,氧气比氢气溶得多 3Fe+4H2OFe3O4+4H2 m1:(m2-m1) 吸收空气中的水和二氧化碳
【解析】
【详解】
(1)锌与稀硫酸反应生成硫酸锌和氢气,锌是固体,稀硫酸是液体,反应是在常温下进行的,故选择的发生装置为固液常温型,选用第二套装置来制取,用盛有浓硫酸的洗气瓶来对氢气进行干燥,气体长管进短管出,氢气难溶于水,密度比空气小,但制取干燥氢气,只能用向下排空气法来收集,短管进长管出,所以正确的连接顺序是b-c-d-g。
(2)①氢气是可燃性的气体,在点燃前一定要验纯,不纯可能会发生爆炸;②氢气在空气中燃烧时是淡蓝色火焰,反应生成了水,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是干燥内壁有水雾生成;氢气在氧气中燃烧会生成水,反应方程式为2H2+O22H2O,在相同条件下,欲使1L氢气完全燃烧,需要氧气的体积是0.5L,所需空气至少约为2.5L。
(3)电解时,水中需加入少量的NaOH,增强导电性。一段时间后,甲、乙两量简中收集的气体体积比略小于1:2的原因可能是在相同条件下,O2较H2稍易溶于水。
(4)由题意可知在高温条件下,铁与水反应生成了四氧化三铁和氢气,该反应的化学方程式为:3Fe+4H2OFe3O4+4H2。
(5)氢气可以还原氧化铜,生成铜单质和水,装置A中的玻璃管和其中物质在反应前后的质量差m1为氧化铜中氧元素的质量,也就是水中氧元素的质量,装置B和其中物质在反应前后的质量差为m2是生成的水的质量,据此可计算出水中O、H元素的质量比为m1:(m2-m1),实验时空气中的H2O、CO2等进入B中或生成的铜又部分被氧化等原因可能导致该比值往往略小于8:1。
22.FeSO4·7H20的相对分子质量为:56+32十16×4+18×7=278
解:设需硫酸亚铁晶体的质量为x。
x×56/278×100%=1.4g x=6.95 g
【解析】解:FeSO4·7H20的相对分子质量为:56+32十16×4+18×7=278;
设需硫酸亚铁晶体的质量为x,
x××100%=1.4g
x=6.95 g。
23.13.4%
【解析】设生成35.2g二氧化碳的需要的甲烷为X
CH4+ 2O2点燃CO2+ 2H2O
16 44
X 35.2g
16/x=44/35.2g
X=12.8g
该天然气水合物样品中甲烷的质量分数为12.8g/95.6g×100%=13.4%
答:该天然气水合物样品中甲烷的质量分数13.4%
一、单选题(每小题只有一个正确答案)
1.下列气体中,对空气有污染的是( )
A.N2 B.O2 C.CO D.CO2
2.墨烯(C60)是首个发现的二维空间材料,从石墨材料中剥离制得。金刚石、石墨、和C60都是由碳元素组成的单质,下列关于三种碳单质的叙述错误的是( )
A.碳原子的排列方式不同 B.都有优良的导电性
C.在氧气中充分燃烧都能生成二氧化碳 D.将石墨剥离制成石墨烯发生了物理变化
3.下列生活用品由合金材料制成的是( )
A.塑料水杯 B.黄铜挂锁 C.汽车橡胶轮胎 D.“的确良”衬衣
4.为人体活动提供能量的主要营养物质是( )
A.蛋白质 B.维生素 C.糖类 D.油脂
5.架空固体燃料,燃烧就会更旺。架空燃料的实质是( )
A.降低可燃物的着火点 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
6.下列物品中是由有机合成材料制成的是( )
A. B. C. D.
7.区别下列物质,且两种方法均能区别开的是( )
选项 需鉴别物质 方法1 方法2
A 硬水和软水 加稀盐酸,观察 加肥皂水,搅拌观察
B 铝丝和铁丝 看一看颜色 取样,插入稀盐酸中观察
C NH4NO3氮肥和KCl钾肥 加水溶解,触摸烧杯 加熟石灰研磨,闻味
D 蚕丝织品和尼龙织品 触摸纺织品 抽丝灼烧观察
8.关于H2、CO、C三种物质,下列说法正确的是( )
A.都是目前最理想的清洁燃料
B.与金属氧化物发生的反应都生成能使澄清石灰水变浑浊的气体
C.在氧气中燃烧,都产生淡蓝色的火焰
D.与金属氧化物反应后,一定有化合物产生
9.茶叶中含锌、硒、茶氨酸(化学式为C7H14N2O3)等多种成分。茶树适宜在pH为5~6的土壤中生长。下列说法不正确的是( )
A.茶氨酸由碳、氧、氧、氮四种元素组成,一个茶氨酸分子中含有3个氧原子
B.茶树不宜在碱性土壤中生长
C.茶氨酸中碳、氢的质量比为42:7
D.茶叶中的锌、硒指单质,茶氨酸属于有机物
10.新修汀的《环境空气质量标准》增设了PM2.5平均浓度限值,PM2.5是指大气中直径小于或等于2.5微米的做粒物.也称为可人肺颐粒物,主要来源于直接排放的r业污染物和汽车尾气等,是形成雾花天气的最大元凶:下列情况不会引起雾霾天气的是( )
A.就地焚烧桔秆 B.鼓励使用太阳能热水器C.鼓励开私家车出行 D.吸烟
11.下列有关说法: ①CO、CO2、SO2、NO2和O3是污染空气的气体成分。②水占地球表面积3/4,因而水资源取之不尽,用之不竭。③煤、石油、天然气和乙醇汽油都是不可再生资源。④水、蛋白质、糖类等是人体六大营养素之一。⑤在田里焚烧秸秆既浪费了资源,也造成了空气污染,是不可取的。⑥木材是造纸的主要原料之一,节约纸张有利于保护森林。⑦铜有良好的导电性,因而大量用于制作电线。正确的组合是( )
A.①②③④ B.④⑤⑥⑦ C.①④⑤⑦ D.②③⑤⑦
12.材料是时代进步的重要标志.下列有关材料的说法中,错误的是( )
A.废弃塑料会带来“白色污染”
B.电木插座具有热固性,破裂后不能热修补
C.塑料、合成纤维、合金都属于有机合成材料
D.蚕丝、棉花都属于天然纤维
13.健康的生活离不开化学,下列说法正确的是( )
A.油脂是重要的营养物质,可大量摄入油脂
B.淀粉属于糖类,可用于为人体提供能量
C.人体缺锌会引起生长发育缓慢,因此锌元素摄入得越多越好
D.某同学体内缺少维生素,该同学饮食中需适量增加的食物是瘦肉、鸡蛋
14.下列物质的转化在给定条件下能实现的是( )
A.
B.
C.
D.
二、填空题
15.海南烩菜 (配料:粉条、瘦肉、食盐、青菜等)中含有的营养素有________(任写两种)。
16.高纯度的单质硅是信息产业的核心材料,没有硅就没有你喜欢的计算机。请用你学过的知识回答下列问题:
(1)地壳中含有大量的硅元素,它的含量仅次于_______元素。
(2)SiO2是沙子的主要成分,工业上制取粗硅的化学方程式为:SiO2+2CSi+2R,
R的化学式为__________;该化学反应的基本类型是_______________。
(3)硅在O2中燃烧生成SiO2,并放出大量的热,有科学家正研究将硅作为新能源。与化石能源相比较,硅燃烧不排放CO2,因而有助于解决的环境问题是______________。
17.生活中出处处有化学。结合你所学的知识回答下列问题:
(1)如图是一种照明用的台灯.其中标示的各部件中,属于合成材料的是 (填序号)。铜质插头是利用了金属铜的 性。
(2)小明在家烧柴火煮饭,他往灶膛里塞满木柴,结果不仅燃烧不旺,反而产生了很多浓烟,这说明可燃物充分燃烧通常要考虑两点:一是燃烧时有足够的空气;二是燃料与空气要有 。同时小明还发现锅底有一层黑色的物质,该黑色的物质是 。
(3)使用硬水会给生活带来许多麻烦,我们常用 的方法来降低水的硬度。
三、推断题
18.A~F都是初中化学中常见的物质,已知:A是一种固体单质,它的组成元素可形成多种形态不同的单质;C是常用于灭火的气体;D为红色固体单质,它们的转化关系如图所示:
请回答:
(1)物质B的化学式为___________。
(2)反应②的化学方程式为___________。
(3)反应③的化学方程式为____________。
(4)由A的组成元素形成的单质较多,请写出其中的任意两种:________。
19.下图所示,A—D是碳和碳的化合物之间的转化关系。图中“→”表示转化关系。已知D是大理石的主要成分,B、C组成元素相同。
(1)写出A的化学式__________________。
(2)①写出C→B化学方程式______________,②写出D→C化学方程式________________。
四、实验题
20.正确选择实验仪器是实验成功的重要保证,下面是实验室中常见的仪器,请按要求填空。
(1)过滤粗盐水所用到的仪器有_______________________(填序号)。
(2)实验室用锌粒和稀硫酸制取氢气,可选上述仪器中的③与⑧组合成发生装置,该反应的化学方程式为_________________。
(3)利用仪器③与⑦可组合成一个贮气装置,收集氢气(氢气难溶于水、密度小于空气)时,气体应从仪器⑦的________(填“a”或“b”)端通入。
21.水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实险的基础上得出的。(浓硫酸能吸水)
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从下列装置中选择并组装一套制取干燥氢气的装置,正确的连接顺序为______(用接口处字母填写)。
(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要______。
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是______。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为______L。
(3)科学家们又用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体反应)。
电解时,水中需加入少量的NaOH,其作用是______。?通电一段时间后,发现甲、乙两量筒中收集的气体体积比略小于1:2,其原因可能是______(写出一条即可)。
(4)拉瓦锡还用另一实验证明水的组成。
他让水蒸气通过一根烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分)生成。该反应的化学方程式为______。
(5)用“氢气还原氧化铜”实验也可以证明水的组成。
装置A中的玻璃管和其中物质在反应前后的质量差为m1,装置B和其中物质(碱石灰可吸收水和二氧化碳)在反应前后的质量差为m2,据此可计算出水中O、H元素的质量比为______(用含?m1、m2的代数式表示)。实验时该比值往往略小于8:1,原因可能是___(写出一条即可)。
五、计算题
22.某贫血患者共需补充1.4g铁元素,服用的药物中相当于需要硫酸亚铁晶体(FeSO4·7H2O)多少克?
23.在海底和冻土层存在着储量巨大的“天然气水合物”,具有良好开发和应用前景。有科学家开采得到一种天然气水合物样品,取95.6克样品放置在一密闭弃器内,该样品迅速转化为甲烧气体(CH4)和水,将甲烷气体分离并完全燃烧,得到35.2克二氧化碳。求该天然气水合物样品中甲烷的质量分数。(精确到0.1%)
试卷第4页,总6页
参考答案
1.C
【解析】A、氮气为空气的主要成分,无毒,不会造成空气污染,错误;B、氧气无毒,排放在空气中,不会造成空气污染,错误;C、CO有毒,排放在空气中,造成空气污染,正确;D、CO2无毒,排放在空气中,不会造成空气污染,错误。故选C。
点睛:氮气为空气的主要成分,不是污染物,而NO、NO2、CO都有毒,排放在空气中,造成空气污染。
2.B
【解析】
【详解】
A、 金刚石、石墨、和C60都是由碳元素组成的单质,三种碳单质,碳原子的排列方式不同,故A正确;
B、石墨和C60都是优良的导电性,金刚石不能导电,故B错误;
C、金刚石、石墨、和C60都是由碳元素组成,在氧气中完全燃烧都生成二氧化碳,故C正确;
D. 石墨烯是从石墨中剥离出的单层石墨片,石墨烯和石墨是同一种物质,将石墨剥离制成石墨烯发生了物理变化,故D正确。故选B。
3.B
【解析】
试题分析:A、塑料属于合成材料,错误;B、黄铜是合金,属于金属材料,正确;C、合成橡胶属于合成材料,错误;D、的确良属于合成材料,错误。故选B
考点:金属材料与合成材料的区分。
4.C
【解析】人类需要的营养物质有糖类、油脂、蛋白质、维生素、水和无机盐,其中糖类、蛋白质、油脂能够为人体提供能量。其中糖类是人体能量的主要供应者。故选C。
5.D
【解析】分析:促进燃烧的方法是:(1)增大可燃物与氧气的接触面积.(2)增大氧气的浓度.根据实际情况选择促进物质燃烧的方法.
解答:解:使可燃物充分燃烧的条件:一是增大可燃物与氧气的接触面积,二是中的氧气的浓度.一般情况下,增大氧气的浓度较难操作,在空气中燃烧的物质,氧气浓度是一定的,要想燃烧更旺,可增大与氧气的接触面积.“火要空心”就是在燃料中间留一些空气,以增大与氧气的接触面积.故选D
6.A
【解析】
试题分析:A、塑料座椅是用塑料制成的,塑料属于三大合成材料之一,正确;B、青花瓷瓶是用泥土烧制制成的,属于无机非金属材料,错误;C、不锈钢杯是用不锈钢制成的,属于金属材料,错误;D、纯棉衬衫是用纯棉制成的,纯棉属于天然材料,错误。
考点:考查合成材料的使用及其对人和环境的影响的知识。
7.C
【解析】
试题分析:A、硬水和软水都能与稀盐酸反应,但无明显现象,错误;B、铝和铁都是银白色,不能通过观察颜色将二者区分。铝丝和铁丝都能与稀盐酸反应,而产生气泡,但是铝反应快,且得氯化铝溶液是无色的,铁反应慢,得氯化亚铁溶液是浅绿色的,能通过和盐酸反应区分开,错误;C、硝酸铵溶于水溶液温度降低,氯化钾溶于水温度不变;硝酸铵和熟石灰混合研磨因生成氨气产生刺激性气味,氯化钾不能;正确。
D、通过触摸不能区分;灼烧时有烧焦羽毛气味的是蚕丝织品,错误。故选C
考点:物质的鉴别。
8.D
【解析】
根据燃烧产物及现象分析。
解:A、氢气燃烧生成水,无污染,是最理想的清洁燃料,而碳不完全燃烧会生成一氧化碳有毒气体,错误;
B、氢气、CO和C能还原金属氧化物,但氢气还原金属氧化物生成物体是该金属氧化物的金属和水,水不能使澄清石灰水变浑浊,错误;
C、碳在氧气中燃烧时发白光,一氧化碳燃烧发出蓝色火焰,错误;
D、氢气与金属氧化物反应后生成水,碳和一氧化碳与金属氧化物反应后生成二氧化碳,都有化合物生成,正确。
所以本题选D。
9.D
【解析】A、由茶氨酸的化学式可知,茶氨酸是由碳、氢、氧、氮四种元素组成,一个茶氨酸分子中含有3个氧原子,正确;B、茶树适宜在pH为5-6的土壤中生长,适宜在偏酸性土壤中生长,不宜在碱性土壤中生长,正确;C、茶氨酸中碳、氢的质量=12×7:1×14=42:7,正确;D、茶叶中的锌、硒指的是元素,不是单质,茶氨酸是含碳的有机物属于有机物,错误。故选D。
点睛:结合新信息、灵活运用化学式的含义是解题的关键。
10.B
【解析】A、就地焚烧桔秆燃烧后可能有不完全燃烧的产物,会引起雾霾,错误;
B、使用太阳能热水器可以减少化石燃料的燃烧,正确;
C、开私家车可能会因化石燃料的燃烧产生固体小颗粒,造成雾霾,错误;
D、吸烟可能引起雾霾,错误。故选B。
11.B
【解析】根据计入空气污染指数的项目分析;
根据水占地球表面积的多少分析;
根据资源类型分析;
根据六大营养素分析;
⑥根据“绿色化学”分析;
⑦根据铜的性质分析。
解:①计入空气污染指数的项目是:CO、SO2、NO2、O3和可吸入颗粒物。错误;
②水占地球表面积的71%。故错误;③乙醇汽油是可再生资源。故错误;④六大营养素是水、蛋白质、糖类、油脂、无机盐、维生素。正确;⑤在田里焚烧秸秆既浪费了资源,也造成了空气污染,是不可取的。正确;⑥木材是造纸的主要原料之一,节约纸张有利于保护森林。正确;⑦铜有良好的导电性,因而大量用于制作电线。正确。
故本题选B。
12.C
【解析】试题分析:A、废弃塑料会带来“白色污染”,正确;B、电木插座具有热固性,破裂后不能热修补,正确;C、合金属于金属材料,错误;D、蚕丝、棉花都属于天然纤维,正确。
考点:考查合成材料的使用及其对人和环境的影响;有机高分子材料的分类及鉴别方法的知识。
13.B
【解析】A.不可大量摄入油脂,否则会危害人体健康,错误;
B.淀粉属于糖类,可为人体提供能量,正确;
C.锌属于微量元素,摄入过多也会引起别的症症,错误;
D.缺少维生素应多吃水果、蔬菜,错误。
14.D
【解析】A.盐与盐反应时,两种均必须可溶,AgCl不溶于水,无法与碳酸钠反应,故A错误;B.弱酸不能制强酸,则CaCl2溶液中通CO2不可能反应生成碳酸钙沉淀和稀盐酸,故B错误;C.Fe在氧气中燃烧生成黑色的四氧化三铁,故C错误;D.硫酸铜溶液中滴加NaOH制得氢氧化铜悬浊液,加入葡萄糖并加热后生成砖红色沉淀Cu2O,故D正确;答案为D。
15.蛋白质、糖类或淀粉
【解析】
【详解】
粉条中富含有糖类,廋肉中富含有蛋白质,食盐中富含有无机盐,青菜中富含有维生素。
16. 氧 CO 置换反应 温室效应
【解析】(1)地壳中的元素含量由多到少的顺序依次是氧、硅、铝、铁。(2)反应前后各种原子的个数相等,故 R的化学式为CO ,单化化单是置换。(3)二氧化碳是引起温室效应的主要气体。
17.
(1)⑤ 导电
(2)足够大的接触面积 碳
(3)煮沸
【解析】
试题分析:
(1)塑料灯座是用塑料制成的,属于合成材料;故填:⑤;铜质插头是利用了金属铜的导电性,故填:导电;
(2)在烧材煮饭时,引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明物质充分燃烧需要的条件:一是燃烧时要有足够多的空气,二是燃料与空气要有足够大的接触面积;同时小明还发现锅底有一层黑色的物质,该黑色的物质是碳;
(3)使用硬水会给生活带来许多麻烦,我们常用煮沸的方法来降低水的硬度。
考点:合成材料的使用及其对人和环境的影响;硬水与软水;金属的物理性质及用途;完全燃烧与不完全燃烧
18.CuO C+CO22CO Fe2O3+3CO2Fe+3CO2 金刚石、石墨
【解析】
【详解】
C是常用于灭火的气体,则C为二氧化碳,A是一种固体单质,它的组成元素可形成多种形态不同的单质,碳元素可形成不同单质,A可能是碳单质,A同时能够和二氧化碳反应生成能够和氧化铁反应的物质,碳与二氧化碳在高温条件下生成一氧化碳,一氧化碳与氧化铁在高温条件下生成铁和二氧化碳,则E为一氧化碳,F为铁。D为红色固体单质,D是铜,氧化铜在高温条件下生成铜和二氧化碳,则B是氧化铜。代入框图,推断合理。(1)B是氧化铜,化学式为CuO。(2)反应②是二氧化碳与碳高温反应生成一氧化碳,化学方程式为C+CO22CO。(3)反应③是一氧化碳与氧化铁高温反应生成铁和二氧化碳,化学方程式为Fe2O3+3CO2Fe+3CO2。(4)碳元素能组成金刚石、石墨等。
【点睛】
在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
19.C CO2+C2CO CaCO3+2HCl===CaCl2+H2O+CO2↑(或CaCO3CaO+CO2↑)
【解析】
【分析】
A—D是碳和碳的化合物之间的转化关系,则A—D均含有碳元素;D是大理石的主要成分,所以D为碳酸钙;C与D(碳酸钙)可以相互转化,则C为二氧化碳;B、C组成元素相同,则B为一氧化碳;A通过化学反应能生成一氧化碳和二氧化碳,则A为碳。
【详解】
(1)由分析可知,A为碳,其化学式为C,故填C。
(2)①反应C→B是二氧化碳与碳在高温的条件下反应生成一氧化碳,故反应的化学方程式写为:CO2+C2CO;
②反应D→C是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,或碳酸钙在高温条件下分解生成氧化钙和二氧化碳,故反应的化学方程式写为CaCO3+2HCl=CaCl2+H2O+CO2↑或CaCO3CaO+CO2↑。
20. ②④⑥⑨ Zn+H2SO4═ZnSO4+ H2↑ b
【解析】本题考查了过滤的装置,化学方程式的书写,氢气的收集等。
(1)过滤粗盐水所用到的仪器有烧杯、漏斗、玻璃棒、铁架台,故选②④⑥⑨;
(2)锌和稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为Zn+H2SO4═ZnSO4+ H2↑;
(3)氢气难溶于水、密度小于空气。利用仪器③与⑦可组合成一个贮气装置,收集氢气时,气体应从仪器⑦的b端通入。
21.b-c-d-g 验纯 淡蓝色火焰,烧杯内壁出现水雾 2.5 增强水的导电性 相同条件下,氧气比氢气溶得多 3Fe+4H2OFe3O4+4H2 m1:(m2-m1) 吸收空气中的水和二氧化碳
【解析】
【详解】
(1)锌与稀硫酸反应生成硫酸锌和氢气,锌是固体,稀硫酸是液体,反应是在常温下进行的,故选择的发生装置为固液常温型,选用第二套装置来制取,用盛有浓硫酸的洗气瓶来对氢气进行干燥,气体长管进短管出,氢气难溶于水,密度比空气小,但制取干燥氢气,只能用向下排空气法来收集,短管进长管出,所以正确的连接顺序是b-c-d-g。
(2)①氢气是可燃性的气体,在点燃前一定要验纯,不纯可能会发生爆炸;②氢气在空气中燃烧时是淡蓝色火焰,反应生成了水,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是干燥内壁有水雾生成;氢气在氧气中燃烧会生成水,反应方程式为2H2+O22H2O,在相同条件下,欲使1L氢气完全燃烧,需要氧气的体积是0.5L,所需空气至少约为2.5L。
(3)电解时,水中需加入少量的NaOH,增强导电性。一段时间后,甲、乙两量简中收集的气体体积比略小于1:2的原因可能是在相同条件下,O2较H2稍易溶于水。
(4)由题意可知在高温条件下,铁与水反应生成了四氧化三铁和氢气,该反应的化学方程式为:3Fe+4H2OFe3O4+4H2。
(5)氢气可以还原氧化铜,生成铜单质和水,装置A中的玻璃管和其中物质在反应前后的质量差m1为氧化铜中氧元素的质量,也就是水中氧元素的质量,装置B和其中物质在反应前后的质量差为m2是生成的水的质量,据此可计算出水中O、H元素的质量比为m1:(m2-m1),实验时空气中的H2O、CO2等进入B中或生成的铜又部分被氧化等原因可能导致该比值往往略小于8:1。
22.FeSO4·7H20的相对分子质量为:56+32十16×4+18×7=278
解:设需硫酸亚铁晶体的质量为x。
x×56/278×100%=1.4g x=6.95 g
【解析】解:FeSO4·7H20的相对分子质量为:56+32十16×4+18×7=278;
设需硫酸亚铁晶体的质量为x,
x××100%=1.4g
x=6.95 g。
23.13.4%
【解析】设生成35.2g二氧化碳的需要的甲烷为X
CH4+ 2O2点燃CO2+ 2H2O
16 44
X 35.2g
16/x=44/35.2g
X=12.8g
该天然气水合物样品中甲烷的质量分数为12.8g/95.6g×100%=13.4%
答:该天然气水合物样品中甲烷的质量分数13.4%
