人教版高中化学必修二3.3 乙酸 课件
文档属性
| 名称 | 人教版高中化学必修二3.3 乙酸 课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 866.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-03 00:00:00 | ||
图片预览











文档简介
课件30张PPT。 二、乙酸 3.3生活中两种常见的有机物用浸过白醋的柔软抹布擦拭卫生间中的瓷砖,
能够去除白色钙化水垢; 少量醋加水浸泡海带,可缩短涨发时间;每天用40%的醋水溶液,加热后洗头可 防治脱发,头屑过多。煨牛肉前加点醋,可使牛肉易酥;烧煮羊肉加少量醋能除膻味;你知道么?——醋的妙用烧鱼时加醋,去除鱼腥味;颜 色:
气 味:
状 态:
沸 点:
熔 点:
溶解性:无色强烈刺激性气味液体(易挥发)一、乙酸的物理性质易溶于水和乙醇熔点16.6℃。当气温低于熔点时,乙酸凝结成类似冰的晶体,所以纯净的乙酸又称冰醋酸。117.9℃16.6℃二、乙酸分子的结构
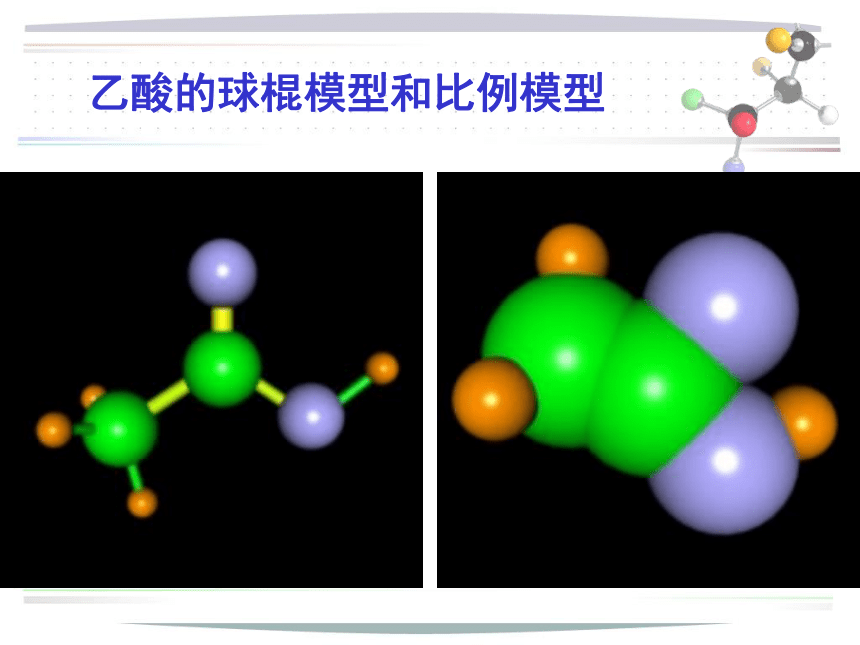
C2H4O2或 CH3COOH(或 —COOH)乙酸的球棍模型和比例模型 为什么可以用醋除去水垢?(水垢的主要成分为CaCO3)
考考你CaCO3 + 2CH3COOH →
(CH3COO)2Ca + CO2↑+ H2O酸性:CH3COOH>H2CO3 H O
H - C-C-O-H
H 乙酸为一元弱酸,其酸性比 H2CO3强,具有酸的通性;其显酸性时断键位置为:使石蕊试液变红
与活泼金属反应(如:Na)
与碱性氧化物反应(如:Na2O)
与碱反应(如:NaOH)
与某些盐反应(如:Na2CO3)1. 酸性(弱酸性)酸的通性三、乙酸的化学性质 [生活小窍门]
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。这是为什么呢?1.加入几颗碎瓷片;
2.往试管中加入3mL乙醇;
3.边振荡边加入2mL浓硫酸,待冷却后再加入 2mL乙酸;
4.按图所示连接装置,缓慢加热,将产物通入到饱和碳
酸钠溶液的液面上。实验步骤:2. 乙酸与乙醇的反应现象:溶液分层,上层有无色透明的油状液体产生,并有香味。酯化反应:酸与醇反应生成酯和水的反应.乙酸乙酯(香味)可逆反应[问题与讨论]
(1)浓硫酸的作用?
(2)装药品的顺序?
(3)饱和碳酸钠溶液的作用是什么?
(4)导气管不能插入Na2CO3溶液中的原因
催化剂、吸水剂①乙醇,②浓硫酸,待冷却加③乙酸。①溶解乙醇;②吸收乙酸;
③降低乙酸乙酯的溶解度,便于分层。防止倒吸 防倒吸装置还有?防倒吸装置还有:第一种方式第二种方式[交流与思考]
酯化反应可能哪些脱水方式? 如何确定?酯化反应实质:酸脱羟基,醇脱氢(羟基上的)CH3 C OH + H 18O C2H5通过同位素原子示踪法测知反应如下:酯化反应也属于取代反应完成下列反应的化学方程式.小结:酸性酯化酯类广泛存在于自然界中酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用饮料、糖果、香水、化妆品中的香料,也可用作指甲油、胶水的溶剂。 是一种重要的化工原料
在日常生活中也有广泛的用途四、乙酸的用途 乙酸是一种重要的有机化工原料,可用于生产醋酸纤维、合成纤维、喷漆溶剂、香料、燃料、医药和农药等。课堂练习:课本p76 4.下列物质中,不能用来区分乙酸、乙醇、苯的是( )
A.金属钠
B.溴水
C.碳酸钠溶液
D.紫色石蕊试液B 6.除去乙酸乙酯中含有的乙酸,有效的处理方法是( )
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液C设计一个实验,比较醋酸和碳酸的酸性强弱.酸性:
CH3COOH > H2CO3 科学探究醋酸碳酸钠溶液澄清石灰水变浑浊作业:第一课时:
课时作业15:第2、3、4、15
作业:第二课时:
课时作业15:剩余题目
能够去除白色钙化水垢; 少量醋加水浸泡海带,可缩短涨发时间;每天用40%的醋水溶液,加热后洗头可 防治脱发,头屑过多。煨牛肉前加点醋,可使牛肉易酥;烧煮羊肉加少量醋能除膻味;你知道么?——醋的妙用烧鱼时加醋,去除鱼腥味;颜 色:
气 味:
状 态:
沸 点:
熔 点:
溶解性:无色强烈刺激性气味液体(易挥发)一、乙酸的物理性质易溶于水和乙醇熔点16.6℃。当气温低于熔点时,乙酸凝结成类似冰的晶体,所以纯净的乙酸又称冰醋酸。117.9℃16.6℃二、乙酸分子的结构
C2H4O2或 CH3COOH(或 —COOH)乙酸的球棍模型和比例模型 为什么可以用醋除去水垢?(水垢的主要成分为CaCO3)
考考你CaCO3 + 2CH3COOH →
(CH3COO)2Ca + CO2↑+ H2O酸性:CH3COOH>H2CO3 H O
H - C-C-O-H
H 乙酸为一元弱酸,其酸性比 H2CO3强,具有酸的通性;其显酸性时断键位置为:使石蕊试液变红
与活泼金属反应(如:Na)
与碱性氧化物反应(如:Na2O)
与碱反应(如:NaOH)
与某些盐反应(如:Na2CO3)1. 酸性(弱酸性)酸的通性三、乙酸的化学性质 [生活小窍门]
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。这是为什么呢?1.加入几颗碎瓷片;
2.往试管中加入3mL乙醇;
3.边振荡边加入2mL浓硫酸,待冷却后再加入 2mL乙酸;
4.按图所示连接装置,缓慢加热,将产物通入到饱和碳
酸钠溶液的液面上。实验步骤:2. 乙酸与乙醇的反应现象:溶液分层,上层有无色透明的油状液体产生,并有香味。酯化反应:酸与醇反应生成酯和水的反应.乙酸乙酯(香味)可逆反应[问题与讨论]
(1)浓硫酸的作用?
(2)装药品的顺序?
(3)饱和碳酸钠溶液的作用是什么?
(4)导气管不能插入Na2CO3溶液中的原因
催化剂、吸水剂①乙醇,②浓硫酸,待冷却加③乙酸。①溶解乙醇;②吸收乙酸;
③降低乙酸乙酯的溶解度,便于分层。防止倒吸 防倒吸装置还有?防倒吸装置还有:第一种方式第二种方式[交流与思考]
酯化反应可能哪些脱水方式? 如何确定?酯化反应实质:酸脱羟基,醇脱氢(羟基上的)CH3 C OH + H 18O C2H5通过同位素原子示踪法测知反应如下:酯化反应也属于取代反应完成下列反应的化学方程式.小结:酸性酯化酯类广泛存在于自然界中酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用饮料、糖果、香水、化妆品中的香料,也可用作指甲油、胶水的溶剂。 是一种重要的化工原料
在日常生活中也有广泛的用途四、乙酸的用途 乙酸是一种重要的有机化工原料,可用于生产醋酸纤维、合成纤维、喷漆溶剂、香料、燃料、医药和农药等。课堂练习:课本p76 4.下列物质中,不能用来区分乙酸、乙醇、苯的是( )
A.金属钠
B.溴水
C.碳酸钠溶液
D.紫色石蕊试液B 6.除去乙酸乙酯中含有的乙酸,有效的处理方法是( )
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液C设计一个实验,比较醋酸和碳酸的酸性强弱.酸性:
CH3COOH > H2CO3 科学探究醋酸碳酸钠溶液澄清石灰水变浑浊作业:第一课时:
课时作业15:第2、3、4、15
作业:第二课时:
课时作业15:剩余题目
