人教版高中化学必修二2.1化学能与热能
文档属性
| 名称 | 人教版高中化学必修二2.1化学能与热能 |
|
|
| 格式 | zip | ||
| 文件大小 | 3.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-03 00:00:00 | ||
图片预览







文档简介
课件21张PPT。第二章 化学反应与能量 化学能与热能1风能 太阳能 水能 燃煤 燃气 燃油 以上能源中,哪些与化学反应有关?2磷的
燃烧氨的
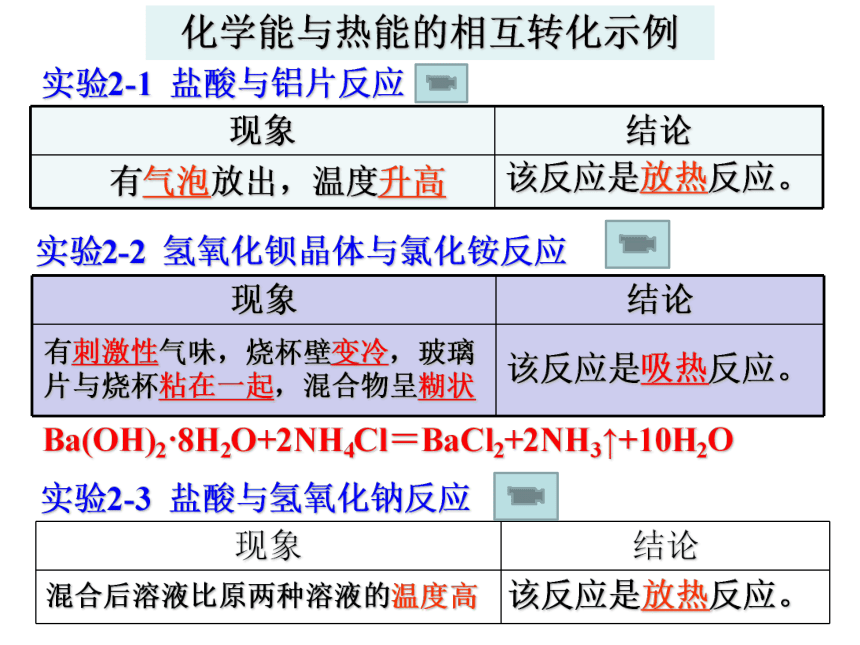
燃烧化学反应总伴随着能量的变化,能量一般表现为热量变化,也可以有其他形式,如光能、电能等化学反应伴随着能量变化是化学反应的基本特征之一。化学能与热能的相互转化示例实验2-1 盐酸与铝片反应 实验2-2 氢氧化钡晶体与氯化铵反应 该反应是放热反应。有气泡放出,温度升高有刺激性气味,烧杯壁变冷,玻璃片与烧杯粘在一起,混合物呈糊状该反应是吸热反应。Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O 实验2-3 盐酸与氢氧化钠反应 混合后溶液比原两种溶液的温度高该反应是放热反应。 化学反应中除了有新物质生成还伴随能量的变化,通常主要表为热量的变化。放热反应 :放出能量
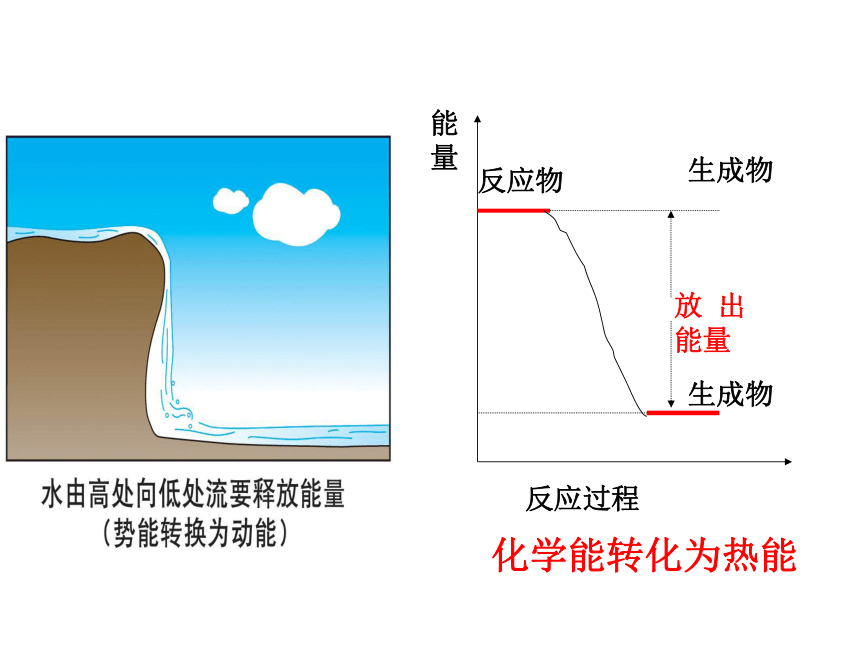
吸热反应 :吸收能量 6放热反应吸热反应③酸碱中和反应②所有的燃烧①金属单质与酸(或水)的反应④大多数化合反应③H2、CO、C做还原剂的反应②大多数分解反应①八水合氢氧化钡与氯化铵反应7NaOH、H2SO4等的溶解 NH4NO3的溶解 它们是物理变化,不属于放热反应和吸热反应吸热 放热生成物生成物化学能转化为热能9反应过程 将水由低处抽向高处需提供能量
(电能转换势能)热能转化为化学能10反应物总能量 > 生成物总能量反应物总能量 < 生成物总能量放热反应:吸热反应:宏观 取决于反应物的总能量与生成物的总能量的相对大小吸收还是放出能量E反 > E生E反 < E生11练习 1、已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的是( )
A、X的能量一定高于M
B、Y的能量一定高于N
C、X、Y的总能量一定高于M、N的总能量
D、该反应为放热反应,故不必加热就
一定能发生12从微观(化学键)角度:化学反应的实质是:
旧键断裂,新键形成 吸收能量释放能量13思考:从微观角度看,一个化学反应是放出还是吸收能量取决于什么呢? 化学键的断裂和形成是化学反应中能量变化的主要原因。
物质的化学反应与体系的能量变化是同时发生的。141、化学反应的本质:旧键断裂,新键形成的过程。释放能量862kJ
吸收能量679kJ,
故反应最终放热
Q=862KJ-679KJ=183KJ。 436KJ/mol243KJ/mol431KJ/mol吸热放热 二、化学键与化学反应中能量变化的关系断键吸收的总能量< 成键放出的总能量断键吸收的总能量 > 成键放出的总能量放热反应:吸热反应:微观 取决于断裂旧键吸收的总能量与形成新键放出的总能量的相对大小吸收还是放出能量Q(吸)< Q(放)Q(吸)> Q(放)16 若Q吸>Q放,反应吸热 若Q吸E生,反应放热 若E生>E反,反应吸热小结:宏观微观17反应放热反应吸热反应E1E2E1E218E反:反应物的总能量E生:生成物的总能量Q吸:断裂旧键吸收的能量Q放:形成新键释放的能量E反+Q吸=E生+Q放根据能量守恒定律:19C(金刚石,s)+O2 (g)==CO2(g); 放出能量Q1,
C(石 墨,s)+O2 (g)==CO2(g); 放出能量Q2.
已知Q1 >Q2,试比较稳定性:金刚石___石墨题4 已知:物质储存能量越高越不稳定。
根据下列反应:<物质储存的总能量越低该物质越稳定[导学15]下表数据是破坏1 mol化学键所消耗的能量: 根据上述数据回答下列问题:
(1)下列氢化物中最稳定的是________。
A.HCl B.HBr C.HI
(2)下列物质本身具有的能量最低的是________。
A.H2 B.Cl2 C.Br2 D.I2
A物质键能越大该物质
越稳定物质储存能量越低键能A
燃烧氨的
燃烧化学反应总伴随着能量的变化,能量一般表现为热量变化,也可以有其他形式,如光能、电能等化学反应伴随着能量变化是化学反应的基本特征之一。化学能与热能的相互转化示例实验2-1 盐酸与铝片反应 实验2-2 氢氧化钡晶体与氯化铵反应 该反应是放热反应。有气泡放出,温度升高有刺激性气味,烧杯壁变冷,玻璃片与烧杯粘在一起,混合物呈糊状该反应是吸热反应。Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O 实验2-3 盐酸与氢氧化钠反应 混合后溶液比原两种溶液的温度高该反应是放热反应。 化学反应中除了有新物质生成还伴随能量的变化,通常主要表为热量的变化。放热反应 :放出能量
吸热反应 :吸收能量 6放热反应吸热反应③酸碱中和反应②所有的燃烧①金属单质与酸(或水)的反应④大多数化合反应③H2、CO、C做还原剂的反应②大多数分解反应①八水合氢氧化钡与氯化铵反应7NaOH、H2SO4等的溶解 NH4NO3的溶解 它们是物理变化,不属于放热反应和吸热反应吸热 放热生成物生成物化学能转化为热能9反应过程 将水由低处抽向高处需提供能量
(电能转换势能)热能转化为化学能10反应物总能量 > 生成物总能量反应物总能量 < 生成物总能量放热反应:吸热反应:宏观 取决于反应物的总能量与生成物的总能量的相对大小吸收还是放出能量E反 > E生E反 < E生11练习 1、已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的是( )
A、X的能量一定高于M
B、Y的能量一定高于N
C、X、Y的总能量一定高于M、N的总能量
D、该反应为放热反应,故不必加热就
一定能发生12从微观(化学键)角度:化学反应的实质是:
旧键断裂,新键形成 吸收能量释放能量13思考:从微观角度看,一个化学反应是放出还是吸收能量取决于什么呢? 化学键的断裂和形成是化学反应中能量变化的主要原因。
物质的化学反应与体系的能量变化是同时发生的。141、化学反应的本质:旧键断裂,新键形成的过程。释放能量862kJ
吸收能量679kJ,
故反应最终放热
Q=862KJ-679KJ=183KJ。 436KJ/mol243KJ/mol431KJ/mol吸热放热 二、化学键与化学反应中能量变化的关系断键吸收的总能量< 成键放出的总能量断键吸收的总能量 > 成键放出的总能量放热反应:吸热反应:微观 取决于断裂旧键吸收的总能量与形成新键放出的总能量的相对大小吸收还是放出能量Q(吸)< Q(放)Q(吸)> Q(放)16 若Q吸>Q放,反应吸热 若Q吸
C(石 墨,s)+O2 (g)==CO2(g); 放出能量Q2.
已知Q1 >Q2,试比较稳定性:金刚石___石墨题4 已知:物质储存能量越高越不稳定。
根据下列反应:<物质储存的总能量越低该物质越稳定[导学15]下表数据是破坏1 mol化学键所消耗的能量: 根据上述数据回答下列问题:
(1)下列氢化物中最稳定的是________。
A.HCl B.HBr C.HI
(2)下列物质本身具有的能量最低的是________。
A.H2 B.Cl2 C.Br2 D.I2
A物质键能越大该物质
越稳定物质储存能量越低键能A
