人教版高中化学必修二2.3《化学反应的限度》
文档属性
| 名称 | 人教版高中化学必修二2.3《化学反应的限度》 |

|
|
| 格式 | zip | ||
| 文件大小 | 215.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-03 00:00:00 | ||
图片预览







文档简介
课件23张PPT。第三节 化学反应限度
活动与探究 2Fe3++2I-==2Fe2++I2溶液由棕黄色变成黄褐色溶液分层,下层变紫红色2Fe3++2I-==2Fe2++I2碘单质被CCl4萃取试管内溶液变成血红色溶液中还有Fe3+在 下,既能向正反应方向进行,
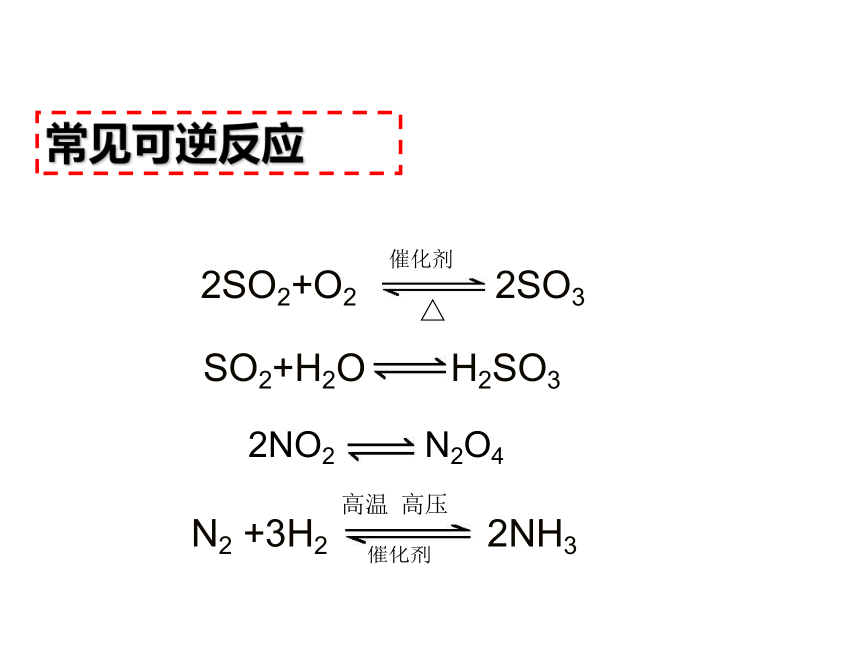
又能向逆反应方向进行的反应。可逆反应:同一条件例如: 2Fe3++2I- 2 Fe2++I2C+CO2 2CO可逆反应的前提:
1)反应物和生成物必须同时存在于同一反应体系中
2)在相同条件下,正逆反应都能自动进行一、可逆反应常见可逆反应2NO2 N2O4 SO2+H2O H2SO3思考与交流1、完成P51思考与交流2、H2SO4(浓)+2HBr===2H2O+Br2+SO2 与2H2O+Br2+SO2 === H2SO4+2HBr属于可逆反应吗?问题:怎么判断反应达到限度,且当可逆反应达到它的限度,化学反应是否就停止了呢?思考 分析实验数据思考:1、SO2与O2反应什么时候达到限度?
2、达到限度时,反应停止了?若没有,为什么各成分浓度会不变?
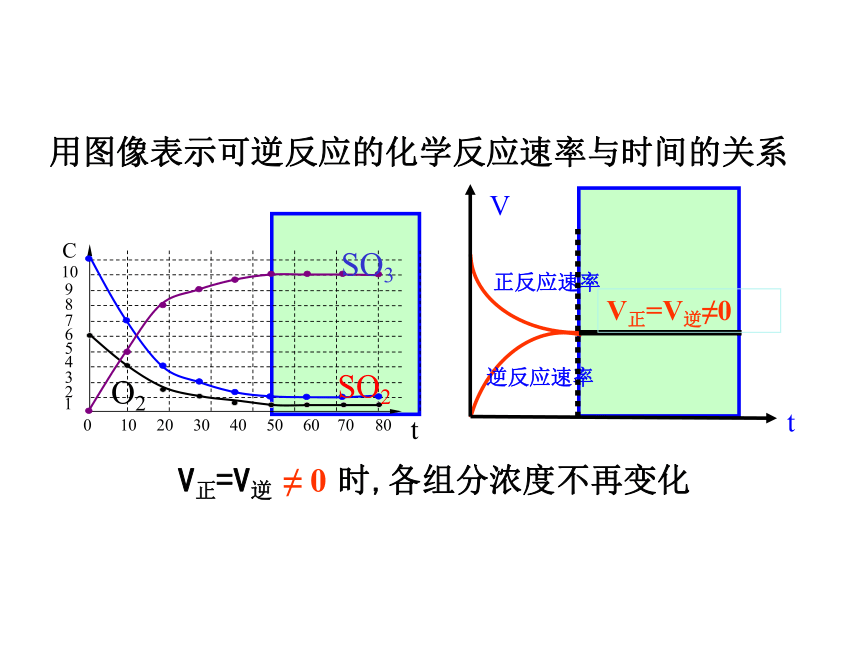
用图像表示可逆反应的化学反应速率与时间的关系V正=V逆 ≠ 0 时,各组分浓度不再变化逆反应速率正反应速率tVV正=V逆≠0(一) 定义:指在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应物和生成物的浓度不再变化的状态。二、化学平衡状态(化学平衡) (二)化学平衡的特征“逆” :
“等” :
“定” :
“动” :
“变” : v(正)= v(逆) ≠0研究对象是可逆反应平衡时各组分的浓度不变动态平衡改变条件,平衡可被打破,并在新条件下建立新平衡(三)反应达到平衡的标志1.本质标志:v(正)= v(逆) ≠0 对于某一可逆反应来说,正反应消耗某一反应物的速率等于逆反应生成该反应物的速率,就表明反应已达平衡1、对于可逆反应 ,达到
平衡的标志为: SO2的消耗速率与SO2的生成速率—————
SO2的消耗速率与SO3的———速率之比等于———
O2的生成速率与SO3的———速率之比等于———
SO2的生成速率与O2的———速率之比等于———相等消耗1 :1生成1 :2消耗2:12.上述标志如果用v正、v逆来表示,则是:v正(SO2)=v逆 (SO2) v正(SO2):v逆 (SO3)=1:1
V逆(O2):v正(SO3)=1:2 v逆(SO2)=v正 (O2)=2:1
2、一定条件下,不属于反应N2+3H2 2NH3达到平衡的标志是
A、 2v正(H2)=3v逆(NH3)
B、一个N≡N键断裂的同时,有三个H-H键断裂
C、一个N≡N键断裂的同时,有六个N-H键断裂
D、1molN2被消耗的同时,有3molH2生成 √(1)必须有正有逆a.可以是两个速率直接标有正逆(2)速率必须相等a.如果用一种物质表示速率,速率必须相等。c.如果用化学方程式中不同侧的物质来表示速率,一种物质用生成来表示,另一种物质必须也用生成来表示。b.如果用化学方程式中同一侧的物质来表示速率,一种物质用生成来表示,另一种物质必须用消耗来表示。b.如果用不同物质表示速率,那速率比就等于系数比。A+3B 2C,下列描述能否说明该反应已处于化学平衡状态:
① V(A)生成=V(A)消耗
② V(A)生成=3V(B)消耗
④单位时间内消耗1molA,同时生成2molC
⑤单位时间内消耗3molB ,同时消耗2molC
√√×小试牛刀×2.量不变这个量一定随着反应的进行会变化,但达到平衡时就不变了。变量:各组分浓度、质量、物质的量、气体体积、质量分数、物质的量分数、气体体积分数、颜色体系总压强?密度?平均摩尔质量?总物质的量?典题剖析在一个横容的密闭容器中进行下列两个可逆反应:
(甲)C(s)+H2O(g) CO(g)+H2(g)
(乙) CO(g)+ H2O(g) CO2(g)+H2(g)
现有下列状态:
(1)混合气体的平均相对分子质量不在改变。
(2)恒温时,气体的压强不在改变。
(3)各气体组分浓度相等。
(4)断裂氢氧键的速率等于断裂氢氢键速率的两倍。
(5)混合气体密度不变
(6)单位时间内水蒸气消耗的物质的量等于氢气消耗的物质的量。
其中能表明甲容器达到平衡的是( )
表明甲容器达到平衡的是( )ρ(气)=m(气)/V√X√XXX√√√√√X(1)(2)(4)(5)(6)(4)( 6) M(气)=m(气)/n(气)小试牛刀1.(双选)在一定温度下,可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是 ( )
A. C的生成速率与C分解的速率相等
B. 单位时间内生成n molA,同时生3n molB
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1:3:2AC2.下列说法中可以充分说明反应:
P(g)+Q(g) R(g)+S(g) , 在恒温下已达平衡状态的是( )
反应容器内压强不随时间变化
B. P和S的生成速率相等
C. 反应容器内P、Q、R、S四者共存
D. 反应容器内总物质的量不随时间而变化 B 3.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明A(s)+3B(g) 2C(g)+D(g)已达平衡状态的 ( )
A.平均摩尔质量
B.混合气体的密度
C.B的物质的量浓度
D.气体的总物质的量
D你收获了什么知识与技能
(1)知道可逆反应的概念,了解可逆反应的基本特征
(2)知道可逆反应在一定条件下能达到平衡状态,并理解化学平衡的本质和标志。
过程与方法
(1)从实验中领悟化学反应是有一定限度的。
(2)利用图形分析体会化学平衡的建立。
情感态度价值观
在分析交流中发现问题,敢于质疑,自己独立思考,与伙伴团队合作拓展应用1.请同学们课后查找生活中常见的存在化学反应限度的实例,与大家分享
2.思考如果你是一家硫酸厂的厂长,你会采取哪些手段来提高SO3的产量?谢谢请批评指正
又能向逆反应方向进行的反应。可逆反应:同一条件例如: 2Fe3++2I- 2 Fe2++I2C+CO2 2CO可逆反应的前提:
1)反应物和生成物必须同时存在于同一反应体系中
2)在相同条件下,正逆反应都能自动进行一、可逆反应常见可逆反应2NO2 N2O4 SO2+H2O H2SO3思考与交流1、完成P51思考与交流2、H2SO4(浓)+2HBr===2H2O+Br2+SO2 与2H2O+Br2+SO2 === H2SO4+2HBr属于可逆反应吗?问题:怎么判断反应达到限度,且当可逆反应达到它的限度,化学反应是否就停止了呢?思考 分析实验数据思考:1、SO2与O2反应什么时候达到限度?
2、达到限度时,反应停止了?若没有,为什么各成分浓度会不变?
用图像表示可逆反应的化学反应速率与时间的关系V正=V逆 ≠ 0 时,各组分浓度不再变化逆反应速率正反应速率tVV正=V逆≠0(一) 定义:指在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应物和生成物的浓度不再变化的状态。二、化学平衡状态(化学平衡) (二)化学平衡的特征“逆” :
“等” :
“定” :
“动” :
“变” : v(正)= v(逆) ≠0研究对象是可逆反应平衡时各组分的浓度不变动态平衡改变条件,平衡可被打破,并在新条件下建立新平衡(三)反应达到平衡的标志1.本质标志:v(正)= v(逆) ≠0 对于某一可逆反应来说,正反应消耗某一反应物的速率等于逆反应生成该反应物的速率,就表明反应已达平衡1、对于可逆反应 ,达到
平衡的标志为: SO2的消耗速率与SO2的生成速率—————
SO2的消耗速率与SO3的———速率之比等于———
O2的生成速率与SO3的———速率之比等于———
SO2的生成速率与O2的———速率之比等于———相等消耗1 :1生成1 :2消耗2:12.上述标志如果用v正、v逆来表示,则是:v正(SO2)=v逆 (SO2) v正(SO2):v逆 (SO3)=1:1
V逆(O2):v正(SO3)=1:2 v逆(SO2)=v正 (O2)=2:1
2、一定条件下,不属于反应N2+3H2 2NH3达到平衡的标志是
A、 2v正(H2)=3v逆(NH3)
B、一个N≡N键断裂的同时,有三个H-H键断裂
C、一个N≡N键断裂的同时,有六个N-H键断裂
D、1molN2被消耗的同时,有3molH2生成 √(1)必须有正有逆a.可以是两个速率直接标有正逆(2)速率必须相等a.如果用一种物质表示速率,速率必须相等。c.如果用化学方程式中不同侧的物质来表示速率,一种物质用生成来表示,另一种物质必须也用生成来表示。b.如果用化学方程式中同一侧的物质来表示速率,一种物质用生成来表示,另一种物质必须用消耗来表示。b.如果用不同物质表示速率,那速率比就等于系数比。A+3B 2C,下列描述能否说明该反应已处于化学平衡状态:
① V(A)生成=V(A)消耗
② V(A)生成=3V(B)消耗
④单位时间内消耗1molA,同时生成2molC
⑤单位时间内消耗3molB ,同时消耗2molC
√√×小试牛刀×2.量不变这个量一定随着反应的进行会变化,但达到平衡时就不变了。变量:各组分浓度、质量、物质的量、气体体积、质量分数、物质的量分数、气体体积分数、颜色体系总压强?密度?平均摩尔质量?总物质的量?典题剖析在一个横容的密闭容器中进行下列两个可逆反应:
(甲)C(s)+H2O(g) CO(g)+H2(g)
(乙) CO(g)+ H2O(g) CO2(g)+H2(g)
现有下列状态:
(1)混合气体的平均相对分子质量不在改变。
(2)恒温时,气体的压强不在改变。
(3)各气体组分浓度相等。
(4)断裂氢氧键的速率等于断裂氢氢键速率的两倍。
(5)混合气体密度不变
(6)单位时间内水蒸气消耗的物质的量等于氢气消耗的物质的量。
其中能表明甲容器达到平衡的是( )
表明甲容器达到平衡的是( )ρ(气)=m(气)/V√X√XXX√√√√√X(1)(2)(4)(5)(6)(4)( 6) M(气)=m(气)/n(气)小试牛刀1.(双选)在一定温度下,可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是 ( )
A. C的生成速率与C分解的速率相等
B. 单位时间内生成n molA,同时生3n molB
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1:3:2AC2.下列说法中可以充分说明反应:
P(g)+Q(g) R(g)+S(g) , 在恒温下已达平衡状态的是( )
反应容器内压强不随时间变化
B. P和S的生成速率相等
C. 反应容器内P、Q、R、S四者共存
D. 反应容器内总物质的量不随时间而变化 B 3.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明A(s)+3B(g) 2C(g)+D(g)已达平衡状态的 ( )
A.平均摩尔质量
B.混合气体的密度
C.B的物质的量浓度
D.气体的总物质的量
D你收获了什么知识与技能
(1)知道可逆反应的概念,了解可逆反应的基本特征
(2)知道可逆反应在一定条件下能达到平衡状态,并理解化学平衡的本质和标志。
过程与方法
(1)从实验中领悟化学反应是有一定限度的。
(2)利用图形分析体会化学平衡的建立。
情感态度价值观
在分析交流中发现问题,敢于质疑,自己独立思考,与伙伴团队合作拓展应用1.请同学们课后查找生活中常见的存在化学反应限度的实例,与大家分享
2.思考如果你是一家硫酸厂的厂长,你会采取哪些手段来提高SO3的产量?谢谢请批评指正
