人教版高中化学选修五 3.2 醛 课件(30张)
文档属性
| 名称 | 人教版高中化学选修五 3.2 醛 课件(30张) |

|
|
| 格式 | zip | ||
| 文件大小 | 481.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-04 00:00:00 | ||
图片预览






文档简介
课件30张PPT。掌握:乙醛的化学性质和醛基的检验.
认识:乙醛的组成和结构.
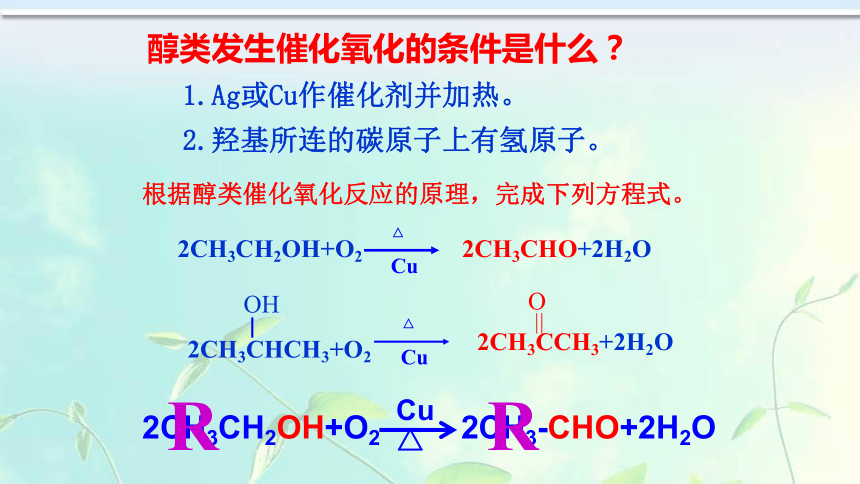
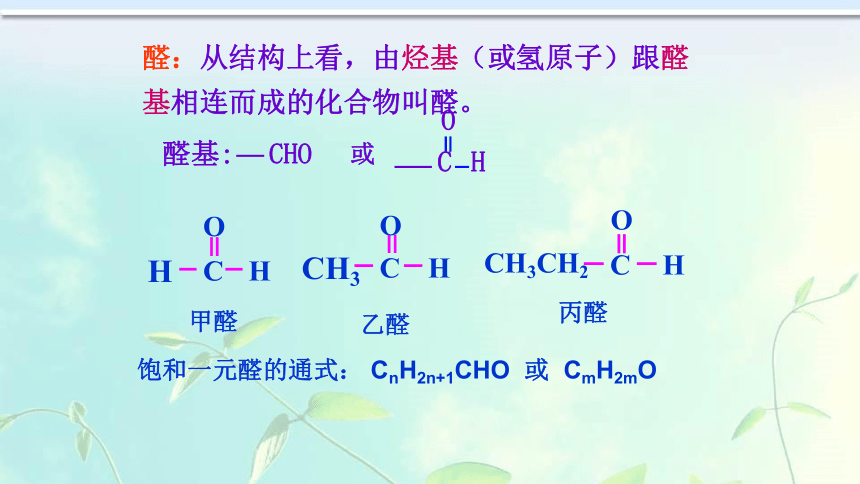
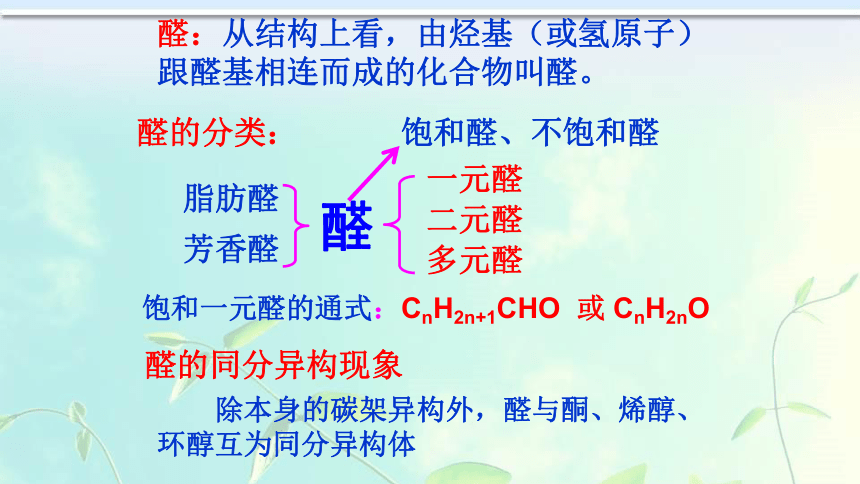
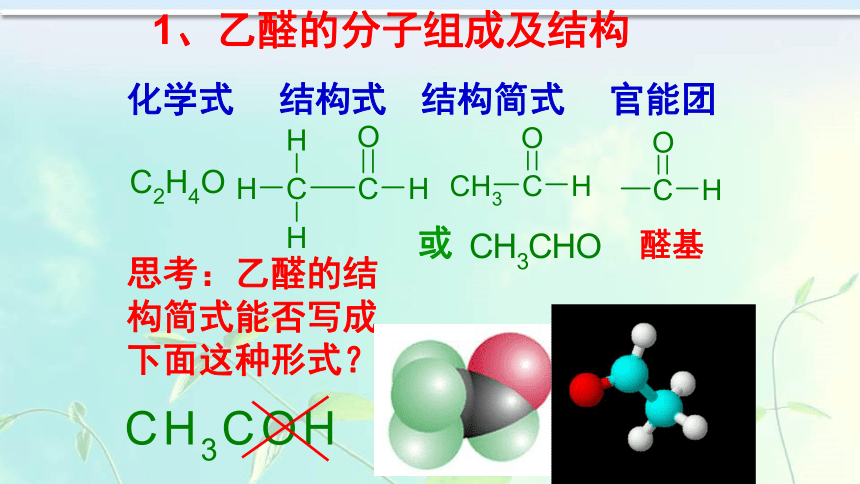
知道:甲醛、乙醛在生产、生活中的应用.第二节 醛根据醇类催化氧化反应的原理,完成下列方程式。醇类发生催化氧化的条件是什么?1.Ag或Cu作催化剂并加热。2.羟基所连的碳原子上有氢原子。2CH3CHO+2H2OR R 醛:从结构上看,由烃基(或氢原子)跟醛基相连而成的化合物叫醛。饱和一元醛的通式: CnH2n+1CHO 或 CmH2mO 醛:从结构上看,由烃基(或氢原子)跟醛基相连而成的化合物叫醛。醛的分类:醛脂肪醛芳香醛一元醛二元醛多元醛饱和醛、不饱和醛CnH2n+1CHO 或 CnH2nO饱和一元醛的通式:醛的同分异构现象 除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体练习:写出C3H6O的所有可能同分异构体。CH2=CH-CH2-OHCH2-CH=CH-OH1、乙醛的分子组成及结构化学式结构式结构简式官能团思考:乙醛的结构简式能否写成下面这种形式? 或醛基思考:通过乙醛的核磁共振氢谱,你能获取什么信息?请你指认出两个吸收峰的归属.2.甲醛
是最简单的醛,分子式为 ,结构简式为 ,为无色、刺激性气味的气体, 溶于水.甲醛是一种重要的有机合成原料,它的水溶液(又称福尔马林)具有 、防腐性能.CH2OHCHO易杀菌物理性质
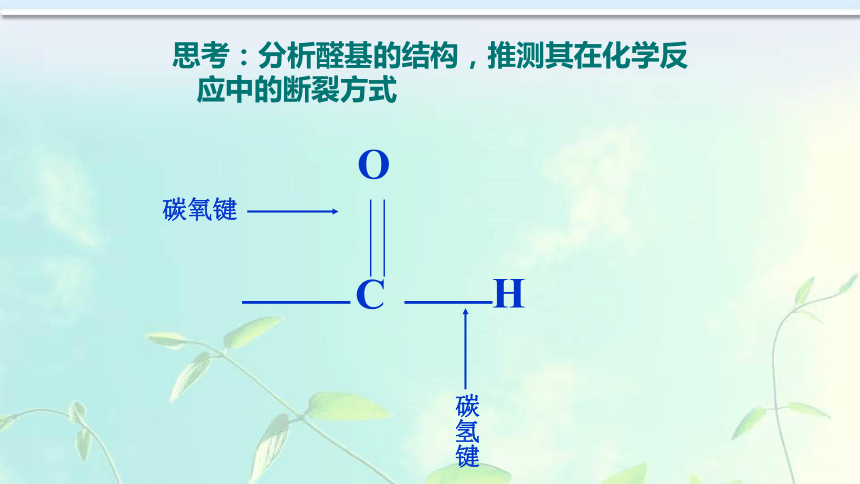
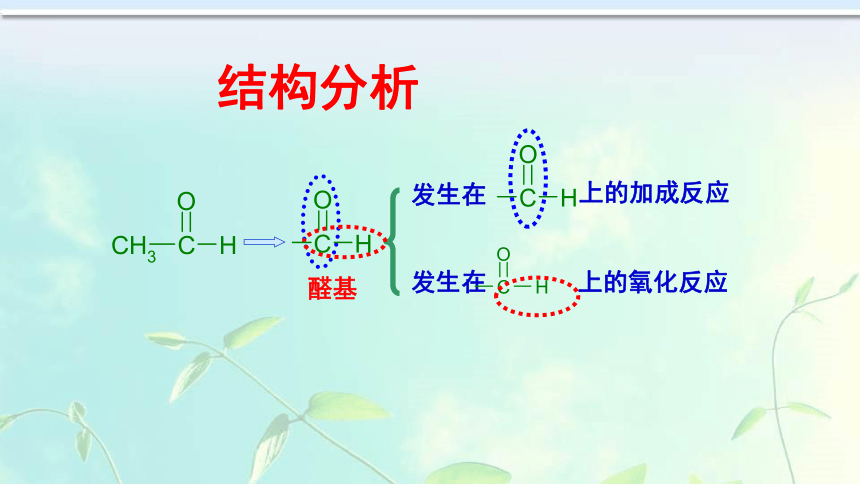
乙醛是无色、具有 气味的液体,密度比水 ,沸点20.8℃,易挥发,易燃烧,能与 、 互溶.刺激性小水乙醇3、乙醛思考:分析醛基的结构,推测其在化学反应中的断裂方式结构分析醛基4.化学性质
(1)氧化反应
①催化氧化
乙醛在催化剂加热的条件下,能被氧气氧化为乙酸,反应的化学方程式为
②银镜反应[实验] 银镜反应 :取一洁净试管,加入1ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。 :在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。1、配制银氨溶液2、水浴加热生成银镜还原剂氧化剂(1)试管内壁必须洁净;如有油污,得不到光亮的银镜而是黑色沉淀。
(2)必须水浴;
(3)加热时不可振荡和摇动试管;
(4)配制银氨溶液时,氨水不能过量,否则生成易爆炸的物质(银氨溶液随配随用,不可久置。)注意:说明:a.生成物,一水、二银、三氨、乙酸铵b.1mol醛基 ~ 2mol Ag
应用:a.检验醛基的存在b.工业上利用此原理制镜和保温瓶胆③与新制Cu(OH)2的反应蓝色沉淀红色沉淀[实验]及注意点1、配制新制的Cu(OH)2悬浊液:在2ml10%NaOH溶液中滴入2%CuSO4溶液4~6滴,振荡。 2、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙醛溶液,碱必须过量加热至沸腾。Cu2O砖红色乙醛和新制的氢氧化铜反应 氧化剂还原剂说明:1mol醛基 ~1mol Cu2O应用:a.检验醛基的存在b. 医院里,利用这一反应原理检查尿糖是否正常(检查葡萄糖的醛基)与酸性高锰酸钾和溴水反应乙醛能使高锰酸钾溶液褪色和溴水褪色。④被强氧化剂氧化写出下列转变的化学方程式:(2)乙醛的加成反应+ H21mol甲醛最多可以还原得到多少mol Ag?即:H2CO3注:由于甲醛分子相当于含有2个醛基,所以1mol甲醛发生银镜反应时最多可生成4molAg
1mol甲醛与新制的氢氧化铜反应最多可生成2molCu2O 先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色知识运用 新制的Cu(OH)21、用一种试剂鉴别乙醇、乙醛、乙酸、甲酸四种无色液体醛类化学性质(1) 和H2加成被还原成醇(2)氧化反应a.燃烧c.被弱氧化剂氧化d.使酸性KMnO4溶液和溴水褪色小结:醛类应该具备哪些重要的化学性质?P.58 科学视野 丙酮 丙酮是最简单的酮类化合物,在常温下,丙酮是无色透明的液体,易挥发,具有令人愉快的气味,能与水、乙醇等混溶,是一种重要的有机溶剂和化工原料。
丙酮不能被银氨溶液、新制氢氧化铜等弱氧化剂氧化,可催化加氢成醇。
认识:乙醛的组成和结构.
知道:甲醛、乙醛在生产、生活中的应用.第二节 醛根据醇类催化氧化反应的原理,完成下列方程式。醇类发生催化氧化的条件是什么?1.Ag或Cu作催化剂并加热。2.羟基所连的碳原子上有氢原子。2CH3CHO+2H2OR R 醛:从结构上看,由烃基(或氢原子)跟醛基相连而成的化合物叫醛。饱和一元醛的通式: CnH2n+1CHO 或 CmH2mO 醛:从结构上看,由烃基(或氢原子)跟醛基相连而成的化合物叫醛。醛的分类:醛脂肪醛芳香醛一元醛二元醛多元醛饱和醛、不饱和醛CnH2n+1CHO 或 CnH2nO饱和一元醛的通式:醛的同分异构现象 除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体练习:写出C3H6O的所有可能同分异构体。CH2=CH-CH2-OHCH2-CH=CH-OH1、乙醛的分子组成及结构化学式结构式结构简式官能团思考:乙醛的结构简式能否写成下面这种形式? 或醛基思考:通过乙醛的核磁共振氢谱,你能获取什么信息?请你指认出两个吸收峰的归属.2.甲醛
是最简单的醛,分子式为 ,结构简式为 ,为无色、刺激性气味的气体, 溶于水.甲醛是一种重要的有机合成原料,它的水溶液(又称福尔马林)具有 、防腐性能.CH2OHCHO易杀菌物理性质
乙醛是无色、具有 气味的液体,密度比水 ,沸点20.8℃,易挥发,易燃烧,能与 、 互溶.刺激性小水乙醇3、乙醛思考:分析醛基的结构,推测其在化学反应中的断裂方式结构分析醛基4.化学性质
(1)氧化反应
①催化氧化
乙醛在催化剂加热的条件下,能被氧气氧化为乙酸,反应的化学方程式为
②银镜反应[实验] 银镜反应 :取一洁净试管,加入1ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。 :在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。1、配制银氨溶液2、水浴加热生成银镜还原剂氧化剂(1)试管内壁必须洁净;如有油污,得不到光亮的银镜而是黑色沉淀。
(2)必须水浴;
(3)加热时不可振荡和摇动试管;
(4)配制银氨溶液时,氨水不能过量,否则生成易爆炸的物质(银氨溶液随配随用,不可久置。)注意:说明:a.生成物,一水、二银、三氨、乙酸铵b.1mol醛基 ~ 2mol Ag
应用:a.检验醛基的存在b.工业上利用此原理制镜和保温瓶胆③与新制Cu(OH)2的反应蓝色沉淀红色沉淀[实验]及注意点1、配制新制的Cu(OH)2悬浊液:在2ml10%NaOH溶液中滴入2%CuSO4溶液4~6滴,振荡。 2、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙醛溶液,碱必须过量加热至沸腾。Cu2O砖红色乙醛和新制的氢氧化铜反应 氧化剂还原剂说明:1mol醛基 ~1mol Cu2O应用:a.检验醛基的存在b. 医院里,利用这一反应原理检查尿糖是否正常(检查葡萄糖的醛基)与酸性高锰酸钾和溴水反应乙醛能使高锰酸钾溶液褪色和溴水褪色。④被强氧化剂氧化写出下列转变的化学方程式:(2)乙醛的加成反应+ H21mol甲醛最多可以还原得到多少mol Ag?即:H2CO3注:由于甲醛分子相当于含有2个醛基,所以1mol甲醛发生银镜反应时最多可生成4molAg
1mol甲醛与新制的氢氧化铜反应最多可生成2molCu2O 先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色知识运用 新制的Cu(OH)21、用一种试剂鉴别乙醇、乙醛、乙酸、甲酸四种无色液体醛类化学性质(1) 和H2加成被还原成醇(2)氧化反应a.燃烧c.被弱氧化剂氧化d.使酸性KMnO4溶液和溴水褪色小结:醛类应该具备哪些重要的化学性质?P.58 科学视野 丙酮 丙酮是最简单的酮类化合物,在常温下,丙酮是无色透明的液体,易挥发,具有令人愉快的气味,能与水、乙醇等混溶,是一种重要的有机溶剂和化工原料。
丙酮不能被银氨溶液、新制氢氧化铜等弱氧化剂氧化,可催化加氢成醇。
