鲁科版高中化学选修5 1.2.1 碳原子的成键方式(21张ppt)
文档属性
| 名称 | 鲁科版高中化学选修5 1.2.1 碳原子的成键方式(21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-05 00:00:00 | ||
图片预览





文档简介
课件21张PPT。有机化合物的结构与性质
(第一课时)碳原子的成键方式联想质疑甲烷乙烯苯燃烧、取代反应燃烧、与高锰酸钾溶液反应、加成反应燃烧、取代反应、加成反应
结构性质知识支持单键:两个原子之间共用一对电子
的共价键。
双键:两个原子之间共用两对电子
的共价键。
叁键:两个原子之间共用三对电子
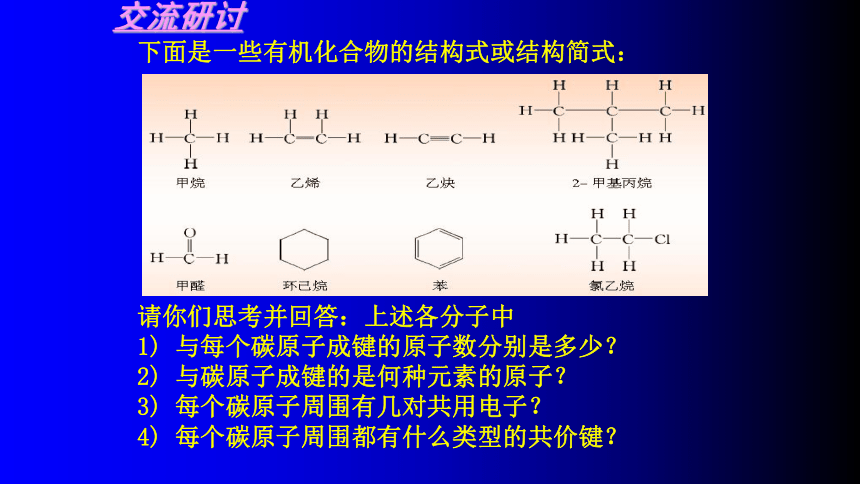
的共价键。共价键的分类及定义交流研讨下面是一些有机化合物的结构式或结构简式:请你们思考并回答:上述各分子中
1) 与每个碳原子成键的原子数分别是多少?
2) 与碳原子成键的是何种元素的原子?
3) 每个碳原子周围有几对共用电子?
4) 每个碳原子周围都有什么类型的共价键?
对比归纳1、每个碳原子周围都有四对共用电子。
2、碳原子最多与四个原子形成共价键,即四个单键。
3、碳原子除了彼此间可以成键外,还跟多种原子(H、O、Cl、N等)形成共价键。
4、碳原子既能形成单键、双键、叁键,还可形成碳链、碳环等多种复杂的结构单元。
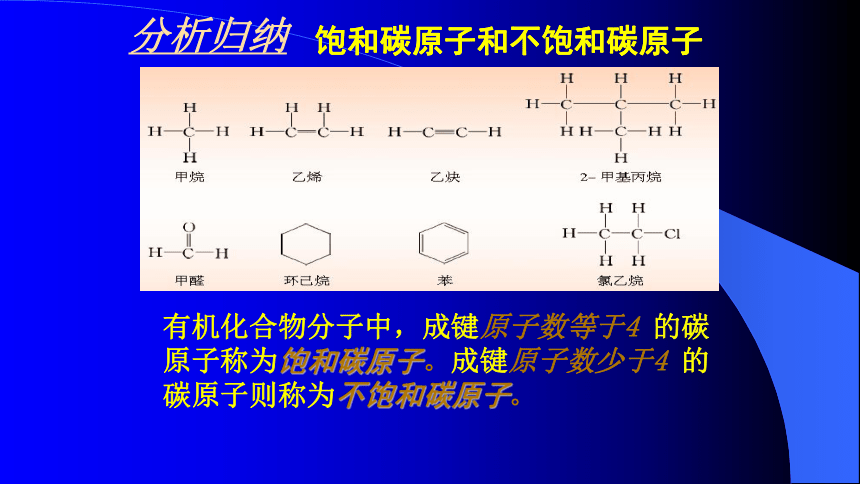
由上述问题的答案总结出有机物中碳原子成键的一些规律: 分析归纳 有机化合物分子中,成键原子数等于4 的碳原子称为饱和碳原子。成键原子数少于4 的碳原子则称为不饱和碳原子。饱和碳原子和不饱和碳原子饱和碳原子和不饱和碳原子知识支持共价键参数1、键能 指101.3kPa、298K时,断开1mol气态AB分子中的化学键,使其生成气态A原子和气态B原子的过程中所吸收的能量。
键能越大,键越牢固。
2、键长 指两个成键原子间的平均核间距。
一般说来,键长越短,键越牢固。
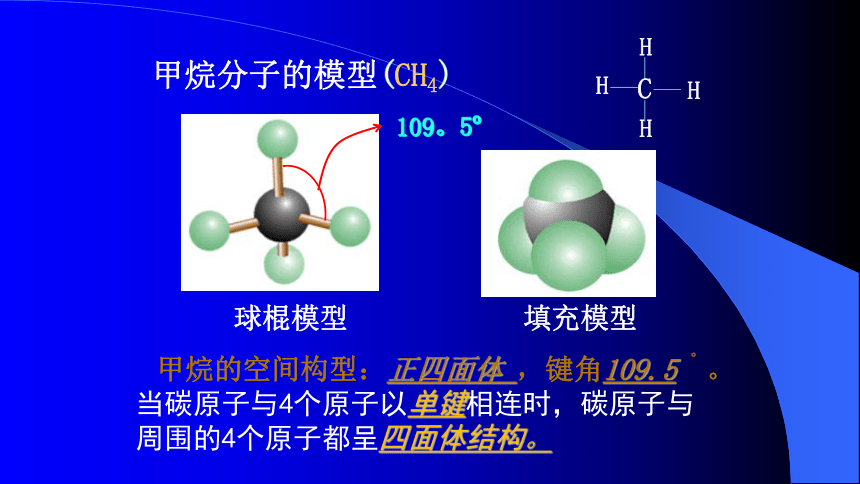
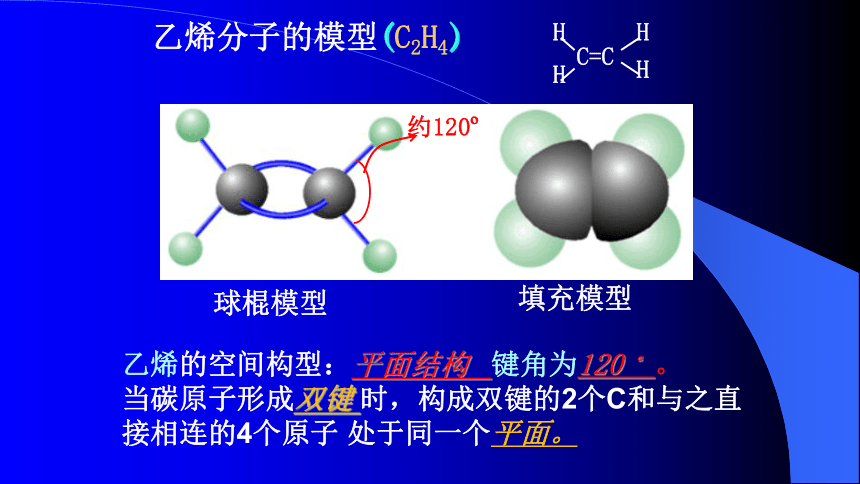
3、键角 指分子中两个共价键之间的夹角。 球棍模型填充模型109。5o甲烷分子的模型(CH4) 甲烷的空间构型:正四面体 ,键角109.5 °。 当碳原子与4个原子以单键相连时,碳原子与周围的4个原子都呈四面体结构。乙烯分子的模型(C2H4)约120o球棍模型填充模型乙烯的空间构型:平面结构 键角为120 。。
当碳原子形成双键 时,构成双键的2个C和与之直接相连的4个原子 处于同一个平面。乙炔分子的模型(C2H2)球棍模型填充模型180o乙炔的空间构型:直线结构 键角180 。
当碳原子形成叁键 时,构成叁键的2个C和与之直接相连的2个原子处在同一直线。H—C≡C—H碳原子的成键方式与空间构型四面体型平面型直线型空间构型分子成键方式分析归纳交流研讨 通过对化学必修课程的学习我们清楚将乙烯或乙炔通入溴水中溶液会退色,而将乙烷通入溴水中溶液颜色却无明显变化。
根据下表所提供的数据,我们能否从键能的角度加以解释?分析归纳 碳碳双键键能小于单键键能的2倍。 碳碳叁键键能不仅小于单键键能的3倍、而且小于单键和双键的键能之和。 叁键中三个键性质不同,其中两个键较另一个容易断裂。
易发生加成反应。 双键中两个键性质不同,其中一个键较另一个容易断裂。易发生加成反应。饱和碳原子——单键——性质稳定
不饱和碳原子——双键、叁键——性质较活泼极性键和非极性键判断的依据是什么?【交流·研讨】分析C—C和C—CI,回答问题.共用电子对是否发生偏移 成键原子是否相同极性键和非极性键 成键双方是同种元素的原子,吸引共用电子的能力相同,共用电子不偏向于成键原子的任何一方, 这样的共价键是非极性共价键(简称非极性键)。
成键双方是不同元素的原子,它们吸引电子的能力不同,共用电子将偏向于吸引电子能力较强的一方,这样的共价键是极性共价键(简称极性键)。课堂巩固1.关于单键、双键、叁键的说法正确的是 ( )
A.单键的键长最短,键能最大。 B.叁键的键长最短,键能最大。
C.双键中两个键都活泼,加成时都断裂。 D.只有碳原子间才能形成双键和叁键B课堂巩固2、某有机物的结构如下,分析其结构并回答下列问题:
CH3—CH=CH—C≡C—CF3
(1)写出其分子式_________
(2)分子中有_____________个不饱和碳原子(3)分子中饱和碳原子有__________个
(4)分子中的极性键有 _________________C6H5F342C—H C—F课堂总结1、有机物中碳原子的成键规律、饱和碳 原子和不饱和碳原子
2、碳原子的成键方式与空间构型的关系
3、通过键能的角度分析有机物的性质
4、极性共价键和非极性共价键
课后思考 共价键的极性对有机化合物的性质有什么影响?
谢谢!请多指教
结构性质知识支持单键:两个原子之间共用一对电子
的共价键。
双键:两个原子之间共用两对电子
的共价键。
叁键:两个原子之间共用三对电子
的共价键。共价键的分类及定义交流研讨下面是一些有机化合物的结构式或结构简式:请你们思考并回答:上述各分子中
1) 与每个碳原子成键的原子数分别是多少?
2) 与碳原子成键的是何种元素的原子?
3) 每个碳原子周围有几对共用电子?
4) 每个碳原子周围都有什么类型的共价键?
对比归纳1、每个碳原子周围都有四对共用电子。
2、碳原子最多与四个原子形成共价键,即四个单键。
3、碳原子除了彼此间可以成键外,还跟多种原子(H、O、Cl、N等)形成共价键。
4、碳原子既能形成单键、双键、叁键,还可形成碳链、碳环等多种复杂的结构单元。
由上述问题的答案总结出有机物中碳原子成键的一些规律: 分析归纳 有机化合物分子中,成键原子数等于4 的碳原子称为饱和碳原子。成键原子数少于4 的碳原子则称为不饱和碳原子。饱和碳原子和不饱和碳原子饱和碳原子和不饱和碳原子知识支持共价键参数1、键能 指101.3kPa、298K时,断开1mol气态AB分子中的化学键,使其生成气态A原子和气态B原子的过程中所吸收的能量。
键能越大,键越牢固。
2、键长 指两个成键原子间的平均核间距。
一般说来,键长越短,键越牢固。
3、键角 指分子中两个共价键之间的夹角。 球棍模型填充模型109。5o甲烷分子的模型(CH4) 甲烷的空间构型:正四面体 ,键角109.5 °。 当碳原子与4个原子以单键相连时,碳原子与周围的4个原子都呈四面体结构。乙烯分子的模型(C2H4)约120o球棍模型填充模型乙烯的空间构型:平面结构 键角为120 。。
当碳原子形成双键 时,构成双键的2个C和与之直接相连的4个原子 处于同一个平面。乙炔分子的模型(C2H2)球棍模型填充模型180o乙炔的空间构型:直线结构 键角180 。
当碳原子形成叁键 时,构成叁键的2个C和与之直接相连的2个原子处在同一直线。H—C≡C—H碳原子的成键方式与空间构型四面体型平面型直线型空间构型分子成键方式分析归纳交流研讨 通过对化学必修课程的学习我们清楚将乙烯或乙炔通入溴水中溶液会退色,而将乙烷通入溴水中溶液颜色却无明显变化。
根据下表所提供的数据,我们能否从键能的角度加以解释?分析归纳 碳碳双键键能小于单键键能的2倍。 碳碳叁键键能不仅小于单键键能的3倍、而且小于单键和双键的键能之和。 叁键中三个键性质不同,其中两个键较另一个容易断裂。
易发生加成反应。 双键中两个键性质不同,其中一个键较另一个容易断裂。易发生加成反应。饱和碳原子——单键——性质稳定
不饱和碳原子——双键、叁键——性质较活泼极性键和非极性键判断的依据是什么?【交流·研讨】分析C—C和C—CI,回答问题.共用电子对是否发生偏移 成键原子是否相同极性键和非极性键 成键双方是同种元素的原子,吸引共用电子的能力相同,共用电子不偏向于成键原子的任何一方, 这样的共价键是非极性共价键(简称非极性键)。
成键双方是不同元素的原子,它们吸引电子的能力不同,共用电子将偏向于吸引电子能力较强的一方,这样的共价键是极性共价键(简称极性键)。课堂巩固1.关于单键、双键、叁键的说法正确的是 ( )
A.单键的键长最短,键能最大。 B.叁键的键长最短,键能最大。
C.双键中两个键都活泼,加成时都断裂。 D.只有碳原子间才能形成双键和叁键B课堂巩固2、某有机物的结构如下,分析其结构并回答下列问题:
CH3—CH=CH—C≡C—CF3
(1)写出其分子式_________
(2)分子中有_____________个不饱和碳原子(3)分子中饱和碳原子有__________个
(4)分子中的极性键有 _________________C6H5F342C—H C—F课堂总结1、有机物中碳原子的成键规律、饱和碳 原子和不饱和碳原子
2、碳原子的成键方式与空间构型的关系
3、通过键能的角度分析有机物的性质
4、极性共价键和非极性共价键
课后思考 共价键的极性对有机化合物的性质有什么影响?
谢谢!请多指教
