鲁科版高中化学选修五 醛和酮(第一课时(21张ppt)
文档属性
| 名称 | 鲁科版高中化学选修五 醛和酮(第一课时(21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-05 00:00:00 | ||
图片预览





文档简介
课件21张PPT。课前检测醇类发生催化氧化的条件是什么?羟基所连的碳原子上有氢原子(α碳原子)醇类催化氧化规律是什么?第3节 醛和酮 (1)1、能根据醛的结构特点,初步预测
醛可能发生的化学反应;
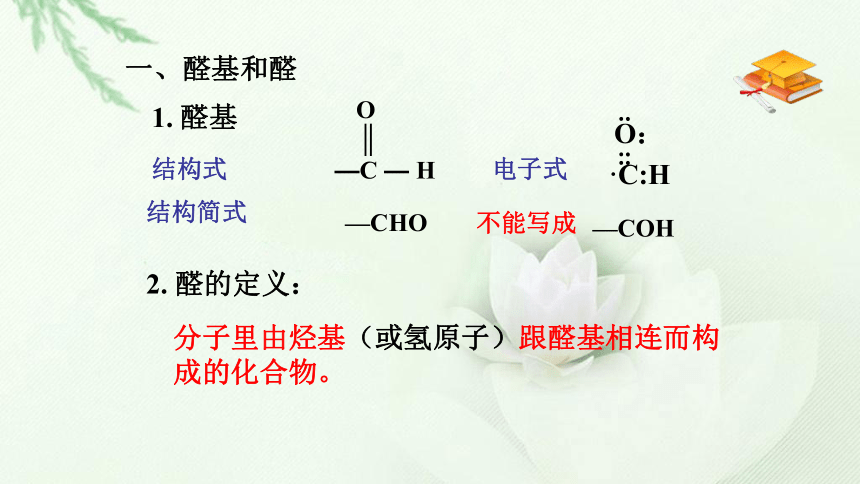
2、熟练掌握醛的化学性质。学习难点:乙醛与银氨溶液、新制Cu(OH)2反应的化学方程式的正确书写学习重点:乙醛的结构特点和主要化学性质1. 醛基2. 醛的定义:结构式结构简式不能写成电子式分子里由烃基(或氢原子)跟醛基相连而构成的化合物。—CHO—COH一、醛基和醛CD当堂训练D:CH3-CH2–CHO以下属于醛的有 A:B:C:E:小结:
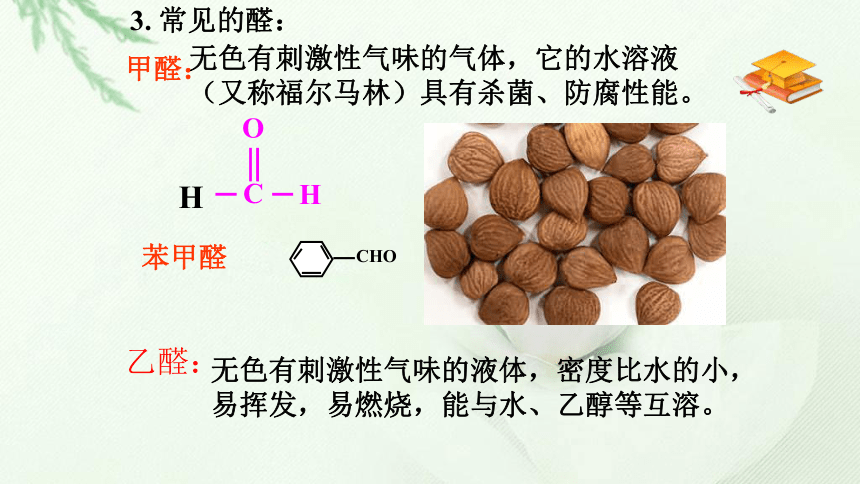
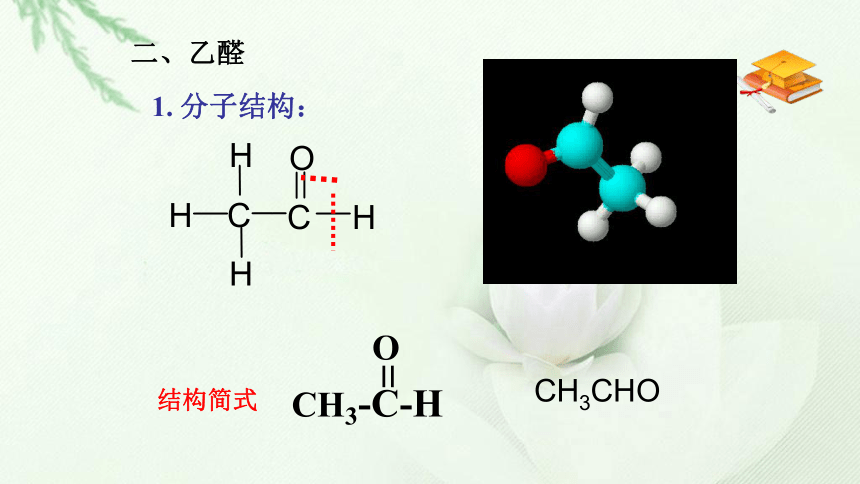
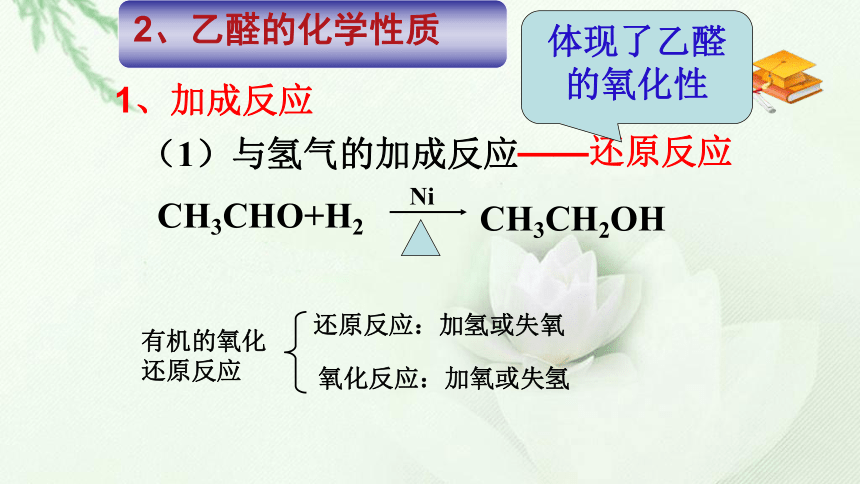
醛一定含有醛基,但含有醛基的不一定是醛3. 常见的醛:甲醛:无色有刺激性气味的气体,它的水溶液(又称福尔马林)具有杀菌、防腐性能。苯甲醛乙醛:无色有刺激性气味的液体,密度比水的小,易挥发,易燃烧,能与水、乙醇等互溶。1. 分子结构:结构简式二、乙醛CH3CH2OH(1)与氢气的加成反应1、加成反应——还原反应体现了乙醛的氧化性有机的氧化还原反应还原反应:加氢或失氧氧化反应:加氧或失氢氢氰酸、氨及氨的衍生物、醇等。(2)与其它试剂的加成反应H-CN H-NH2 R-O-H知识拓展(1)乙醛与氧气(2)乙醛被强氧化剂氧化(如酸性KMnO4溶液、溴水等)—燃烧反应催化氧化反应(氧化成酸)探究一褪色2、氧化反应——体现乙醛的还原性常见的极性试剂有:
氢氰酸、氨及氨的衍生物、醇等。(2)与极性试剂的加成反应H-CN H-NH2 R-O-H与氢氰酸的反应——使碳链增长(3) 与银氨溶液的反应① 配制银氨溶液:取一洁净试管,加入2mL2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解: 银镜反应---(氢氧化二氨合银) 注意:银镜反应要求在碱性环境下进行,
但氨水不应过量太多探究二..注意2、水浴加热形成银镜:在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
(1)试管内壁必须洁净;
(2)必须水浴加热;
(3)加热时不可振荡和摇动试管;
(4)须用新配制的银氨溶液;
(5)乙醛用量不可太多;
(6)碱性环境下,乙醛被氧化成乙酸后又与 NH3反应生成乙酸铵银镜反应很简单,生成物是羧酸铵,
还有一水二银三个氨。 若银镜反应得不到预期的现象,可从试管是否洁净、操作方法、药品用量等方面寻找原因。银镜反应的应用:①检验含有醛基的物质②确定醛基的数目或反应的一元醛的物质的量:R-CHO → 2Ag③用于镀镜或瓶胆(4)与新制氢氧化铜悬浊液的反应配制Cu(OH)2悬浊液:在试管里加 入10%NaOH溶液2mL,滴入2%CuSO4溶液4~6滴,振荡。CuSO4+2NaOH=Cu(OH)2↓+Na2SO4反应:向新制Cu(OH)2悬浊液中加入乙醛溶液0.5mL,用酒精灯加热至沸腾。探究三应用:该反应也可用于检验醛基;还用于糖尿病的检验。砖红色 若与新制氢氧化铜悬浊液反应得不到预期的现象,可从试管是否洁净、操作方法、药品用量等方面寻找原因。 先取待测液少量于试管中,加足量的银氨溶液[或新制的Cu(OH)2]使醛基氧化。然后再滴加酸性KMnO4溶液,若酸性KMnO4溶液退色则证明含有碳碳双键.小 结CH3CH2OH氧化反应2、氧化反应1、加成反应(还原反应)结论:醛既有氧化性又有还原性学以致用以乙烯为有机原料(无机物自选)设计合成路线制取乙酸。写出有关反应方程式课后作业课本P791(1)(2)(3)(5)(6)
醛可能发生的化学反应;
2、熟练掌握醛的化学性质。学习难点:乙醛与银氨溶液、新制Cu(OH)2反应的化学方程式的正确书写学习重点:乙醛的结构特点和主要化学性质1. 醛基2. 醛的定义:结构式结构简式不能写成电子式分子里由烃基(或氢原子)跟醛基相连而构成的化合物。—CHO—COH一、醛基和醛CD当堂训练D:CH3-CH2–CHO以下属于醛的有 A:B:C:E:小结:
醛一定含有醛基,但含有醛基的不一定是醛3. 常见的醛:甲醛:无色有刺激性气味的气体,它的水溶液(又称福尔马林)具有杀菌、防腐性能。苯甲醛乙醛:无色有刺激性气味的液体,密度比水的小,易挥发,易燃烧,能与水、乙醇等互溶。1. 分子结构:结构简式二、乙醛CH3CH2OH(1)与氢气的加成反应1、加成反应——还原反应体现了乙醛的氧化性有机的氧化还原反应还原反应:加氢或失氧氧化反应:加氧或失氢氢氰酸、氨及氨的衍生物、醇等。(2)与其它试剂的加成反应H-CN H-NH2 R-O-H知识拓展(1)乙醛与氧气(2)乙醛被强氧化剂氧化(如酸性KMnO4溶液、溴水等)—燃烧反应催化氧化反应(氧化成酸)探究一褪色2、氧化反应——体现乙醛的还原性常见的极性试剂有:
氢氰酸、氨及氨的衍生物、醇等。(2)与极性试剂的加成反应H-CN H-NH2 R-O-H与氢氰酸的反应——使碳链增长(3) 与银氨溶液的反应① 配制银氨溶液:取一洁净试管,加入2mL2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解: 银镜反应---(氢氧化二氨合银) 注意:银镜反应要求在碱性环境下进行,
但氨水不应过量太多探究二..注意2、水浴加热形成银镜:在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
(1)试管内壁必须洁净;
(2)必须水浴加热;
(3)加热时不可振荡和摇动试管;
(4)须用新配制的银氨溶液;
(5)乙醛用量不可太多;
(6)碱性环境下,乙醛被氧化成乙酸后又与 NH3反应生成乙酸铵银镜反应很简单,生成物是羧酸铵,
还有一水二银三个氨。 若银镜反应得不到预期的现象,可从试管是否洁净、操作方法、药品用量等方面寻找原因。银镜反应的应用:①检验含有醛基的物质②确定醛基的数目或反应的一元醛的物质的量:R-CHO → 2Ag③用于镀镜或瓶胆(4)与新制氢氧化铜悬浊液的反应配制Cu(OH)2悬浊液:在试管里加 入10%NaOH溶液2mL,滴入2%CuSO4溶液4~6滴,振荡。CuSO4+2NaOH=Cu(OH)2↓+Na2SO4反应:向新制Cu(OH)2悬浊液中加入乙醛溶液0.5mL,用酒精灯加热至沸腾。探究三应用:该反应也可用于检验醛基;还用于糖尿病的检验。砖红色 若与新制氢氧化铜悬浊液反应得不到预期的现象,可从试管是否洁净、操作方法、药品用量等方面寻找原因。 先取待测液少量于试管中,加足量的银氨溶液[或新制的Cu(OH)2]使醛基氧化。然后再滴加酸性KMnO4溶液,若酸性KMnO4溶液退色则证明含有碳碳双键.小 结CH3CH2OH氧化反应2、氧化反应1、加成反应(还原反应)结论:醛既有氧化性又有还原性学以致用以乙烯为有机原料(无机物自选)设计合成路线制取乙酸。写出有关反应方程式课后作业课本P791(1)(2)(3)(5)(6)
