第1节 金属材料 同步练习
图片预览

文档简介
第2章 物质转化与材料利用 第1节 金属材料 同步练习题
1.下列生活中的物品由金属材料制成的是( )
2.“金银铜铁锡”俗称五金,相关叙述错误的是( )
A.铁锅应用了铁的导热性
B.金属银可与硝酸铜溶液发生置换反应
C.金的化学性质最不活泼
D.焊锡(锡铅合金)比锡熔点低
3.下列说法中正确的是( )
A.废旧电池可以随意丢弃
B.铁矿石可以随意开采
C.被腐蚀的铁制品应该加以回收利用
D.铁丝在氧气中燃烧生成氧化铁
4.铁在下列哪种情况下最容易生锈( )
A.在干燥的空气中 B.部分浸入食盐水中
C.在潮湿的空气中 D.浸没在植物油中
5. 人类的生活和生产都离不开金属材料。下列金属制品中,主要利用金属导热性的是( )
6. 我国第四套人民币硬币中,一元币为钢芯镀镍合金,伍角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时,不需要考虑的因素是( )
A.金属的硬度 B.金属的导热性
C.金属的耐腐蚀性 D.金属价格与硬币面值的吻合度
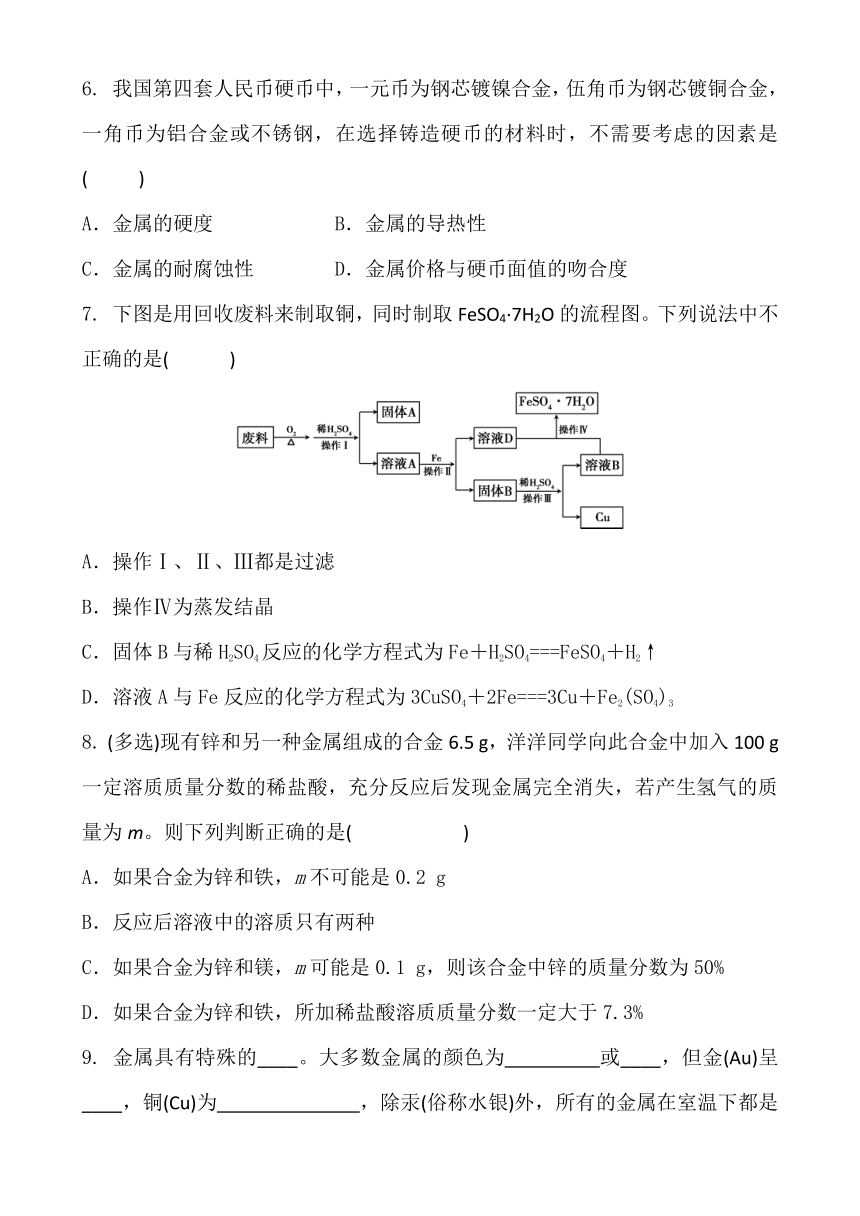
7. 下图是用回收废料来制取铜,同时制取FeSO4·7H2O的流程图。下列说法中不正确的是( )
A.操作Ⅰ、Ⅱ、Ⅲ都是过滤
B.操作Ⅳ为蒸发结晶
C.固体B与稀H2SO4反应的化学方程式为Fe+H2SO4===FeSO4+H2↑
D.溶液A与Fe反应的化学方程式为3CuSO4+2Fe===3Cu+Fe2(SO4)3
8. (多选)现有锌和另一种金属组成的合金6.5 g,洋洋同学向此合金中加入100 g一定溶质质量分数的稀盐酸,充分反应后发现金属完全消失,若产生氢气的质量为m。则下列判断正确的是( )
A.如果合金为锌和铁,m不可能是0.2 g
B.反应后溶液中的溶质只有两种
C.如果合金为锌和镁,m可能是0.1 g,则该合金中锌的质量分数为50%
D.如果合金为锌和铁,所加稀盐酸溶质质量分数一定大于7.3%
9. 金属具有特殊的____。大多数金属的颜色为 或____,但金(Au)呈____,铜(Cu)为 ,除汞(俗称水银)外,所有的金属在室温下都是____。
10. 金属具有良好的 、 和延展性,而非金属的____、____性能均较差,也没有延展性。
11. 把一种金属跟其他一种或几种金属(或非金属)一起熔合而成的具有金属特性的物质,就称为____。合金往往比 具有更好的性能。钢是一种由____和____等元素形成的合金,质地____,有____和 ,机械性能好。
12. 像铅、镉等有毒的金属被腐蚀后会溶于水中形成 ,污染土壤和 。可以回收的金属包括____、____、____、____、____、____、银和金等。
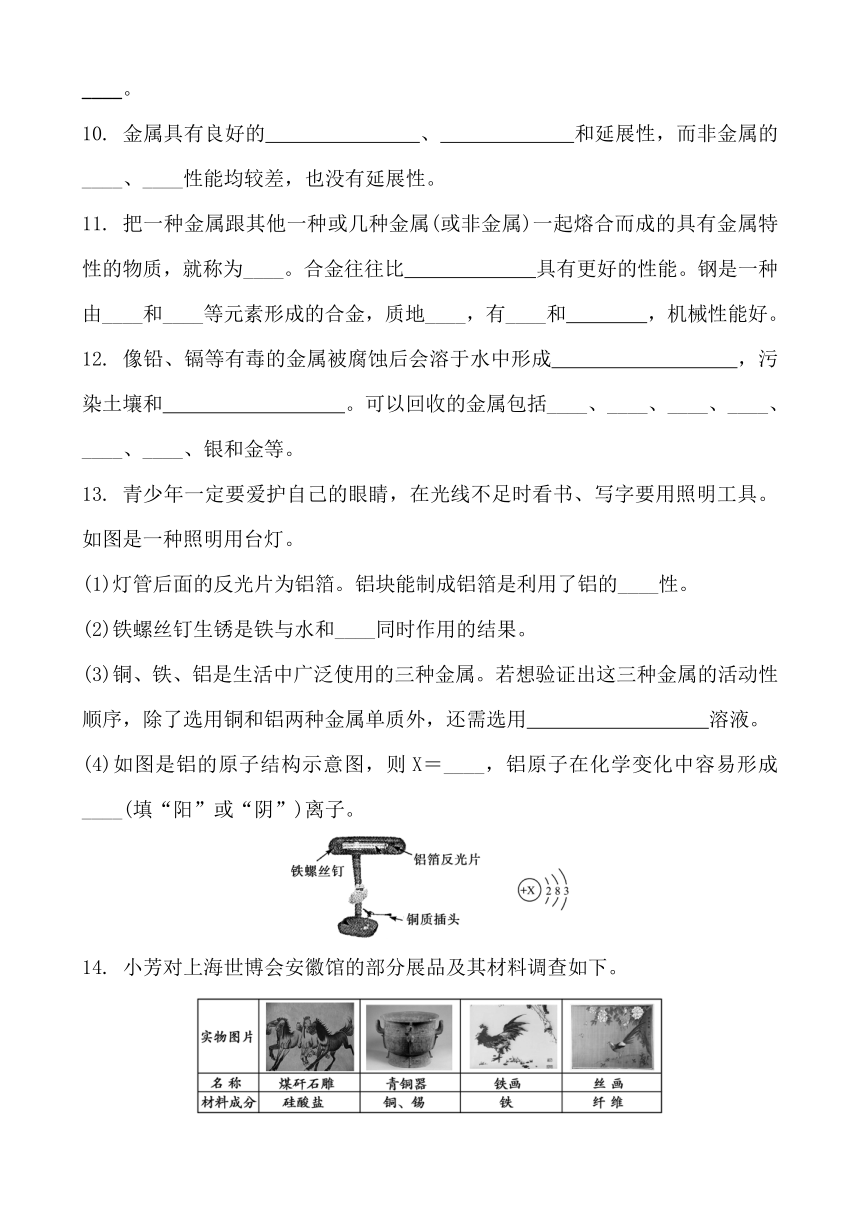
13. 青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具。如图是一种照明用台灯。
(1)灯管后面的反光片为铝箔。铝块能制成铝箔是利用了铝的____性。
(2)铁螺丝钉生锈是铁与水和____同时作用的结果。
(3)铜、铁、铝是生活中广泛使用的三种金属。若想验证出这三种金属的活动性顺序,除了选用铜和铝两种金属单质外,还需选用 溶液。
(4)如图是铝的原子结构示意图,则X=____,铝原子在化学变化中容易形成____(填“阳”或“阴”)离子。
14. 小芳对上海世博会安徽馆的部分展品及其材料调查如下。
(1)上述展品使用的金属材料是 (写一种即可)。
(2)煤矸石雕的组成元素之一——硅属于 (填“金属”或“非金属”)元素。
(3)下列关于铁、锡、铜性质的说法错误的是____(填字母序号)。
a.均可以导电 b.均可以和氧气反应 c.均可以和稀盐酸反应
(4)写出直接表示铁比铜活泼的化学方程式: 。
15. 没有金属,生活是难以想象的。请你根据对金属和金属材料的认识,回答下列问题。
(1)如图标出的是组成灯泡的物质,所标出的物质中不属于金属材料的是____。
(2)钢铁厂常常用赤铁矿石冶炼生铁,赤铁矿石的主要成分是 ;很多大型场馆的建设使用了大量的钢材而不是纯铁,
主要是因为钢比纯铁具有 的优良性能。
(3)工人师傅切割铁板时,用硫酸铜溶液在铁板上划线可以留下红色痕迹,该变化的原理是 (用化学方程式表示)。
16. 将玻璃管插入金属钠块中,拔出玻璃管,玻璃管内留有一小截金属钠(见图1);把带有橡皮塞的玻璃管插入盛有浅绿色氯气的烧瓶中(见图2,烧瓶底部铺有少量的细沙);向玻璃管中滴入几滴水,堵塞玻璃管的钠块成滴落下(见图3);烧瓶内产生少量白烟,继而燃烧,浅绿色逐渐消失(见图4);最终,白色的烟雾充满烧瓶(见图5)。
从以上实验推断:金属钠的 、熔点____。
水可以与金属钠反应____(填“吸收”或“放出”)热量,烧瓶中充满的白色烟雾可能是 。
17. 小红同学在网店花了200元买了一个10 g重的手镯(银锌合金),她想探究此手镯中银的含量,于是请化学老师和她一起探究:在实验室用足量的稀硫酸分多次与手镯充分反应,实验结果如下表:
稀硫酸/g
10
10
10
10
10
剩余固体质量/g
8.7
7.4
6.1
4.8
4.8
根据上表中的数据分析,完成下列问题:
如果小红用所得的银制作一枚戒指,其质量不超过多少克?
(2)计算所用稀硫酸的溶质质量分数是多少?
参考答案:
1---7 CBCBD BD
8. AD
9. 光泽 银白色 灰色 黄色 紫红色 固体
10. 导电性 导热性 导电 导热
11. 合金 纯金属 碳 铁 坚硬 弹性 延展性
12. 金属离子 地下水源 铝 铅 铁 铜 锡 锌
13. (1) 延展
(2) 氧气
(3) 硫酸亚铁
(4) 13 阳
14. (1) 铜(铁或锡)
(2) 非金属
(3) c
(4) Fe+CuSO4===FeSO4+Cu
15. (1) 玻璃、氮气
(2) Fe2O3 硬度大
(3) Fe+CuSO4===FeSO4+Cu
16. 硬度小 低 放出 氯化钠
17. (1)小红用所得的银制作一枚戒指,其质量不超过4.8 g
(2)19.6%
1.下列生活中的物品由金属材料制成的是( )
2.“金银铜铁锡”俗称五金,相关叙述错误的是( )
A.铁锅应用了铁的导热性
B.金属银可与硝酸铜溶液发生置换反应
C.金的化学性质最不活泼
D.焊锡(锡铅合金)比锡熔点低
3.下列说法中正确的是( )
A.废旧电池可以随意丢弃
B.铁矿石可以随意开采
C.被腐蚀的铁制品应该加以回收利用
D.铁丝在氧气中燃烧生成氧化铁
4.铁在下列哪种情况下最容易生锈( )
A.在干燥的空气中 B.部分浸入食盐水中
C.在潮湿的空气中 D.浸没在植物油中
5. 人类的生活和生产都离不开金属材料。下列金属制品中,主要利用金属导热性的是( )
6. 我国第四套人民币硬币中,一元币为钢芯镀镍合金,伍角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时,不需要考虑的因素是( )
A.金属的硬度 B.金属的导热性
C.金属的耐腐蚀性 D.金属价格与硬币面值的吻合度
7. 下图是用回收废料来制取铜,同时制取FeSO4·7H2O的流程图。下列说法中不正确的是( )
A.操作Ⅰ、Ⅱ、Ⅲ都是过滤
B.操作Ⅳ为蒸发结晶
C.固体B与稀H2SO4反应的化学方程式为Fe+H2SO4===FeSO4+H2↑
D.溶液A与Fe反应的化学方程式为3CuSO4+2Fe===3Cu+Fe2(SO4)3
8. (多选)现有锌和另一种金属组成的合金6.5 g,洋洋同学向此合金中加入100 g一定溶质质量分数的稀盐酸,充分反应后发现金属完全消失,若产生氢气的质量为m。则下列判断正确的是( )
A.如果合金为锌和铁,m不可能是0.2 g
B.反应后溶液中的溶质只有两种
C.如果合金为锌和镁,m可能是0.1 g,则该合金中锌的质量分数为50%
D.如果合金为锌和铁,所加稀盐酸溶质质量分数一定大于7.3%
9. 金属具有特殊的____。大多数金属的颜色为 或____,但金(Au)呈____,铜(Cu)为 ,除汞(俗称水银)外,所有的金属在室温下都是____。
10. 金属具有良好的 、 和延展性,而非金属的____、____性能均较差,也没有延展性。
11. 把一种金属跟其他一种或几种金属(或非金属)一起熔合而成的具有金属特性的物质,就称为____。合金往往比 具有更好的性能。钢是一种由____和____等元素形成的合金,质地____,有____和 ,机械性能好。
12. 像铅、镉等有毒的金属被腐蚀后会溶于水中形成 ,污染土壤和 。可以回收的金属包括____、____、____、____、____、____、银和金等。
13. 青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具。如图是一种照明用台灯。
(1)灯管后面的反光片为铝箔。铝块能制成铝箔是利用了铝的____性。
(2)铁螺丝钉生锈是铁与水和____同时作用的结果。
(3)铜、铁、铝是生活中广泛使用的三种金属。若想验证出这三种金属的活动性顺序,除了选用铜和铝两种金属单质外,还需选用 溶液。
(4)如图是铝的原子结构示意图,则X=____,铝原子在化学变化中容易形成____(填“阳”或“阴”)离子。
14. 小芳对上海世博会安徽馆的部分展品及其材料调查如下。
(1)上述展品使用的金属材料是 (写一种即可)。
(2)煤矸石雕的组成元素之一——硅属于 (填“金属”或“非金属”)元素。
(3)下列关于铁、锡、铜性质的说法错误的是____(填字母序号)。
a.均可以导电 b.均可以和氧气反应 c.均可以和稀盐酸反应
(4)写出直接表示铁比铜活泼的化学方程式: 。
15. 没有金属,生活是难以想象的。请你根据对金属和金属材料的认识,回答下列问题。
(1)如图标出的是组成灯泡的物质,所标出的物质中不属于金属材料的是____。
(2)钢铁厂常常用赤铁矿石冶炼生铁,赤铁矿石的主要成分是 ;很多大型场馆的建设使用了大量的钢材而不是纯铁,
主要是因为钢比纯铁具有 的优良性能。
(3)工人师傅切割铁板时,用硫酸铜溶液在铁板上划线可以留下红色痕迹,该变化的原理是 (用化学方程式表示)。
16. 将玻璃管插入金属钠块中,拔出玻璃管,玻璃管内留有一小截金属钠(见图1);把带有橡皮塞的玻璃管插入盛有浅绿色氯气的烧瓶中(见图2,烧瓶底部铺有少量的细沙);向玻璃管中滴入几滴水,堵塞玻璃管的钠块成滴落下(见图3);烧瓶内产生少量白烟,继而燃烧,浅绿色逐渐消失(见图4);最终,白色的烟雾充满烧瓶(见图5)。
从以上实验推断:金属钠的 、熔点____。
水可以与金属钠反应____(填“吸收”或“放出”)热量,烧瓶中充满的白色烟雾可能是 。
17. 小红同学在网店花了200元买了一个10 g重的手镯(银锌合金),她想探究此手镯中银的含量,于是请化学老师和她一起探究:在实验室用足量的稀硫酸分多次与手镯充分反应,实验结果如下表:
稀硫酸/g
10
10
10
10
10
剩余固体质量/g
8.7
7.4
6.1
4.8
4.8
根据上表中的数据分析,完成下列问题:
如果小红用所得的银制作一枚戒指,其质量不超过多少克?
(2)计算所用稀硫酸的溶质质量分数是多少?
参考答案:
1---7 CBCBD BD
8. AD
9. 光泽 银白色 灰色 黄色 紫红色 固体
10. 导电性 导热性 导电 导热
11. 合金 纯金属 碳 铁 坚硬 弹性 延展性
12. 金属离子 地下水源 铝 铅 铁 铜 锡 锌
13. (1) 延展
(2) 氧气
(3) 硫酸亚铁
(4) 13 阳
14. (1) 铜(铁或锡)
(2) 非金属
(3) c
(4) Fe+CuSO4===FeSO4+Cu
15. (1) 玻璃、氮气
(2) Fe2O3 硬度大
(3) Fe+CuSO4===FeSO4+Cu
16. 硬度小 低 放出 氯化钠
17. (1)小红用所得的银制作一枚戒指,其质量不超过4.8 g
(2)19.6%
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
