浙江省中考科学(化学部分)第二篇主题1第三单元空气(2)(课件 33张ppt)
文档属性
| 名称 | 浙江省中考科学(化学部分)第二篇主题1第三单元空气(2)(课件 33张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-03-10 00:00:00 | ||
图片预览









文档简介
第三单元 空气(2)
1.[2018·枣庄]氧气与世间万物如影随形。下列关于氧气说法错误的是 ( )
A.空气中的氧气与水中溶解的氧气化学性质同样活泼
B.工业上可以利用分离冷冻空气法制取氧气
C.氧气可以支持燃烧,说明氧气具有可燃性
D.氧气能供给呼吸,它和体内物质反应,释放能量,维持 生命活动
C
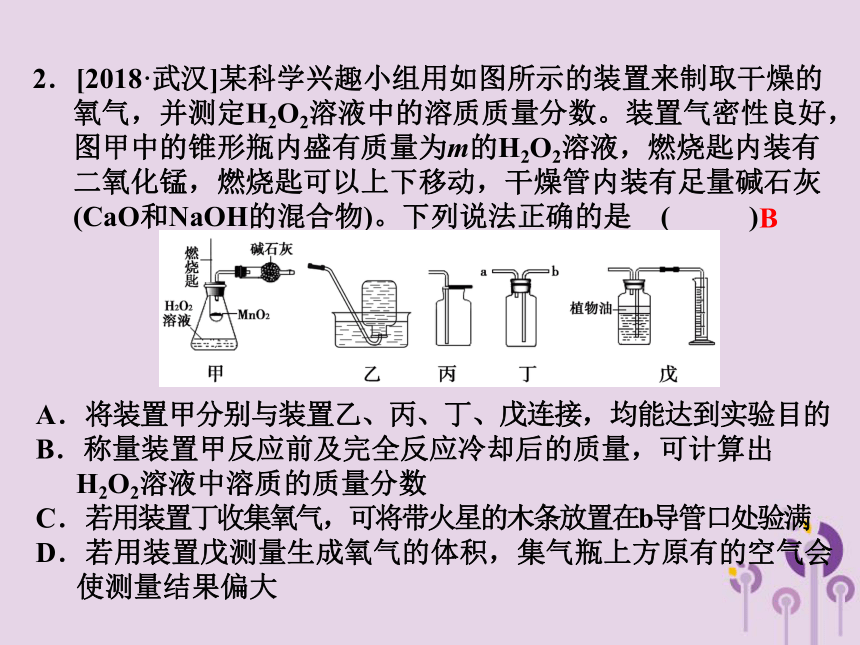
2.[2018·武汉]某科学兴趣小组用如图所示的装置来制取干燥的氧气,并测定H2O2溶液中的溶质质量分数。装置气密性良好,图甲中的锥形瓶内盛有质量为m的H2O2溶液,燃烧匙内装有二氧化锰,燃烧匙可以上下移动,干燥管内装有足量碱石灰(CaO和NaOH的混合物)。下列说法正确的是 ( )
B
A.将装置甲分别与装置乙、丙、丁、戊连接,均能达到实验目的
B.称量装置甲反应前及完全反应冷却后的质量,可计算出H2O2溶液中溶质的质量分数
C.若用装置丁收集氧气,可将带火星的木条放置在b导管口处验满
D.若用装置戊测量生成氧气的体积,集气瓶上方原有的空气会使测量结果偏大
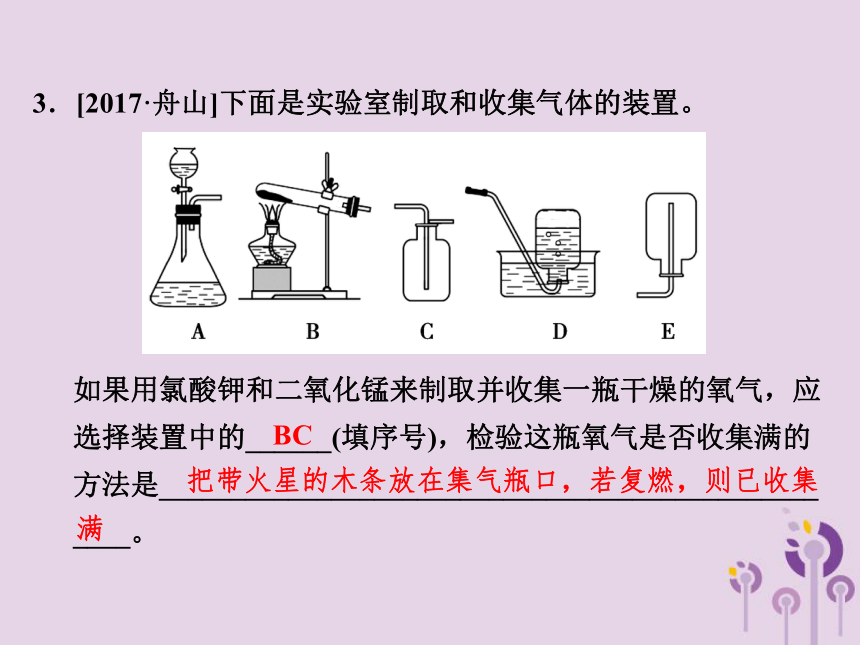
3.[2017·舟山]下面是实验室制取和收集气体的装置。
如果用氯酸钾和二氧化锰来制取并收集一瓶干燥的氧气,应选择装置中的______(填序号),检验这瓶氧气是否收集满的方法是______________________________________________ ____。
BC
把带火星的木条放在集气瓶口,若复燃,则已收集
满
4.[2017·温州]在用氯酸钾和二氧化锰的混合物制取氧气实验后, 为了进一步探究二氧化锰的
用量对氯酸钾分解速度的影响,小
明用如图装置,以及实验室提供
的实验所需药品和器材进行实验。
老师对实验的建议:①每组实验
氯酸钾用量可取4g,二氧化锰质量不宜超过2g。②实验应设计4组。
(1)结合老师建议,补充完整实验步骤①之后的其他步骤。
①检查装置的气密性;
……
(2)实验结束后,小明回收了二氧化锰。如果要证明二氧化
锰是氯酸钾分解的催化剂,还需验证该二氧化锰的______
_________保持不变。
质量和
化学性质
【答案】 (1)②取4g氯酸钾与0.5g二氧化锰,均匀混合后加入试管中,连接好装置;③开始加热试管,用秒表记录量筒收集一定体积氧气的时间;④换用三支相同的试管,各加入4g氯酸钾,分别与1g、1.5g、2g二氧化锰均匀混合,用相同装置重复步骤②、③;⑤比较实验记录的四次时间长短,判断氯酸钾的分解速度与二氧化锰用量的关系。(其他合理答案也可以)
氧气
氧气的物理性质:通常状况下,氧气是______________的气体,不易溶于水,密度比空气密度略大。
无色、无味
1.氧气的实验室制法
排水集气法
向上排空气法
集气瓶口
复燃
集气瓶中
复燃
液面以下
移出导气管
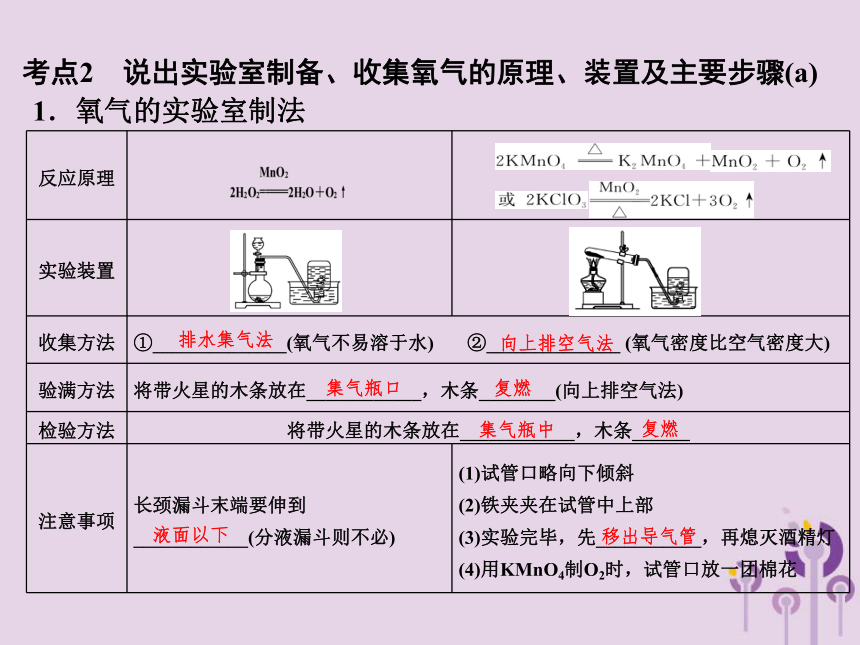
考点2 说出实验室制备、收集氧气的原理、装置及主要步骤(a)
反应原理
实验装置
收集方法 ①______________(氧气不易溶于水) ②______________ (氧气密度比空气密度大)
验满方法 将带火星的木条放在____________,木条________(向上排空气法)
检验方法 将带火星的木条放在____________,木条______
注意事项 长颈漏斗末端要伸到____________(分液漏斗则不必) (1)试管口略向下倾斜
(2)铁夹夹在试管中上部
(3)实验完毕,先___________,再熄灭酒精灯
(4)用KMnO4制O2时,试管口放一团棉花
2. 氧气的工业制法:空气冷冻分离法,利用液氧、液氮的沸点不同进行分离,属于物理变化。
制氧气口诀
口诀1:二氧化锰氯酸钾,混合均匀把热加。
制氧装置有特点,底高口低略倾斜。
口诀2:实验先查气密性,受热均匀试管倾。
收集常用排水法,先撤导管后移灯。
口诀3:查装定点收离熄(谐音:茶庄定点收利息)。
记忆卡片
考点3 举例说明氧气的主要化学性质——氧化性(b)
氧气的化学性质比较活泼,表现为有__________和________ __。
区分物质燃烧时产生的火焰、烟、雾
可燃性气
体
易气
化的固、液体
物质
固体小
颗粒
助燃性
氧化性
名称 定义 特征 举例
火焰 可燃性气体或易气化的固、液体物质燃烧时的特征 需__________ ____或______ __________________ 氢气、甲烷、一氧化碳、酒精、汽油、煤油、石蜡、木材、硫等物质燃烧均能形成火焰
烟 可燃物燃烧时,产生的大量固体小颗粒分散悬浮于空气而形成的 形成________ ______ 红磷燃烧生成细小的五氧化二磷颗粒,形成白烟
小液滴
氧气的主要用途:______________________。如急救时常用氧气来帮助病人________;氧气与燃料燃烧后产生的高温火焰可用于切割或焊接金属。
将带火星的木条放在____________,木条________。
供给呼吸和帮助燃烧
呼吸
集气瓶中
复燃
雾 小液滴分散悬浮于空气而形成的 形成________ __ 打开浓盐酸瓶可见白雾,是由于挥发出来的氯化氢与空气中水蒸气结合形成了盐酸液滴
类型一 氧气的性质及应用
典例 [2017·苏州]下列关于氧气的说法中,不正确的是 ( )
A.氧气能支持燃烧,所以氧气可作燃料
B.氧气能使带火星的木条复燃
C.红磷在氧气中燃烧,产生浓厚的白烟
D.实验室加热高锰酸钾制取氧气时,试管内靠近导管处放 一团蓬松的棉花
A
跟踪训练 [2017·滨州改编]下列关于氧气的说法中错误的是 ( )
A.铁丝在氧气中燃烧的实验中,铁丝上绑火柴是为了引燃铁丝
B.氧气支持燃烧,是一种高能清洁燃料
C.硫在氧气中燃烧的实验中,集气瓶底放一些水是为了吸收二
氧化硫防止空气污染
D.氧气可用排水法或向上排空气法收集
【解析】 氧气能支持燃烧,但不具有可燃性,不能作高能清洁燃料。
【点悟】 氧气的助燃性不等于可燃性,这是一个常见的易错点。
B
类型二 掌握氧气的制取、检验与性质综合题
典例 [2017·庆阳]如图所示的仪器常用于实验室制取气体。请回答下列问题:
(1)仪器⑧的名称是____________。
长颈漏斗
③④⑥⑨
(3)用排水法收集氧气的原因是__________________。如果要做铁丝在氧气中燃烧的实验,收集氧气时要在瓶底留一些水,其原因是______________________________。
【解析】 使用高锰酸钾制取氧气,是固体加热型反应,故需要的仪器有③④⑥⑨。
【点悟】 气体发生装置和收集装置的选择是常见的气体题目考查内容,需要根据反应的条件和反应物的状态选择合适的发生装置,根据气体的密度和溶解性选择合适的收集方法。
氧气不易溶于水
防止高温熔融物溅落炸裂瓶底
跟踪训练 [2018·广州]如图是实验室制备气体的部分装置。
(1)加热混有二氧化锰的氯酸钾制备一瓶氧气用于性质实验。
3O2↑
②可选用_____与_____(填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后________________,观察到有气泡冒出,说明装置气密性良好。
(2)氢气被认为是理想的清洁、高能燃料。
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用_____(填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器→检查装置气密性→装入药品制备氢气→________→点燃。
②电解水也可制得H2。装置如图F,______管中产生的是氢气。
B
C
双手捂住试管
A
验纯
甲
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是_______。
A.用矿石生产锌和硫酸,再相互反应
B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水
D.利用风能、水力发电,再电解水
BD
类型三 关于影响氧气制取速率因素的综合题
典例 [2016·杭州]小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持仪器略去)进行了两次实验,两次实验的部分设计如表所示:
(1)实验2中应加入5%的H2O2______mL。
(2)在两次实验中,可通过_________________________________ ____________来比较H2O2分解反应速率的大小。
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有_____________ ______________________________________________。
(4)实验结束后若要将MnO2从混合物中分离出来,可采取的方法是________。
40
收集相同体积的氧气所需要的时间
(合理即可)
温度较高,
水蒸发较快,导致氧气中含较多水蒸气(合理即可)
过滤
实验1 实验2
MnO2的质量(g) 0.5 0.5
5%的H2O2体积(mL) 40 待填
水浴温度(℃) 20 80
…
跟踪训练 [2018·金华]小君
和小英同学发现:带火星的
竹签在空气中不会复燃,若
用装有60%水的集气瓶倒
置在水槽中收集氧气,得到
的气体能使带火星的竹签复
燃,为了找到能使带火星竹
签复燃的氧气含量最小值,她们进行了如下探究:
【设计实验】小君设计了如图的装置,该装置的圆底烧瓶中放入25mL水的目的是______________________________________ ______。
稀释过氧化氢溶液,减缓过氧化氢的分解
速度
【实验研究】第一组实验:取3只集气瓶,编号为①②③,分别装入15%、30%和45%的水,盖上盖玻片倒置在水槽中。当气泡______________放出后,导管口伸入集气瓶把其中的水全部排出,将相同的3支带火星竹签分别插入①~③号瓶中,记录实验现象。
获得第一组实验现象后,小君又做了第二组实验,并记录实验现象,两组实验数据和现象见表:
连续、均匀
实验分组 第一组 第二组
实验序号 ① ② ③ ④ ⑤ ⑥
集气瓶装水的体积分数(%) 15 30 45 34 38 42
带火星的竹签状况 亮 很亮 复燃 很亮 复燃 复燃
得出上述两组实验现象后,小英认为还不能确定能使带火星的竹签复燃的氧气含量最小值,需继续进行实验。则实验序号⑦的集气瓶装水的体积分数应该是______%。
【实验结论】再经过数次实验并计算后得出:能使带火星的竹签复燃的氧气含量最小值为48.7%。
【继续探究】小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的措施:_______________________ ______________________________。
36
收集氧气前增加气体的
干燥装置,再用排油法收集氧气
不理解制取氧气时各物质质量变化致错
典例 [2017·重庆B卷]已知FeCl3也可以催化H2O2的分解,现向一定量的H2O2溶液中滴入几滴一定溶质质量分数的FeCl3溶液,充分反应(忽略水的挥发)。下列图像正确的是( )
【错解】选D
【析错】向一定量的H2O2溶液中滴入几滴一定溶质质量分数的FeCl3溶液,过氧化氢完全反应后,氧气质量不再变化;过氧化氢分解为氧气和水,溶剂质量增加,完全反应后,溶剂质量不再变化;过氧化氢分解为氧气和水,过氧化氢的质量分数减小,完全反应后,过氧化氢的质量为0,质量分数为0;FeCl3是催化剂,反应前后质量不变,过氧化氢分解为氧气和水,溶液质量减小,FeCl3的质量分数变大。
【正解】选B
A.固体中氧元素的质量
B.生成O2的质量
C.固体中MnO2的质量
D.固体中钾元素的质量分数
A
氧气的制取和性质研究
1.教材实验原理图
2.实验原理
3.实验结论
(1)结论一:木炭在氧气中能剧烈燃烧,发出白光。
(2)结论二:铝箔在氧气中能剧烈燃烧,发出耀眼的白光,放出大量的热,生成白色粉末状固体。
4.实验关键点
(1)实验仪器及操作注意事项
酒精灯:实验开始时,先点燃酒精灯,再收集氧气;集中加热前要预热试管;实验结束时,先将导管移出水面,再熄灭酒精灯。
集气瓶:待导管口连续、均匀冒气泡后,再收集气体。
试管:试管口加棉花,试管口略向下倾斜。
导管:导管口只能在集气瓶口处。
(2)遇到问题的处理方法
a.试管口未塞棉花,导致导管口被高锰酸钾粉末堵住。应重新做实验。
b.试管口未略向下倾斜,导致冷凝水倒流,使试管破裂。应重新做实验。
5.实验拓展
(1)将氧气的制取,与可燃物燃烧的条件相结合的综合题型。
(2)将氧气的制取和应用,与二氧化碳和氢气的制取和应用相结合的综合题型。
(3)探究氧气制取过程中影响氧气制取速率的因素。
典例 [2018·衢州]小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
(1)小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星的木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到______________________________________ _____为氧气集满的标准。
当气泡从瓶口冒出时(或观察到瓶中水排尽
时)
收集方法 向上排空气法 排水法
氧气浓度(%) 79.6 79.7 79.9 90.0 89.8 89.3
氧气平均浓度(%) 79.7 89.7
(2)以上两种方法中,________法收集到的氧气更纯净。
(3)向上排空气法收集到的氧气浓度只有80%左右的原因有________。
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星的木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
排水
ACD
1.[2018·枣庄]氧气与世间万物如影随形。下列关于氧气说法错误的是 ( )
A.空气中的氧气与水中溶解的氧气化学性质同样活泼
B.工业上可以利用分离冷冻空气法制取氧气
C.氧气可以支持燃烧,说明氧气具有可燃性
D.氧气能供给呼吸,它和体内物质反应,释放能量,维持 生命活动
C
2.[2018·武汉]某科学兴趣小组用如图所示的装置来制取干燥的氧气,并测定H2O2溶液中的溶质质量分数。装置气密性良好,图甲中的锥形瓶内盛有质量为m的H2O2溶液,燃烧匙内装有二氧化锰,燃烧匙可以上下移动,干燥管内装有足量碱石灰(CaO和NaOH的混合物)。下列说法正确的是 ( )
B
A.将装置甲分别与装置乙、丙、丁、戊连接,均能达到实验目的
B.称量装置甲反应前及完全反应冷却后的质量,可计算出H2O2溶液中溶质的质量分数
C.若用装置丁收集氧气,可将带火星的木条放置在b导管口处验满
D.若用装置戊测量生成氧气的体积,集气瓶上方原有的空气会使测量结果偏大
3.[2017·舟山]下面是实验室制取和收集气体的装置。
如果用氯酸钾和二氧化锰来制取并收集一瓶干燥的氧气,应选择装置中的______(填序号),检验这瓶氧气是否收集满的方法是______________________________________________ ____。
BC
把带火星的木条放在集气瓶口,若复燃,则已收集
满
4.[2017·温州]在用氯酸钾和二氧化锰的混合物制取氧气实验后, 为了进一步探究二氧化锰的
用量对氯酸钾分解速度的影响,小
明用如图装置,以及实验室提供
的实验所需药品和器材进行实验。
老师对实验的建议:①每组实验
氯酸钾用量可取4g,二氧化锰质量不宜超过2g。②实验应设计4组。
(1)结合老师建议,补充完整实验步骤①之后的其他步骤。
①检查装置的气密性;
……
(2)实验结束后,小明回收了二氧化锰。如果要证明二氧化
锰是氯酸钾分解的催化剂,还需验证该二氧化锰的______
_________保持不变。
质量和
化学性质
【答案】 (1)②取4g氯酸钾与0.5g二氧化锰,均匀混合后加入试管中,连接好装置;③开始加热试管,用秒表记录量筒收集一定体积氧气的时间;④换用三支相同的试管,各加入4g氯酸钾,分别与1g、1.5g、2g二氧化锰均匀混合,用相同装置重复步骤②、③;⑤比较实验记录的四次时间长短,判断氯酸钾的分解速度与二氧化锰用量的关系。(其他合理答案也可以)
氧气
氧气的物理性质:通常状况下,氧气是______________的气体,不易溶于水,密度比空气密度略大。
无色、无味
1.氧气的实验室制法
排水集气法
向上排空气法
集气瓶口
复燃
集气瓶中
复燃
液面以下
移出导气管
考点2 说出实验室制备、收集氧气的原理、装置及主要步骤(a)
反应原理
实验装置
收集方法 ①______________(氧气不易溶于水) ②______________ (氧气密度比空气密度大)
验满方法 将带火星的木条放在____________,木条________(向上排空气法)
检验方法 将带火星的木条放在____________,木条______
注意事项 长颈漏斗末端要伸到____________(分液漏斗则不必) (1)试管口略向下倾斜
(2)铁夹夹在试管中上部
(3)实验完毕,先___________,再熄灭酒精灯
(4)用KMnO4制O2时,试管口放一团棉花
2. 氧气的工业制法:空气冷冻分离法,利用液氧、液氮的沸点不同进行分离,属于物理变化。
制氧气口诀
口诀1:二氧化锰氯酸钾,混合均匀把热加。
制氧装置有特点,底高口低略倾斜。
口诀2:实验先查气密性,受热均匀试管倾。
收集常用排水法,先撤导管后移灯。
口诀3:查装定点收离熄(谐音:茶庄定点收利息)。
记忆卡片
考点3 举例说明氧气的主要化学性质——氧化性(b)
氧气的化学性质比较活泼,表现为有__________和________ __。
区分物质燃烧时产生的火焰、烟、雾
可燃性气
体
易气
化的固、液体
物质
固体小
颗粒
助燃性
氧化性
名称 定义 特征 举例
火焰 可燃性气体或易气化的固、液体物质燃烧时的特征 需__________ ____或______ __________________ 氢气、甲烷、一氧化碳、酒精、汽油、煤油、石蜡、木材、硫等物质燃烧均能形成火焰
烟 可燃物燃烧时,产生的大量固体小颗粒分散悬浮于空气而形成的 形成________ ______ 红磷燃烧生成细小的五氧化二磷颗粒,形成白烟
小液滴
氧气的主要用途:______________________。如急救时常用氧气来帮助病人________;氧气与燃料燃烧后产生的高温火焰可用于切割或焊接金属。
将带火星的木条放在____________,木条________。
供给呼吸和帮助燃烧
呼吸
集气瓶中
复燃
雾 小液滴分散悬浮于空气而形成的 形成________ __ 打开浓盐酸瓶可见白雾,是由于挥发出来的氯化氢与空气中水蒸气结合形成了盐酸液滴
类型一 氧气的性质及应用
典例 [2017·苏州]下列关于氧气的说法中,不正确的是 ( )
A.氧气能支持燃烧,所以氧气可作燃料
B.氧气能使带火星的木条复燃
C.红磷在氧气中燃烧,产生浓厚的白烟
D.实验室加热高锰酸钾制取氧气时,试管内靠近导管处放 一团蓬松的棉花
A
跟踪训练 [2017·滨州改编]下列关于氧气的说法中错误的是 ( )
A.铁丝在氧气中燃烧的实验中,铁丝上绑火柴是为了引燃铁丝
B.氧气支持燃烧,是一种高能清洁燃料
C.硫在氧气中燃烧的实验中,集气瓶底放一些水是为了吸收二
氧化硫防止空气污染
D.氧气可用排水法或向上排空气法收集
【解析】 氧气能支持燃烧,但不具有可燃性,不能作高能清洁燃料。
【点悟】 氧气的助燃性不等于可燃性,这是一个常见的易错点。
B
类型二 掌握氧气的制取、检验与性质综合题
典例 [2017·庆阳]如图所示的仪器常用于实验室制取气体。请回答下列问题:
(1)仪器⑧的名称是____________。
长颈漏斗
③④⑥⑨
(3)用排水法收集氧气的原因是__________________。如果要做铁丝在氧气中燃烧的实验,收集氧气时要在瓶底留一些水,其原因是______________________________。
【解析】 使用高锰酸钾制取氧气,是固体加热型反应,故需要的仪器有③④⑥⑨。
【点悟】 气体发生装置和收集装置的选择是常见的气体题目考查内容,需要根据反应的条件和反应物的状态选择合适的发生装置,根据气体的密度和溶解性选择合适的收集方法。
氧气不易溶于水
防止高温熔融物溅落炸裂瓶底
跟踪训练 [2018·广州]如图是实验室制备气体的部分装置。
(1)加热混有二氧化锰的氯酸钾制备一瓶氧气用于性质实验。
3O2↑
②可选用_____与_____(填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后________________,观察到有气泡冒出,说明装置气密性良好。
(2)氢气被认为是理想的清洁、高能燃料。
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用_____(填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器→检查装置气密性→装入药品制备氢气→________→点燃。
②电解水也可制得H2。装置如图F,______管中产生的是氢气。
B
C
双手捂住试管
A
验纯
甲
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是_______。
A.用矿石生产锌和硫酸,再相互反应
B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水
D.利用风能、水力发电,再电解水
BD
类型三 关于影响氧气制取速率因素的综合题
典例 [2016·杭州]小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持仪器略去)进行了两次实验,两次实验的部分设计如表所示:
(1)实验2中应加入5%的H2O2______mL。
(2)在两次实验中,可通过_________________________________ ____________来比较H2O2分解反应速率的大小。
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有_____________ ______________________________________________。
(4)实验结束后若要将MnO2从混合物中分离出来,可采取的方法是________。
40
收集相同体积的氧气所需要的时间
(合理即可)
温度较高,
水蒸发较快,导致氧气中含较多水蒸气(合理即可)
过滤
实验1 实验2
MnO2的质量(g) 0.5 0.5
5%的H2O2体积(mL) 40 待填
水浴温度(℃) 20 80
…
跟踪训练 [2018·金华]小君
和小英同学发现:带火星的
竹签在空气中不会复燃,若
用装有60%水的集气瓶倒
置在水槽中收集氧气,得到
的气体能使带火星的竹签复
燃,为了找到能使带火星竹
签复燃的氧气含量最小值,她们进行了如下探究:
【设计实验】小君设计了如图的装置,该装置的圆底烧瓶中放入25mL水的目的是______________________________________ ______。
稀释过氧化氢溶液,减缓过氧化氢的分解
速度
【实验研究】第一组实验:取3只集气瓶,编号为①②③,分别装入15%、30%和45%的水,盖上盖玻片倒置在水槽中。当气泡______________放出后,导管口伸入集气瓶把其中的水全部排出,将相同的3支带火星竹签分别插入①~③号瓶中,记录实验现象。
获得第一组实验现象后,小君又做了第二组实验,并记录实验现象,两组实验数据和现象见表:
连续、均匀
实验分组 第一组 第二组
实验序号 ① ② ③ ④ ⑤ ⑥
集气瓶装水的体积分数(%) 15 30 45 34 38 42
带火星的竹签状况 亮 很亮 复燃 很亮 复燃 复燃
得出上述两组实验现象后,小英认为还不能确定能使带火星的竹签复燃的氧气含量最小值,需继续进行实验。则实验序号⑦的集气瓶装水的体积分数应该是______%。
【实验结论】再经过数次实验并计算后得出:能使带火星的竹签复燃的氧气含量最小值为48.7%。
【继续探究】小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的措施:_______________________ ______________________________。
36
收集氧气前增加气体的
干燥装置,再用排油法收集氧气
不理解制取氧气时各物质质量变化致错
典例 [2017·重庆B卷]已知FeCl3也可以催化H2O2的分解,现向一定量的H2O2溶液中滴入几滴一定溶质质量分数的FeCl3溶液,充分反应(忽略水的挥发)。下列图像正确的是( )
【错解】选D
【析错】向一定量的H2O2溶液中滴入几滴一定溶质质量分数的FeCl3溶液,过氧化氢完全反应后,氧气质量不再变化;过氧化氢分解为氧气和水,溶剂质量增加,完全反应后,溶剂质量不再变化;过氧化氢分解为氧气和水,过氧化氢的质量分数减小,完全反应后,过氧化氢的质量为0,质量分数为0;FeCl3是催化剂,反应前后质量不变,过氧化氢分解为氧气和水,溶液质量减小,FeCl3的质量分数变大。
【正解】选B
A.固体中氧元素的质量
B.生成O2的质量
C.固体中MnO2的质量
D.固体中钾元素的质量分数
A
氧气的制取和性质研究
1.教材实验原理图
2.实验原理
3.实验结论
(1)结论一:木炭在氧气中能剧烈燃烧,发出白光。
(2)结论二:铝箔在氧气中能剧烈燃烧,发出耀眼的白光,放出大量的热,生成白色粉末状固体。
4.实验关键点
(1)实验仪器及操作注意事项
酒精灯:实验开始时,先点燃酒精灯,再收集氧气;集中加热前要预热试管;实验结束时,先将导管移出水面,再熄灭酒精灯。
集气瓶:待导管口连续、均匀冒气泡后,再收集气体。
试管:试管口加棉花,试管口略向下倾斜。
导管:导管口只能在集气瓶口处。
(2)遇到问题的处理方法
a.试管口未塞棉花,导致导管口被高锰酸钾粉末堵住。应重新做实验。
b.试管口未略向下倾斜,导致冷凝水倒流,使试管破裂。应重新做实验。
5.实验拓展
(1)将氧气的制取,与可燃物燃烧的条件相结合的综合题型。
(2)将氧气的制取和应用,与二氧化碳和氢气的制取和应用相结合的综合题型。
(3)探究氧气制取过程中影响氧气制取速率的因素。
典例 [2018·衢州]小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
(1)小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星的木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到______________________________________ _____为氧气集满的标准。
当气泡从瓶口冒出时(或观察到瓶中水排尽
时)
收集方法 向上排空气法 排水法
氧气浓度(%) 79.6 79.7 79.9 90.0 89.8 89.3
氧气平均浓度(%) 79.7 89.7
(2)以上两种方法中,________法收集到的氧气更纯净。
(3)向上排空气法收集到的氧气浓度只有80%左右的原因有________。
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星的木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
排水
ACD
同课章节目录
