浙江省中考科学(化学部分)第二篇主题2第一单元构成物质的微粒、元素(课件 43张ppt)
文档属性
| 名称 | 浙江省中考科学(化学部分)第二篇主题2第一单元构成物质的微粒、元素(课件 43张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-03-10 00:00:00 | ||
图片预览










文档简介
第一单元 构成物质的微粒、元素
主题2 物质的结构
1.[2017·萧山模拟]微粒是构成化学物质的基础,下列对微粒的描述正确的是 ( )
A.仅由碳原子构成的物质属于纯净物
B.原子中一定含有质子、中子、电子
C.NaCl是由离子构成的,所以HCl也是由离子构成的
D.氯原子和氯离子的核电荷数一定相等
D
2.[2017·天水改编]硼氢化钠(NaBH4,其中氢元素的化合价为-1)是一种安全车载氢源。有关硼氢化钠的说法正确的是 ( )
A.硼元素的化合价为+3
B.只含一种非金属元素
C.硼氢化钠由一个钠元素、一个硼元素和四个氢元素组成
D.含2个氢分子
A
3.[绵阳中考]把磨得很光滑的铅片和金片紧压在一起,在室温下放置5年后再将它们切开,可以看到它们相互渗入约1mm深。这个现象说明 ( )
A.固体分子在不停地运动
B.温度越高,固体分子运动越剧烈
C.固体分子之间存在着引力和斥力
D.固体分子之间只有引力,没有斥力
A
4.[2017·金华期末]如图为原子结构模型的演变图,其中①为道尔顿原子模型,④为近代量子力学原子模型。下列排列符合历史演变顺序的一组是 ( )
A.①③②⑤④ B.①②③④⑤
C.①⑤③②④ D.①③⑤④②
A
【解析】 ①19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。③1897年,英国科学家汤姆生发现了电子,1904年提出“葡萄干面包式的”原子结构模型。②1911年英国物理学家卢瑟福(汤姆生的学生)提出了带核的原子结构模型。⑤1913年丹麦物理学家波尔(卢瑟福学生)引入量子论观点,提出电子在一定轨道上运动的原子结构模型。④奥地利物理学家薛定谔提出电子云模型(几率说),为近代量子力学原子模型(图中为氢原子电子云模型)。
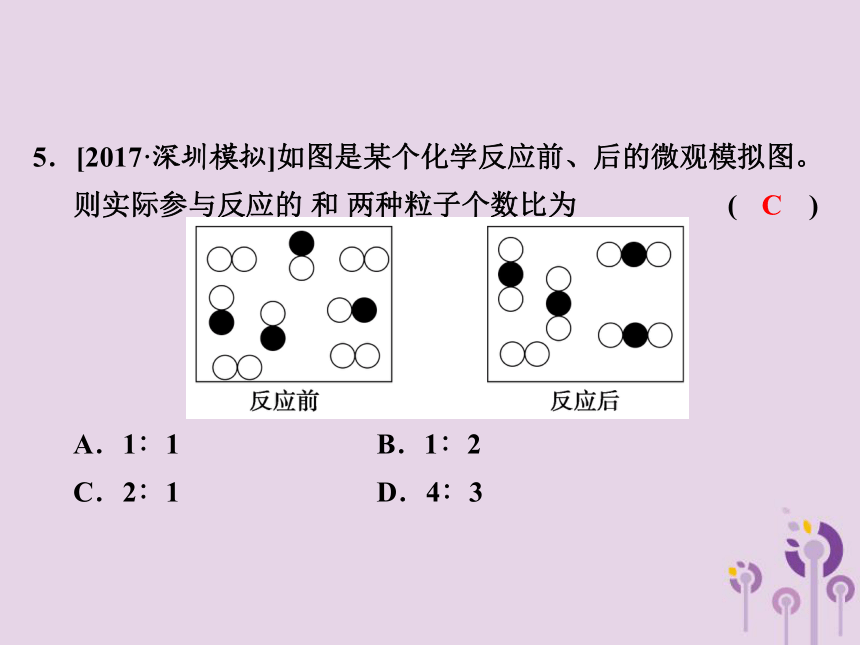
5.[2017·深圳模拟]如图是某个化学反应前、后的微观模拟图。则实际参与反应的 和 两种粒子个数比为 ( )
A.1∶1 B.1∶2
C.2∶1 D.4∶3
C
6.[2017·杭州]2017年5月,中科院、国家语委和全国科技名词委正式定 名118号元素为“ ”,其部分信息如图所示。则下列有关的说法正确的是 ( )
A.元素符号为Og
B.相对原子质量为118
C.原子的核电荷数为179
D.原子的核外电子数为297
7.[2017·温州改编]构成人体骨骼和牙齿的无机盐称为骨盐,其中含有氟化钙,已知氟化钙中氟(F)元素的化合价为-1价,则氟化钙的化学式为________。
A
CaF2
8.[2018·佛山顺德区模拟]某复合肥的部分说明书如图所示。请回答:
(1)从肥效的角度看,共有有效
元素_____种。
(2)该复合肥的有效成分之一是硫
酸铵[(NH4)2SO4],则其中氮元素
的化合价为_________。
3
-3价
一、物质的构成
考点1 说出构成物质的三种微粒(a)
1.构成物质的微粒有____________________。由分子构成的物质中________是保持物质化学性质的最小微粒;________是化学变化中的最小微粒;________是得失电子的原子或原子团。
2.分子的特性
(1)分子是构成物质的一种极其微小的粒子。
(2)固体、液体和气体的分子之间都___________。
分子、原子和离子
分子
原子
离子
存在空隙
(3)分子不停地做无规则运动,物体的温度越高,分子的无规则运动越剧烈,这种运动叫__________。
(4)物质由大量做无规则运动的分子构成,分子之间存在着相互作用的______________。分子间的引力不仅存在于物体内部,而且存在于___________________。分子间的斥力使物体内部的分子保持一定的距离。
考点2 了解分子、原子和离子微粒的大小数量级(a)
原子半径一般在10-10米数量级,分子质量的数量级约为10-26千克。
热运动
引力和斥力
两个物体的接触面
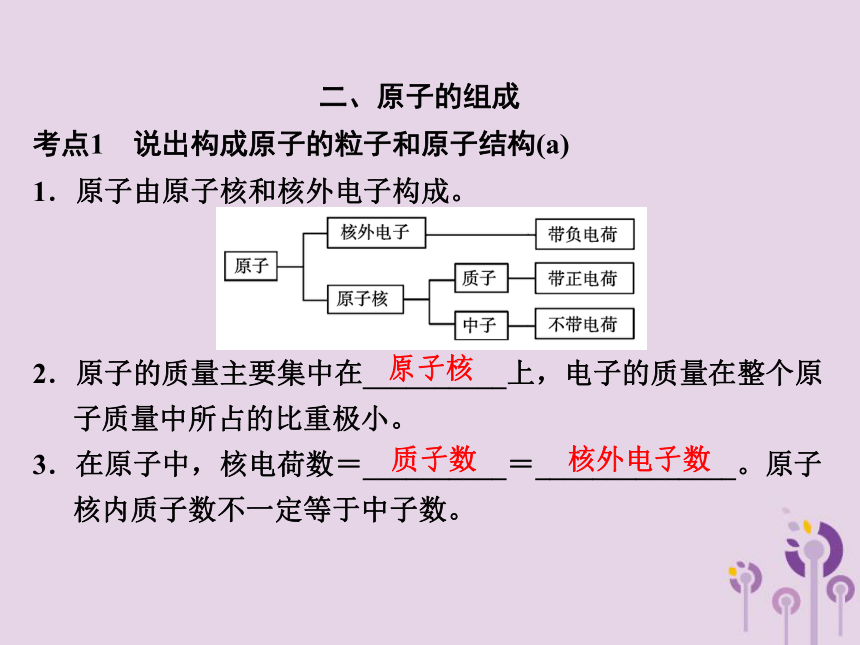
二、原子的组成
考点1 说出构成原子的粒子和原子结构(a)
1.原子由原子核和核外电子构成。
2.原子的质量主要集中在__________上,电子的质量在整个原子质量中所占的比重极小。
3.在原子中,核电荷数=__________=______________。原子核内质子数不一定等于中子数。
原子核
质子数
核外电子数
考点2 说出质子、中子由夸克构成(a)
原子核由质子和中子构成,质子和中子都由更微小的基本粒子——________构成。
夸克
三、原子结构模型的发展过程
考点1 了解原子结构模型在历史上的发展过程(a)
原子结构模型建立的过程
(1)道尔顿——实心球模型——首先提出原子论。
(2)汤姆生——葡萄干面包模型(枣糕模型)——发现电子。
(3)卢瑟福——核式结构模型——α粒子散射实验、提出了原子核。
(4)玻尔——分层模型。
(5)现代——电子云模型。
考点2 会识读、建立简单模型(a)
考点3 体验建立模型的思想方法(a)
从原子结构模型建立的过程中,我们可以发现建立模型往往需要一个____________、____________的过程,使模型更接近事物的本质。
不断完善
不断修正
四、物质由元素组成
考点1 说出具体物质的元素组成(a)
1.元素是具有相同______________________的一类原子的总称。
2.元素与原子的区别和联系
核电荷数(即质子数)
相同核电荷数
元素 原子
含义 具有________________(即质子数)的一类原子的总称(抽象的宏观概念) 化学变化中的最小微粒(具体的微观粒子)
区别 只讲种类,不讲个数。如不能说水由两个氢元素和一个氧元素组成 既讲种类,又讲个数。如每个水分子由两个氢原子和一个氧原子构成
宏观
微观
总体和个体
一类
适用范围 用于描述物质的________组成。如水是由氢、氧两种元素组成的 用于描述分子或某些物质粒子的________结构。如水分子是由氢原子和氧原子构成的
联系 元素和原子是______________的关系,元素是________原子的总称
考点2 根据物质的组成元素区别单质和化合物(b)
单质和化合物的区别:组成元素是一种还是多种。
同种元素
不同种元素
同种原子
不同种原子
单质 化合物
宏观组成 ____________ ______________
微观构成 由___________构成的分子 由______________构成的同一种分子
化学性质 不能发生分解反应 一定条件下可以发生分解反应
五、知道组成人体的主要元素(H、O、C、N),重要化学肥料的
有效元素(N、P、K)
考点1 说出组成人体的主要元素(a)
人体内大约含有30多种元素,其中11种为大量元素(碳、氢、氧、氮、硫、磷、氯、钙、镁、钠、钾),约占99.95%,其余为微量元素。
考点2 列举植物所需要的常见的几种有效元素,描述它们与植物生长的关系(a)
化肥中的有效元素:植物生长过程中需要量较多的是含氮、磷、钾元素的无机盐。植物生长缺乏______元素时,植物矮小,叶色发黄;缺乏______元素时,根弱,植物暗绿带红;缺乏______元素时,植株矮小,茎不粗壮,易倒伏,叶片上带有许多褐斑。
缺乏______元素时,植株矮小,茎不粗壮,易倒伏,叶片上带有许多褐斑。
氮
磷
记忆卡片
氮叶、钾茎、磷促生,不同盐类功能不同。
氮黄红磷褐钾。
钾
六、元素符号
考点1 书写常见元素的符号(H、O、C、N、S、Si、P、I、
Na、Mg、Al、K、Ca、Cl、Fe、Cu、Ag)(b)
元素符号的表示方法
用该元素的拉丁文的第一个大写字母来表示,若有重复则取前两个字母,第二个字母小写。
在元素周期表中,每一种元素占有一个格,每一个格子均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容。如图所示。
考点3 说明元素符号所表示的几种含义(b)
元素符号表示的意义
(1)宏观上表示一种________,如元素符号“N”可以表示氮元素。
(2)微观上表示该元素的一个________,如元素符号“N”也可以表示一个氮原子。
(3)如果物质是由原子直接构成的,则元素符号还能表示一种________,如元素符号“Fe”既可以表示铁元素,又可以表示一个铁原子,还可以表示铁这种物质。
【注意】 元素不讲个数,只讲种类,如果元素符号前面加上数字,则只能表示一个意义,即该元素的原子个数。如“3N”只能表示3个氮原子,不能表示氮元素。
元素
原子
物质
七、同位素
原子核内有质子和中子,质子数决定元素的种类,同一种元素的原子核内的中子数不一定相同,具有不同__________的同种元素互为同位素。
中子数
八、元素周期表
考点 初步了解元素周期表(不要求记忆周期数和族数)(a)
1.元素周期表中的信息
2.元素周期表中,金属元素位于元素周期表的左下方;非金属元素位于元素周期表的右上方。
九、元素的化合价
考点1 说出常见元素的化合价(a)
考点2 用化合价写出简单的化学式(b)
考点3 根据化学式推断元素的化合价(c)
1.在常见的化合物中,氧显“-2”价,氢显“+1”价。
2.在化合物中,金属元素__________;非金属元素跟氧化合时____________,跟氢化合时显________。
3.单质中元素的化合价为______;在化合物中,元素正负化合价的__________为零。
显正价
常显正价
负价
零
代数和
化合价口诀
一价钾钠氯氢银,二价氧钙钡镁锌;
三铝四硅五价磷,铜一二铁二三;
原子团也要记清,氢氧负一铵正一;
酸根所有价为负,一硝二硫碳三磷。
记忆卡片
4.化合价的应用:应用化合价检验和书写已知物质的化学式;应用化合价检验和书写离子符号(化合价与离子所带电荷数在数值上相等)。
类型一 原子结构模型
典例 [2017·绥化三模]如图为某原子结构模型
的示意图,其中a、b、c是构成该原子的
三种不同粒子,下列说法正确的是( )
A.决定该原子种类的粒子是b
B.原子中b与c的数目一定相同
C.原子的质量集中在a和c上
D.原子中a与c的数目一定相同
D
跟踪训练 [2017·新泰期末]原子结构模型的建立,经过了几代科学家的艰辛努力,直到现在仍在探索中。如图是锂原子结构的行星模型,图中原子核内有3个质子、4个中子。不能根据原子结构的行星模型得出的结论是 ( )
A
A.原子始终在做无规则的运动
B.原子核的体积只占整个原子体积的很小部分
C.构成原子核的粒子之间存在一种互相吸引的力
D.原子呈电中性
【解析】 根据锂原子结构的行星模型图可以看出原子核的体积占原子的体积很小,原子核是由质子和中子构成的,质子带正电,中子不带电;原子核上的正电荷和电子所带的负电荷相等,整个原子对外不显电性;但是看不出原子始终在做无规则运动,而是电子绕原子核沿一定轨道运动。
类型二 化学符号及周围数字的意义
典例 [丹东中考改编]下列化学用语关于“3”的意义,说法正确的是 ( )
①3Hg ②Fe3+ ③SO3 ④2O3 ⑤3O2- ⑥3CH4
A.表示分子个数的是①
B.表示离子所带电荷数的是②⑤
C.表示离子个数的是⑤
D.表示一个分子中原子个数的是③⑥
C
跟踪训练 [2018·玉林]C60的发现使人类了解到一个全新的碳世界,下列说法正确的是 ( )
A.足球由C60构成
B.C60这种物质由碳原子直接构成
C.C60是一种新型化合物
D.C60在氧气中完全燃烧生成CO2
D
类型三 物质的组成
典例 [2017·自贡]每100g黑木耳中含铁185mg,是常见天然食品中最高的,这里的“铁”应理解为 ( )
A.分子 B.原子
C.离子 D.元素
D
跟踪训练 [2019·预测]臭氧(O3)、二氧化氯(ClO2)、双氧水(H2O2)等都是生产、生活中常用的消毒剂,三种物质的分子中都含有 ( )
A.氧分子 B.氧离子
C.氧原子 D.氧元素
【点悟】 物质由元素组成;分子由原子构成。
C
类型四 化合价的相关计算
典例 [2017·株洲]下列含氯化合物中,氯元素的化合价最高的是 ( )
A.KClO3 B.NaCl
C.Ca(ClO)2 D.HClO4
D
跟踪训练 [2017·雅安]含磷的洗涤剂因含有Na5P3O10造成水生植物大量繁殖而污染环境,因此我们提倡使用无磷洗涤剂。下列化合价在Na5P3O10中没有出现的是 ( )
A.-2 B.+1
C.+4 D.+5
【解析】 钠元素显+1价,氧元素显-2价,设磷元素的化合价是x,根据化合物中正负化合价代数和为零可得:(+1)×5+3x+(-2)×10=0,则x=+5。
C
对粒子概念理解不清致错
典例 [南宁中考]下列关于分子和原子的说法,错误的是( )
A.分子和原子都可以构成物质
B.由分子构成的物质,分子是保持其化学性质的最小粒子
C.在化学变化中,分子可以分成原子,原子又可以结合成 新的分子
D.分子和原子之间都有空隙,分子之间空隙较大,原子之 间空隙较小
【错解】选B
【析错】误以为保持物质的化学性质的最小粒子为原子;误以为原子组成分子,所以分子间空隙大。
【正解】选D
跟踪训练 [2018·呼和浩特]下列对客观事实的解释正确的是 ( )
B
选项 事实 解释
A Fe、Fe2+、Fe3+化学性质不同 微粒中的质子数不同
B 水通电产生氢气和氧气 在化学变化中分子可分,原子不可分
C 稀盐酸、稀硫酸均显酸性 溶液中都含有氢元素
D 冰水混合物属于纯净物 冰和水都含有相同的原子
【解析】 Fe、Fe2+、Fe3+化学性质不同,是因为微粒中所含电子数不同;水在通电条件下生成氢气和氧气,有新物质氢气、氧气生成,属于化学变化,能证明分子在化学反应中可以再分,原子不能再分;稀盐酸、稀硫酸均显酸性,是因为溶液中都含有氢离子;冰水混合物属于纯净物,是因为冰和水都含有相同的分子。
微观粒子模型在化学中的应用
1.微粒观点的应用
从物质的微粒性角度来分析解决实际问题。即运用分子、原子或离子等微观粒子的知识来分析解释实际问题。
2.模型图的应用
是指把看不见的、抽象的微观粒子,用能够看到的模型图的形式形象展现出来,以便用来解释抽象的概念、化学反应或实际问题等。
3.微观粒子模型在化学中的应用
命题方向主要是通过创设相关问题情境或图表信息等,来考查学生对微粒观点及模型图的应用的理解和掌握情况,以及考查阅读、分析、推断能力和对知识的迁移能力。此类试题提高了试题的趣味性和可读性。并且,经常将其与物质的组成和构成、物质的分类和类别辨析、分子和原子的辨析、化学式和化学方程式的书写、化学反应类型、质量守恒定律等相关知识联系起来,进行综合考查。
典例 在宏观、微观和符号之间建立联系,是化学学科的特点,如图是某化学反应的微观过程示意图(“○”表示氧原子,“●”表示氢原子)。
(1)从宏观角度看,物质C属于__________(选填“混合物”或“纯净物”)。
混合物
(2)以上变化的基本反应类型是____________。
(3)从微观角度看,物质B是由________(选填“分子”“原子”或“离子”)构成的。
(4)参加反应的A与B的微粒个数比为________。
化合反应
分子
2∶1
主题2 物质的结构
1.[2017·萧山模拟]微粒是构成化学物质的基础,下列对微粒的描述正确的是 ( )
A.仅由碳原子构成的物质属于纯净物
B.原子中一定含有质子、中子、电子
C.NaCl是由离子构成的,所以HCl也是由离子构成的
D.氯原子和氯离子的核电荷数一定相等
D
2.[2017·天水改编]硼氢化钠(NaBH4,其中氢元素的化合价为-1)是一种安全车载氢源。有关硼氢化钠的说法正确的是 ( )
A.硼元素的化合价为+3
B.只含一种非金属元素
C.硼氢化钠由一个钠元素、一个硼元素和四个氢元素组成
D.含2个氢分子
A
3.[绵阳中考]把磨得很光滑的铅片和金片紧压在一起,在室温下放置5年后再将它们切开,可以看到它们相互渗入约1mm深。这个现象说明 ( )
A.固体分子在不停地运动
B.温度越高,固体分子运动越剧烈
C.固体分子之间存在着引力和斥力
D.固体分子之间只有引力,没有斥力
A
4.[2017·金华期末]如图为原子结构模型的演变图,其中①为道尔顿原子模型,④为近代量子力学原子模型。下列排列符合历史演变顺序的一组是 ( )
A.①③②⑤④ B.①②③④⑤
C.①⑤③②④ D.①③⑤④②
A
【解析】 ①19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。③1897年,英国科学家汤姆生发现了电子,1904年提出“葡萄干面包式的”原子结构模型。②1911年英国物理学家卢瑟福(汤姆生的学生)提出了带核的原子结构模型。⑤1913年丹麦物理学家波尔(卢瑟福学生)引入量子论观点,提出电子在一定轨道上运动的原子结构模型。④奥地利物理学家薛定谔提出电子云模型(几率说),为近代量子力学原子模型(图中为氢原子电子云模型)。
5.[2017·深圳模拟]如图是某个化学反应前、后的微观模拟图。则实际参与反应的 和 两种粒子个数比为 ( )
A.1∶1 B.1∶2
C.2∶1 D.4∶3
C
6.[2017·杭州]2017年5月,中科院、国家语委和全国科技名词委正式定 名118号元素为“ ”,其部分信息如图所示。则下列有关的说法正确的是 ( )
A.元素符号为Og
B.相对原子质量为118
C.原子的核电荷数为179
D.原子的核外电子数为297
7.[2017·温州改编]构成人体骨骼和牙齿的无机盐称为骨盐,其中含有氟化钙,已知氟化钙中氟(F)元素的化合价为-1价,则氟化钙的化学式为________。
A
CaF2
8.[2018·佛山顺德区模拟]某复合肥的部分说明书如图所示。请回答:
(1)从肥效的角度看,共有有效
元素_____种。
(2)该复合肥的有效成分之一是硫
酸铵[(NH4)2SO4],则其中氮元素
的化合价为_________。
3
-3价
一、物质的构成
考点1 说出构成物质的三种微粒(a)
1.构成物质的微粒有____________________。由分子构成的物质中________是保持物质化学性质的最小微粒;________是化学变化中的最小微粒;________是得失电子的原子或原子团。
2.分子的特性
(1)分子是构成物质的一种极其微小的粒子。
(2)固体、液体和气体的分子之间都___________。
分子、原子和离子
分子
原子
离子
存在空隙
(3)分子不停地做无规则运动,物体的温度越高,分子的无规则运动越剧烈,这种运动叫__________。
(4)物质由大量做无规则运动的分子构成,分子之间存在着相互作用的______________。分子间的引力不仅存在于物体内部,而且存在于___________________。分子间的斥力使物体内部的分子保持一定的距离。
考点2 了解分子、原子和离子微粒的大小数量级(a)
原子半径一般在10-10米数量级,分子质量的数量级约为10-26千克。
热运动
引力和斥力
两个物体的接触面
二、原子的组成
考点1 说出构成原子的粒子和原子结构(a)
1.原子由原子核和核外电子构成。
2.原子的质量主要集中在__________上,电子的质量在整个原子质量中所占的比重极小。
3.在原子中,核电荷数=__________=______________。原子核内质子数不一定等于中子数。
原子核
质子数
核外电子数
考点2 说出质子、中子由夸克构成(a)
原子核由质子和中子构成,质子和中子都由更微小的基本粒子——________构成。
夸克
三、原子结构模型的发展过程
考点1 了解原子结构模型在历史上的发展过程(a)
原子结构模型建立的过程
(1)道尔顿——实心球模型——首先提出原子论。
(2)汤姆生——葡萄干面包模型(枣糕模型)——发现电子。
(3)卢瑟福——核式结构模型——α粒子散射实验、提出了原子核。
(4)玻尔——分层模型。
(5)现代——电子云模型。
考点2 会识读、建立简单模型(a)
考点3 体验建立模型的思想方法(a)
从原子结构模型建立的过程中,我们可以发现建立模型往往需要一个____________、____________的过程,使模型更接近事物的本质。
不断完善
不断修正
四、物质由元素组成
考点1 说出具体物质的元素组成(a)
1.元素是具有相同______________________的一类原子的总称。
2.元素与原子的区别和联系
核电荷数(即质子数)
相同核电荷数
元素 原子
含义 具有________________(即质子数)的一类原子的总称(抽象的宏观概念) 化学变化中的最小微粒(具体的微观粒子)
区别 只讲种类,不讲个数。如不能说水由两个氢元素和一个氧元素组成 既讲种类,又讲个数。如每个水分子由两个氢原子和一个氧原子构成
宏观
微观
总体和个体
一类
适用范围 用于描述物质的________组成。如水是由氢、氧两种元素组成的 用于描述分子或某些物质粒子的________结构。如水分子是由氢原子和氧原子构成的
联系 元素和原子是______________的关系,元素是________原子的总称
考点2 根据物质的组成元素区别单质和化合物(b)
单质和化合物的区别:组成元素是一种还是多种。
同种元素
不同种元素
同种原子
不同种原子
单质 化合物
宏观组成 ____________ ______________
微观构成 由___________构成的分子 由______________构成的同一种分子
化学性质 不能发生分解反应 一定条件下可以发生分解反应
五、知道组成人体的主要元素(H、O、C、N),重要化学肥料的
有效元素(N、P、K)
考点1 说出组成人体的主要元素(a)
人体内大约含有30多种元素,其中11种为大量元素(碳、氢、氧、氮、硫、磷、氯、钙、镁、钠、钾),约占99.95%,其余为微量元素。
考点2 列举植物所需要的常见的几种有效元素,描述它们与植物生长的关系(a)
化肥中的有效元素:植物生长过程中需要量较多的是含氮、磷、钾元素的无机盐。植物生长缺乏______元素时,植物矮小,叶色发黄;缺乏______元素时,根弱,植物暗绿带红;缺乏______元素时,植株矮小,茎不粗壮,易倒伏,叶片上带有许多褐斑。
缺乏______元素时,植株矮小,茎不粗壮,易倒伏,叶片上带有许多褐斑。
氮
磷
记忆卡片
氮叶、钾茎、磷促生,不同盐类功能不同。
氮黄红磷褐钾。
钾
六、元素符号
考点1 书写常见元素的符号(H、O、C、N、S、Si、P、I、
Na、Mg、Al、K、Ca、Cl、Fe、Cu、Ag)(b)
元素符号的表示方法
用该元素的拉丁文的第一个大写字母来表示,若有重复则取前两个字母,第二个字母小写。
在元素周期表中,每一种元素占有一个格,每一个格子均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容。如图所示。
考点3 说明元素符号所表示的几种含义(b)
元素符号表示的意义
(1)宏观上表示一种________,如元素符号“N”可以表示氮元素。
(2)微观上表示该元素的一个________,如元素符号“N”也可以表示一个氮原子。
(3)如果物质是由原子直接构成的,则元素符号还能表示一种________,如元素符号“Fe”既可以表示铁元素,又可以表示一个铁原子,还可以表示铁这种物质。
【注意】 元素不讲个数,只讲种类,如果元素符号前面加上数字,则只能表示一个意义,即该元素的原子个数。如“3N”只能表示3个氮原子,不能表示氮元素。
元素
原子
物质
七、同位素
原子核内有质子和中子,质子数决定元素的种类,同一种元素的原子核内的中子数不一定相同,具有不同__________的同种元素互为同位素。
中子数
八、元素周期表
考点 初步了解元素周期表(不要求记忆周期数和族数)(a)
1.元素周期表中的信息
2.元素周期表中,金属元素位于元素周期表的左下方;非金属元素位于元素周期表的右上方。
九、元素的化合价
考点1 说出常见元素的化合价(a)
考点2 用化合价写出简单的化学式(b)
考点3 根据化学式推断元素的化合价(c)
1.在常见的化合物中,氧显“-2”价,氢显“+1”价。
2.在化合物中,金属元素__________;非金属元素跟氧化合时____________,跟氢化合时显________。
3.单质中元素的化合价为______;在化合物中,元素正负化合价的__________为零。
显正价
常显正价
负价
零
代数和
化合价口诀
一价钾钠氯氢银,二价氧钙钡镁锌;
三铝四硅五价磷,铜一二铁二三;
原子团也要记清,氢氧负一铵正一;
酸根所有价为负,一硝二硫碳三磷。
记忆卡片
4.化合价的应用:应用化合价检验和书写已知物质的化学式;应用化合价检验和书写离子符号(化合价与离子所带电荷数在数值上相等)。
类型一 原子结构模型
典例 [2017·绥化三模]如图为某原子结构模型
的示意图,其中a、b、c是构成该原子的
三种不同粒子,下列说法正确的是( )
A.决定该原子种类的粒子是b
B.原子中b与c的数目一定相同
C.原子的质量集中在a和c上
D.原子中a与c的数目一定相同
D
跟踪训练 [2017·新泰期末]原子结构模型的建立,经过了几代科学家的艰辛努力,直到现在仍在探索中。如图是锂原子结构的行星模型,图中原子核内有3个质子、4个中子。不能根据原子结构的行星模型得出的结论是 ( )
A
A.原子始终在做无规则的运动
B.原子核的体积只占整个原子体积的很小部分
C.构成原子核的粒子之间存在一种互相吸引的力
D.原子呈电中性
【解析】 根据锂原子结构的行星模型图可以看出原子核的体积占原子的体积很小,原子核是由质子和中子构成的,质子带正电,中子不带电;原子核上的正电荷和电子所带的负电荷相等,整个原子对外不显电性;但是看不出原子始终在做无规则运动,而是电子绕原子核沿一定轨道运动。
类型二 化学符号及周围数字的意义
典例 [丹东中考改编]下列化学用语关于“3”的意义,说法正确的是 ( )
①3Hg ②Fe3+ ③SO3 ④2O3 ⑤3O2- ⑥3CH4
A.表示分子个数的是①
B.表示离子所带电荷数的是②⑤
C.表示离子个数的是⑤
D.表示一个分子中原子个数的是③⑥
C
跟踪训练 [2018·玉林]C60的发现使人类了解到一个全新的碳世界,下列说法正确的是 ( )
A.足球由C60构成
B.C60这种物质由碳原子直接构成
C.C60是一种新型化合物
D.C60在氧气中完全燃烧生成CO2
D
类型三 物质的组成
典例 [2017·自贡]每100g黑木耳中含铁185mg,是常见天然食品中最高的,这里的“铁”应理解为 ( )
A.分子 B.原子
C.离子 D.元素
D
跟踪训练 [2019·预测]臭氧(O3)、二氧化氯(ClO2)、双氧水(H2O2)等都是生产、生活中常用的消毒剂,三种物质的分子中都含有 ( )
A.氧分子 B.氧离子
C.氧原子 D.氧元素
【点悟】 物质由元素组成;分子由原子构成。
C
类型四 化合价的相关计算
典例 [2017·株洲]下列含氯化合物中,氯元素的化合价最高的是 ( )
A.KClO3 B.NaCl
C.Ca(ClO)2 D.HClO4
D
跟踪训练 [2017·雅安]含磷的洗涤剂因含有Na5P3O10造成水生植物大量繁殖而污染环境,因此我们提倡使用无磷洗涤剂。下列化合价在Na5P3O10中没有出现的是 ( )
A.-2 B.+1
C.+4 D.+5
【解析】 钠元素显+1价,氧元素显-2价,设磷元素的化合价是x,根据化合物中正负化合价代数和为零可得:(+1)×5+3x+(-2)×10=0,则x=+5。
C
对粒子概念理解不清致错
典例 [南宁中考]下列关于分子和原子的说法,错误的是( )
A.分子和原子都可以构成物质
B.由分子构成的物质,分子是保持其化学性质的最小粒子
C.在化学变化中,分子可以分成原子,原子又可以结合成 新的分子
D.分子和原子之间都有空隙,分子之间空隙较大,原子之 间空隙较小
【错解】选B
【析错】误以为保持物质的化学性质的最小粒子为原子;误以为原子组成分子,所以分子间空隙大。
【正解】选D
跟踪训练 [2018·呼和浩特]下列对客观事实的解释正确的是 ( )
B
选项 事实 解释
A Fe、Fe2+、Fe3+化学性质不同 微粒中的质子数不同
B 水通电产生氢气和氧气 在化学变化中分子可分,原子不可分
C 稀盐酸、稀硫酸均显酸性 溶液中都含有氢元素
D 冰水混合物属于纯净物 冰和水都含有相同的原子
【解析】 Fe、Fe2+、Fe3+化学性质不同,是因为微粒中所含电子数不同;水在通电条件下生成氢气和氧气,有新物质氢气、氧气生成,属于化学变化,能证明分子在化学反应中可以再分,原子不能再分;稀盐酸、稀硫酸均显酸性,是因为溶液中都含有氢离子;冰水混合物属于纯净物,是因为冰和水都含有相同的分子。
微观粒子模型在化学中的应用
1.微粒观点的应用
从物质的微粒性角度来分析解决实际问题。即运用分子、原子或离子等微观粒子的知识来分析解释实际问题。
2.模型图的应用
是指把看不见的、抽象的微观粒子,用能够看到的模型图的形式形象展现出来,以便用来解释抽象的概念、化学反应或实际问题等。
3.微观粒子模型在化学中的应用
命题方向主要是通过创设相关问题情境或图表信息等,来考查学生对微粒观点及模型图的应用的理解和掌握情况,以及考查阅读、分析、推断能力和对知识的迁移能力。此类试题提高了试题的趣味性和可读性。并且,经常将其与物质的组成和构成、物质的分类和类别辨析、分子和原子的辨析、化学式和化学方程式的书写、化学反应类型、质量守恒定律等相关知识联系起来,进行综合考查。
典例 在宏观、微观和符号之间建立联系,是化学学科的特点,如图是某化学反应的微观过程示意图(“○”表示氧原子,“●”表示氢原子)。
(1)从宏观角度看,物质C属于__________(选填“混合物”或“纯净物”)。
混合物
(2)以上变化的基本反应类型是____________。
(3)从微观角度看,物质B是由________(选填“分子”“原子”或“离子”)构成的。
(4)参加反应的A与B的微粒个数比为________。
化合反应
分子
2∶1
同课章节目录
