第四单元 第二节 物质组成表示(同步提优学案)
文档属性
| 名称 | 第四单元 第二节 物质组成表示(同步提优学案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-03-12 00:00:00 | ||
图片预览




文档简介
第二节 物质组成的表示
学习目标
中考考点关注
1、正确书写常见物质的化学式,并能读出化学式,说出化学式表示的意义(重点)
2、熟知常见元素常见的化合价,能依据化合价写出物质的化学式,会计算化合物中某元的化合价(重点、难点)
3、能根据化学式进行简单的计算(重点)
1、化学式及其意义(必考点)
2、化合价(常考点)
3、化学式的写法(必考点)
4、化合物的读法(必考点)
5、有关化学式的计算(常考点)
教材知识精析
知识点1、化学式及其意义(重点)
1.化学式的定义
用元素符号和数字的组合表示物质组成的式子。每种纯净物只有一个化学式。
2、物质的组成与化学式的关系
3.化学式的意义
Ⅰ、由分子构成的物质
化学式的意义
以“ H2O ”为例
宏观
表示一种物质
表示水
表示该物质的元素组成
表示水由氢元素和氧元素组成
微观
表示该物质一个分子
表示一个水分子
表示该物质的分子构成
表示一个水分子由2个氢原子和1个氧原子构成的
Ⅱ、由原子构成的物质
化学式的意义
以“ Cu ” 为例
宏观
表示某物质
表示铜这种物质
表示该物质的组成元素
表示金属铜由铜元素元素组成
微观
表示该物质的一个原子
表示1个铜原子
Ⅲ、由离子构成的物质
化学式的意义
以“ MgCl2 ”为例
宏观
表示氯化镁这种物质
表示该物质的元素组成
表示氯化钠由镁元素和氯元素组成
微观
表示离子的个数比
表示氯化镁中氯离子和镁离子的个数比为1:2
☆尖子生笔记☆
【拓展延伸】
1、关于化学式
①任何纯净物都可以用化学式表示。
②对由分子构成的物质,用分子式作为化学式,化学式中元素符号右下角的数字为一个分子中原子的个数;由原子构成的物质用元素符号作为化学式;由离子构成的物质,在元素符号右下角标出离子个数比。
③各种物质的化学式都是通过实验测定的,一种物质只有一个化学式。
④化学式前边的数字为分子的个数,此时,只有微观意义。如:2CO:表示两个一氧化碳分子。
知识点2、化合价(重点、难点)
1、化合价概念
化合物中,不同元素的原子(离子)总以一定的个数比相互结合的性质,叫元素的化合价。
2、化合价的确定
①由离子构成的化合物中,元素的化合价的数值就是一个原子得到或失去的电子数。正价等于失电子数;负价等于得电子数。(掌握)
②由分子构成的化合物中,化合价的数值就是一个原子与其他原子形成的共用电子对的数值。(了解)
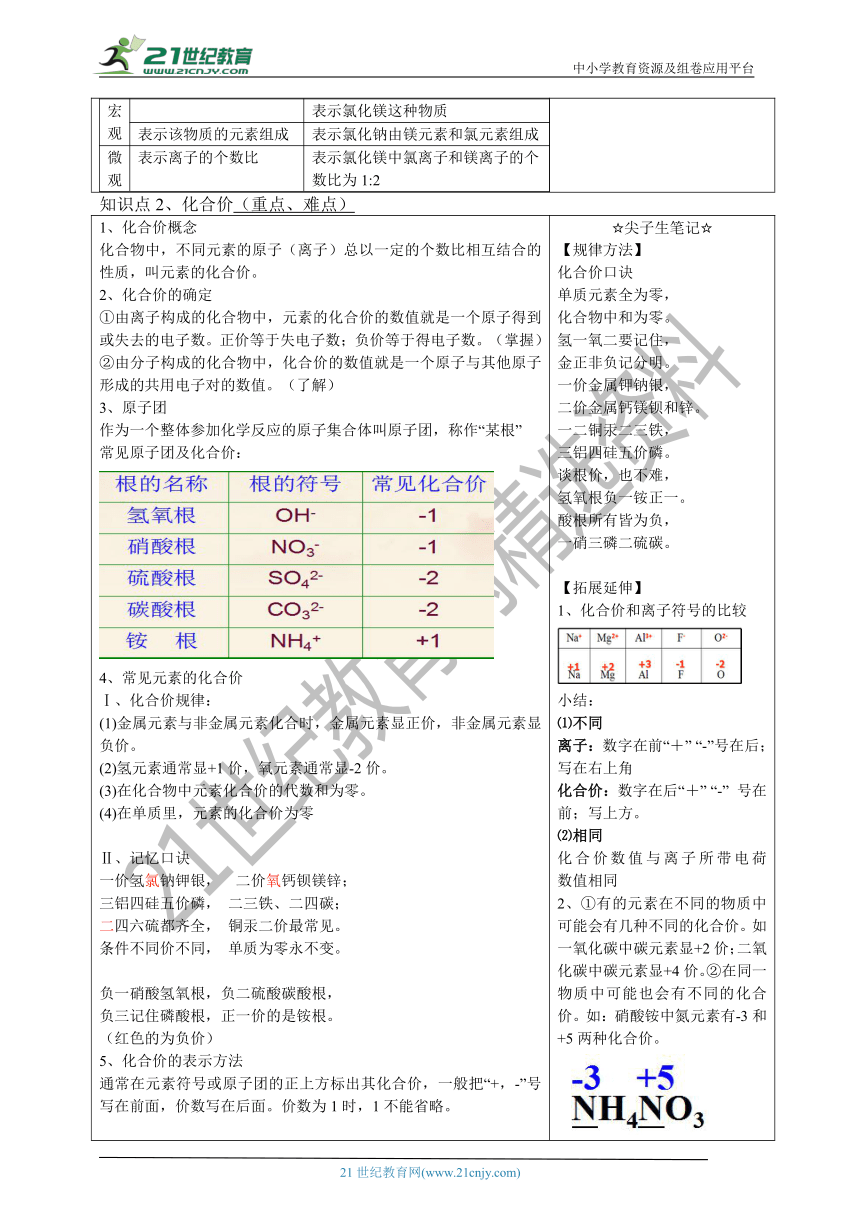
3、原子团
作为一个整体参加化学反应的原子集合体叫原子团,称作“某根”
常见原子团及化合价:
4、常见元素的化合价
Ⅰ、化合价规律:
(1)金属元素与非金属元素化合时,金属元素显正价,非金属元素显负价。
(2)氢元素通常显+1价,氧元素通常显-2价。
(3)在化合物中元素化合价的代数和为零。
(4)在单质里,元素的化合价为零
Ⅱ、记忆口诀
一价氢氯钠钾银, 二价氧钙钡镁锌;
三铝四硅五价磷, 二三铁、二四碳;
二四六硫都齐全, 铜汞二价最常见。
条件不同价不同, 单质为零永不变。
负一硝酸氢氧根,负二硫酸碳酸根,
负三记住磷酸根,正一价的是铵根。
(红色的为负价)
5、化合价的表示方法
通常在元素符号或原子团的正上方标出其化合价,一般把“+,-”号写在前面,价数写在后面。价数为1时,1不能省略。
6、数字或符号的意义
Ⅰ、符号的意义
H:氢元素 或 1个氢原子
2H:2个氢原子
H2:①氢气 ②氢气由氢元素组成 ③1个氢分子
④1个分子由2个氢原子构成
2H2:2个氢分子
2H+:2个氢离子
Ⅱ、数字的意义
“R”代表元素符号
a(左前方):表示有a个R粒子(原子、分子或离子等)
b(右下角):表示一个粒子中含有b个某原子
c(右上角):表示一个R离子带c个正(或负)电荷
d(正上方):表示(某化合物中)R元素的化合价为±d价
☆尖子生笔记☆
【规律方法】
化合价口诀
单质元素全为零,
化合物中和为零。
氢一氧二要记住,
金正非负记分明。
一价金属钾钠银,
二价金属钙镁钡和锌。
一二铜汞二三铁,
三铝四硅五价磷。
谈根价,也不难,
氢氧根负一铵正一。
酸根所有皆为负,
一硝三磷二硫碳。
【拓展延伸】
1、化合价和离子符号的比较
小结:
⑴不同
离子:数字在前“+” “-”号在后;写在右上角
化合价:数字在后“+” “-” 号在前;写上方。
⑵相同
化合价数值与离子所带电荷 数值相同
2、①有的元素在不同的物质中可能会有几种不同的化合价。如一氧化碳中碳元素显+2价;二氧化碳中碳元素显+4价。②在同一物质中可能也会有不同的化合价。如:硝酸铵中氮元素有-3和+5两种化合价。
知识点3、化学式与化合价的关系(重点、难点)
1、根据化学式求某一元素化合价
依据:化合物里正负化合价的代数和为零
例:试确定氯酸钾(KClO3)中氯元素的化合价
解:设氯元素的化合价为x,则
(+1)+ x +(-2)×3=0
x = +5
所以,在氯酸钾中,氯元素的化合价为+5价
2、根据化合价推写化学式
依据:化合物里正负化合价的代数和为零
最小公倍数法
3、单质的化学式
①由原子构成,它们的化学式用元素符号直接表示。
如:铜:Cu
②气态非金属:由分子构成,它们的化学式写法是:在元素符号的右下角写出表示一个分子中原子个数的数字。
☆尖子生笔记☆
【易错点津】
化合价计算的化合价要写明正负
【拓展延伸】
1、数字交叉法写化合物的化学式
a.写符号
b.标化合价
c.化合价绝对值交叉放置元素符号右下角
d.约简(至最简整数比)
e.检查
例:已知磷为+3价,氧为- 2价,写出磷的这种化合物的化学式。
2、判断化学式正误的方法
⑴看元素符号书写是否正确。一个字母的要大写;两个字母的,第一个大写,第二个小写。
⑵右下角的数字是否遗漏
⑶由两种元素组成,其中一种是氧的化合物,氧元素是否写在右边。
⑷有金属元素时,金属元素是否写在左边。
3、根据化合价写代数式(口诀):正写前来负在后,化合价暗暗记心头,交叉约简再写数,写完检验不要丢。
知识点4、常见化合物的读法(重点、难点)
1、由两种元素组成的化合物的读法:
通常规定从右向左读即(顺写反读),读作“某化某”、“几某化几某”
如:NaCl:读作氯化钠;CO2:读作二氧化碳
2、含有原子团的化合物,要读出原子团的名称,如CuSO4:读作硫酸铜。
3、+2价铁在化合物中读作“亚铁”;如:FeCl2:氯化亚铁
☆尖子生笔记☆
【规律方法】
知识点5、化学式的计算(重点、难点)
1、相对分子质量
定义:化学式中各原子的相对原子质量的总和,就是该物质的化学式量,对于由分子构成的物质,其化学式量也叫相对分子质量
【例1】H2O的相对分子质量=1×2+16×1=18
【例2】(NH4)2SO4的相对分子质量
=(14+1×4)×2+32+16×4=132
2.计算物质组成元素的质量比
各元素之间的质量比=各原子的相对原子质量总和之比
例:求Fe2O3中铁元素和氧元素的质量比。
Fe:O=(56×2):(16×3)=112:48=7:3
3.计算物质中某元素的质量分数
例:⑴计算二氧化硫中硫元素的质量分数
⑵计算64t二氧化硫中含硫元素的质量。
☆尖子生笔记☆
【规律方法】
1、相对分子质量的单位为1,不写,也不读。
2、计算化学式量时元素的相对原子质量与元素符号右下角的数字之间用“ⅹ”号,不同元素之间用“+”。
3、化学式原子团右下角的数字表示原子团的个数,计算时可以先求出一个原子团的式量,再乘以其个数。
【拓展延伸】
注意事项:
①质量分数——用百分数来表示
②意义:每100克物质中含有某元素的质量
解题能力突破
题型1 、元素符号及其周围数字的意义
【例1】(2017·中考)下列化学用语书写正确的是
A.两个氢分子:2H B.2个硫酸根离子:2SO4-2
C.水中氧元素的化合价为-2 价: D.两个氮原子: N2
【答案】C
【解析】
A.两个氢分子:2H2 ; 2H 表示两个氢原子; B.离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写;离子符号前加数字,表示离子的个数。2个硫酸根离子:2SO42-;C.元素化合价的书写:在元素符号的正上方标化合价的数值,正负号在左,数字在右。水中氧元素的化合价为-2 价: D.元素符号的前边加数字表示原子的个数,两个氮原子: 2N;选C
【解法归纳】熟记各种化学用语的书写、意义及周围数字的意义。
符号:①化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写;
②单质的化学式的书写:在元素符号右下角标上一个分子中原子的个数。③离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写;④元素符号的书写:一个字母大写,两个字母第一个字母大写,第二个字母小写。⑤元素化合价的书写:在元素符号的正上方标化合价的数值,正负号在左,数字在右。
数字:①化学式中元素符号右下角的数字为一个分子中原子的个数。②离子符号前加数字,表示离子的个数。③元素符号的前边加数字表示原子的个数;④元素符号右上角的数字表示一个离子带电荷的数值,⑤化学式前边的数字表示分子的个数。⑥元素符号正上方的数字为元素的化合价
【题组训练1】(2017·临沂)用化学符号或化学式填空.
(1)2个氮原子 ;
(2)3个五氧化二磷分子 ;
(3)小苏打 ;(4)铝元素 .
【题组训练2】下列化学用语中,数字“2”的说法正确的是( )
A.表示离子个数⑤⑥
B.表示离子所带电荷数的是④⑤
C.表示一个分子中所含原子个数的是③⑦
D.表示分子个数的是①②
【题组训练3】(2017·连云港)下列化学用语表示正确的是
A.60个碳原子:C60
B.2个氢氧根离子:2OH
C.金刚石:Au
D.3个二氧化硫分子:3SO2
题型2、化合价及应用
【例2】(2017·江西)我省参与制造的C919大飞机采用的复合材料中使用了高温陶瓷材料氮化硅(Si3N4),其中硅元索的化合价为+4价,则氮元素的化合价为
A.-3 B.+2 C.+3 D.+4
【答案】A
【解析】根据化合物中各元素正负化合价代数和为0可知,氮元素的化合价为[0-(+4×3)]÷4=-3。
【解法归纳】
化合价的规律:①单质中元素的化合价为零②化合物中元素化合价的代数和为零。
应用:①书写化学式。②计算化合物中某元素的化合价
【题组训练4】(2017?雅安)含磷的洗涤剂因含有 Na5P3O10易造成水生植物大量繁殖而污染环境, 因此提倡使用无磷洗涤剂。下列化合价在 Na5P3O10 中没有出现的是
A. - 2 B. +1 C. +4 D.+ 5
【题组训练5】(2017·邵阳)某同学书写的试剂标签如下图所示,其中错误的是
【题组训练6】最近,科学家成功制备出了一种含铱元素(铱元素符号:Ir)和氧元素的阳离子,在这种离子中,铱元素显+9价。该离子与氯离子结合成的化合物的化学式可能是( )
A.IrO2Cl B.IrO3Cl C.IrO4Cl D.IrO5Cl
题型3 、化学式的意义与计算
【例4】(2017?营口)某汽水中含有的柠檬酸的化学式为C6H8O7,下列说法正确的是( )
A.柠檬酸是混合物
B.柠檬酸由碳、氢、氧三种原子构成
C.柠檬酸中碳、氢、氧三种元素的质量比为6:8:7
D.8g柠檬酸中含有3g碳元素
【答案】D
【解析】:A、柠檬酸有固定的组成,是纯净物,故错误;B、柠檬酸由柠檬酸分子构成,柠檬酸分子是由碳、氢、氧三种原子构成,故错误;C、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得柠檬酸中碳、氢、氧元素质量比为:(12×6):(1×8):(16×7)=9:2:14;故错误; D、8g柠檬酸含碳元素的质量为8g×=3g,故正确.
故选D.
【答案】
【解法归纳】
【题组训练7】(2017·泰安)“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的物态.大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒只能怪的乙醇生成乙酸乙酯.如表中是几种常见的酯,请完成下列问题:
酯的名称
甲酸甲酯
甲酸乙酯
乙酸甲酯
乙酸乙酯
化学式
C2H4O2
C3H6O2
C3H6O2
X
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为 ;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为 (计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X额定化学式为 .
【题组训练8】(2017·滨州)我市邹平特产“长山山药”中含有被医学界成为“药用黄金”的薯蓣皂素,其化学式为C27H42O3,下列有关薯蓣皂素的说法正确的是( )
A.薯蓣皂素中质量分数最大的是碳元素
B.薯蓣皂素的相对分子质量为228
C.薯蓣皂素中含有21个氢分子
D.薯蓣皂素是由27个碳原子、42个氢原子和3个氧原子构成的
【题组训练9】下图中四位同学正在讨论某化学式的意义,他们描述的化学式是( )
A.CO2 B.H2O2 C.Fe D.Cl2
(2017·天水)青少年过多摄人蛋糕里的人造奶油会产生一种影响身体发育的反式脂肪酸,其化学式为C18H34O2,请计算.
(1)该反式脂肪酸中碳、氧元素的质量比 .
(2)141g该反式脂肪酸中含氢元素的质量为 g.
得分高手体验(可或缺)
【例题】(综合题)(2017·广东)2017年5月18日,中国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。可燃冰是在高压低温环境条件下,水分子笼中装有甲烷分子而成的“冰块”,可直接点燃。己知某种可燃冰的化学式为:CH4·8H2O。请回答:
(1)这种可燃冰中含有______种元素:原子个数比:C:H:O=________;
(2)这种可燃冰中甲烷的质量分数为________%;936g(约1升)该可燃冰常温下可释放出____升甲烷(常温下甲烷密度为0.72g/L)。
【解法归纳】
1、熟记化学式的意义:宏观:表示一种物质和该物质的组成元素;微观:表示一个分子及分子的构成。2、能根据化学式计算相对分子质量==(相对原子质量×原子个数)之和;化合物中元素的质量比=(相对原子质量×原子个数)之比;。
综合培优训练
能力通关
1、(2017·德州)化学用语是学习化学的重要工具。下列化学用语表示正确的是( )
A.两个氯原子:Cl2 B.氧化铝:AlO C.钙离子:Ca+2 D.钾元素:K
2、(2017?玉林)钛酸亚铁(FeTiO3)中铁元素显+2价,则钛元素的化合价是
A.+2 B.+3 C.+4 D.+5
3、(2017·北京)下列符号能表示两个氢分子的是
A.2H B.2H2 C.H2 D.2H2O2
4、(2017?北京)下图为尿素【CO(NH2)2】中各个元素质量分数的示意图,其中表示氮元素质量分数的是
A.① B.② C.③ D.④
5、(2017?泰安)下列化学符号中的数字“2”表示的意义不正确的是
A.2Na:“2”表示两个钠元素
B.NO2:“2"表示一个二氧化氮分子含有两个氧原子
C.2OH- :“2”表示两个氢氧根离子
D.:“ +2"表示镁元素的化合价为+2价
6、(2017·青岛)已知元素周期表中第三周期各元素原子结构示意图如下, 下列分析错误的是
A.以上原子的核外都有三个电子层 B.Na+和Mg2+的核外电子数不相同
C.Na与S形成化合物的化学式为Na2S D.在化学反应中氯原子容易得到电子
7、(2017·荆州)下列关于维生素C(C6H8O6)的说法不正确的是
A.1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成
B.维生素C的相对分子质量为176
C.维生素C中C、H、O三种元素的质量比为3﹕4﹕3
D.维生素C中氢元素的质量分数约为4.5%
8、(2017·聊城)青蒿素(C15H22O5)是一种治疗疟疾的药物,我国女科学家屠呦呦因发现青蒿素荣获诺贝尔奖.下列说法正确的是( )
A.青蒿素中共含有42个原子 B.青蒿素中C、H、O三种元素的质量比是15:22:5
C.青蒿素的相对分子质量为282g D.青蒿素中碳元素的质量分数最高
9、 (2017·青岛)剧烈运动时肌肉里产生乳酸(C3H6O3),会导致肌肉酸痛。下列说法错误的是
A.乳酸的相对分子质量为90 B.乳酸由碳、氢、氧三种元素组成
C.乳酸中氧元素的质量分数最大 D.乳酸中碳、氢、氧元素质量之比为1:2:1
10、(2017?随州改编)从H、C、N、O、Na、S、K七种元素中,选取有关的元素,用适当化学用语填空:
(l)不含电子的离子_______; (2)空气中含量最多的气体单质_______;
(3)含有10个电子的分子_______;(4)Na2CO3中碳元素的化合价_______;
(5)生成物都是单质的分解反应_______。
11、(2017?兰州)中国是把香椿当做蔬菜的唯一国家,它不仅营养丰富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙中各元素的质量之比是____________________(最简整数比);
(2)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
2、巅峰训练
(2017·龙东)炒菜时加入料酒和食醋,炒出的菜別具香味,其原因之一是料酒中的乙醇与食醋中的乙酸反应生成乙酸乙酯(C4H8O2),试计算:
(1)乙酸乙酯的相对分子质量为_________;
(2)乙酸乙酯中碳、氢元素的质量比为___________;(答最简整数比)
(3)17.6 g乙酸乙酯中所含氧元素的质量为_______g。
参考答案
【题组训练】
1、【答案】:(1)2N;(2)3P2O5;(3)NaHCO3;(4)Al;
【解析】:(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个氮原子,就可表示为:2N;
(2)分子的表示方法:正确书写物质的化学式,如五氧化二磷分子是多原子分子,可表示为:P2O5,表示多个该分子,就在其化学式前加上相应的数字,所以3个五氧化二磷分子可表示为3P2O5;(3)小苏打是碳酸氢钠的俗称,其化学式为:NaHCO3;(4)铝元素的元素符号为:Al;
2、【答案】D
【解析】①表示两个氢原子,②表示两个氨气分子;③表示一个一个二氧化硫分子中有两个氧原子;④表示氧化铜中铜元素的化合价为+2价;⑤表示一个镁离子带两个单位正电荷;⑥表示两个氢氧根离子;⑦表示一个水分子中有两个氢原子;
3、【答案】D
【解析】A.60个碳原子:60C.故A错误。 B.2个氢氧根离子:2OH-。故B错误。C.金刚石:C。故C错误。D.3个二氧化硫分子:3SO2 。故D正确。
4、【答案】C
【解析】根据“在化合物中,正负化合价的代数和为零”的原则,已知钠的化合价为+1价,O的化合价为-2价,设Na5P3O10中P的化合价为x,则(+1)×5+3x+(-2)×10=0,解得x=+5,故没有出现的化合价是+4价。故选C。
5、【答案】B
【解析】化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉
约减,得化学式右下角的数字,数字为1时不写;钠元素显+1价,碳酸根显-2价,所以碳酸钠的化学式为Na2CO3,选B
6、【答案】C
【解析】离子所带电荷的数值与元素或根显的化合价的数值相同、正负号也相同。铱元素(铱元素符号:Ir)和氧元素的阳离子,说明二者形成的原子团显正价,则与之结合的氯离子显负价,氯元素的负价为-1,四个选项的化学式中氯离子个数均为1,可推知铱元素(铱元素符号:Ir)和氧元素形成的原子团显+1价,由元素化合价的代数和计算,确定化学式为IrO4Cl。
7、答案】:(1) 6:1:8 ;
(2) 48.6% ;
(3) C4H8O2
【解析】:(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为:(12×2):(1×4):(16×2)=6:1:8;故填:6:1:8;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为=48.6%;故填:48.6%;
(3)根据甲酸甲酯、甲酸乙酯的化学式可知,乙酸乙酯的一个分子里比乙酸甲酯的一个分子里多1个碳原子、2个氢原子,因此乙酸乙酯的化学式为C4H8O2;故填:C4H8O2.
8、【答案】A
【解析】:A.薯蓣皂素中,碳、氢、氧元素的质量比为:(12×27):(1×42):(16×3)=324:42:48,可见其中碳元素的质量分数最大,故正确;
B.薯蓣皂素的相对分子质量为12×27+1×42+16×3=414,故错误;
C.薯蓣皂素是由薯蓣皂素分子构成的,每个薯蓣皂素分子中含有42个氢原子,不含氢分子,故错误;
D.薯蓣皂素是由分子构成的,而不是由原子直接构成的,故错误.故选A.
9、【答案】:(1)27:4;(2)17.
【解答】解:(1)该反式脂肪酸中碳、氧元素的质量比(12×18):(16×2)=27:4;故填:27:4;
(2)141g该反式脂肪酸中含氢元素的质量为141g×=17g;故填:17.
得分高手体验(可或缺)
【例题】
【答案】(1)三: 1:20:8;(2)10%; 130L
【解析】(1)这种可燃冰中含有碳、氢、氧三种元素:化学式中元素符号右下角的数字为一个分子中原子的个数,这种可燃冰原子个数比:C:H:O=1:20:8;(2)这种可燃冰中甲烷的质量分数为 ;该可燃冰和甲烷的质量比为160:16;936g(约1升)该可燃冰常温下可释放出甲烷的质量93.6g;体积为130L。
【解法归纳】
1、熟记化学式的意义:宏观:表示一种物质和该物质的组成元素;微观:表示一个分子及分子的构成。2、能根据化学式计算相对分子质量==(相对原子质量×原子个数)之和;化合物中元素的质量比=(相对原子质量×原子个数)之比;。
综合培优训练
能力通关
1、【答案】D
【解析】两个氯原子应为2Cl,氧化铝化学式为Al2O3 ,钙离子为Ca2+ ,钾元素符号为K。故选D。
2、【答案】C
【解析】化合物中元素的化合价的代数和为零,设钛元素的化合价为x,则x+(+2)+(-2)×3=0, x=+4
3、(2017·北京)下列符号能表示两个氢分子的是
A.2H B.2H2 C.H2 D.2H2O2
【答案】B
【解析】根据符号的意义进行选取。
4、【答案】A
【解析】某元素的质量分数=,
通过计算氮元素的质量分数最大,结合图示A项正确。
5、【答案】A
【解析】A.元素符号前加数字表示原子的个数,2Na:“2”表示两个钠原子;B.化学式中元素符号右下角的数字为一个分子中原子的个数,NO2:“2"表示一个二氧化氮分子含有两个氧原子;C.离子符号前边的数字为离子的个数,2OH- :“2”表示两个氢氧根离子;D.元素符号上方的数字为元素的化合价,:“ +2"表示氧化镁中镁元素的化合价为+2价。
6、【答案】B
【解析】在原子结构示意图中,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。原子的化学性质主要由最外层电子数决定,当最外层电子数小于4时,反应中易失去电子成为阳离子;当最外层电子数大于4时,反应中易得到电子成为阴离子;原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,不易得失电子。A.以上原子的核外都有三个电子层; B.Na+和Mg2+的核外电子数相同,都是8;C.Na与S形成化合物的化学式为Na2S D.在化学反应中氯原子容易得到电子;选B
7、 【答案】C
【解析】A.1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成,正确;B.维生素C的相对分子质量为12×6+1×8+16×6=176,正确;C.维生素C中C、H、O三种元素的原子个数比为3﹕4﹕3,故说法错误;D.维生素C中氢元素的质量分数约为 =4.5%。故选C。
8、【答案】D
【解析】:A.青蒿素是由青蒿素分子构成的而不是由原子直接构成的,故错误;B.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,故错误;
C.相对分子质量的单位不是“g”而是“1”,通常省略不写,故错误;
D.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,由此可见其中碳元素的质量分数最高,故正确.故选D.
9、 【答案】D
【解析】A.相对分子质量=(相对原子质量×原子个数)之和,乳酸的相对分子质量为90 ; B.由化学式可知乳酸由碳、氢、氧三种元素组成;C.,乳酸中氧元素的质量分数最大 ;D.乳酸中碳、氢、氧原子个数之比为1:2:1;选D
10、【答案】(1)H+;(2)N2;(3)CH4或NH3或H2O(任写一种即可)(4)+4;(5)KNO3;(6)H2OH2↑+O2↑
【解析】由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;由两种元素组成,且其中一种是氧的化合物叫氧化物。溶于水产生的阳离子只有氢离子的化合物是酸 。由金属或铵根和酸根组成的化合物叫盐,由金属或铵根和氢氧根组成的化合物叫碱。化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写;单质的化学式的书写:在元素符号右下角标上一个分子中原子的个数。(l)氢原子中只有一个电子,其离子中没有电子,H+; 2)空气中含量最多的气体单质氮气,占空气的体积 的78% ,N2;;(3)一个水分子由一个氧原子和两个氢原子构成,一个氧原子中有8个电子,一个氢原子中有一个电子,一个水分子含有10个电子,H2O(CH4或NH3);(4)化合物中各元素化合价的代数和为零,由于钠元素为+1价,氧元素是-2价,Na2CO3中碳元素的化合价为+4;(5)生成物都是单质的分解反应H2O H2↑+O2↑
11、 【答案】(1)54:7:8;(2) 82.8g
【解析】(1)化合物中元素的质量比=(相对原子质量×原子个数)之比,皂甙中各元素的质量之比是
27×12:1×42:3×16=54:7:8;(2)含氢元素8.4 g的皂甙的质量为8.4÷(
)=82.8g
2、巅峰训练
【答案】(1) 88 (2) 6:1 (3)6.4
【解析】(1) 相对分子质量=(相对原子质量×原子个数)之和,乙酸乙酯的相对分子质量为4×12+1×8+2×16=88;(2) 化合物中元素的质量比=(相对原子质量×原子个数)之比,乙酸乙酯中碳、氢元素的质量比为4×12:1×8=6:1;⑶,17.6 g乙酸乙酯中所含氧元素的质量为17.6 g× =6.4g
备用题
(2017·丽水)儿童缺锌会引起食欲不振、发育不良等症状。如图为某补锌口服液说明书的部分信息,回答下列问题:
(1)葡萄糖酸锌由 种元素组成;
(2)葡萄糖酸锌中碳、氢元素的质量比为 ;
(3)要满足儿童身体正常的需要,在某一时间段需要适量补锌。若儿童1千克体重每日需要0.5毫克锌,每天从食物中只能摄入所需锌的一半。体重为20千克的儿童,理论上一天还需服该口服液多少支?
【答案】(1)四 (2)72:11(3)1支
2017?六盘水)元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
(l)溴的相对原子质量是_______。
(2)溴元素的化学性质与图二哪种元素的化学性质相似_______(填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为:_______。
(4)若图二中C表示离子,则离子符号是_______。
【答案】(1)79.90;(2)B;(3)KBr;(4)S2-;
1、(2017·济宁)观看足球比赛时,经常会看到绿茵场上运动员因拼抢摔倒受伤,医生向受伤部位喷射氯乙烷(CH3CH2Cl),并用药棉不断揉搓,运动员疼痛很快消除,重新投入比赛.
请阅读信息后,回答:
(1)氯乙烷中C、H、Cl三种元素的原子个数比为 ;
(2)氯乙烷中C、H、Cl三种元素的质量比为 .
【解答】解:(1)由化学式可知,1个氯乙烷分子是由2个碳原子、5个氢原子和1个氯原子构成的,则氯乙烷中C、H、Cl三种元素的原子个数比为2:5:1;故填:2:5:1;
(2)氯乙烷中碳、氢、氯三种元素的质量比为(12×2):(1×5):(35.5×1)=48:10:71,故填:48:10:71.
(2017·福建)PLA是一种新型可降解塑料,以乳酸(C3H6O3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )【来源:21cnj*y.co*m】
A.乳酸是由碳、氢、氧三种元素组成
B.乳酸分子中含有12个原子
C.乳酸的相对分子质量是90
D.乳酸中氧元素的质量分数最大
(2017·青岛)太阳能吸附式制冷结露法空气取水器可用于野外获取淡
水,工作原理如下图所示。
(1)蒸发冷凝器中发生的是________
(填“物理”或“化学”)变化。
(2)吸附剂中主要物质为SiO2和CaCl2,
SiO2中硅元素的化合价为_________,CaCl2
中钙、氯元素的质量比为________。
【答案】
(1)物理(2)+4 40:71
【解析】
(1)由图可知,湿空气进入蒸发冷凝器中,将气态水变为液态水,最后进入到集水器中,整个过程水的状态发生改变,未生成新的物质,故为物理变化;
(2)SiO2中的Si元素的化合价为+4价,CaCl2中钙、氯元素的的质量比为40:35.5×2=40:71。
(2017·自贡)标出硝酸钠中各元素的化合价_______。
【答案】氮气;
【解析】
根据化合价的表示方法:在其化学式中该元素的正上
方用正负号和数字表示,且正负号在前,数字在后,
则硝酸钠中各元素的化合价表示为 。
(2017·聊城)地壳中元素含量(质量分数)由高到低依次是氧、硅、铝、铁等.如图分别是硅元素在元素周期表中的信息和铝元素的原子结构示意图.请回答下列问题:
(1)硅原子的核外电子数是 14 .
(2)铝离子的符号 Al3+ .
(3)铁在地壳中主要以铁矿石的形式存在,其中赤铁矿的主要成分是Fe2O3.Fe2O3中铁元素的化合价为 +3 价.
【解答】解:(1)由元素周期表的信息可知,硅元素的原子序数为14,因为在原子中,原子序数=质子数=核外电子数,所以硅原子的核外电子数为14;故填:14;
(2)由铝原子结构示意图可知,铝原子的最外层有3个电子,在化学反应易失去最外层的三个电子而形成带有三个单位正电荷的铝离子,其离子符号为Al3+;故填:Al3+;
(3)氧化铁中,氧元素显﹣2价,设铁元素的化合价为x,则2x+(﹣2)×3=0,x=+3;故填:+3.
(2017·威海)2017年1月27日,南京理工大学化学学院胡炳成团队成功合成世界上首个超高能全氨阴离子(N5-)钴(Co)盐【化学式为:Co(N5)2(H2O)4】。下列有关说法正确的是
A.该物质属于混合物 B.该物质中钴元素的质量分数比氧元素的质量分数小
C.该物质中钴元素的化合价为+5价 D.该物质属于有机物
【答案】B
【解析】A、由化学式可知该物质有固定的组成和结构,是纯净物,B.该物质中钻元素的质量分数比氧元素的质量分数小;C.化合物中元素的化合价的代数和为零,离子带电荷的数值等于该元素的化合价的数值,全氨阴离子(N5-),故该物质中钴元素的化台价为+1价;D.除一氧化碳、二氧化碳、碳酸、碳酸盐以外的含碳化合物称为有机物。该物质没有碳元素,属于无机物;选B
(2017·潍坊)我国自主研制的首艘货运飞船“天舟一号”已于2017年4月20日发射成功,这标志着我国航天事业又跨入了一个崭新的时代。肼(N2H4)是航天事业的功臣,常用作火箭燃料。下列有关肼的说法正确的是
A.肼是一种混合物 B.一个N2H4分子由1个N2分子和2个H2分子组成
C.肼的化学式可简写为NH2 D.N2H4的相对分子质量为32
【答案】D
【解析】A、由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;肼是化合物;B化学式中元素符号右下角的数字是一个分子中原子的个数,所以一个N2H4分子由2个氮原子和4个氢原子构成;C化学式表示一个分子,构成物质的分子是一定的,所以肼的化学式不可简写为NH2;D相对分子质量=(相对原子质量×原子个数)之和,N2H4的相对分子质量为32;选D
(2017·广州)N(NO2)3是科学家近年发现的一种新型火箭燃料。下列关于N(NO2)3说法正确的是
A.N(NO2)3的相对分子质量为152
B.N(NO2)3中氮元素与氧元素的质量比是2:3
C.N(NO2)3中总共有3个N原子和6个O原子
D.N(NO2)3中氮元素的质量分数为
【答案】A
【解析】N(NO2)3的相对分子质量为14×4+16×6=152;N(NO2)3中氮元素与氧元素的质量比是(14×4):(16×6)=7:12;N(NO2)3的一个分子中共有3个N原子和6个O原子;N(NO2)3中氮元素的质量分数为,故选A。
学习目标
中考考点关注
1、正确书写常见物质的化学式,并能读出化学式,说出化学式表示的意义(重点)
2、熟知常见元素常见的化合价,能依据化合价写出物质的化学式,会计算化合物中某元的化合价(重点、难点)
3、能根据化学式进行简单的计算(重点)
1、化学式及其意义(必考点)
2、化合价(常考点)
3、化学式的写法(必考点)
4、化合物的读法(必考点)
5、有关化学式的计算(常考点)
教材知识精析
知识点1、化学式及其意义(重点)
1.化学式的定义
用元素符号和数字的组合表示物质组成的式子。每种纯净物只有一个化学式。
2、物质的组成与化学式的关系
3.化学式的意义
Ⅰ、由分子构成的物质
化学式的意义
以“ H2O ”为例
宏观
表示一种物质
表示水
表示该物质的元素组成
表示水由氢元素和氧元素组成
微观
表示该物质一个分子
表示一个水分子
表示该物质的分子构成
表示一个水分子由2个氢原子和1个氧原子构成的
Ⅱ、由原子构成的物质
化学式的意义
以“ Cu ” 为例
宏观
表示某物质
表示铜这种物质
表示该物质的组成元素
表示金属铜由铜元素元素组成
微观
表示该物质的一个原子
表示1个铜原子
Ⅲ、由离子构成的物质
化学式的意义
以“ MgCl2 ”为例
宏观
表示氯化镁这种物质
表示该物质的元素组成
表示氯化钠由镁元素和氯元素组成
微观
表示离子的个数比
表示氯化镁中氯离子和镁离子的个数比为1:2
☆尖子生笔记☆
【拓展延伸】
1、关于化学式
①任何纯净物都可以用化学式表示。
②对由分子构成的物质,用分子式作为化学式,化学式中元素符号右下角的数字为一个分子中原子的个数;由原子构成的物质用元素符号作为化学式;由离子构成的物质,在元素符号右下角标出离子个数比。
③各种物质的化学式都是通过实验测定的,一种物质只有一个化学式。
④化学式前边的数字为分子的个数,此时,只有微观意义。如:2CO:表示两个一氧化碳分子。
知识点2、化合价(重点、难点)
1、化合价概念
化合物中,不同元素的原子(离子)总以一定的个数比相互结合的性质,叫元素的化合价。
2、化合价的确定
①由离子构成的化合物中,元素的化合价的数值就是一个原子得到或失去的电子数。正价等于失电子数;负价等于得电子数。(掌握)
②由分子构成的化合物中,化合价的数值就是一个原子与其他原子形成的共用电子对的数值。(了解)
3、原子团
作为一个整体参加化学反应的原子集合体叫原子团,称作“某根”
常见原子团及化合价:
4、常见元素的化合价
Ⅰ、化合价规律:
(1)金属元素与非金属元素化合时,金属元素显正价,非金属元素显负价。
(2)氢元素通常显+1价,氧元素通常显-2价。
(3)在化合物中元素化合价的代数和为零。
(4)在单质里,元素的化合价为零
Ⅱ、记忆口诀
一价氢氯钠钾银, 二价氧钙钡镁锌;
三铝四硅五价磷, 二三铁、二四碳;
二四六硫都齐全, 铜汞二价最常见。
条件不同价不同, 单质为零永不变。
负一硝酸氢氧根,负二硫酸碳酸根,
负三记住磷酸根,正一价的是铵根。
(红色的为负价)
5、化合价的表示方法
通常在元素符号或原子团的正上方标出其化合价,一般把“+,-”号写在前面,价数写在后面。价数为1时,1不能省略。
6、数字或符号的意义
Ⅰ、符号的意义
H:氢元素 或 1个氢原子
2H:2个氢原子
H2:①氢气 ②氢气由氢元素组成 ③1个氢分子
④1个分子由2个氢原子构成
2H2:2个氢分子
2H+:2个氢离子
Ⅱ、数字的意义
“R”代表元素符号
a(左前方):表示有a个R粒子(原子、分子或离子等)
b(右下角):表示一个粒子中含有b个某原子
c(右上角):表示一个R离子带c个正(或负)电荷
d(正上方):表示(某化合物中)R元素的化合价为±d价
☆尖子生笔记☆
【规律方法】
化合价口诀
单质元素全为零,
化合物中和为零。
氢一氧二要记住,
金正非负记分明。
一价金属钾钠银,
二价金属钙镁钡和锌。
一二铜汞二三铁,
三铝四硅五价磷。
谈根价,也不难,
氢氧根负一铵正一。
酸根所有皆为负,
一硝三磷二硫碳。
【拓展延伸】
1、化合价和离子符号的比较
小结:
⑴不同
离子:数字在前“+” “-”号在后;写在右上角
化合价:数字在后“+” “-” 号在前;写上方。
⑵相同
化合价数值与离子所带电荷 数值相同
2、①有的元素在不同的物质中可能会有几种不同的化合价。如一氧化碳中碳元素显+2价;二氧化碳中碳元素显+4价。②在同一物质中可能也会有不同的化合价。如:硝酸铵中氮元素有-3和+5两种化合价。
知识点3、化学式与化合价的关系(重点、难点)
1、根据化学式求某一元素化合价
依据:化合物里正负化合价的代数和为零
例:试确定氯酸钾(KClO3)中氯元素的化合价
解:设氯元素的化合价为x,则
(+1)+ x +(-2)×3=0
x = +5
所以,在氯酸钾中,氯元素的化合价为+5价
2、根据化合价推写化学式
依据:化合物里正负化合价的代数和为零
最小公倍数法
3、单质的化学式
①由原子构成,它们的化学式用元素符号直接表示。
如:铜:Cu
②气态非金属:由分子构成,它们的化学式写法是:在元素符号的右下角写出表示一个分子中原子个数的数字。
☆尖子生笔记☆
【易错点津】
化合价计算的化合价要写明正负
【拓展延伸】
1、数字交叉法写化合物的化学式
a.写符号
b.标化合价
c.化合价绝对值交叉放置元素符号右下角
d.约简(至最简整数比)
e.检查
例:已知磷为+3价,氧为- 2价,写出磷的这种化合物的化学式。
2、判断化学式正误的方法
⑴看元素符号书写是否正确。一个字母的要大写;两个字母的,第一个大写,第二个小写。
⑵右下角的数字是否遗漏
⑶由两种元素组成,其中一种是氧的化合物,氧元素是否写在右边。
⑷有金属元素时,金属元素是否写在左边。
3、根据化合价写代数式(口诀):正写前来负在后,化合价暗暗记心头,交叉约简再写数,写完检验不要丢。
知识点4、常见化合物的读法(重点、难点)
1、由两种元素组成的化合物的读法:
通常规定从右向左读即(顺写反读),读作“某化某”、“几某化几某”
如:NaCl:读作氯化钠;CO2:读作二氧化碳
2、含有原子团的化合物,要读出原子团的名称,如CuSO4:读作硫酸铜。
3、+2价铁在化合物中读作“亚铁”;如:FeCl2:氯化亚铁
☆尖子生笔记☆
【规律方法】
知识点5、化学式的计算(重点、难点)
1、相对分子质量
定义:化学式中各原子的相对原子质量的总和,就是该物质的化学式量,对于由分子构成的物质,其化学式量也叫相对分子质量
【例1】H2O的相对分子质量=1×2+16×1=18
【例2】(NH4)2SO4的相对分子质量
=(14+1×4)×2+32+16×4=132
2.计算物质组成元素的质量比
各元素之间的质量比=各原子的相对原子质量总和之比
例:求Fe2O3中铁元素和氧元素的质量比。
Fe:O=(56×2):(16×3)=112:48=7:3
3.计算物质中某元素的质量分数
例:⑴计算二氧化硫中硫元素的质量分数
⑵计算64t二氧化硫中含硫元素的质量。
☆尖子生笔记☆
【规律方法】
1、相对分子质量的单位为1,不写,也不读。
2、计算化学式量时元素的相对原子质量与元素符号右下角的数字之间用“ⅹ”号,不同元素之间用“+”。
3、化学式原子团右下角的数字表示原子团的个数,计算时可以先求出一个原子团的式量,再乘以其个数。
【拓展延伸】
注意事项:
①质量分数——用百分数来表示
②意义:每100克物质中含有某元素的质量
解题能力突破
题型1 、元素符号及其周围数字的意义
【例1】(2017·中考)下列化学用语书写正确的是
A.两个氢分子:2H B.2个硫酸根离子:2SO4-2
C.水中氧元素的化合价为-2 价: D.两个氮原子: N2
【答案】C
【解析】
A.两个氢分子:2H2 ; 2H 表示两个氢原子; B.离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写;离子符号前加数字,表示离子的个数。2个硫酸根离子:2SO42-;C.元素化合价的书写:在元素符号的正上方标化合价的数值,正负号在左,数字在右。水中氧元素的化合价为-2 价: D.元素符号的前边加数字表示原子的个数,两个氮原子: 2N;选C
【解法归纳】熟记各种化学用语的书写、意义及周围数字的意义。
符号:①化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写;
②单质的化学式的书写:在元素符号右下角标上一个分子中原子的个数。③离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写;④元素符号的书写:一个字母大写,两个字母第一个字母大写,第二个字母小写。⑤元素化合价的书写:在元素符号的正上方标化合价的数值,正负号在左,数字在右。
数字:①化学式中元素符号右下角的数字为一个分子中原子的个数。②离子符号前加数字,表示离子的个数。③元素符号的前边加数字表示原子的个数;④元素符号右上角的数字表示一个离子带电荷的数值,⑤化学式前边的数字表示分子的个数。⑥元素符号正上方的数字为元素的化合价
【题组训练1】(2017·临沂)用化学符号或化学式填空.
(1)2个氮原子 ;
(2)3个五氧化二磷分子 ;
(3)小苏打 ;(4)铝元素 .
【题组训练2】下列化学用语中,数字“2”的说法正确的是( )
A.表示离子个数⑤⑥
B.表示离子所带电荷数的是④⑤
C.表示一个分子中所含原子个数的是③⑦
D.表示分子个数的是①②
【题组训练3】(2017·连云港)下列化学用语表示正确的是
A.60个碳原子:C60
B.2个氢氧根离子:2OH
C.金刚石:Au
D.3个二氧化硫分子:3SO2
题型2、化合价及应用
【例2】(2017·江西)我省参与制造的C919大飞机采用的复合材料中使用了高温陶瓷材料氮化硅(Si3N4),其中硅元索的化合价为+4价,则氮元素的化合价为
A.-3 B.+2 C.+3 D.+4
【答案】A
【解析】根据化合物中各元素正负化合价代数和为0可知,氮元素的化合价为[0-(+4×3)]÷4=-3。
【解法归纳】
化合价的规律:①单质中元素的化合价为零②化合物中元素化合价的代数和为零。
应用:①书写化学式。②计算化合物中某元素的化合价
【题组训练4】(2017?雅安)含磷的洗涤剂因含有 Na5P3O10易造成水生植物大量繁殖而污染环境, 因此提倡使用无磷洗涤剂。下列化合价在 Na5P3O10 中没有出现的是
A. - 2 B. +1 C. +4 D.+ 5
【题组训练5】(2017·邵阳)某同学书写的试剂标签如下图所示,其中错误的是
【题组训练6】最近,科学家成功制备出了一种含铱元素(铱元素符号:Ir)和氧元素的阳离子,在这种离子中,铱元素显+9价。该离子与氯离子结合成的化合物的化学式可能是( )
A.IrO2Cl B.IrO3Cl C.IrO4Cl D.IrO5Cl
题型3 、化学式的意义与计算
【例4】(2017?营口)某汽水中含有的柠檬酸的化学式为C6H8O7,下列说法正确的是( )
A.柠檬酸是混合物
B.柠檬酸由碳、氢、氧三种原子构成
C.柠檬酸中碳、氢、氧三种元素的质量比为6:8:7
D.8g柠檬酸中含有3g碳元素
【答案】D
【解析】:A、柠檬酸有固定的组成,是纯净物,故错误;B、柠檬酸由柠檬酸分子构成,柠檬酸分子是由碳、氢、氧三种原子构成,故错误;C、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得柠檬酸中碳、氢、氧元素质量比为:(12×6):(1×8):(16×7)=9:2:14;故错误; D、8g柠檬酸含碳元素的质量为8g×=3g,故正确.
故选D.
【答案】
【解法归纳】
【题组训练7】(2017·泰安)“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的物态.大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒只能怪的乙醇生成乙酸乙酯.如表中是几种常见的酯,请完成下列问题:
酯的名称
甲酸甲酯
甲酸乙酯
乙酸甲酯
乙酸乙酯
化学式
C2H4O2
C3H6O2
C3H6O2
X
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为 ;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为 (计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X额定化学式为 .
【题组训练8】(2017·滨州)我市邹平特产“长山山药”中含有被医学界成为“药用黄金”的薯蓣皂素,其化学式为C27H42O3,下列有关薯蓣皂素的说法正确的是( )
A.薯蓣皂素中质量分数最大的是碳元素
B.薯蓣皂素的相对分子质量为228
C.薯蓣皂素中含有21个氢分子
D.薯蓣皂素是由27个碳原子、42个氢原子和3个氧原子构成的
【题组训练9】下图中四位同学正在讨论某化学式的意义,他们描述的化学式是( )
A.CO2 B.H2O2 C.Fe D.Cl2
(2017·天水)青少年过多摄人蛋糕里的人造奶油会产生一种影响身体发育的反式脂肪酸,其化学式为C18H34O2,请计算.
(1)该反式脂肪酸中碳、氧元素的质量比 .
(2)141g该反式脂肪酸中含氢元素的质量为 g.
得分高手体验(可或缺)
【例题】(综合题)(2017·广东)2017年5月18日,中国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。可燃冰是在高压低温环境条件下,水分子笼中装有甲烷分子而成的“冰块”,可直接点燃。己知某种可燃冰的化学式为:CH4·8H2O。请回答:
(1)这种可燃冰中含有______种元素:原子个数比:C:H:O=________;
(2)这种可燃冰中甲烷的质量分数为________%;936g(约1升)该可燃冰常温下可释放出____升甲烷(常温下甲烷密度为0.72g/L)。
【解法归纳】
1、熟记化学式的意义:宏观:表示一种物质和该物质的组成元素;微观:表示一个分子及分子的构成。2、能根据化学式计算相对分子质量==(相对原子质量×原子个数)之和;化合物中元素的质量比=(相对原子质量×原子个数)之比;。
综合培优训练
能力通关
1、(2017·德州)化学用语是学习化学的重要工具。下列化学用语表示正确的是( )
A.两个氯原子:Cl2 B.氧化铝:AlO C.钙离子:Ca+2 D.钾元素:K
2、(2017?玉林)钛酸亚铁(FeTiO3)中铁元素显+2价,则钛元素的化合价是
A.+2 B.+3 C.+4 D.+5
3、(2017·北京)下列符号能表示两个氢分子的是
A.2H B.2H2 C.H2 D.2H2O2
4、(2017?北京)下图为尿素【CO(NH2)2】中各个元素质量分数的示意图,其中表示氮元素质量分数的是
A.① B.② C.③ D.④
5、(2017?泰安)下列化学符号中的数字“2”表示的意义不正确的是
A.2Na:“2”表示两个钠元素
B.NO2:“2"表示一个二氧化氮分子含有两个氧原子
C.2OH- :“2”表示两个氢氧根离子
D.:“ +2"表示镁元素的化合价为+2价
6、(2017·青岛)已知元素周期表中第三周期各元素原子结构示意图如下, 下列分析错误的是
A.以上原子的核外都有三个电子层 B.Na+和Mg2+的核外电子数不相同
C.Na与S形成化合物的化学式为Na2S D.在化学反应中氯原子容易得到电子
7、(2017·荆州)下列关于维生素C(C6H8O6)的说法不正确的是
A.1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成
B.维生素C的相对分子质量为176
C.维生素C中C、H、O三种元素的质量比为3﹕4﹕3
D.维生素C中氢元素的质量分数约为4.5%
8、(2017·聊城)青蒿素(C15H22O5)是一种治疗疟疾的药物,我国女科学家屠呦呦因发现青蒿素荣获诺贝尔奖.下列说法正确的是( )
A.青蒿素中共含有42个原子 B.青蒿素中C、H、O三种元素的质量比是15:22:5
C.青蒿素的相对分子质量为282g D.青蒿素中碳元素的质量分数最高
9、 (2017·青岛)剧烈运动时肌肉里产生乳酸(C3H6O3),会导致肌肉酸痛。下列说法错误的是
A.乳酸的相对分子质量为90 B.乳酸由碳、氢、氧三种元素组成
C.乳酸中氧元素的质量分数最大 D.乳酸中碳、氢、氧元素质量之比为1:2:1
10、(2017?随州改编)从H、C、N、O、Na、S、K七种元素中,选取有关的元素,用适当化学用语填空:
(l)不含电子的离子_______; (2)空气中含量最多的气体单质_______;
(3)含有10个电子的分子_______;(4)Na2CO3中碳元素的化合价_______;
(5)生成物都是单质的分解反应_______。
11、(2017?兰州)中国是把香椿当做蔬菜的唯一国家,它不仅营养丰富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙中各元素的质量之比是____________________(最简整数比);
(2)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
2、巅峰训练
(2017·龙东)炒菜时加入料酒和食醋,炒出的菜別具香味,其原因之一是料酒中的乙醇与食醋中的乙酸反应生成乙酸乙酯(C4H8O2),试计算:
(1)乙酸乙酯的相对分子质量为_________;
(2)乙酸乙酯中碳、氢元素的质量比为___________;(答最简整数比)
(3)17.6 g乙酸乙酯中所含氧元素的质量为_______g。
参考答案
【题组训练】
1、【答案】:(1)2N;(2)3P2O5;(3)NaHCO3;(4)Al;
【解析】:(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个氮原子,就可表示为:2N;
(2)分子的表示方法:正确书写物质的化学式,如五氧化二磷分子是多原子分子,可表示为:P2O5,表示多个该分子,就在其化学式前加上相应的数字,所以3个五氧化二磷分子可表示为3P2O5;(3)小苏打是碳酸氢钠的俗称,其化学式为:NaHCO3;(4)铝元素的元素符号为:Al;
2、【答案】D
【解析】①表示两个氢原子,②表示两个氨气分子;③表示一个一个二氧化硫分子中有两个氧原子;④表示氧化铜中铜元素的化合价为+2价;⑤表示一个镁离子带两个单位正电荷;⑥表示两个氢氧根离子;⑦表示一个水分子中有两个氢原子;
3、【答案】D
【解析】A.60个碳原子:60C.故A错误。 B.2个氢氧根离子:2OH-。故B错误。C.金刚石:C。故C错误。D.3个二氧化硫分子:3SO2 。故D正确。
4、【答案】C
【解析】根据“在化合物中,正负化合价的代数和为零”的原则,已知钠的化合价为+1价,O的化合价为-2价,设Na5P3O10中P的化合价为x,则(+1)×5+3x+(-2)×10=0,解得x=+5,故没有出现的化合价是+4价。故选C。
5、【答案】B
【解析】化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉
约减,得化学式右下角的数字,数字为1时不写;钠元素显+1价,碳酸根显-2价,所以碳酸钠的化学式为Na2CO3,选B
6、【答案】C
【解析】离子所带电荷的数值与元素或根显的化合价的数值相同、正负号也相同。铱元素(铱元素符号:Ir)和氧元素的阳离子,说明二者形成的原子团显正价,则与之结合的氯离子显负价,氯元素的负价为-1,四个选项的化学式中氯离子个数均为1,可推知铱元素(铱元素符号:Ir)和氧元素形成的原子团显+1价,由元素化合价的代数和计算,确定化学式为IrO4Cl。
7、答案】:(1) 6:1:8 ;
(2) 48.6% ;
(3) C4H8O2
【解析】:(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为:(12×2):(1×4):(16×2)=6:1:8;故填:6:1:8;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为=48.6%;故填:48.6%;
(3)根据甲酸甲酯、甲酸乙酯的化学式可知,乙酸乙酯的一个分子里比乙酸甲酯的一个分子里多1个碳原子、2个氢原子,因此乙酸乙酯的化学式为C4H8O2;故填:C4H8O2.
8、【答案】A
【解析】:A.薯蓣皂素中,碳、氢、氧元素的质量比为:(12×27):(1×42):(16×3)=324:42:48,可见其中碳元素的质量分数最大,故正确;
B.薯蓣皂素的相对分子质量为12×27+1×42+16×3=414,故错误;
C.薯蓣皂素是由薯蓣皂素分子构成的,每个薯蓣皂素分子中含有42个氢原子,不含氢分子,故错误;
D.薯蓣皂素是由分子构成的,而不是由原子直接构成的,故错误.故选A.
9、【答案】:(1)27:4;(2)17.
【解答】解:(1)该反式脂肪酸中碳、氧元素的质量比(12×18):(16×2)=27:4;故填:27:4;
(2)141g该反式脂肪酸中含氢元素的质量为141g×=17g;故填:17.
得分高手体验(可或缺)
【例题】
【答案】(1)三: 1:20:8;(2)10%; 130L
【解析】(1)这种可燃冰中含有碳、氢、氧三种元素:化学式中元素符号右下角的数字为一个分子中原子的个数,这种可燃冰原子个数比:C:H:O=1:20:8;(2)这种可燃冰中甲烷的质量分数为 ;该可燃冰和甲烷的质量比为160:16;936g(约1升)该可燃冰常温下可释放出甲烷的质量93.6g;体积为130L。
【解法归纳】
1、熟记化学式的意义:宏观:表示一种物质和该物质的组成元素;微观:表示一个分子及分子的构成。2、能根据化学式计算相对分子质量==(相对原子质量×原子个数)之和;化合物中元素的质量比=(相对原子质量×原子个数)之比;。
综合培优训练
能力通关
1、【答案】D
【解析】两个氯原子应为2Cl,氧化铝化学式为Al2O3 ,钙离子为Ca2+ ,钾元素符号为K。故选D。
2、【答案】C
【解析】化合物中元素的化合价的代数和为零,设钛元素的化合价为x,则x+(+2)+(-2)×3=0, x=+4
3、(2017·北京)下列符号能表示两个氢分子的是
A.2H B.2H2 C.H2 D.2H2O2
【答案】B
【解析】根据符号的意义进行选取。
4、【答案】A
【解析】某元素的质量分数=,
通过计算氮元素的质量分数最大,结合图示A项正确。
5、【答案】A
【解析】A.元素符号前加数字表示原子的个数,2Na:“2”表示两个钠原子;B.化学式中元素符号右下角的数字为一个分子中原子的个数,NO2:“2"表示一个二氧化氮分子含有两个氧原子;C.离子符号前边的数字为离子的个数,2OH- :“2”表示两个氢氧根离子;D.元素符号上方的数字为元素的化合价,:“ +2"表示氧化镁中镁元素的化合价为+2价。
6、【答案】B
【解析】在原子结构示意图中,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。原子的化学性质主要由最外层电子数决定,当最外层电子数小于4时,反应中易失去电子成为阳离子;当最外层电子数大于4时,反应中易得到电子成为阴离子;原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,不易得失电子。A.以上原子的核外都有三个电子层; B.Na+和Mg2+的核外电子数相同,都是8;C.Na与S形成化合物的化学式为Na2S D.在化学反应中氯原子容易得到电子;选B
7、 【答案】C
【解析】A.1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成,正确;B.维生素C的相对分子质量为12×6+1×8+16×6=176,正确;C.维生素C中C、H、O三种元素的原子个数比为3﹕4﹕3,故说法错误;D.维生素C中氢元素的质量分数约为 =4.5%。故选C。
8、【答案】D
【解析】:A.青蒿素是由青蒿素分子构成的而不是由原子直接构成的,故错误;B.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,故错误;
C.相对分子质量的单位不是“g”而是“1”,通常省略不写,故错误;
D.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,由此可见其中碳元素的质量分数最高,故正确.故选D.
9、 【答案】D
【解析】A.相对分子质量=(相对原子质量×原子个数)之和,乳酸的相对分子质量为90 ; B.由化学式可知乳酸由碳、氢、氧三种元素组成;C.,乳酸中氧元素的质量分数最大 ;D.乳酸中碳、氢、氧原子个数之比为1:2:1;选D
10、【答案】(1)H+;(2)N2;(3)CH4或NH3或H2O(任写一种即可)(4)+4;(5)KNO3;(6)H2OH2↑+O2↑
【解析】由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;由两种元素组成,且其中一种是氧的化合物叫氧化物。溶于水产生的阳离子只有氢离子的化合物是酸 。由金属或铵根和酸根组成的化合物叫盐,由金属或铵根和氢氧根组成的化合物叫碱。化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写;单质的化学式的书写:在元素符号右下角标上一个分子中原子的个数。(l)氢原子中只有一个电子,其离子中没有电子,H+; 2)空气中含量最多的气体单质氮气,占空气的体积 的78% ,N2;;(3)一个水分子由一个氧原子和两个氢原子构成,一个氧原子中有8个电子,一个氢原子中有一个电子,一个水分子含有10个电子,H2O(CH4或NH3);(4)化合物中各元素化合价的代数和为零,由于钠元素为+1价,氧元素是-2价,Na2CO3中碳元素的化合价为+4;(5)生成物都是单质的分解反应H2O H2↑+O2↑
11、 【答案】(1)54:7:8;(2) 82.8g
【解析】(1)化合物中元素的质量比=(相对原子质量×原子个数)之比,皂甙中各元素的质量之比是
27×12:1×42:3×16=54:7:8;(2)含氢元素8.4 g的皂甙的质量为8.4÷(
)=82.8g
2、巅峰训练
【答案】(1) 88 (2) 6:1 (3)6.4
【解析】(1) 相对分子质量=(相对原子质量×原子个数)之和,乙酸乙酯的相对分子质量为4×12+1×8+2×16=88;(2) 化合物中元素的质量比=(相对原子质量×原子个数)之比,乙酸乙酯中碳、氢元素的质量比为4×12:1×8=6:1;⑶,17.6 g乙酸乙酯中所含氧元素的质量为17.6 g× =6.4g
备用题
(2017·丽水)儿童缺锌会引起食欲不振、发育不良等症状。如图为某补锌口服液说明书的部分信息,回答下列问题:
(1)葡萄糖酸锌由 种元素组成;
(2)葡萄糖酸锌中碳、氢元素的质量比为 ;
(3)要满足儿童身体正常的需要,在某一时间段需要适量补锌。若儿童1千克体重每日需要0.5毫克锌,每天从食物中只能摄入所需锌的一半。体重为20千克的儿童,理论上一天还需服该口服液多少支?
【答案】(1)四 (2)72:11(3)1支
2017?六盘水)元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
(l)溴的相对原子质量是_______。
(2)溴元素的化学性质与图二哪种元素的化学性质相似_______(填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为:_______。
(4)若图二中C表示离子,则离子符号是_______。
【答案】(1)79.90;(2)B;(3)KBr;(4)S2-;
1、(2017·济宁)观看足球比赛时,经常会看到绿茵场上运动员因拼抢摔倒受伤,医生向受伤部位喷射氯乙烷(CH3CH2Cl),并用药棉不断揉搓,运动员疼痛很快消除,重新投入比赛.
请阅读信息后,回答:
(1)氯乙烷中C、H、Cl三种元素的原子个数比为 ;
(2)氯乙烷中C、H、Cl三种元素的质量比为 .
【解答】解:(1)由化学式可知,1个氯乙烷分子是由2个碳原子、5个氢原子和1个氯原子构成的,则氯乙烷中C、H、Cl三种元素的原子个数比为2:5:1;故填:2:5:1;
(2)氯乙烷中碳、氢、氯三种元素的质量比为(12×2):(1×5):(35.5×1)=48:10:71,故填:48:10:71.
(2017·福建)PLA是一种新型可降解塑料,以乳酸(C3H6O3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )【来源:21cnj*y.co*m】
A.乳酸是由碳、氢、氧三种元素组成
B.乳酸分子中含有12个原子
C.乳酸的相对分子质量是90
D.乳酸中氧元素的质量分数最大
(2017·青岛)太阳能吸附式制冷结露法空气取水器可用于野外获取淡
水,工作原理如下图所示。
(1)蒸发冷凝器中发生的是________
(填“物理”或“化学”)变化。
(2)吸附剂中主要物质为SiO2和CaCl2,
SiO2中硅元素的化合价为_________,CaCl2
中钙、氯元素的质量比为________。
【答案】
(1)物理(2)+4 40:71
【解析】
(1)由图可知,湿空气进入蒸发冷凝器中,将气态水变为液态水,最后进入到集水器中,整个过程水的状态发生改变,未生成新的物质,故为物理变化;
(2)SiO2中的Si元素的化合价为+4价,CaCl2中钙、氯元素的的质量比为40:35.5×2=40:71。
(2017·自贡)标出硝酸钠中各元素的化合价_______。
【答案】氮气;
【解析】
根据化合价的表示方法:在其化学式中该元素的正上
方用正负号和数字表示,且正负号在前,数字在后,
则硝酸钠中各元素的化合价表示为 。
(2017·聊城)地壳中元素含量(质量分数)由高到低依次是氧、硅、铝、铁等.如图分别是硅元素在元素周期表中的信息和铝元素的原子结构示意图.请回答下列问题:
(1)硅原子的核外电子数是 14 .
(2)铝离子的符号 Al3+ .
(3)铁在地壳中主要以铁矿石的形式存在,其中赤铁矿的主要成分是Fe2O3.Fe2O3中铁元素的化合价为 +3 价.
【解答】解:(1)由元素周期表的信息可知,硅元素的原子序数为14,因为在原子中,原子序数=质子数=核外电子数,所以硅原子的核外电子数为14;故填:14;
(2)由铝原子结构示意图可知,铝原子的最外层有3个电子,在化学反应易失去最外层的三个电子而形成带有三个单位正电荷的铝离子,其离子符号为Al3+;故填:Al3+;
(3)氧化铁中,氧元素显﹣2价,设铁元素的化合价为x,则2x+(﹣2)×3=0,x=+3;故填:+3.
(2017·威海)2017年1月27日,南京理工大学化学学院胡炳成团队成功合成世界上首个超高能全氨阴离子(N5-)钴(Co)盐【化学式为:Co(N5)2(H2O)4】。下列有关说法正确的是
A.该物质属于混合物 B.该物质中钴元素的质量分数比氧元素的质量分数小
C.该物质中钴元素的化合价为+5价 D.该物质属于有机物
【答案】B
【解析】A、由化学式可知该物质有固定的组成和结构,是纯净物,B.该物质中钻元素的质量分数比氧元素的质量分数小;C.化合物中元素的化合价的代数和为零,离子带电荷的数值等于该元素的化合价的数值,全氨阴离子(N5-),故该物质中钴元素的化台价为+1价;D.除一氧化碳、二氧化碳、碳酸、碳酸盐以外的含碳化合物称为有机物。该物质没有碳元素,属于无机物;选B
(2017·潍坊)我国自主研制的首艘货运飞船“天舟一号”已于2017年4月20日发射成功,这标志着我国航天事业又跨入了一个崭新的时代。肼(N2H4)是航天事业的功臣,常用作火箭燃料。下列有关肼的说法正确的是
A.肼是一种混合物 B.一个N2H4分子由1个N2分子和2个H2分子组成
C.肼的化学式可简写为NH2 D.N2H4的相对分子质量为32
【答案】D
【解析】A、由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;肼是化合物;B化学式中元素符号右下角的数字是一个分子中原子的个数,所以一个N2H4分子由2个氮原子和4个氢原子构成;C化学式表示一个分子,构成物质的分子是一定的,所以肼的化学式不可简写为NH2;D相对分子质量=(相对原子质量×原子个数)之和,N2H4的相对分子质量为32;选D
(2017·广州)N(NO2)3是科学家近年发现的一种新型火箭燃料。下列关于N(NO2)3说法正确的是
A.N(NO2)3的相对分子质量为152
B.N(NO2)3中氮元素与氧元素的质量比是2:3
C.N(NO2)3中总共有3个N原子和6个O原子
D.N(NO2)3中氮元素的质量分数为
【答案】A
【解析】N(NO2)3的相对分子质量为14×4+16×6=152;N(NO2)3中氮元素与氧元素的质量比是(14×4):(16×6)=7:12;N(NO2)3的一个分子中共有3个N原子和6个O原子;N(NO2)3中氮元素的质量分数为,故选A。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
