18.4 玻尔原子模型 16张PPT
文档属性
| 名称 | 18.4 玻尔原子模型 16张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2019-03-12 00:00:00 | ||
图片预览






文档简介
玻尔的原子模型
19世纪末20世纪初,人类叩开了微观世界的大门,物理学家根据有研究提出了关于原子结构的各种模型,卢瑟福的核式结构模型能够很好的解释实验现象,得到了多数人的支持,但是与经典的电磁理论发生了矛盾.
按照经典物理学的观点去推断,在轨道上运动的电子带有电荷,运动中要辐射电磁波,电子损失了能量,其轨道半径不断缩小,最终落在原子核上.由于电子轨道的变化是连续的,辐射电磁波的频率也会连续变化.
??事实上,原子是稳定的,辐射电磁波的频率也只是某些确定的值.
1、围绕原子核运动的电子轨道半径只能是某些分立的数值,这些现象叫做轨道量子化;
2、不同的轨道对应着不同的状态,在这些状态中,尽管电子在做变速运动,却不辐射能量,因此这些状态是稳定的;
3、原子在不同的状态之中具有不同的能量,所以原子的能量也是量子化的。
1913年玻尔提出了自己的原子结构假说
玻尔
?玻尔从上述假设出发,利用库仑定律和牛顿运动定律,计算出了氢的电子可能的轨道半径和对应的能量.
氢原子能级
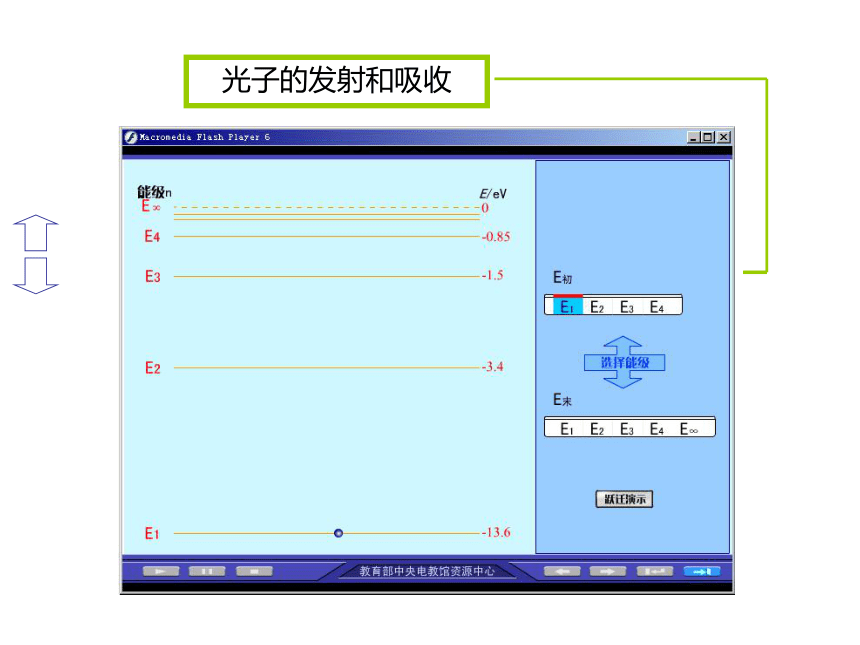
光子的发射和吸收
原子也可以从激发态向基态跃迁,电子所受库仑力做正功减小电势能,原子的能量减少要辐射出能量,这一能量以光子的形式放出.
原子最低能级所对应的状态叫做基态,比基态能量高的状态叫激发态.
原子从基态向激发态跃迁,电子克服库仑引力做功增大电势能,原子的能量增加要吸收能量.
光子的发射和吸收
原子在始、末两个能级Em和En( Em>En )间跃迁时发射光子的频率可以由下式决定:
光子的发射和吸收
人们早在了解原子内部结构之前就已经观察到了气体光谱,不过那时候无法解释为什么气体光谱只有几条互不相连的特定谱线,玻尔理论很好的解释了氢原子的光谱.
人们早在了解原子内部结构之前就已经观察到了气体光谱,不过那时候无法解释为什么气体光谱只有几条互不相连的特定谱线,玻尔理论很好的解释了氢原子的光谱.
??原子从高能级跃迁到低能级时,辐射光子的能量等于前后两个能级之差.由于原子的能级不连续,所以辐射的光子的能量也不连续,从光谱上看,原子辐射光波的频率只有若干分立的值.
玻尔理论成功的解释并预言了氢原子辐射的电磁波的问题,但是也有它的局限性.
在解决核外电子的运动时成功引入了量子化的观念
同时又应用了“轨道”等经典概念和有关牛顿力学规律
??除了氢原子光谱外,在解决其他问题上遇到了很大的困难.
玻尔理论解决了原子的稳定性和辐射的频率条件问题,把原子结构的理论向前推进了一步 .
达标练习:
1、对玻尔理论的下列说法中,正确的是( )
A、继承了卢瑟福的原子模型,但对原子能量和电子轨道引入了量子化假设
B、对经典电磁理论中关于“做加速运动的电荷要辐射电磁波”的观点提出了异议
C、用能量转化与守恒建立了原子发光频率与原子能量变化之间的定量关系
D、玻尔的两个公式是在他的理论基础上利用经典电磁理论和牛顿力学计算出来的
ABCD
2、下面关于玻尔理论的解释中,不正确的说法是( )
A、原子只能处于一系列不连续的状态中,每个状态都对应一定的能量
B、原子中,虽然核外电子不断做加速运动,但只要能量状态不改变,就不会向外辐射能量
C、原子从一种定态跃迁到另一种定态时,一定要辐射一定频率的光子
D、原子的每一个能量状态都对应一个电子轨道,并且这些轨道是不连续的
C
3、根据玻尔理论,氢原子中,量子数N越大,则下列说法中正确的是( )
A、电子轨道半径越大 B、核外电子的速率越大
C、氢原子能级的能量越大 D、核外电子的电势能越大
4、根据玻尔的原子理论,原子中电子绕核运动的半径( )
A、可以取任意值 B、可以在某一范围内取任意值
C、可以取一系列不连续的任意值
D、是一系列不连续的特定值
D
ACD
5、按照玻尔理论,一个氢原子中的电子从一半径为ra的圆轨道自发地直接跃迁到一半径为rb的圆轨道上,已知ra>rb,则在此过程中( )
A、原子要发出一系列频率的光子
B、原子要吸收一系列频率的光子
C、原子要发出某一频率的光子
D、原子要吸收某一频率的光子
C
19世纪末20世纪初,人类叩开了微观世界的大门,物理学家根据有研究提出了关于原子结构的各种模型,卢瑟福的核式结构模型能够很好的解释实验现象,得到了多数人的支持,但是与经典的电磁理论发生了矛盾.
按照经典物理学的观点去推断,在轨道上运动的电子带有电荷,运动中要辐射电磁波,电子损失了能量,其轨道半径不断缩小,最终落在原子核上.由于电子轨道的变化是连续的,辐射电磁波的频率也会连续变化.
??事实上,原子是稳定的,辐射电磁波的频率也只是某些确定的值.
1、围绕原子核运动的电子轨道半径只能是某些分立的数值,这些现象叫做轨道量子化;
2、不同的轨道对应着不同的状态,在这些状态中,尽管电子在做变速运动,却不辐射能量,因此这些状态是稳定的;
3、原子在不同的状态之中具有不同的能量,所以原子的能量也是量子化的。
1913年玻尔提出了自己的原子结构假说
玻尔
?玻尔从上述假设出发,利用库仑定律和牛顿运动定律,计算出了氢的电子可能的轨道半径和对应的能量.
氢原子能级
光子的发射和吸收
原子也可以从激发态向基态跃迁,电子所受库仑力做正功减小电势能,原子的能量减少要辐射出能量,这一能量以光子的形式放出.
原子最低能级所对应的状态叫做基态,比基态能量高的状态叫激发态.
原子从基态向激发态跃迁,电子克服库仑引力做功增大电势能,原子的能量增加要吸收能量.
光子的发射和吸收
原子在始、末两个能级Em和En( Em>En )间跃迁时发射光子的频率可以由下式决定:
光子的发射和吸收
人们早在了解原子内部结构之前就已经观察到了气体光谱,不过那时候无法解释为什么气体光谱只有几条互不相连的特定谱线,玻尔理论很好的解释了氢原子的光谱.
人们早在了解原子内部结构之前就已经观察到了气体光谱,不过那时候无法解释为什么气体光谱只有几条互不相连的特定谱线,玻尔理论很好的解释了氢原子的光谱.
??原子从高能级跃迁到低能级时,辐射光子的能量等于前后两个能级之差.由于原子的能级不连续,所以辐射的光子的能量也不连续,从光谱上看,原子辐射光波的频率只有若干分立的值.
玻尔理论成功的解释并预言了氢原子辐射的电磁波的问题,但是也有它的局限性.
在解决核外电子的运动时成功引入了量子化的观念
同时又应用了“轨道”等经典概念和有关牛顿力学规律
??除了氢原子光谱外,在解决其他问题上遇到了很大的困难.
玻尔理论解决了原子的稳定性和辐射的频率条件问题,把原子结构的理论向前推进了一步 .
达标练习:
1、对玻尔理论的下列说法中,正确的是( )
A、继承了卢瑟福的原子模型,但对原子能量和电子轨道引入了量子化假设
B、对经典电磁理论中关于“做加速运动的电荷要辐射电磁波”的观点提出了异议
C、用能量转化与守恒建立了原子发光频率与原子能量变化之间的定量关系
D、玻尔的两个公式是在他的理论基础上利用经典电磁理论和牛顿力学计算出来的
ABCD
2、下面关于玻尔理论的解释中,不正确的说法是( )
A、原子只能处于一系列不连续的状态中,每个状态都对应一定的能量
B、原子中,虽然核外电子不断做加速运动,但只要能量状态不改变,就不会向外辐射能量
C、原子从一种定态跃迁到另一种定态时,一定要辐射一定频率的光子
D、原子的每一个能量状态都对应一个电子轨道,并且这些轨道是不连续的
C
3、根据玻尔理论,氢原子中,量子数N越大,则下列说法中正确的是( )
A、电子轨道半径越大 B、核外电子的速率越大
C、氢原子能级的能量越大 D、核外电子的电势能越大
4、根据玻尔的原子理论,原子中电子绕核运动的半径( )
A、可以取任意值 B、可以在某一范围内取任意值
C、可以取一系列不连续的任意值
D、是一系列不连续的特定值
D
ACD
5、按照玻尔理论,一个氢原子中的电子从一半径为ra的圆轨道自发地直接跃迁到一半径为rb的圆轨道上,已知ra>rb,则在此过程中( )
A、原子要发出一系列频率的光子
B、原子要吸收一系列频率的光子
C、原子要发出某一频率的光子
D、原子要吸收某一频率的光子
C
