2019年中考科学复习-化学-7、酸碱盐综合复习2
文档属性
| 名称 | 2019年中考科学复习-化学-7、酸碱盐综合复习2 |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-03-13 00:00:00 | ||
图片预览

文档简介
浙教版中考复习化学-7、酸碱盐综合复习2
一、一些常用化肥的名称和作用
氮肥 磷肥 钾肥 复合肥
举例 尿素CO(NH2)2硝酸铵NH4NO3 过磷酸钙:Ca(H2PO4)2和CaSO4的混合物 硫酸钾K2SO4氯化钾KCl草木灰主要成分K2CO3 磷酸二氢铵 NH4H2PO4硝酸钾KNO3
作用 氮是植物体内蛋白质、核酸和叶绿素的组成元素,氮肥提供植物生长所需的氮元素 磷肥可以促进植物生长,还可以增强作物的抗寒抗旱能力 保证植物各种新陈代谢过程顺利进行,促进植物生长,增强抗病虫害和抗倒伏的能力 能同时均匀的供给作物集中养分,充分发挥营养元素间的相互作用,有效成分高
影响 缺氮会造成植物生长发育缓慢或停滞,光合作用减慢,品质下降 缺磷的植物生长迟缓,产量降低,过量会引起作物晚熟,结实率下降 缺钾:抗性下降。植株茎干柔弱,易倒伏,抗旱、抗寒性降低。叶色变黄、叶缘焦枯。
铵态氮肥的检验:加入熟石灰研磨,产生有刺激性气味的气体
.酸碱性对生命活动和农作物生长的影响
化工生产中许多反应必须在一定的pH溶液里才能进行;农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长;测定雨水的pH可以了解空气的污染情况(因为溶解有二氧化碳,正常雨水的pH约为5.6,酸雨的pH小于5.6);测定人体内或排出液体的pH。可以了解人体的健康情况。
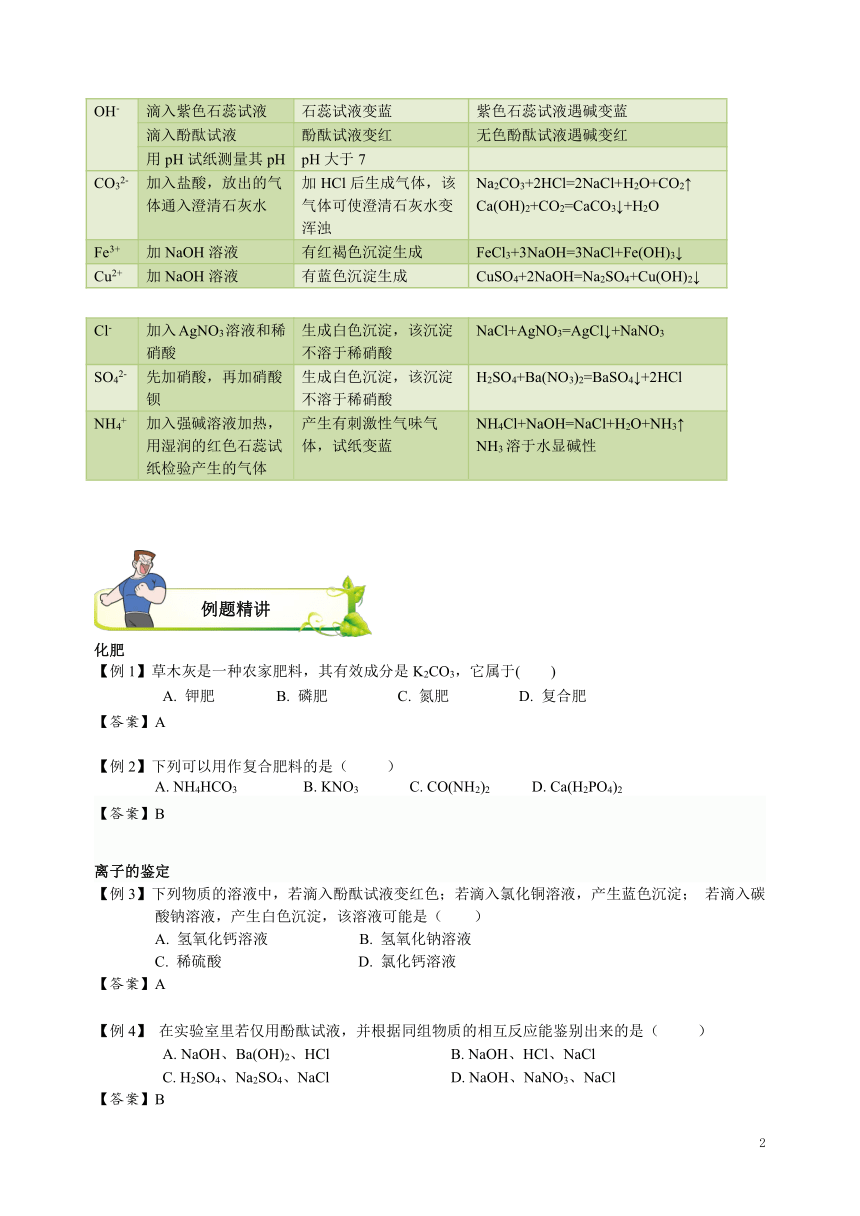
二、溶液中常见离子的检验
离子 检验方法 现象 结论或化学方程式
H+ 滴入紫色石蕊试液 石蕊试液变红 紫色石蕊试液遇酸变红
加入锌粒 有无色无味气体放出 Zn+2HCl=ZnCl2+H2↑
用pH试纸测量其pH pH小于7
OH- 滴入紫色石蕊试液 石蕊试液变蓝 紫色石蕊试液遇碱变蓝
滴入酚酞试液 酚酞试液变红 无色酚酞试液遇碱变红
用pH试纸测量其pH pH大于7
CO32- 加入盐酸,放出的气体通入澄清石灰水 加HCl后生成气体,该气体可使澄清石灰水变浑浊 Na2CO3+2HCl=2NaCl+H2O+CO2↑Ca(OH)2+CO2=CaCO3↓+H2O
Fe3+ 加NaOH溶液 有红褐色沉淀生成 FeCl3+3NaOH=3NaCl+Fe(OH)3↓
Cu2+ 加NaOH溶液 有蓝色沉淀生成 CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
Cl- 加入AgNO3溶液和稀硝酸 生成白色沉淀,该沉淀不溶于稀硝酸 NaCl+AgNO3=AgCl↓+NaNO3
SO42- 先加硝酸,再加硝酸钡 生成白色沉淀,该沉淀不溶于稀硝酸 H2SO4+Ba(NO3)2=BaSO4↓+2HCl
NH4+ 加入强碱溶液加热,用湿润的红色石蕊试纸检验产生的气体 产生有刺激性气味气体,试纸变蓝 NH4Cl+NaOH=NaCl+H2O+NH3↑NH3溶于水显碱性
化肥
【例1】草木灰是一种农家肥料,其有效成分是K2CO3,它属于( )
A. 钾肥 B. 磷肥 C. 氮肥 D. 复合肥
【答案】A
【例2】下列可以用作复合肥料的是( )
A. NH4HCO3 B. KNO3 C. CO(NH2)2 D. Ca(H2PO4)2
【答案】B
离子的鉴定
【例3】下列物质的溶液中,若滴入酚酞试液变红色;若滴入氯化铜溶液,产生蓝色沉淀; 若滴入碳
酸钠溶液,产生白色沉淀,该溶液可能是( )
A. 氢氧化钙溶液 B. 氢氧化钠溶液
C. 稀硫酸 D. 氯化钙溶液
【答案】A
【例4】 在实验室里若仅用酚酞试液,并根据同组物质的相互反应能鉴别出来的是( )1世
A. NaOH、Ba(OH)2、HCl B. NaOH、HCl、NaCl
C. H2SO4、Na2SO4、NaCl D. NaOH、NaNO3、NaCl
【答案】B
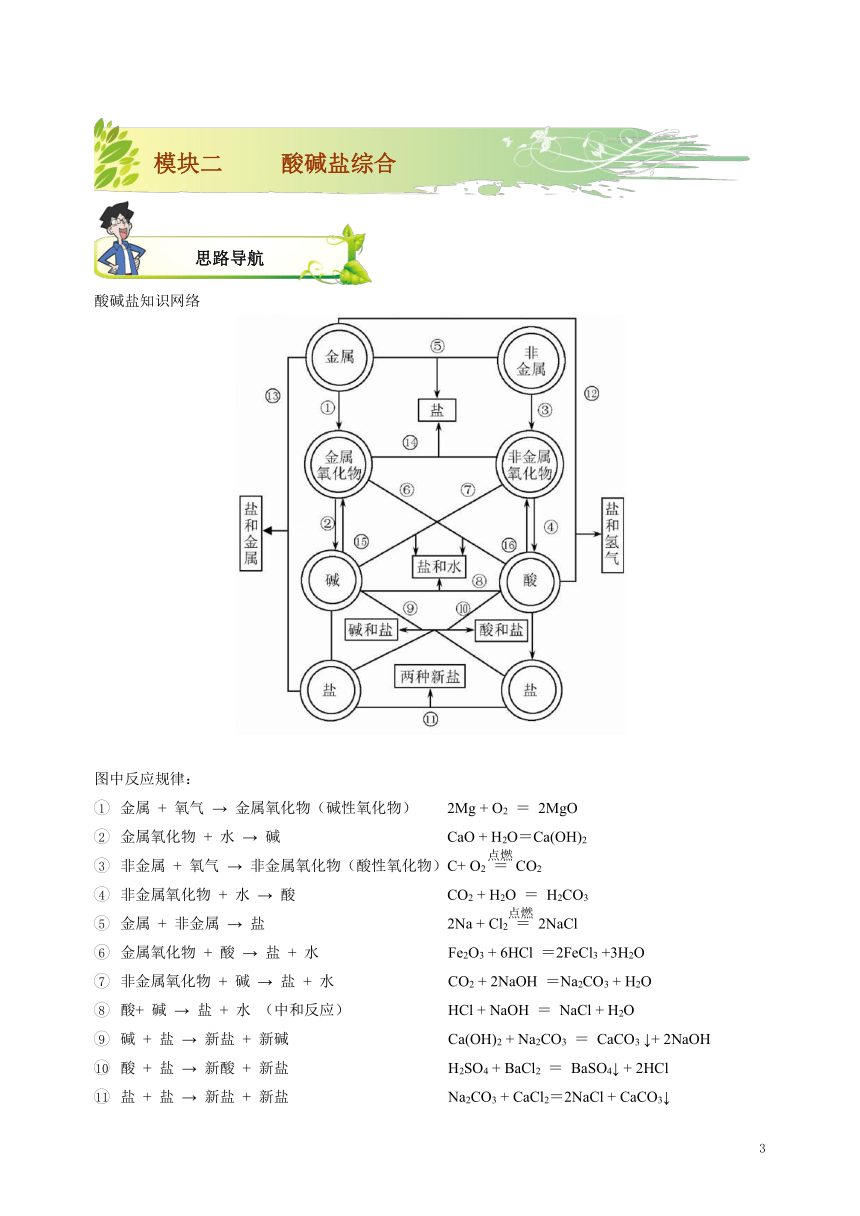
酸碱盐知识网络
图中反应规律:
金属 + 氧气 → 金属氧化物(碱性氧化物) 2Mg + O2 = 2MgO
金属氧化物 + 水 → 碱 CaO + H2O=Ca(OH)2
非金属 + 氧气 → 非金属氧化物(酸性氧化物)C+ O2 = CO2
非金属氧化物 + 水 → 酸 CO2 + H2O = H2CO3
金属 + 非金属 → 盐 2Na + Cl2 = 2NaCl
金属氧化物 + 酸 → 盐 + 水 Fe2O3 + 6HCl =2FeCl3 +3H2O
非金属氧化物 + 碱 → 盐 + 水 CO2 + 2NaOH =Na2CO3 + H2O
酸+ 碱 → 盐 + 水 (中和反应) HCl + NaOH = NaCl + H2O
碱 + 盐 → 新盐 + 新碱 Ca(OH)2 + Na2CO3 = CaCO3 ↓+ 2NaOH
酸 + 盐 → 新酸 + 新盐 H2SO4 + BaCl2 = BaSO4↓ + 2HCl
盐 + 盐 → 新盐 + 新盐 Na2CO3 + CaCl2=2NaCl + CaCO3↓
金属 + 酸 → 盐 + 氢气 Zn + H2SO4 = ZnSO4 + H2↑
金属 + 盐 → 新金属 + 新盐 Fe + CuCl2 = Cu + FeCl2
图表图像类
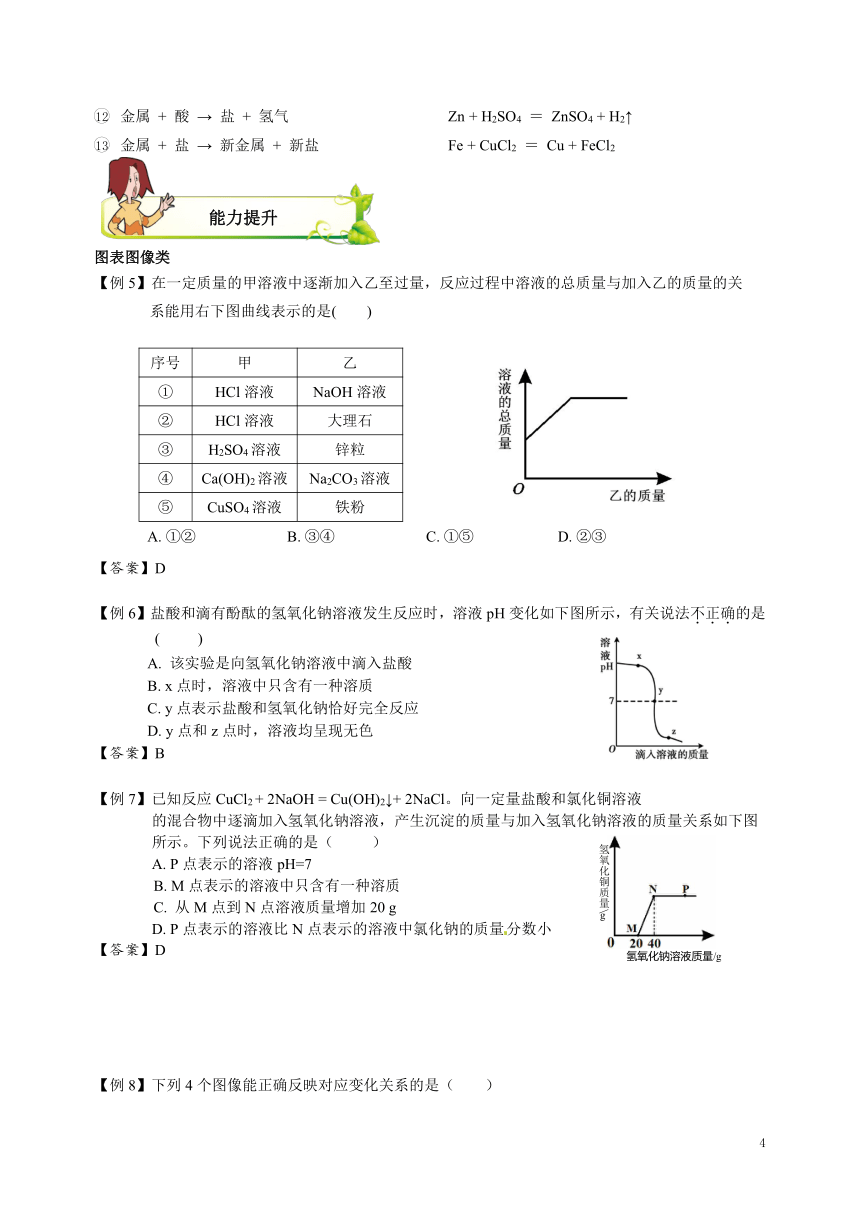
【例5】在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关
系能用右下图曲线表示的是( )
序号 甲 乙
① HCl溶液 NaOH溶液
② HCl溶液 大理石
③ H2SO4溶液 锌粒
④ Ca(OH)2溶液 Na2CO3溶液
⑤ CuSO4溶液 铁粉
A. ①② B. ③④ C. ①⑤ D. ②③
【答案】D
【例6】盐酸和滴有酚酞的氢氧化钠溶液发生反应时,溶液pH变化如下图所示,有关说法不正确的是
( )
A. 该实验是向氢氧化钠溶液中滴入盐酸
B. x点时,溶液中只含有一种溶质
C. y点表示盐酸和氢氧化钠恰好完全反应
D. y点和z点时,溶液均呈现无色
【答案】B
【例7】已知反应CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl。向一定量盐酸和氯化铜溶液
的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如下图
所示。下列说法正确的是( )[来源:Z|xx|k.Com]
A. P点表示的溶液pH=7
B. M点表示的溶液中只含有一种溶质
C. 从M点到N点溶液质量增加20 g
D. P点表示的溶液比N点表示的溶液中氯化钠的质量分数小
【答案】D
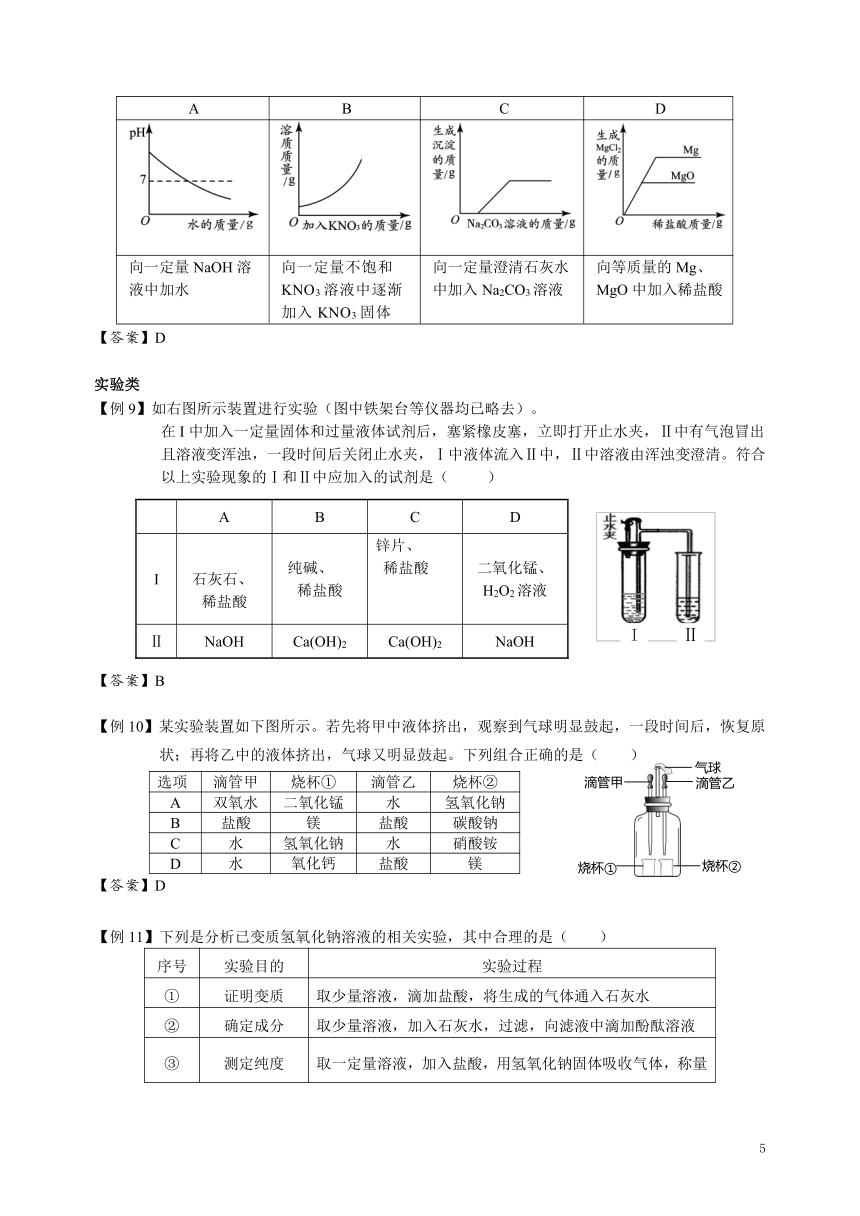
【例8】下列4个图像能正确反映对应变化关系的是( )
A B C D
向一定量NaOH溶液中加水 向一定量不饱和KNO3溶液中逐渐加入KNO3固体 向一定量澄清石灰水中加入Na2CO3溶液 向等质量的Mg、MgO中加入稀盐酸
【答案】D
实验类
【例9】如右图所示装置进行实验(图中铁架台等仪器均已略去)。
在I中加入一定量固体和过量液体试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出
且溶液变浑浊,一段时间后关闭止水夹,Ⅰ中液体流入Ⅱ中,Ⅱ中溶液由浑浊变澄清。符合
以上实验现象的Ⅰ和Ⅱ中应加入的试剂是( )
A B C D
I 石灰石、[来稀盐酸 纯碱、稀盐酸 锌片、 稀盐酸[来源:Z+xx+k.Com] 二氧化锰、 H2O2溶液
Ⅱ NaOH Ca(OH)2 Ca(OH)2 NaOH
【答案】B
【例10】某实验装置如下图所示。若先将甲中液体挤出,观察到气球明显鼓起,一段时间后,恢复原
状;再将乙中的液体挤出,气球又明显鼓起。下列组合正确的是( )
选项 滴管甲 烧杯① 滴管乙 烧杯②
A 双氧水 二氧化锰 水 氢氧化钠
B 盐酸 镁 盐酸 碳酸钠
C 水 氢氧化钠 水 硝酸铵
D 水 氧化钙 盐酸 镁
【答案】D
【例11】下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是( )
序号 实验目的 实验过程
① 证明变质 取少量溶液,滴加盐酸,将生成的气体通入石灰水
② 确定成分 取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液
③ 测定纯度 取一定量溶液,加入盐酸,用氢氧化钠固体吸收气体,称量
④ 除去杂质 取溶液,滴加石灰水至恰好完全反应,过滤
A. ②③ B. ①③ C. ②④ D. ①④
【答案】D
【例12】实验室有四瓶未贴标签的无色溶液,分别是稀盐酸、饱和石灰水、氢氧化钠溶液和碳酸钠溶
液。欲鉴别这四种溶液,三位同学设计了不同的实验方案。
【小花方案】小花将四瓶溶液编号,借助pH试纸进行实验,并将实验过程记录如下。
实验步骤 实验现象 实验结论
① B溶液的pH<7, 其余溶液的pH>7
②分别取少量的A、C、D溶液于三支试管,各滴加适量B溶液 其余溶液无明显变化 A是碳酸钠溶液
③ C溶液变浑浊, D中无明显变化 C是饱和石灰水 D是氢氧化钠溶液
【小刚方案】
小刚将四瓶溶液重新编号,各取少量溶液于四支试管中,分别加热。A中产生刺激性的气味,B、
C无明显变化,D中溶液变浑浊。冷却后,再取少量澄清D溶液滴入B、C中,B无明显变化,
C溶液变浑浊。通过以上实验,小刚也能鉴别出四种溶液。其中A溶液是 ;加热D溶
液变浑浊的原因是 。
【小明方案】小明又将四瓶溶液重新编号,分别取少量溶液于试管中,将试管中的溶液两两混合,
实验现象如右图所示。(“↓”表示有沉淀产生,“↑”表示有气体产生,“—”表示无明显
变化)
通过以上实验,小明也能鉴别出四种溶液。其中A溶液是 ;C与D反应的化学方程
式是 。
【实验反思】若各取等质量的四种溶液两两混合,混合后溶液的总质量减少,则可能的组合
是 。(填化学式)
【答案】
【小花方案】①用干净滴管分别吸取少量四种被测液,滴到四片pH试纸上,把试纸显示的颜色与标准比色卡比较
②A溶液中有气泡冒出
③分别取少量的C、D溶液于两支试管中,各滴加适量A溶液
【小刚方案】稀盐酸 氢氧化钙的溶解度随温度的升高而减小
【小明方案】碳酸钠 NaOH + HCl = NaCl + H2O
【实验反思】Ca(OH)2、Na2CO3和HCl、Na2CO3
【例13】在“课内比教学”活动中,老师和化学兴趣小组的同学一起对初中化学常
见物质进行了如下探究。
【活动与探究一】
右图是实验室制汽水配方。为了检验汽水中是否含有二氧化碳,小
燕和小苗设计了如下两个实验方案:
小燕:取汽水样品于试管中,滴入紫色石蕊溶液,观察到
溶液 。
小苗:振荡汽水瓶,将产生的气体通入澄清石灰水,观察到
澄清石灰水 ,该反应的化学方程式是 。
以上两个方案中,我认为 (填“小燕”或“小苗”)的方案是正确的。
【活动与探究二】
有一包粉末可能含有铁和氧化铜中的一种或二种,小艺进行如下探究。
实验步骤 实验现象 实验结论
取少量粉末于试管中,加入过量稀硫酸。 可观察到的现象有 (填序号)。①有气泡产生;②溶液颜色有明显变化;③反应结束后试管中仍有少量固体。 粉末中含有铁和氧化铜
写出其中任意一个反应的化学方程式 。
【活动与探究三】
实验桌上老师提供了六瓶失去标签的无色溶液,分别是碳酸钠、盐酸、氯化钠、硫酸锌、氢氧化
钠和氢氧化钡,为了区分它们,给六瓶溶液编号为A、B、C、D、E、F。小组同学进行如下探究:
资料: ZnCO3和Zn(OH)2均为难溶于水的白色沉淀
实验步骤和现象 实验结论
步骤一 A是 溶液, (填化学式,下同) B是 溶液,
步骤二 C是 溶液。
小组同学发现利用A、B、C三种溶液可以确定D、E、F的成份,他们进一步展开如下探究:
实验步骤 实验现象 实验目的
步骤三 D、E、F溶液中的现象分别是 。 确定F溶液成份。
步骤四 D、E溶液中的现象分别是 。 确定D、E溶液成份。
【答案】【活动与探究一】
变红 变浑浊 CO2 + Ca(OH)2 = CaCO3 ↓+ H2O ,小苗
【活动与探究二】
①②③
Fe+H2SO4=FeSO4+H2↑ 或 CuO+H2SO4=CuSO4+ H2O或Fe +CuSO4=FeSO4+Cu
【活动与探究三】
A是HCl B是Na2CO3 C是ZnSO4
产生白色沉淀 产生白色沉淀 无明显现象
B 产生白色沉淀 无明显现象 (D、E中现象可以交换)
【例14】小丽来到实验室,看到实验桌上有一瓶敞口放置的氢氧化钠固体,于是对其是否变质产生了
兴趣。她和同学们准备对这瓶固体进行探究。
【查阅资料】a.碳酸钠溶液显碱性,氯化钙溶液呈中性。
b.碳酸钠溶液与氯化钙溶液可以发生反应:Na2CO3 + CaCl2=CaCO3↓+2NaCl。
【作出猜想】猜想1.固体没有变质
猜想2.固体部分变质
猜想3.
【设计方案】
实验操作 实验现象 实验结论
方案一 取少量固体放入试管中,滴加几滴稀盐酸 无明显现象 猜想1正确
方案二 取少量固体放入试管中加水溶解,滴加足量澄清石灰水 产生白色沉淀 猜想2正确
取上层清液放入另一只试管中,滴加酚酞溶液 溶液变为红色
同学们经过讨论,认为两个方案都不合理。方案一不合理的原因是 ;
方案二不合理的原因是 。同学们重新设计了方案并进行了实验。
【实验探究】
实验操作 实验现象 实验结论
取少量固体放入试管中加水溶解,滴加足量 产生白色沉淀 猜想2正确
取上层清液放入另一只试管中,滴加酚酞溶液
若猜想3正确,该实验的现象应该是 。
【继续探究】同学们继续探究该氢氧化钠固体样品中碳酸钠的质量分数。利用以下装置进行
了实验。
你认为她们需要测的数据是 (填字母序号)。
a.固体样品的质量 b.碱石灰实验前后的质量
c.浓硫酸实验前后的质量 d.氢氧化钠溶液实验前后的质量
e.所用稀硫酸的质量
【实验反思】根据所得数据进行计算发现结果比实际偏小,原因可能是 。
【答案】【作出猜想】固体完全变质
【设计方案】
方案一:若样品变质,加入的少量稀盐酸先与NaOH反应,无明显现象;若样品完全变质,
加入的几滴稀盐酸与Na2CO3反应,产生NaHCO3,也无明显现象
方案二:碳酸钠与石灰水反应产生的氢氧化钠也能使滤液中的酚酞变红
【实验探究】
实验操作 实验现象 实验结论
CaCl2溶液
溶液由无色变为变红色
滴加足量CaCl2后产生白色沉淀,取上层清液滴加酚酞溶液后不变色
【继续探究】ad
【实验反思】A、B容器内还有剩余的CO2没有完全被氢氧化钠吸收
【练习1】向盛有某液体的烧杯中逐滴加入x溶液至过量(如图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )
烧杯中的物质 x溶液
A H2SO4和CuSO4溶液 NaOH溶液
B NaHCO3和NaCl溶液 稀盐酸
C 镁铝合金 稀盐酸
D 稀盐酸和稀硫酸 Na2CO3溶液
【答案】A
【练习2】下列图像与所述实验相符的是 ( )
① ② ③ ④
A. ①表示向一定量锌粒中加入过量稀硫酸
B. ②表示向一定量氯化钠饱和溶液中不断加水
C. ③表示向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水
D. ④表示20℃时,向一定量不饱和的硝酸钾溶液中加入过量的硝酸钾晶体
【答案】D
【练习3】根据右图函数图象分析得出的下列结论中,正确的是( )
① x可以表示向水中加入稀硫酸的过程
② x可以表示向水中加入氢氧化钠溶液的过程
③ y可以表示向水中加入食盐的过程
④ z可以表示向盐酸中加入水的过程
⑤ z可以表示向盐酸中加入氢氧化钠的过程
A.①③④ B.②③④ C.②③⑤ D.②③④⑤
【答案】B
模块一 化肥及离子的鉴定
例题精讲
模块二 酸碱盐综合
思路导航
点燃
点燃
能力提升
氢氧化铜质量\
氢氧化钠溶液质量/g
g
Ⅱ
I
气球
滴管甲
滴管乙
烧杯①
烧杯②
复习巩固
图1
图2
X溶液质量/g
沉淀
或气体质
量/g
1
