2019年中考科学总复习第31讲 质量守恒定律及化学方程式(精练)(课件 17张PPT)
文档属性
| 名称 | 2019年中考科学总复习第31讲 质量守恒定律及化学方程式(精练)(课件 17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 917.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-03-24 00:00:00 | ||
图片预览




文档简介
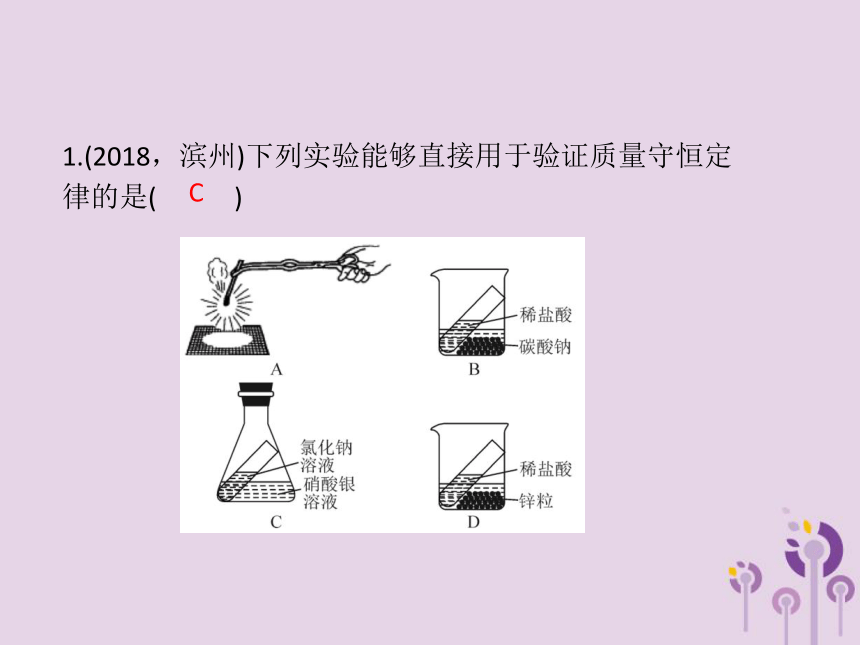
课件17张PPT。1.(2018,滨州)下列实验能够直接用于验证质量守恒定律的是( )C2.(2018,长沙)根据化学方程式不能获得该反应的信息是( )
A.化学反应的快慢 B.生成物
C.反应条件 D.反应物
3.(2018,襄阳)下列关于催化剂的说法正确的是( )
A.化学反应前后催化剂的质量不变
B.化学反应前后催化剂的性质不变
C.催化剂只能加快化学反应速率
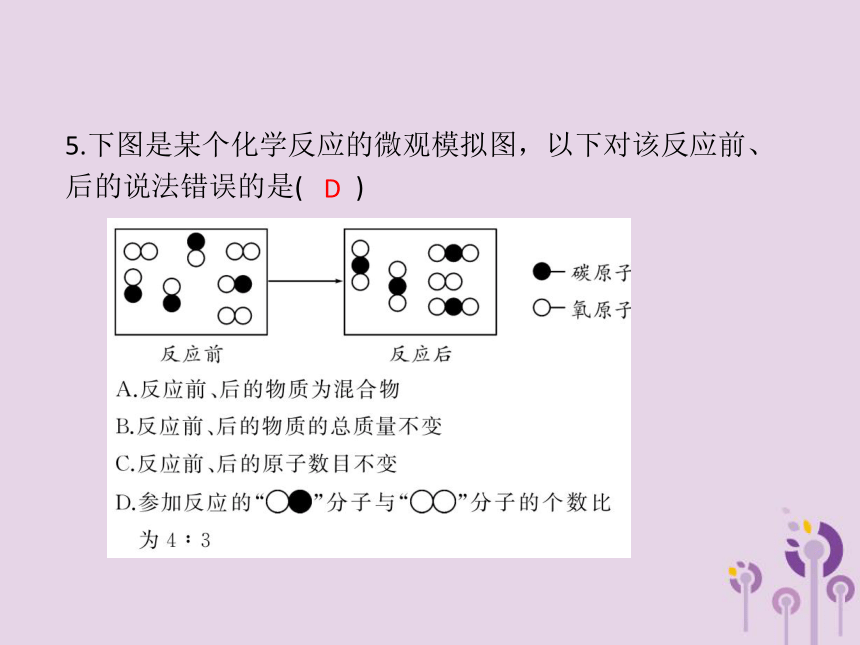
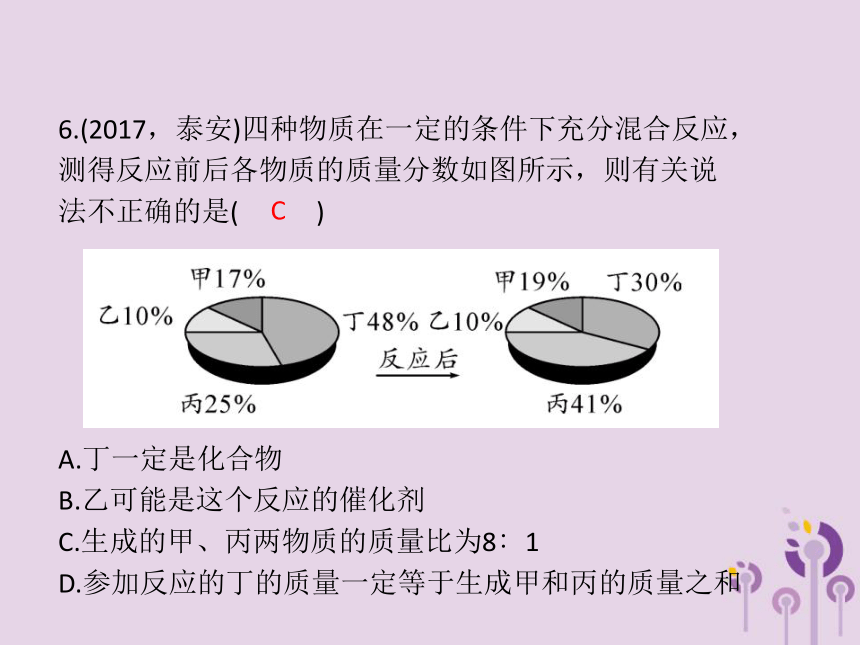
D.没有催化剂化学反应不能发生AA5.下图是某个化学反应的微观模拟图,以下对该反应前、后的说法错误的是( )D6.(2017,泰安)四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法不正确的是( )
A.丁一定是化合物
B.乙可能是这个反应的催化剂
C.生成的甲、丙两物质的质量比为8∶1
D.参加反应的丁的质量一定等于生成甲和丙的质量之和C7.(2018,南通)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X。取一定质量的AgNO3固体充分光照,测得反应后生成Ag、O2、X的质量分别为21.6 g、mg、9.2 g。下列说法正确的是( )
A.AgNO3固体应密封保存在无色细口瓶中
B.m=3.2
C.X的化学式为NO
D.该反应方程式中Ag与O2的化学计量数之比为3∶2B10.(2018,天津)在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7∶8,当2.8 gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.9.6 g B.8.8 g C.6.8 g D.4.4 gB12.(2018,温州)二氧化锰和过氧化氢酶均能催化过氧化氢分解制取氧气。为比较两者的催化能力,小明按图甲所示装置进行了如下实验。①取1.5毫克过氧化氢酶和8毫升蒸馏水加入容器中,搅拌后塞紧橡皮塞。
②用注射器A从容器中抽出2毫升气体,用注射器B将2毫升H2O2溶液注入容器中,采集数据。直至反应结束。
③用3.1毫克、5.6毫克过氧化氢酶及1.5毫克、5.6毫克、10.7毫克二氧化锰重复上述实验,获取数据如图乙。
(1)步骤②将注射器B中的2mL H2O2溶液全部注入容器前,用注射器A先从容器中抽出2毫升气体,其目的是
。调整密闭容器内的压强,使得测定结果更准确(2)小明分析相关数据,得出“过氧化氢酶对过氧化氢的催化能力比二氧化锰强”这一结论,其依据是
。
(3)查阅资料得知:过氧化氢分解为放热反应。小明推测:过氧化氢酶质量过大,可能导致实验过程中过氧化氢分解突然变慢。请说明其理由:
在相同时间内,加入过氧化氢酶的容器内压强更大过氧化氢酶质量过大反应速率加快,过氧化氢酶的活性受热后降低,所以催化效果减弱,反应速率突然变慢 。13.(2017,杭州)在海底和冻土层存在着储量巨大的“天然气水合物”,具有良好开发和应用前景。有科学家开采得到一种天然气水合物样品,取95.6克样品放置在一密闭容器内,该样品迅速转化为甲烷气体(CH4)和水,将甲烷气体分离并完全燃烧,得到35.2克二氧化碳。求该天然气水合物样品中甲烷的质量分数。(精确到0.1%)14.(2018,台州)某同学用如图装置验证质量守恒定律。称取一定质量的碳酸钠装入气球,将气球套在锥形瓶上。将药品全部倒入装有足量稀盐酸的锥形瓶中,气球迅速胀大。称量反应前后装置的总质量,实验数据如下表所示。(1)计算第1次反应产生的二氧化碳质量。
(2)分析数据发现每次反应前后装置的总质量均不相等,请以第1次反应为例,通过计算说明该反应是否遵循质量守恒定律。(空气密度取1.3克/升,二氧化碳密度取2.0克/升,结果精确到0.01)
A.化学反应的快慢 B.生成物
C.反应条件 D.反应物
3.(2018,襄阳)下列关于催化剂的说法正确的是( )
A.化学反应前后催化剂的质量不变
B.化学反应前后催化剂的性质不变
C.催化剂只能加快化学反应速率
D.没有催化剂化学反应不能发生AA5.下图是某个化学反应的微观模拟图,以下对该反应前、后的说法错误的是( )D6.(2017,泰安)四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法不正确的是( )
A.丁一定是化合物
B.乙可能是这个反应的催化剂
C.生成的甲、丙两物质的质量比为8∶1
D.参加反应的丁的质量一定等于生成甲和丙的质量之和C7.(2018,南通)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X。取一定质量的AgNO3固体充分光照,测得反应后生成Ag、O2、X的质量分别为21.6 g、mg、9.2 g。下列说法正确的是( )
A.AgNO3固体应密封保存在无色细口瓶中
B.m=3.2
C.X的化学式为NO
D.该反应方程式中Ag与O2的化学计量数之比为3∶2B10.(2018,天津)在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7∶8,当2.8 gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.9.6 g B.8.8 g C.6.8 g D.4.4 gB12.(2018,温州)二氧化锰和过氧化氢酶均能催化过氧化氢分解制取氧气。为比较两者的催化能力,小明按图甲所示装置进行了如下实验。①取1.5毫克过氧化氢酶和8毫升蒸馏水加入容器中,搅拌后塞紧橡皮塞。
②用注射器A从容器中抽出2毫升气体,用注射器B将2毫升H2O2溶液注入容器中,采集数据。直至反应结束。
③用3.1毫克、5.6毫克过氧化氢酶及1.5毫克、5.6毫克、10.7毫克二氧化锰重复上述实验,获取数据如图乙。
(1)步骤②将注射器B中的2mL H2O2溶液全部注入容器前,用注射器A先从容器中抽出2毫升气体,其目的是
。调整密闭容器内的压强,使得测定结果更准确(2)小明分析相关数据,得出“过氧化氢酶对过氧化氢的催化能力比二氧化锰强”这一结论,其依据是
。
(3)查阅资料得知:过氧化氢分解为放热反应。小明推测:过氧化氢酶质量过大,可能导致实验过程中过氧化氢分解突然变慢。请说明其理由:
在相同时间内,加入过氧化氢酶的容器内压强更大过氧化氢酶质量过大反应速率加快,过氧化氢酶的活性受热后降低,所以催化效果减弱,反应速率突然变慢 。13.(2017,杭州)在海底和冻土层存在着储量巨大的“天然气水合物”,具有良好开发和应用前景。有科学家开采得到一种天然气水合物样品,取95.6克样品放置在一密闭容器内,该样品迅速转化为甲烷气体(CH4)和水,将甲烷气体分离并完全燃烧,得到35.2克二氧化碳。求该天然气水合物样品中甲烷的质量分数。(精确到0.1%)14.(2018,台州)某同学用如图装置验证质量守恒定律。称取一定质量的碳酸钠装入气球,将气球套在锥形瓶上。将药品全部倒入装有足量稀盐酸的锥形瓶中,气球迅速胀大。称量反应前后装置的总质量,实验数据如下表所示。(1)计算第1次反应产生的二氧化碳质量。
(2)分析数据发现每次反应前后装置的总质量均不相等,请以第1次反应为例,通过计算说明该反应是否遵循质量守恒定律。(空气密度取1.3克/升,二氧化碳密度取2.0克/升,结果精确到0.01)
同课章节目录
