人教版高中化学选修5课件:1.4 研究有机化合物的一般步骤和方法(36张PPT)
文档属性
| 名称 | 人教版高中化学选修5课件:1.4 研究有机化合物的一般步骤和方法(36张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 839.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-07 00:00:00 | ||
图片预览











文档简介
课件36张PPT。第四节 研究有机化合物的一般步骤和方法槟榔是我国的四大南药之一,《本草纲目》中记载,槟榔有“下水肿、通关节、健脾调中、治心痛
积聚”等诸多病症。但长期嚼食槟榔的人罹患口腔
癌的机率比一般人高20倍。在食用槟榔前,要研究
其中哪些是有害成分,哪些是有益成分。那么研究
有机物的方法还有哪些呢?1.了解研究有机化合物的一般步骤,掌握有机物分离、提纯的常用方法。
2.了解确定有机化合物结构的化学方法和某些物理方法(如质谱、红外光谱、核磁共振氢谱等) 。(重点)
3.初步了解测定 有机化合物的元素含量、相对分子质量的一般方法,并能根据其确定有机化合物的分子式 。(难点)【问题导入】1.从天然资源中提取的有机物成分,以及在工厂
生产、实验室合成的有机物往往都是混合物,如
何进行分离、提纯呢?2.要鉴定和研究未知有机物的结构和性质,需要
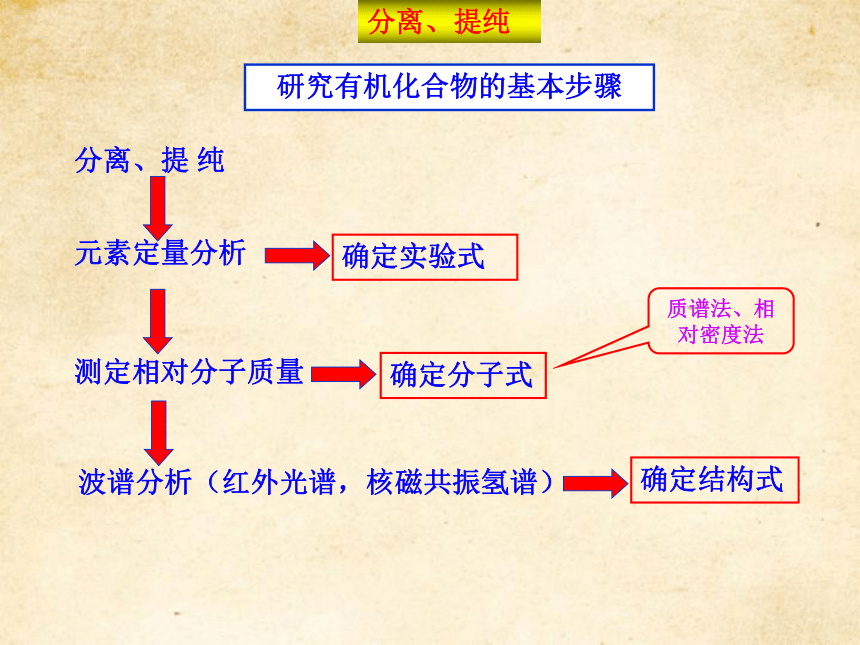
经过哪些流程?分离、提纯分离、提 纯元素定量分析测定相对分子质量波谱分析(红外光谱,核磁共振氢谱)确定实验式确定分子式质谱法、相对密度法确定结构式研究有机化合物的基本步骤分离、提纯1.常用的分离、提纯物质的方法有哪些?
2.归纳分离、提纯物质的总原则是什么?不引入新杂质;不减少提纯物质的量;易分离;易复原。蒸馏 、重结晶、萃取分液、洗气、过滤、 渗析、盐析。【思考与交流】分离、提纯【探究实验】含有杂质的工业乙醇的蒸馏(1)在250mL蒸馏烧瓶中,通过分液漏斗倒入100mL工业乙
醇,再在烧杯中通入1~2粒素烧瓷片。装好蒸馏装置,
往冷凝器中通入冷却水,加热蒸馏,蒸馏产物以每秒
3~4滴为宜,收集不同温度范围的馏分。实验步骤:(2)77℃以下得到的主要是__________;
77~79℃得到的主要是________;
79℃以上得到的主要是__________。甲醇水乙醇 蒸馏原理:利用混合物的沸点不同,除去难挥发或不挥发的杂质。条件:有机物热稳定性较强;与杂质的沸点相差较大(一般约大于30 ℃)。蒸馏烧瓶内液体不能超过容积的2/3。蒸馏注意:温度计水银球位于蒸馏烧瓶的支管口处加入沸石(或碎瓷片)的作用:防止液体暴沸入水
口出水口 蒸馏1.下列属于分离、提纯液态有机物的操作是( )
A.蒸馏 B.蒸发 C.重结晶 D.过滤
2.欲用96%的工业酒精制取无水乙醇时,可选用的方法是 ( )
A.加入无水CuSO4,再过滤
B.加入生石灰,再蒸馏
C.加入浓硫酸,再加热,蒸出乙醇
D.将96%的乙醇溶液直接加热蒸馏AB【即时巩固】 蒸馏【探究实验】苯甲酸的重结晶1.实验步骤
(1)加热溶解:将1 g粗苯甲酸加入到100 mL的烧
杯中,再加入50 mL蒸馏水,将烧杯放在石棉网上边搅拌边加热,使粗苯甲酸溶解,全部溶解后再加入少量蒸馏水。
(2)趁热过滤:用短颈漏斗趁热将溶液过滤到另一个
100 mL的烧杯中。
(3)冷却结晶:将滤液静置,使其缓慢冷却结晶。
(4)分离晶体:过滤分离滤液,得到晶体。 重结晶 为了减少趁热过滤过程中损失苯甲酸,一般在高温溶解固体后再加入少量蒸馏水。2.实验流程图3.注意事项 重结晶【思考交流】
1.为什么要趁热过滤?2.在苯甲酸重结晶的实验中,温度越低,苯甲酸的溶解度越小,为了得到更多的苯甲酸晶体,结晶时的温度是不是越低越好? 不是,冷却结晶时,并不是温度越低越好。因为温度过低,杂质的溶解度也会降低,部分杂质也会析出,达不到提纯苯甲酸的目的;温度极低时,溶剂(水)也会结晶,给实验操作带来麻烦。一方面除去不溶性的杂质,另一方面尽量减小因温度低导致过滤过程中苯甲酸的析出而造成损失。 重结晶溶剂选择的条件:
1.杂质在此溶剂中溶解度很小或很大。
2.被提纯的有机物在此溶剂中的溶解度受温度的影响较大。重结晶的步骤【归纳总结】 重结晶【特别提醒】重结晶的原理
1.重结晶是提纯固体化合物常用的方法之一,固体化合物在
溶剂中的溶解度随温度变化而改变,一般温度升高溶解度增
加,反之则溶解度降低。
2.如果把固体化合物溶解在热的溶剂中制成饱和溶液,然后
冷却至室温或室温以下,则溶解度下降,溶液变成过饱和溶
液而析出晶体。
3.利用被提纯物质和杂质在溶剂中的溶解度的不同,使杂质
在热过滤时被滤出或冷却后留在母液中与晶体分离,从而达
到提纯的目的。 重结晶在重结晶操作中,不属于玻璃棒的作用的是( )
A.引流
B.搅拌,加速溶解
C.搅拌,防止固体因局部过热而飞溅
D.蘸取溶液D【即时巩固】 重结晶原理:利用有机物在两种互不相溶的溶剂中的溶解性的不同,将有机物从一种溶剂中转移到另一种溶剂。主要
仪器:
分液
漏斗萃取剂选择的条件:
1.萃取剂和原溶剂互不相溶,不发生化学反应。
2.溶质在萃取剂中的溶解度大于在原溶剂中的溶解度。 萃取使用前必须检漏。分液时,下层液体从下口流出,上层液体从上口倒出。(双选)下列每项中各有三组物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,己烷和水BD【即时巩固】 萃取【例题】5.8 g某有机物完全燃烧,生成CO2 13.2g,H2O 5.4 g,则该有机物中含有哪些元素?含C 3.6 g(0.3 mol)含H 0.6 g(0.6 mol)分子式为C3H6O有机物组成元素的确定能否直接确定含有氧?如何确定?能否直接确定该有机物的分子式?
实验式和分子式有何区别?含O 1.6 g(0.1 mol)【问题探究】有机物分子式的确定计算组成各原子的整数比(确定实验式)测定相对分子质量(确定分子式)鉴定分子结构(确定物质)定量分析确定物质的步骤有机物分子式的确定实验式:表示化合物分子中所含元素的原子数目
最简整数比的式子。
分子式:表示化合物所含元素的原子种类及数目
的式子,表示物质的真实组成。【特别说明】有机物分子式的确定D1.验证某有机物属于烃,应完成的实验内容是( )
A.只测定它的C、H个数比
B.只要证明它完全燃烧后产物只有H2O和CO2
C.只测定其燃烧产物中H2O与CO2的物质的量的比值
D.测定该试样的质量及试样完全燃烧后生成CO2和H2O
的质量【即时巩固】有机物分子式的确定2.实验测得某碳氢化合物A中,含碳80%、含氢20%,
求该化合物的实验式。又测得该化合物的相对分子质量是30,求该化合物的分子式。实验式是CH3,分子式是C2H6。有机物分子式的确定【原理】它是用高能电子流等轰击样品分子,使该分子失去电子变成带正电荷的分子离子和碎片离子。这些不同离子具有不同的相对质量,质量不同的离子在磁场作用下到达检测器的时间有差异,其结果被记录为质谱图。 【提示】相对分子质量的测定——质谱法。【想一想】如何利用简便的方法测定有机物的相对分子质量?质谱法【思考与交流】
1. 质荷比是什么?
分子离子、碎片离子的相对质量与其电荷的比值。
2.如何确定有机物的相对分子质量?由于分子离子的质荷比越大,到达检测器需要的时间越长,因此质谱图中的质荷比最大的就是未知物的相对分子质量。质谱法质谱法是让极少量的(10-9g)化合
物通过质谱仪的离子化室使样品分
子大量离子化,少量分子碎裂成更
小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+
……,然后测定其质荷比。设H+的质荷比为β,某有机
物样品的质荷比如图所示(假设离子均带一个单位的正电
荷,信号强度与该离子的多少有关),则该有机物可能
是( )
A.甲醇 B.甲烷 C.丙烷 D.乙烯B【即时巩固】质谱法由于有机物中组成化学键或官能团的原子处于不断
振动的状态,且振动频率与红外光的振动频率相当。
所以,当用红外线照射有机物分子时,分子中的化
学键或官能团可发生振动吸收,不同的化学键或官
能团吸收频率不同,在红外光谱图中将处于不同位
置。因此,我们就可以根据红外光谱图,推知有机
物含有哪些化学键、官能团,以确定有机物的结构。红外光谱分子结构的鉴定——红外光谱【即时巩固】某有机物的相对分子质量为74,其红外光谱图如下:则下列有关该有机物的叙述正确的是( )
A.该有机物属于醚类
B.该有机物分子中共有5个碳原子
C.该有机物具有环状结构
D.该有机物分子中有四种化学环境不同的氢原子A红外光谱核磁共振氢谱乙醇和甲醚的分子式都是C2H6O,
二者是同分异构体。分子结构的鉴定——核磁共振氢谱对于CH3CH2OH、CH3—O—CH3这两种物质来说,除了
氧原子的位置、连接方式不同外,碳原子、氢原子
的连接方式也不同、所处的化学环境不同,即等效
碳、等效氢的种数不同。
明确:不同化学环境的氢原子(等效氢原子)因产
生共振时吸收的频率不同,被核磁共振仪记录下来
的吸收峰的面积不同。所以,可以从核磁共振谱图
上推知氢原子的类型及它们的相对数目。核磁共振氢谱核磁共振氢谱是根据不同化学环境的氢原子在核磁共振氢谱中给出的信号不同来确定有机物分子中的不同的氢原子。下列有机物分子在核磁共振氢谱中只给出一种信号的是( )
A.HCHO B.CH3OH
C.HCOOH D.CH3COOCH3A【即时巩固】核磁共振氢谱研究有机物的步骤和方法分离、提纯元素的定量分析测定相对分子质量鉴定分子结构蒸馏法重结晶法萃取法测定元素质量分数确定实验式红外光谱、核磁共振氢谱质谱法1.有机物的天然提取和人工合成往往得到的是混合物,
假设给你一种这样的有机混合物让你研究,一般要采取
的几个步骤是
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯√2.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,下列说法正确的是
A.分子中C、H、O个数之比为1:2:3
B.分子中C、H个数之比为1:4
C.分子中一定含有氧原子
D.此有机物的最简式为CH4√3.下列物质中的杂质(括号中是杂质)分别可以用什么方法除去。
(1)KNO3(NaCl)
(2)乙酸乙酯(乙醇)
(3)NaCl(泥沙)
(4)单质溴(水)
(5)CO2(HCl)溶解、过滤 萃取 用饱和碳酸氢钠溶液洗气 结晶或重结晶 蒸馏 这个宇宙整体的真理就是无常,没有所谓的完全的正义与完全的邪恶。 ——沙加
积聚”等诸多病症。但长期嚼食槟榔的人罹患口腔
癌的机率比一般人高20倍。在食用槟榔前,要研究
其中哪些是有害成分,哪些是有益成分。那么研究
有机物的方法还有哪些呢?1.了解研究有机化合物的一般步骤,掌握有机物分离、提纯的常用方法。
2.了解确定有机化合物结构的化学方法和某些物理方法(如质谱、红外光谱、核磁共振氢谱等) 。(重点)
3.初步了解测定 有机化合物的元素含量、相对分子质量的一般方法,并能根据其确定有机化合物的分子式 。(难点)【问题导入】1.从天然资源中提取的有机物成分,以及在工厂
生产、实验室合成的有机物往往都是混合物,如
何进行分离、提纯呢?2.要鉴定和研究未知有机物的结构和性质,需要
经过哪些流程?分离、提纯分离、提 纯元素定量分析测定相对分子质量波谱分析(红外光谱,核磁共振氢谱)确定实验式确定分子式质谱法、相对密度法确定结构式研究有机化合物的基本步骤分离、提纯1.常用的分离、提纯物质的方法有哪些?
2.归纳分离、提纯物质的总原则是什么?不引入新杂质;不减少提纯物质的量;易分离;易复原。蒸馏 、重结晶、萃取分液、洗气、过滤、 渗析、盐析。【思考与交流】分离、提纯【探究实验】含有杂质的工业乙醇的蒸馏(1)在250mL蒸馏烧瓶中,通过分液漏斗倒入100mL工业乙
醇,再在烧杯中通入1~2粒素烧瓷片。装好蒸馏装置,
往冷凝器中通入冷却水,加热蒸馏,蒸馏产物以每秒
3~4滴为宜,收集不同温度范围的馏分。实验步骤:(2)77℃以下得到的主要是__________;
77~79℃得到的主要是________;
79℃以上得到的主要是__________。甲醇水乙醇 蒸馏原理:利用混合物的沸点不同,除去难挥发或不挥发的杂质。条件:有机物热稳定性较强;与杂质的沸点相差较大(一般约大于30 ℃)。蒸馏烧瓶内液体不能超过容积的2/3。蒸馏注意:温度计水银球位于蒸馏烧瓶的支管口处加入沸石(或碎瓷片)的作用:防止液体暴沸入水
口出水口 蒸馏1.下列属于分离、提纯液态有机物的操作是( )
A.蒸馏 B.蒸发 C.重结晶 D.过滤
2.欲用96%的工业酒精制取无水乙醇时,可选用的方法是 ( )
A.加入无水CuSO4,再过滤
B.加入生石灰,再蒸馏
C.加入浓硫酸,再加热,蒸出乙醇
D.将96%的乙醇溶液直接加热蒸馏AB【即时巩固】 蒸馏【探究实验】苯甲酸的重结晶1.实验步骤
(1)加热溶解:将1 g粗苯甲酸加入到100 mL的烧
杯中,再加入50 mL蒸馏水,将烧杯放在石棉网上边搅拌边加热,使粗苯甲酸溶解,全部溶解后再加入少量蒸馏水。
(2)趁热过滤:用短颈漏斗趁热将溶液过滤到另一个
100 mL的烧杯中。
(3)冷却结晶:将滤液静置,使其缓慢冷却结晶。
(4)分离晶体:过滤分离滤液,得到晶体。 重结晶 为了减少趁热过滤过程中损失苯甲酸,一般在高温溶解固体后再加入少量蒸馏水。2.实验流程图3.注意事项 重结晶【思考交流】
1.为什么要趁热过滤?2.在苯甲酸重结晶的实验中,温度越低,苯甲酸的溶解度越小,为了得到更多的苯甲酸晶体,结晶时的温度是不是越低越好? 不是,冷却结晶时,并不是温度越低越好。因为温度过低,杂质的溶解度也会降低,部分杂质也会析出,达不到提纯苯甲酸的目的;温度极低时,溶剂(水)也会结晶,给实验操作带来麻烦。一方面除去不溶性的杂质,另一方面尽量减小因温度低导致过滤过程中苯甲酸的析出而造成损失。 重结晶溶剂选择的条件:
1.杂质在此溶剂中溶解度很小或很大。
2.被提纯的有机物在此溶剂中的溶解度受温度的影响较大。重结晶的步骤【归纳总结】 重结晶【特别提醒】重结晶的原理
1.重结晶是提纯固体化合物常用的方法之一,固体化合物在
溶剂中的溶解度随温度变化而改变,一般温度升高溶解度增
加,反之则溶解度降低。
2.如果把固体化合物溶解在热的溶剂中制成饱和溶液,然后
冷却至室温或室温以下,则溶解度下降,溶液变成过饱和溶
液而析出晶体。
3.利用被提纯物质和杂质在溶剂中的溶解度的不同,使杂质
在热过滤时被滤出或冷却后留在母液中与晶体分离,从而达
到提纯的目的。 重结晶在重结晶操作中,不属于玻璃棒的作用的是( )
A.引流
B.搅拌,加速溶解
C.搅拌,防止固体因局部过热而飞溅
D.蘸取溶液D【即时巩固】 重结晶原理:利用有机物在两种互不相溶的溶剂中的溶解性的不同,将有机物从一种溶剂中转移到另一种溶剂。主要
仪器:
分液
漏斗萃取剂选择的条件:
1.萃取剂和原溶剂互不相溶,不发生化学反应。
2.溶质在萃取剂中的溶解度大于在原溶剂中的溶解度。 萃取使用前必须检漏。分液时,下层液体从下口流出,上层液体从上口倒出。(双选)下列每项中各有三组物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,己烷和水BD【即时巩固】 萃取【例题】5.8 g某有机物完全燃烧,生成CO2 13.2g,H2O 5.4 g,则该有机物中含有哪些元素?含C 3.6 g(0.3 mol)含H 0.6 g(0.6 mol)分子式为C3H6O有机物组成元素的确定能否直接确定含有氧?如何确定?能否直接确定该有机物的分子式?
实验式和分子式有何区别?含O 1.6 g(0.1 mol)【问题探究】有机物分子式的确定计算组成各原子的整数比(确定实验式)测定相对分子质量(确定分子式)鉴定分子结构(确定物质)定量分析确定物质的步骤有机物分子式的确定实验式:表示化合物分子中所含元素的原子数目
最简整数比的式子。
分子式:表示化合物所含元素的原子种类及数目
的式子,表示物质的真实组成。【特别说明】有机物分子式的确定D1.验证某有机物属于烃,应完成的实验内容是( )
A.只测定它的C、H个数比
B.只要证明它完全燃烧后产物只有H2O和CO2
C.只测定其燃烧产物中H2O与CO2的物质的量的比值
D.测定该试样的质量及试样完全燃烧后生成CO2和H2O
的质量【即时巩固】有机物分子式的确定2.实验测得某碳氢化合物A中,含碳80%、含氢20%,
求该化合物的实验式。又测得该化合物的相对分子质量是30,求该化合物的分子式。实验式是CH3,分子式是C2H6。有机物分子式的确定【原理】它是用高能电子流等轰击样品分子,使该分子失去电子变成带正电荷的分子离子和碎片离子。这些不同离子具有不同的相对质量,质量不同的离子在磁场作用下到达检测器的时间有差异,其结果被记录为质谱图。 【提示】相对分子质量的测定——质谱法。【想一想】如何利用简便的方法测定有机物的相对分子质量?质谱法【思考与交流】
1. 质荷比是什么?
分子离子、碎片离子的相对质量与其电荷的比值。
2.如何确定有机物的相对分子质量?由于分子离子的质荷比越大,到达检测器需要的时间越长,因此质谱图中的质荷比最大的就是未知物的相对分子质量。质谱法质谱法是让极少量的(10-9g)化合
物通过质谱仪的离子化室使样品分
子大量离子化,少量分子碎裂成更
小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+
……,然后测定其质荷比。设H+的质荷比为β,某有机
物样品的质荷比如图所示(假设离子均带一个单位的正电
荷,信号强度与该离子的多少有关),则该有机物可能
是( )
A.甲醇 B.甲烷 C.丙烷 D.乙烯B【即时巩固】质谱法由于有机物中组成化学键或官能团的原子处于不断
振动的状态,且振动频率与红外光的振动频率相当。
所以,当用红外线照射有机物分子时,分子中的化
学键或官能团可发生振动吸收,不同的化学键或官
能团吸收频率不同,在红外光谱图中将处于不同位
置。因此,我们就可以根据红外光谱图,推知有机
物含有哪些化学键、官能团,以确定有机物的结构。红外光谱分子结构的鉴定——红外光谱【即时巩固】某有机物的相对分子质量为74,其红外光谱图如下:则下列有关该有机物的叙述正确的是( )
A.该有机物属于醚类
B.该有机物分子中共有5个碳原子
C.该有机物具有环状结构
D.该有机物分子中有四种化学环境不同的氢原子A红外光谱核磁共振氢谱乙醇和甲醚的分子式都是C2H6O,
二者是同分异构体。分子结构的鉴定——核磁共振氢谱对于CH3CH2OH、CH3—O—CH3这两种物质来说,除了
氧原子的位置、连接方式不同外,碳原子、氢原子
的连接方式也不同、所处的化学环境不同,即等效
碳、等效氢的种数不同。
明确:不同化学环境的氢原子(等效氢原子)因产
生共振时吸收的频率不同,被核磁共振仪记录下来
的吸收峰的面积不同。所以,可以从核磁共振谱图
上推知氢原子的类型及它们的相对数目。核磁共振氢谱核磁共振氢谱是根据不同化学环境的氢原子在核磁共振氢谱中给出的信号不同来确定有机物分子中的不同的氢原子。下列有机物分子在核磁共振氢谱中只给出一种信号的是( )
A.HCHO B.CH3OH
C.HCOOH D.CH3COOCH3A【即时巩固】核磁共振氢谱研究有机物的步骤和方法分离、提纯元素的定量分析测定相对分子质量鉴定分子结构蒸馏法重结晶法萃取法测定元素质量分数确定实验式红外光谱、核磁共振氢谱质谱法1.有机物的天然提取和人工合成往往得到的是混合物,
假设给你一种这样的有机混合物让你研究,一般要采取
的几个步骤是
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯√2.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,下列说法正确的是
A.分子中C、H、O个数之比为1:2:3
B.分子中C、H个数之比为1:4
C.分子中一定含有氧原子
D.此有机物的最简式为CH4√3.下列物质中的杂质(括号中是杂质)分别可以用什么方法除去。
(1)KNO3(NaCl)
(2)乙酸乙酯(乙醇)
(3)NaCl(泥沙)
(4)单质溴(水)
(5)CO2(HCl)溶解、过滤 萃取 用饱和碳酸氢钠溶液洗气 结晶或重结晶 蒸馏 这个宇宙整体的真理就是无常,没有所谓的完全的正义与完全的邪恶。 ——沙加
