人教版高中化学选修5课件:3.1.1 醇36张PPT
文档属性
| 名称 | 人教版高中化学选修5课件:3.1.1 醇36张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-07 00:00:00 | ||
图片预览










文档简介
课件36张PPT。第一节 醇 酚
第1课时 醇第三章 烃的含氧衍生物 古往今来无数咏叹酒的诗篇都证明酒是一种奇特
而富有魅力的饮料。其中的溶质——酒精有哪些性
质呢?借问酒家何处有,
牧童遥指杏花村。明月几时有,
把酒问青天。1.了解乙醇的组成、结构特点及物理性质。
2.掌握乙醇的主要化学性质。(重点)
3.理解官能团在有机化合物中的作用,并结合同系物原理加以应用。
4.了解实验室制取乙烯的注意事项。醇的分类和命名 请同学们快速阅读课本第48~49页的内容,明
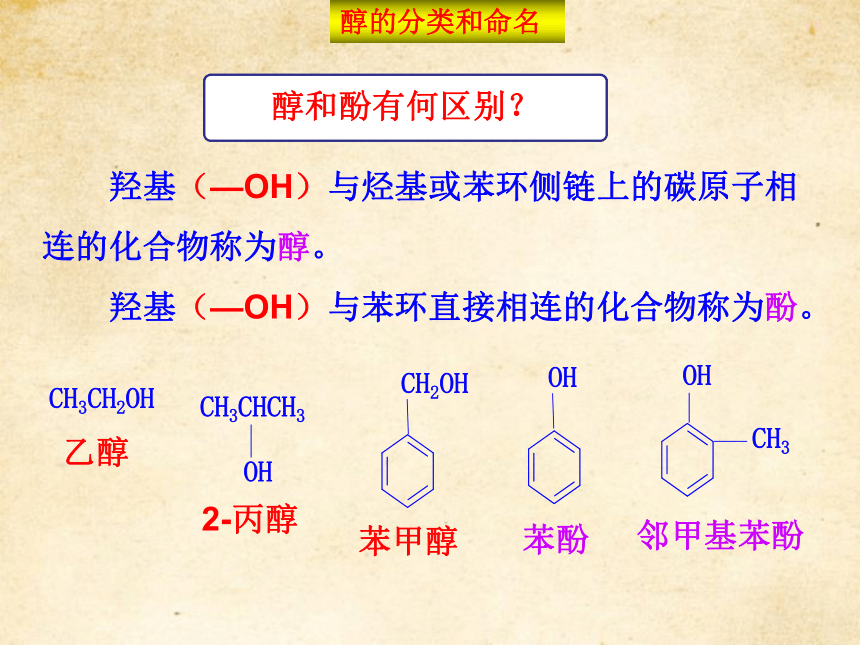
确下列知识点。 羟基(—OH)与烃基或苯环侧链上的碳原子相
连的化合物称为醇。
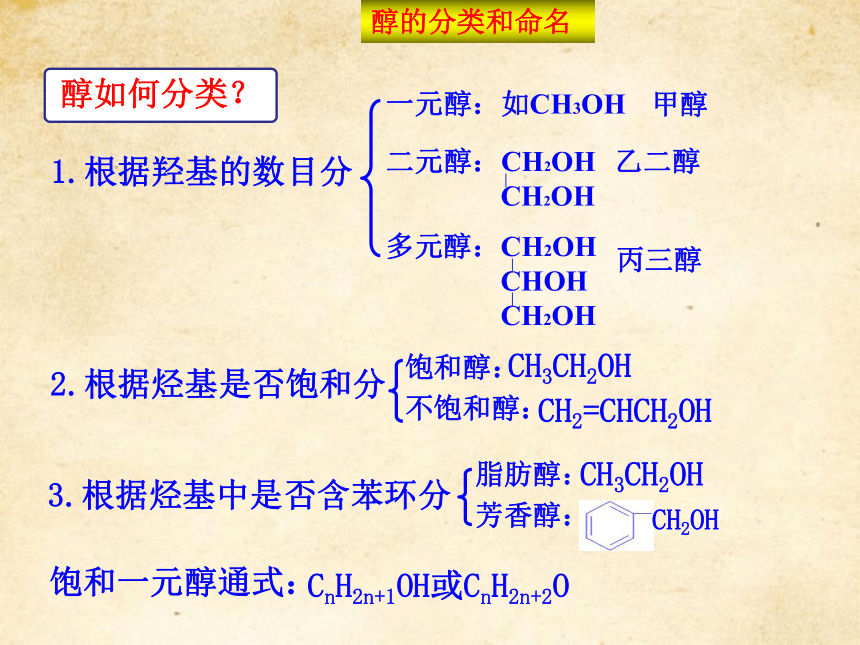
羟基(—OH)与苯环直接相连的化合物称为酚。OHCH3OHCH3CH2OH 乙醇2-丙醇 苯酚 邻甲基苯酚CH2OH 苯甲醇 醇的分类和命名1.根据羟基的数目分一元醇:如CH3OH甲醇2.根据烃基是否饱和分饱和醇:
不饱和醇:3.根据烃基中是否含苯环分脂肪醇:
芳香醇:饱和一元醇通式:CnH2n+1OH或CnH2n+2OCH3CH2OHCH2=CHCH2OHCH3CH2OH醇的分类和命名 乙二醇和丙三醇都是无色、黏稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。 乙二醇可用于汽车防冻液,丙三醇可用于配制化妆品。醇的分类和命名1.选主链:选含—OH最长碳链为主链,称某醇
2.编号:从离—OH最近的一端起依次编号
3.写名称:取代基位置-取代基名称-羟基位置-母体名称(羟基位置用阿拉伯数字表示;羟基的个数用“二”“三”等表示),如:1,2,3-丙三醇(或甘油、丙三醇)2-丁醇醇的分类和命名写出下列醇的名称。①2-丁醇2,3-二甲基-3-戊醇【即时巩固】醇的分类和命名相对分子质量相近的醇和烷烃,醇的沸点远远高于
烷烃。
解释:醇分子间形成氢键,使醇分子间作用力增
强,导致醇的沸点远远高于烷烃。通过分析“相对分子质量相近的醇与烷烃的沸点比较”的表格中的数据可得出以下结论:【思考与交流】 醇的物理性质【提示】随着碳原子的数目增多,醇的溶解性减小。醇分子间形成氢键示意图:原因:由于醇分子中羟基的氧原子与另一醇分子中羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。(分子间形成了氢键) 醇的物理性质通过“表3-2 一些醇的沸点”表格中的数据你能得出什么结论?
乙二醇的沸点高于乙醇;1,2,3-丙三醇的沸点高
于1,2-丙二醇;1,2-丙二醇的沸点高于1-丙醇。
原因:由于羟基数目增多,使得分子间形成的氢键
增多,分子间作用力增强,沸点升高。 【学与问】 醇的物理性质乙醇 请同学们快速阅读课本第50~52页的内容,3分
钟后,看哪位同学能够准确回答下列知识点。1.乙醇的结构
从乙烷分子中的1个氢原子被—OH(羟基)取代衍变成乙醇O—H、C—O 键的极性较大,易断键乙醇的结构球棍模型比例模型⑤④③②①⑤④③①乙醇的球棍模型和比例模型:乙醇的结构颜 色:
气 味:
状 态:
挥发性:
密 度:
溶解性:无色透明特殊香味液 体比水小易挥发跟水以任意比例互溶,能够溶解多种
无机物和有机物乙醇的物理性质 根据水与钠反应的方程式,试写出乙醇跟金属钠反应的化学方程式。比较乙醇与水中羟基上的H的活泼性强弱。2H-O-H+2Na====2NaOH+H2↑乙醇的化学性质断键位置:
脱去—OH和与—OH相邻的碳原子上的1个H
浓硫酸的作用:催化剂和脱水剂消去反应:浓硫酸乙醇的化学性质制乙烯实验装置:为何使液体温度迅速升到170℃,不能过高或过低?酒精与浓硫酸混合液如何配制?放入几片碎瓷片的作用是什么? 用排水集气法收集 浓硫酸的作用是什么?温度计的位置?催化剂和
脱水剂防止暴沸 酒精与浓硫酸
体积比要为1∶3。因为浓硫酸是催
化剂和脱水剂,
为了保证有足够
的脱水性,要
用98%的浓硫
酸,酒精要用
无水酒精,酒
精与浓硫酸体
积比以1:3为宜。温度计水银球要置于反应物的中央位置,因为需要测量的是反应物的温度。因为无水酒精和浓硫酸的混合物在170℃的温度
下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。乙醇的化学性质氢氧化钠除去CO2、SO2等酸性气体探究实验 乙烯的制取【实验】按如图装置制取乙烯,随反
应的进行液体逐渐变黑,为什么?导
气管通入NaOH溶液中,作用是什么? 【交流与讨论】
得到的黑色物质是什么?
它是如何形成的?结论:浓硫酸具有强氧化性、脱水性。
在加热的条件下,浓硫酸和无水酒精反
应生成碳的单质、CO2、SO2等多种物质,
碳的单质使烧瓶内的液体带上了黑色。如果导气管不通入NaOH溶液中,
对乙烯气体的验证有影响吗?有。因为SO2也能使溴水褪色乙醇的消去反应乙醇的化学性质反应条件化学键的断裂化学键的生成NaOH的乙醇溶液、加热C—Br键、C—H键C—O键、C—H键C=C键C=C键CH2=CH2、HBrCH2=CH2、H2O浓硫酸、加热到170℃ 溴乙烷与乙醇都能发生消去反应,它们有什么异同?【学与问】【提示】醇发生消去反应的分子结构条件:与C-OH相邻的碳原子上有氢原子。乙醇的化学性质下列物质中属于醇类且能发生消去反应的是( ) 【即时巩固】C【提示】分析醇的消去反应时,首先要看该醇分子
中是否含有两个或两个以上的碳原子,再看与羟基
相连的碳原子的邻位碳原子上是否有氢原子,由此
判断该醇是否能发生消去反应。乙醇的化学性质浓H2SO4
△ 1.分子间取代2.乙醇的酯化反应
CH3CH2OH+CH3COOH CH3COOC2H5+H2O
3.乙醇与HX反应:乙醇的化学性质氧化反应:②催化氧化:铜丝由红色变黑色,然后由黑色变为红色,产生
有刺激性气味的液体。乙醇的化学性质 有机物的氧化反应、还原反应的含义:
氧化反应:有机物分子中失去氢原子或加入氧原子的反应(失H或加O)
还原反应:有机物分子中加入氢原子或失去氧原子的反应(加H或失O )乙醇的催化氧化断哪些键?
是不是所有的醇都能发生催化氧化?乙醇的化学性质都属于与乙醇同类的烃的衍生物,它们能否发生像乙醇那样的催化氧化反应?若能,得到什么产物?
结论:羟基碳上有2个氢原子的醇被催化氧化成醛。
羟基碳上有1个氢原子的醇被催化氧化成酮。
羟基碳上没有氢原子的醇不能被催化氧化。【思考与交流】 乙醇的化学性质结论:羟基碳上有2个氢原子的醇被氧化成酸。
羟基碳上有1个氢原子的醇被氧化成酮。
羟基碳上没有氢原子的醇不能被氧化。③强氧化剂氧化
乙醇可被酸性高锰酸钾溶液或重铬酸钾酸性溶液氧化生成乙酸。氧化过程可分为两步:乙醇的化学性质1.登录互联网,查阅乙醇的有关用途。
2.家庭小实验:制作酒酿
将糯米洗净,在锅中蒸熟,冷却至 30 ℃左右,加入研碎的酒曲,充分混合均匀,在30 ℃左右的环境中保温,放置3天3夜即可制成酒酿。【练习与实践】 乙醇的用途分子间脱水与HX反应②④②①③①②与金属反应消去反应催化氧化①乙醇的化学性质与结构的关系: A.C2H5OH B. 1.判断下列物质中不属于醇类的是 C. D. √ CH3
∣
B.CH3—C—OH
∣
CH32.下列各醇,能发生催化氧化生成醛的是C.CH3—CH—CH3
∣
OH CH3
∣
D.C6H5—C—CH3
∣
OHA.√3.下列化学方程式书写正确的是
A.
B.
C.
D.C2H5Br + H2O C2H5OH+H2ONaOH
醇溶液√4.下列检验方法或现象描述不正确的是
A.乙烷中是否混有乙烯,可用通过溴水是否褪色进
行检验
B.乙醇中是否混有水,可用加无水硫酸铜粉末是否
变蓝进行检验
C.乙醇中是否混有乙酸,可用加入金属钠是否产生
气体进行检验
D.乙酸乙酯中是否混有乙酸,可用加石蕊溶液是否
变红进行检测√若将此题改为“分子式为C4H10O且能被催化氧化成醛的醇有几种(不含立体异构)”,则答案应为?5.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)
A.3种 B.4种
C.5种 D.6种√注意啦!
与醇分子中的羟基相连的碳有氢才氧化,相邻的碳有
氢才消去。分子式为C4H10O能氧化成醛的结构则可以
写成C3H7-CH2OH的形式,只要分析C3H7-同分异构即可。在科学上进步而道义上落后的人,不是前进,而是后退。
——亚里士多德
第1课时 醇第三章 烃的含氧衍生物 古往今来无数咏叹酒的诗篇都证明酒是一种奇特
而富有魅力的饮料。其中的溶质——酒精有哪些性
质呢?借问酒家何处有,
牧童遥指杏花村。明月几时有,
把酒问青天。1.了解乙醇的组成、结构特点及物理性质。
2.掌握乙醇的主要化学性质。(重点)
3.理解官能团在有机化合物中的作用,并结合同系物原理加以应用。
4.了解实验室制取乙烯的注意事项。醇的分类和命名 请同学们快速阅读课本第48~49页的内容,明
确下列知识点。 羟基(—OH)与烃基或苯环侧链上的碳原子相
连的化合物称为醇。
羟基(—OH)与苯环直接相连的化合物称为酚。OHCH3OHCH3CH2OH 乙醇2-丙醇 苯酚 邻甲基苯酚CH2OH 苯甲醇 醇的分类和命名1.根据羟基的数目分一元醇:如CH3OH甲醇2.根据烃基是否饱和分饱和醇:
不饱和醇:3.根据烃基中是否含苯环分脂肪醇:
芳香醇:饱和一元醇通式:CnH2n+1OH或CnH2n+2OCH3CH2OHCH2=CHCH2OHCH3CH2OH醇的分类和命名 乙二醇和丙三醇都是无色、黏稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。 乙二醇可用于汽车防冻液,丙三醇可用于配制化妆品。醇的分类和命名1.选主链:选含—OH最长碳链为主链,称某醇
2.编号:从离—OH最近的一端起依次编号
3.写名称:取代基位置-取代基名称-羟基位置-母体名称(羟基位置用阿拉伯数字表示;羟基的个数用“二”“三”等表示),如:1,2,3-丙三醇(或甘油、丙三醇)2-丁醇醇的分类和命名写出下列醇的名称。①2-丁醇2,3-二甲基-3-戊醇【即时巩固】醇的分类和命名相对分子质量相近的醇和烷烃,醇的沸点远远高于
烷烃。
解释:醇分子间形成氢键,使醇分子间作用力增
强,导致醇的沸点远远高于烷烃。通过分析“相对分子质量相近的醇与烷烃的沸点比较”的表格中的数据可得出以下结论:【思考与交流】 醇的物理性质【提示】随着碳原子的数目增多,醇的溶解性减小。醇分子间形成氢键示意图:原因:由于醇分子中羟基的氧原子与另一醇分子中羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。(分子间形成了氢键) 醇的物理性质通过“表3-2 一些醇的沸点”表格中的数据你能得出什么结论?
乙二醇的沸点高于乙醇;1,2,3-丙三醇的沸点高
于1,2-丙二醇;1,2-丙二醇的沸点高于1-丙醇。
原因:由于羟基数目增多,使得分子间形成的氢键
增多,分子间作用力增强,沸点升高。 【学与问】 醇的物理性质乙醇 请同学们快速阅读课本第50~52页的内容,3分
钟后,看哪位同学能够准确回答下列知识点。1.乙醇的结构
从乙烷分子中的1个氢原子被—OH(羟基)取代衍变成乙醇O—H、C—O 键的极性较大,易断键乙醇的结构球棍模型比例模型⑤④③②①⑤④③①乙醇的球棍模型和比例模型:乙醇的结构颜 色:
气 味:
状 态:
挥发性:
密 度:
溶解性:无色透明特殊香味液 体比水小易挥发跟水以任意比例互溶,能够溶解多种
无机物和有机物乙醇的物理性质 根据水与钠反应的方程式,试写出乙醇跟金属钠反应的化学方程式。比较乙醇与水中羟基上的H的活泼性强弱。2H-O-H+2Na====2NaOH+H2↑乙醇的化学性质断键位置:
脱去—OH和与—OH相邻的碳原子上的1个H
浓硫酸的作用:催化剂和脱水剂消去反应:浓硫酸乙醇的化学性质制乙烯实验装置:为何使液体温度迅速升到170℃,不能过高或过低?酒精与浓硫酸混合液如何配制?放入几片碎瓷片的作用是什么? 用排水集气法收集 浓硫酸的作用是什么?温度计的位置?催化剂和
脱水剂防止暴沸 酒精与浓硫酸
体积比要为1∶3。因为浓硫酸是催
化剂和脱水剂,
为了保证有足够
的脱水性,要
用98%的浓硫
酸,酒精要用
无水酒精,酒
精与浓硫酸体
积比以1:3为宜。温度计水银球要置于反应物的中央位置,因为需要测量的是反应物的温度。因为无水酒精和浓硫酸的混合物在170℃的温度
下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。乙醇的化学性质氢氧化钠除去CO2、SO2等酸性气体探究实验 乙烯的制取【实验】按如图装置制取乙烯,随反
应的进行液体逐渐变黑,为什么?导
气管通入NaOH溶液中,作用是什么? 【交流与讨论】
得到的黑色物质是什么?
它是如何形成的?结论:浓硫酸具有强氧化性、脱水性。
在加热的条件下,浓硫酸和无水酒精反
应生成碳的单质、CO2、SO2等多种物质,
碳的单质使烧瓶内的液体带上了黑色。如果导气管不通入NaOH溶液中,
对乙烯气体的验证有影响吗?有。因为SO2也能使溴水褪色乙醇的消去反应乙醇的化学性质反应条件化学键的断裂化学键的生成NaOH的乙醇溶液、加热C—Br键、C—H键C—O键、C—H键C=C键C=C键CH2=CH2、HBrCH2=CH2、H2O浓硫酸、加热到170℃ 溴乙烷与乙醇都能发生消去反应,它们有什么异同?【学与问】【提示】醇发生消去反应的分子结构条件:与C-OH相邻的碳原子上有氢原子。乙醇的化学性质下列物质中属于醇类且能发生消去反应的是( ) 【即时巩固】C【提示】分析醇的消去反应时,首先要看该醇分子
中是否含有两个或两个以上的碳原子,再看与羟基
相连的碳原子的邻位碳原子上是否有氢原子,由此
判断该醇是否能发生消去反应。乙醇的化学性质浓H2SO4
△ 1.分子间取代2.乙醇的酯化反应
CH3CH2OH+CH3COOH CH3COOC2H5+H2O
3.乙醇与HX反应:乙醇的化学性质氧化反应:②催化氧化:铜丝由红色变黑色,然后由黑色变为红色,产生
有刺激性气味的液体。乙醇的化学性质 有机物的氧化反应、还原反应的含义:
氧化反应:有机物分子中失去氢原子或加入氧原子的反应(失H或加O)
还原反应:有机物分子中加入氢原子或失去氧原子的反应(加H或失O )乙醇的催化氧化断哪些键?
是不是所有的醇都能发生催化氧化?乙醇的化学性质都属于与乙醇同类的烃的衍生物,它们能否发生像乙醇那样的催化氧化反应?若能,得到什么产物?
结论:羟基碳上有2个氢原子的醇被催化氧化成醛。
羟基碳上有1个氢原子的醇被催化氧化成酮。
羟基碳上没有氢原子的醇不能被催化氧化。【思考与交流】 乙醇的化学性质结论:羟基碳上有2个氢原子的醇被氧化成酸。
羟基碳上有1个氢原子的醇被氧化成酮。
羟基碳上没有氢原子的醇不能被氧化。③强氧化剂氧化
乙醇可被酸性高锰酸钾溶液或重铬酸钾酸性溶液氧化生成乙酸。氧化过程可分为两步:乙醇的化学性质1.登录互联网,查阅乙醇的有关用途。
2.家庭小实验:制作酒酿
将糯米洗净,在锅中蒸熟,冷却至 30 ℃左右,加入研碎的酒曲,充分混合均匀,在30 ℃左右的环境中保温,放置3天3夜即可制成酒酿。【练习与实践】 乙醇的用途分子间脱水与HX反应②④②①③①②与金属反应消去反应催化氧化①乙醇的化学性质与结构的关系: A.C2H5OH B. 1.判断下列物质中不属于醇类的是 C. D. √ CH3
∣
B.CH3—C—OH
∣
CH32.下列各醇,能发生催化氧化生成醛的是C.CH3—CH—CH3
∣
OH CH3
∣
D.C6H5—C—CH3
∣
OHA.√3.下列化学方程式书写正确的是
A.
B.
C.
D.C2H5Br + H2O C2H5OH+H2ONaOH
醇溶液√4.下列检验方法或现象描述不正确的是
A.乙烷中是否混有乙烯,可用通过溴水是否褪色进
行检验
B.乙醇中是否混有水,可用加无水硫酸铜粉末是否
变蓝进行检验
C.乙醇中是否混有乙酸,可用加入金属钠是否产生
气体进行检验
D.乙酸乙酯中是否混有乙酸,可用加石蕊溶液是否
变红进行检测√若将此题改为“分子式为C4H10O且能被催化氧化成醛的醇有几种(不含立体异构)”,则答案应为?5.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)
A.3种 B.4种
C.5种 D.6种√注意啦!
与醇分子中的羟基相连的碳有氢才氧化,相邻的碳有
氢才消去。分子式为C4H10O能氧化成醛的结构则可以
写成C3H7-CH2OH的形式,只要分析C3H7-同分异构即可。在科学上进步而道义上落后的人,不是前进,而是后退。
——亚里士多德
