人教版高中化学选修5课件:3.3 羧酸 酯(30张PPT)
文档属性
| 名称 | 人教版高中化学选修5课件:3.3 羧酸 酯(30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-07 00:00:00 | ||
图片预览








文档简介
课件30张PPT。 第三节 羧酸 酯 据有文献记载的酿醋历史至少也在三千年以上。
“醋”在中国古称“酢”、“苦酒”等,经常喝
醋能够起到消除疲劳等作用,醋还有治感冒的作用。
醋是乙酸的水溶液,乙酸具有哪些性质呢?1.了解羧酸和酯的组成和结构特点。
2.了解羧酸的分类及乙酸、酯的物理性质及存在。
3.掌握乙酸和乙酸乙酯的结构特点和主要性质,理解
乙酸的酯化反应和乙酸乙酯水解反应的基本规律。
(重点)
4.掌握羧酸和酯之间的相互转化,学会其在合成与推
断中的应用。 (难点)羧酸的概念和分类请同学们根据下列知识点快速阅读课本第60~61页
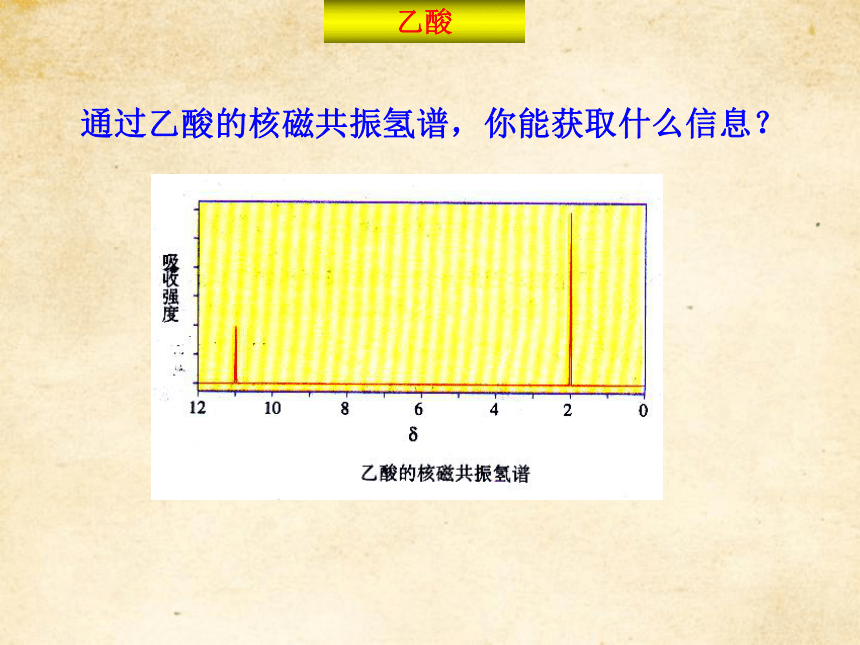
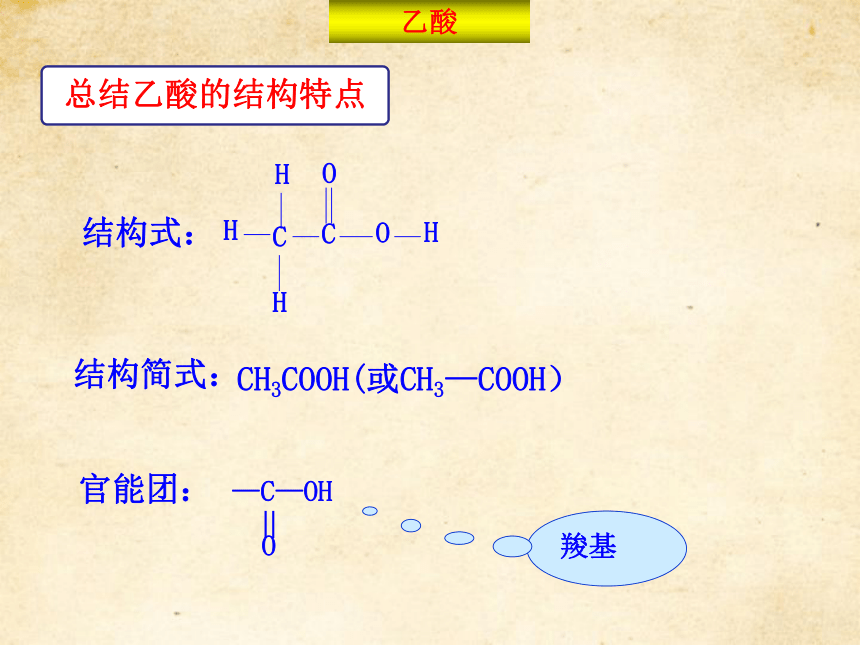
的内容。1.定义:由烃基与羧基相连构成的有机化合物。烃基不同羧基数目脂肪酸芳香酸一元羧酸二元羧酸多元羧酸2.分类3.饱和一元羧酸通式:CnH2n+1COOH或CnH2nO2羧酸的概念和分类通过乙酸的核磁共振氢谱,你能获取什么信息?乙酸—C—OHCH3COOH(或CH3—COOH)结构简式:结构式:官能团:乙酸常温下为无色液体强烈刺激性气味与水、酒精以任意比互溶16.6℃,当温度低于熔点时,易凝结成
冰一样的晶体。(冰醋酸由此得名)气味:色态:溶解性:熔点:乙酸下列关于乙酸的说法中不正确的是( )
A.乙酸是一种重要的有机酸,是具有强烈刺激性气
味的液体
B.乙酸分子中含有四个氢原子,所以乙酸是四元酸
C.无水乙酸又称冰醋酸,它是纯净物
D.乙酸易溶于水和乙醇【即时巩固】B乙酸1.乙酸具有酸的通性:①使紫色石蕊试液变色:②与活泼金属反应:2CH3COOH+Fe (CH3COO)2Fe+H2↑日常生活中,为什么可以用醋除去水垢(水垢的
主要成分包括CaCO3) ?说明乙酸具有什么性质?③与碱性氧化物反应:2CH3COOH+Na2O 2CH3COONa+H2O④与碱反应:CH3COOH+NaOH CH3COONa+H2O⑤与盐反应:2CH3COOH+Na2CO3 2CH3COONa+H2O+CO2↑乙酸可以用几种方法证明乙酸是弱酸?证明乙酸是弱酸的方法:
(1)配制一定浓度的乙酸测定pH;
(2)在相同条件下与同浓度的盐酸比较导电性;
(3)在相同条件下与同浓度的盐酸比较与金属反应的速率;
(4)测定乙酸钠溶液的酸碱性。【思考与交流】 乙酸酸性:乙酸>碳酸>苯酚探究实验 乙酸、碳酸、苯酚的酸性强弱【实验】某化学兴趣小组用下面两套实验装置来验证
乙酸、碳酸、苯酚的酸性强弱,你认为哪套更合理?
并写出有关反应的化学方程式。乙酸根据下表比较醇、酚、羧酸中羟基活泼性比碳
酸弱比碳酸强能能能能能不能不能不能能,不
产生CO2不能能 能增 强中性乙酸自然界中的有机酸
(1)甲酸:HCOOH(蚁酸)
(2)苯甲酸:C6H5COOH (安息香酸)
(3)草酸:HOOC-COOH (乙二酸)
(4)乳酸: 厨师烧鱼时常加醋并加点酒,这样鱼的味道就变
得无腥、香醇,特别鲜美。这是为什么?乙酸1.定义:
含氧酸和醇起作用,生成酯和水的反应叫做酯
化反应。
浓硫酸作用:催化剂、吸水剂什么是酯化反应?其反应本质是什么?乙酸方式一:酸脱氢、醇脱羟基方式二:酸脱羟基、醇脱氢2.探究酯化反应可能的脱水方式
——同位素示踪法乙酸实验验证:同位素示踪法酯化反应的本质:酸脱羟基、醇脱羟基氢。 CH3—C—O—H + H—18O—C2H5 OCH3—C—18O—C2H5+H2OO乙酸酯化反应属于( )
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应【即时巩固】D乙酸
1.酯的定义:羧酸分子羧基中的-OH被-OR′取代后
的产物。
2.羧酸酯的一般通式为R1—C—O—R2
3.饱和一元羧酸和饱和一元醇反应生成酯的通式为
CnH2nO2
4.饱和一元羧酸与上述碳原子数相同的酯互为同分
异构体。酯1.酯的物理性质 ①低级酯是具有芳香气味的液体。 ②密度一般比水的小。 ③难溶于水,易溶于乙醇和乙醚等有机溶剂。 酯存在于各种水果和花草中。如香蕉里含有乙酸异戊酯,苹果里含有戊酸戊酯等。酯可用作溶剂,也可用作制备饮料和糖果的香料。 酯 酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。 酯的化学性质之一是可以发生水解反应,在酸性、
碱性条件下,水解程度是否相同?酯课本63页:思考与交流(1)由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸
出乙酸乙酯可提高其产率。(2)使用过量的乙醇,可提高乙酸转化为乙酸乙酯的
产率。根据化学平衡原理,提高乙酸乙酯产率的措施有:(3)使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。生成乙酸乙酯的反应酯一、乙酸:
官能团为羧基, 能解离出H+,使乙酸显酸性;
羧基中的-OH易发生取代反应。二、酯化与水解的关系:羧酸+醇 酯+水。三、酯水解的规律:酯在无机酸、碱的催化下,均
能发生水解反应,其中在酸性条件下水解是可逆
的,在碱性条件下水解是不可逆的。1.食醋的主要成分是乙酸,下列物质中,能与乙酸发生反应的是
①石蕊 ②乙醇 ③金属铝 ④氧化镁
⑤碳酸钙 ⑥氢氧化铜A.①③④⑤⑥
C.①④⑤⑥B.②③④⑤
D.全部√2. 与足量的 NaOH溶
液充分反应,消耗的NaOH的物质的量为
A.5 mol B.4 mol C.3 mol D.2 mol√将此酯基反写后改为-COO-,答案是什么?注意啦!
1 mol由羧酸与苯酚形成的酯基官能团,与NaOH反应时,消耗2mol NaOH。3.若乙酸分子中的氧都是18O,乙醇分子中的氧都
是16O,二者在浓硫酸作用下发生反应,一段时间后,分子中含有18O的物质有
A. 1种 B. 2种 C. 3 种 D. 4种√4. 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制
得乙酸丁酯,反应温度为115~125℃,
反应装置如图所示,下列对该实验的
描述错误的是
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、NaOH溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率√5.某羧酸酯的分子式为C18H26O5,1 mol该酯完全水解可得到1 mol羧酸和2 mol乙醇,该羧酸的分子式为
A.C14H18O5 B.C14H16O4
C.C16H22O5 D.C16H20O5√有许多人是用青春的幸福作为成功的代价的。
——莫扎特
“醋”在中国古称“酢”、“苦酒”等,经常喝
醋能够起到消除疲劳等作用,醋还有治感冒的作用。
醋是乙酸的水溶液,乙酸具有哪些性质呢?1.了解羧酸和酯的组成和结构特点。
2.了解羧酸的分类及乙酸、酯的物理性质及存在。
3.掌握乙酸和乙酸乙酯的结构特点和主要性质,理解
乙酸的酯化反应和乙酸乙酯水解反应的基本规律。
(重点)
4.掌握羧酸和酯之间的相互转化,学会其在合成与推
断中的应用。 (难点)羧酸的概念和分类请同学们根据下列知识点快速阅读课本第60~61页
的内容。1.定义:由烃基与羧基相连构成的有机化合物。烃基不同羧基数目脂肪酸芳香酸一元羧酸二元羧酸多元羧酸2.分类3.饱和一元羧酸通式:CnH2n+1COOH或CnH2nO2羧酸的概念和分类通过乙酸的核磁共振氢谱,你能获取什么信息?乙酸—C—OHCH3COOH(或CH3—COOH)结构简式:结构式:官能团:乙酸常温下为无色液体强烈刺激性气味与水、酒精以任意比互溶16.6℃,当温度低于熔点时,易凝结成
冰一样的晶体。(冰醋酸由此得名)气味:色态:溶解性:熔点:乙酸下列关于乙酸的说法中不正确的是( )
A.乙酸是一种重要的有机酸,是具有强烈刺激性气
味的液体
B.乙酸分子中含有四个氢原子,所以乙酸是四元酸
C.无水乙酸又称冰醋酸,它是纯净物
D.乙酸易溶于水和乙醇【即时巩固】B乙酸1.乙酸具有酸的通性:①使紫色石蕊试液变色:②与活泼金属反应:2CH3COOH+Fe (CH3COO)2Fe+H2↑日常生活中,为什么可以用醋除去水垢(水垢的
主要成分包括CaCO3) ?说明乙酸具有什么性质?③与碱性氧化物反应:2CH3COOH+Na2O 2CH3COONa+H2O④与碱反应:CH3COOH+NaOH CH3COONa+H2O⑤与盐反应:2CH3COOH+Na2CO3 2CH3COONa+H2O+CO2↑乙酸可以用几种方法证明乙酸是弱酸?证明乙酸是弱酸的方法:
(1)配制一定浓度的乙酸测定pH;
(2)在相同条件下与同浓度的盐酸比较导电性;
(3)在相同条件下与同浓度的盐酸比较与金属反应的速率;
(4)测定乙酸钠溶液的酸碱性。【思考与交流】 乙酸酸性:乙酸>碳酸>苯酚探究实验 乙酸、碳酸、苯酚的酸性强弱【实验】某化学兴趣小组用下面两套实验装置来验证
乙酸、碳酸、苯酚的酸性强弱,你认为哪套更合理?
并写出有关反应的化学方程式。乙酸根据下表比较醇、酚、羧酸中羟基活泼性比碳
酸弱比碳酸强能能能能能不能不能不能能,不
产生CO2不能能 能增 强中性乙酸自然界中的有机酸
(1)甲酸:HCOOH(蚁酸)
(2)苯甲酸:C6H5COOH (安息香酸)
(3)草酸:HOOC-COOH (乙二酸)
(4)乳酸: 厨师烧鱼时常加醋并加点酒,这样鱼的味道就变
得无腥、香醇,特别鲜美。这是为什么?乙酸1.定义:
含氧酸和醇起作用,生成酯和水的反应叫做酯
化反应。
浓硫酸作用:催化剂、吸水剂什么是酯化反应?其反应本质是什么?乙酸方式一:酸脱氢、醇脱羟基方式二:酸脱羟基、醇脱氢2.探究酯化反应可能的脱水方式
——同位素示踪法乙酸实验验证:同位素示踪法酯化反应的本质:酸脱羟基、醇脱羟基氢。 CH3—C—O—H + H—18O—C2H5 OCH3—C—18O—C2H5+H2OO乙酸酯化反应属于( )
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应【即时巩固】D乙酸
1.酯的定义:羧酸分子羧基中的-OH被-OR′取代后
的产物。
2.羧酸酯的一般通式为R1—C—O—R2
3.饱和一元羧酸和饱和一元醇反应生成酯的通式为
CnH2nO2
4.饱和一元羧酸与上述碳原子数相同的酯互为同分
异构体。酯1.酯的物理性质 ①低级酯是具有芳香气味的液体。 ②密度一般比水的小。 ③难溶于水,易溶于乙醇和乙醚等有机溶剂。 酯存在于各种水果和花草中。如香蕉里含有乙酸异戊酯,苹果里含有戊酸戊酯等。酯可用作溶剂,也可用作制备饮料和糖果的香料。 酯 酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。 酯的化学性质之一是可以发生水解反应,在酸性、
碱性条件下,水解程度是否相同?酯课本63页:思考与交流(1)由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸
出乙酸乙酯可提高其产率。(2)使用过量的乙醇,可提高乙酸转化为乙酸乙酯的
产率。根据化学平衡原理,提高乙酸乙酯产率的措施有:(3)使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。生成乙酸乙酯的反应酯一、乙酸:
官能团为羧基, 能解离出H+,使乙酸显酸性;
羧基中的-OH易发生取代反应。二、酯化与水解的关系:羧酸+醇 酯+水。三、酯水解的规律:酯在无机酸、碱的催化下,均
能发生水解反应,其中在酸性条件下水解是可逆
的,在碱性条件下水解是不可逆的。1.食醋的主要成分是乙酸,下列物质中,能与乙酸发生反应的是
①石蕊 ②乙醇 ③金属铝 ④氧化镁
⑤碳酸钙 ⑥氢氧化铜A.①③④⑤⑥
C.①④⑤⑥B.②③④⑤
D.全部√2. 与足量的 NaOH溶
液充分反应,消耗的NaOH的物质的量为
A.5 mol B.4 mol C.3 mol D.2 mol√将此酯基反写后改为-COO-,答案是什么?注意啦!
1 mol由羧酸与苯酚形成的酯基官能团,与NaOH反应时,消耗2mol NaOH。3.若乙酸分子中的氧都是18O,乙醇分子中的氧都
是16O,二者在浓硫酸作用下发生反应,一段时间后,分子中含有18O的物质有
A. 1种 B. 2种 C. 3 种 D. 4种√4. 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制
得乙酸丁酯,反应温度为115~125℃,
反应装置如图所示,下列对该实验的
描述错误的是
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、NaOH溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率√5.某羧酸酯的分子式为C18H26O5,1 mol该酯完全水解可得到1 mol羧酸和2 mol乙醇,该羧酸的分子式为
A.C14H18O5 B.C14H16O4
C.C16H22O5 D.C16H20O5√有许多人是用青春的幸福作为成功的代价的。
——莫扎特
