2018-2019学年高中化学人教版选修3课件:第1章第1节原子结构(41张)
文档属性
| 名称 | 2018-2019学年高中化学人教版选修3课件:第1章第1节原子结构(41张) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-20 00:00:00 | ||
图片预览









文档简介
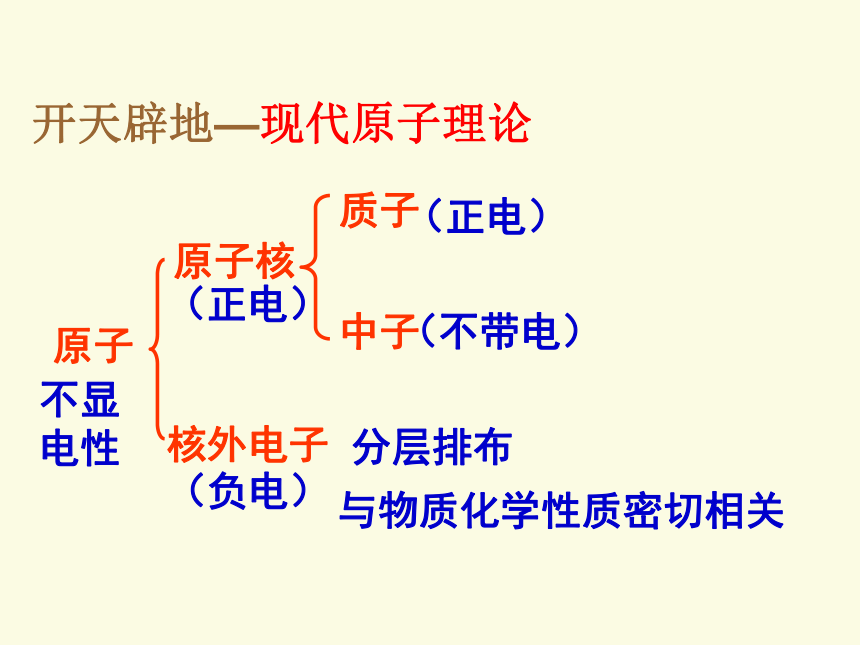
课件41张PPT。原子结构宇宙大爆炸宇宙大爆炸开天辟地—原子的诞生——勒梅特近代原子论发现电子带核原子结构模型轨道原子结构模型电子云模型开天辟地—原子理论发展:原子原子核核外电子质子中子(正电)不显
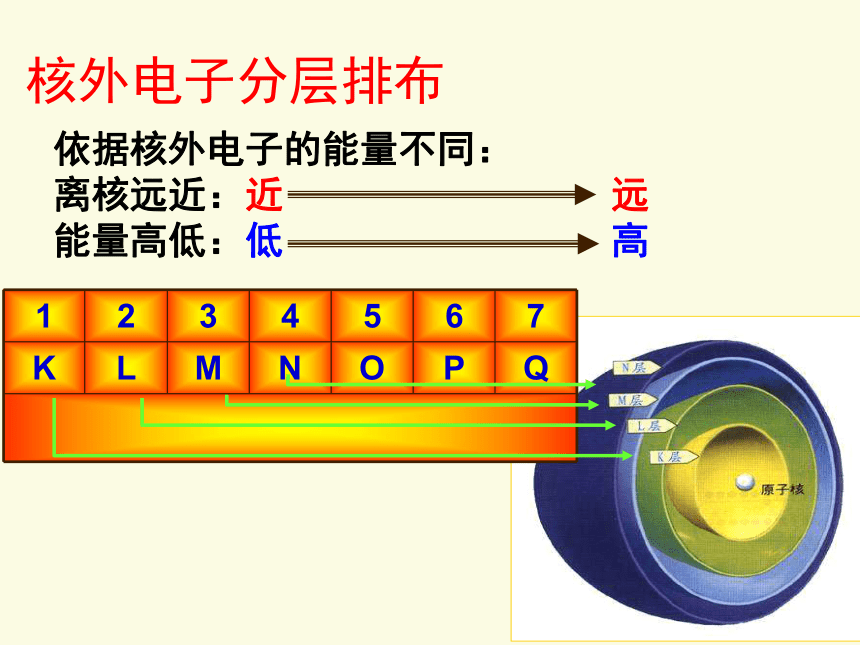
电性 (负电)(正电)(不带电)分层排布与物质化学性质密切相关 开天辟地—现代原子理论二、能层与能级(1)能层 在多电子的原子核外电子的能量是不同的,按电子的能量差异,可以将核外电子分成不同的能层。依据核外电子的能量不同:
离核远近:近 远
能量高低:低 高核外电子分层排布(1)各能层最多能容纳2n2个电子。
即:能层序号 1 2 3 4 5 6 7
符 号 K L M N O P Q
最多电子数 2 8 18 32 50 72 98
(2)最外层电子数目不超过8个(K层为最外层时
不超过2个);次外层电子数最多不超过18
个;倒数第三层不超过32个。原子核外电子分层排布规律:(3)核外电子总是尽先排满能量最低、离核最近
的能层,然后才由里往外,依次排在能量
较高能层。而失电子总是先失最外层电子。注意: 以上几点是相互联系的,不能孤立地理解,必须同时满足各项要求。
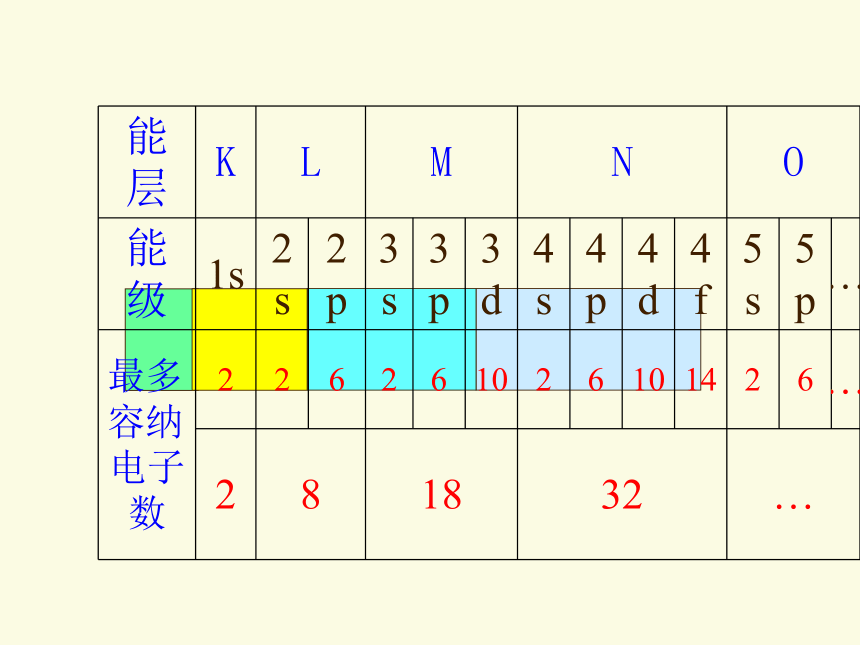
(2)能级表示方法及各能级所容纳的最多电子数: 在多电子原子中,同一能层的电子,能量可以不同,还可以把它们分成能级。能层最多可容纳的电子数为2n2个。【学与问】1.原子核外电子的每一个能层最多可容纳的电子数与能层的序数(n)间存在什么关系?【学与问】2.不同的能层分别有多少个能级,与能层的序数(n)间存在什么关系?第一能层只有1个能级(1s),第二能层有2个能级(2s和2p),第3能层有3个能级(3s、3p和3d),依次类推。以s、p、d、f······排序的各能级可容纳的最多电子数依次为1、3、5、7的二倍!【学与问】3.英文字母相同的不同能级中所容纳的最多电子数是否相同? 不同能级中的s级,所容纳的电子数是相同的,但是能量是不同的。①能层的能级数等于该能层序数。
②任一能层的能级总是从s能级开始。
③在每一能层中,能级符号与能量大小的顺序是:ns<np<nd<nf…总结:A.前者大于后者 B.后者大于前者 C.前者等于后者 D.无法确定B练习1:在同一个原子中,M能层上的电子与Q能层上的电子的能量( )能表示核外电子排布【思考】怎样用能层,能级表示核外电子排布?原子结构构造原理与电子排布式练习2:依据以上各能级最多容纳电子数C原子的核外电子排布式可以表示为:1S22S22P2
依照上式请书写 N O F Na Mg Al 的电子排布式问题探究 根据已有知识,试写出K原子的可能电子排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 猜想二: 1s22s22p63s23p64s1 三、构造原理与电子排布式 构造原理:P5
随原子核电荷数递增,绝大多数原子核外电子的排布遵循如右图的排布顺序,这个排布顺序被称为构造原理。【思考】:有何规律?能级交错核 外 电 子 填 充 顺 序 图构造原理: 1s;2s 2p;3s 3p;4s 3d 4p;
规律 5s 4d 5p; 6s 4f 5d 6p;7s 5f 6d问题解释: 猜想一: 1s22s22p63s23p63d1 猜想二: 1s22s22p63s23p64s1 各能层能级能量关系 构造原理中排布顺序的实质(1)相同能层的不同能级的能量高低顺序 :
(2)英文字母相同的不同能级的能量高低顺序:
(3) 不同层不同能级可由下面的公式得出:
-----各能级的能量高低顺序 ns<np<nd<nf1s<2s<3s<4s;2p<3p<4p; 3d<4dns<(n-2)f<(n-1)d<np (n为能层序数)2、根据2n2的规律推算第一到第四电子层最多可以容纳的电子数目为? ???????? 。1、按能量由低到高的顺序排列,正确的一组是:( )
A.1s、2p、3d、4s B.1s、2s、3s、2p
C.2s、2p、3s、3p D.4p、3d、4s、3p2、8、18、32C练习:钙Ca 1s22s22p63s23p64s2钙Ca电子排布式:氢 H
钠 Na
铝 Al1s22s22p63s11s22s22p63s23p11s1 用数字在能级符号右上角表明该能级上的排布的电子数。原子结构示意图电子排布式Li: 1s22s1请写出4~10号元素原子的电子排布式。 4 铍Be
5 硼B
6 碳C
7 氮N
8 氧O
9 氟F
10 氖Ne1s2 2s2
1s2 2s22p1
1s2 2s22p2
1s2 2s22p3
1s2 2s22p4
1s2 2s22p5
1s2 2s22p6【练习】试书写N、Cl、K、26Fe原子的核外电子排布式。 Cl:
K:
26Fe:1s2 2s22p6 3s23p51s2 2s22p6 3s23p6 4s11s2 2s22p6 3s23p63d6 4s2注意书写:1s2 2s22p6 3s23p64s2 3d6练习:请根据构造原理,写出下列元素基态原子的电子排布式:
(1)Ne?????????????? ??? ?? ???。
(2)S ???????????????? ??????。
(3)29Cu ????????? ??? ?????????。
(4)32Ge ????????????? ??????。1s22s22p61s22s22p63s23p41s22s22p63s23p63d104s11s22s22p63s23p63d104s24p2练习:请写出第四周期21—36号元素原子的基态电子排布式。钪Sc: ;
钛Ti: ;
钒V: ;
铬Cr: ;
锰Mn: ;
1s22s22p63s23p63d14s21s22s22p63s23p63d24s21s22s22p63s23p63d34s21s22s22p63s23p63d54s11s22s22p63s23p63d54s2练习:请写出第四周期21—36号元素原子的基态电子排布式。铁Fe: ;
钴Co: ;
镍Ni: ;1s22s22p63s23p63d64s21s22s22p63s23p63d74s21s22s22p63s23p63d84s21s22s22p63s23p63d104s11s22s22p63s23p63d104s21s22s22p63s23p63d104s24p1铜Cu: ;
锌Zn: ;
镓Ga: ; 练习:请写出第四周期21—36号元素原子的基态电子排布式。锗Ge: ;
砷As: ;
硒Se: ;
溴Br: ;
氪Kr: ;1s22s22p63s23p63d104s24p21s22s22p63s23p63d104s24p31s22s22p63s23p63d104s24p41s22s22p63s23p63d104s24p51s22s22p63s23p63d104s24p6P7
【思考与交流】11s22s22p63s23p63d54s11s22s22p63s23p63d104s1练习:1~36号元素中是否都遵循构造原理?
举出能否具体的例子?注 意原子的简化电子排布:原子实[Ne]3s1练习:写出第8号元素氧、第14号元素硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4[Ne]3s23p2[Ar]3d64s2P7
【思考与交流】2下列各原子或离子的电子排布式错误的是( )A. Ca2+ 1s22s22p63s23p6B. O2- 1s22s23p4C. Cl- 1s22s22p63s23p5D. Ar 1s22s22p63s23p6BC练习 1:练习2:
1、电子排布式为1s22s22p63s23p6 某原子, 则该元素的核电荷数是____________ 2、某元素原子的价电子构型为3s23p4, 则此元素在周期表的位置是____________18第3周期,第VIA族4、构造原理揭示的电子排布能级顺序,实质是 各能级能量高低,若以E 表示某能级的能量,下列能量大小顺序中正确的是 ( )
A.E(3s)>E(2s)>E(1s)
B.E(3s)>E(3p)>E(3d)
C.E(4f)>E(4s)>E(3d)
D.E(5s)>E(4s)>E(4f) 3、一个电子排布为1s22s22p63s23p1的元素最可能的价态是( )
A.+1 B.+2 C.+3 D.-1 CA5、下列各原子或离子的电子排布式错误的是( )
A.Al 1s22s22p63s23p1 B.O2- 1s22s22p6
C.Na+ 1s22s22p6 D.Si 1s22s22p2
6、下列表达方式错误的是( )
A.甲烷的电子式
B.氟化钠的电子式
C.硫离子的核外电子排布式 1s22s22p63s23p4
D.碳-12原子符号 126CDC小 结
电性 (负电)(正电)(不带电)分层排布与物质化学性质密切相关 开天辟地—现代原子理论二、能层与能级(1)能层 在多电子的原子核外电子的能量是不同的,按电子的能量差异,可以将核外电子分成不同的能层。依据核外电子的能量不同:
离核远近:近 远
能量高低:低 高核外电子分层排布(1)各能层最多能容纳2n2个电子。
即:能层序号 1 2 3 4 5 6 7
符 号 K L M N O P Q
最多电子数 2 8 18 32 50 72 98
(2)最外层电子数目不超过8个(K层为最外层时
不超过2个);次外层电子数最多不超过18
个;倒数第三层不超过32个。原子核外电子分层排布规律:(3)核外电子总是尽先排满能量最低、离核最近
的能层,然后才由里往外,依次排在能量
较高能层。而失电子总是先失最外层电子。注意: 以上几点是相互联系的,不能孤立地理解,必须同时满足各项要求。
(2)能级表示方法及各能级所容纳的最多电子数: 在多电子原子中,同一能层的电子,能量可以不同,还可以把它们分成能级。能层最多可容纳的电子数为2n2个。【学与问】1.原子核外电子的每一个能层最多可容纳的电子数与能层的序数(n)间存在什么关系?【学与问】2.不同的能层分别有多少个能级,与能层的序数(n)间存在什么关系?第一能层只有1个能级(1s),第二能层有2个能级(2s和2p),第3能层有3个能级(3s、3p和3d),依次类推。以s、p、d、f······排序的各能级可容纳的最多电子数依次为1、3、5、7的二倍!【学与问】3.英文字母相同的不同能级中所容纳的最多电子数是否相同? 不同能级中的s级,所容纳的电子数是相同的,但是能量是不同的。①能层的能级数等于该能层序数。
②任一能层的能级总是从s能级开始。
③在每一能层中,能级符号与能量大小的顺序是:ns<np<nd<nf…总结:A.前者大于后者 B.后者大于前者 C.前者等于后者 D.无法确定B练习1:在同一个原子中,M能层上的电子与Q能层上的电子的能量( )能表示核外电子排布【思考】怎样用能层,能级表示核外电子排布?原子结构构造原理与电子排布式练习2:依据以上各能级最多容纳电子数C原子的核外电子排布式可以表示为:1S22S22P2
依照上式请书写 N O F Na Mg Al 的电子排布式问题探究 根据已有知识,试写出K原子的可能电子排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 猜想二: 1s22s22p63s23p64s1 三、构造原理与电子排布式 构造原理:P5
随原子核电荷数递增,绝大多数原子核外电子的排布遵循如右图的排布顺序,这个排布顺序被称为构造原理。【思考】:有何规律?能级交错核 外 电 子 填 充 顺 序 图构造原理: 1s;2s 2p;3s 3p;4s 3d 4p;
规律 5s 4d 5p; 6s 4f 5d 6p;7s 5f 6d问题解释: 猜想一: 1s22s22p63s23p63d1 猜想二: 1s22s22p63s23p64s1 各能层能级能量关系 构造原理中排布顺序的实质(1)相同能层的不同能级的能量高低顺序 :
(2)英文字母相同的不同能级的能量高低顺序:
(3) 不同层不同能级可由下面的公式得出:
-----各能级的能量高低顺序 ns<np<nd<nf1s<2s<3s<4s;2p<3p<4p; 3d<4dns<(n-2)f<(n-1)d<np (n为能层序数)2、根据2n2的规律推算第一到第四电子层最多可以容纳的电子数目为? ???????? 。1、按能量由低到高的顺序排列,正确的一组是:( )
A.1s、2p、3d、4s B.1s、2s、3s、2p
C.2s、2p、3s、3p D.4p、3d、4s、3p2、8、18、32C练习:钙Ca 1s22s22p63s23p64s2钙Ca电子排布式:氢 H
钠 Na
铝 Al1s22s22p63s11s22s22p63s23p11s1 用数字在能级符号右上角表明该能级上的排布的电子数。原子结构示意图电子排布式Li: 1s22s1请写出4~10号元素原子的电子排布式。 4 铍Be
5 硼B
6 碳C
7 氮N
8 氧O
9 氟F
10 氖Ne1s2 2s2
1s2 2s22p1
1s2 2s22p2
1s2 2s22p3
1s2 2s22p4
1s2 2s22p5
1s2 2s22p6【练习】试书写N、Cl、K、26Fe原子的核外电子排布式。 Cl:
K:
26Fe:1s2 2s22p6 3s23p51s2 2s22p6 3s23p6 4s11s2 2s22p6 3s23p63d6 4s2注意书写:1s2 2s22p6 3s23p64s2 3d6练习:请根据构造原理,写出下列元素基态原子的电子排布式:
(1)Ne?????????????? ??? ?? ???。
(2)S ???????????????? ??????。
(3)29Cu ????????? ??? ?????????。
(4)32Ge ????????????? ??????。1s22s22p61s22s22p63s23p41s22s22p63s23p63d104s11s22s22p63s23p63d104s24p2练习:请写出第四周期21—36号元素原子的基态电子排布式。钪Sc: ;
钛Ti: ;
钒V: ;
铬Cr: ;
锰Mn: ;
1s22s22p63s23p63d14s21s22s22p63s23p63d24s21s22s22p63s23p63d34s21s22s22p63s23p63d54s11s22s22p63s23p63d54s2练习:请写出第四周期21—36号元素原子的基态电子排布式。铁Fe: ;
钴Co: ;
镍Ni: ;1s22s22p63s23p63d64s21s22s22p63s23p63d74s21s22s22p63s23p63d84s21s22s22p63s23p63d104s11s22s22p63s23p63d104s21s22s22p63s23p63d104s24p1铜Cu: ;
锌Zn: ;
镓Ga: ; 练习:请写出第四周期21—36号元素原子的基态电子排布式。锗Ge: ;
砷As: ;
硒Se: ;
溴Br: ;
氪Kr: ;1s22s22p63s23p63d104s24p21s22s22p63s23p63d104s24p31s22s22p63s23p63d104s24p41s22s22p63s23p63d104s24p51s22s22p63s23p63d104s24p6P7
【思考与交流】11s22s22p63s23p63d54s11s22s22p63s23p63d104s1练习:1~36号元素中是否都遵循构造原理?
举出能否具体的例子?注 意原子的简化电子排布:原子实[Ne]3s1练习:写出第8号元素氧、第14号元素硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4[Ne]3s23p2[Ar]3d64s2P7
【思考与交流】2下列各原子或离子的电子排布式错误的是( )A. Ca2+ 1s22s22p63s23p6B. O2- 1s22s23p4C. Cl- 1s22s22p63s23p5D. Ar 1s22s22p63s23p6BC练习 1:练习2:
1、电子排布式为1s22s22p63s23p6 某原子, 则该元素的核电荷数是____________ 2、某元素原子的价电子构型为3s23p4, 则此元素在周期表的位置是____________18第3周期,第VIA族4、构造原理揭示的电子排布能级顺序,实质是 各能级能量高低,若以E 表示某能级的能量,下列能量大小顺序中正确的是 ( )
A.E(3s)>E(2s)>E(1s)
B.E(3s)>E(3p)>E(3d)
C.E(4f)>E(4s)>E(3d)
D.E(5s)>E(4s)>E(4f) 3、一个电子排布为1s22s22p63s23p1的元素最可能的价态是( )
A.+1 B.+2 C.+3 D.-1 CA5、下列各原子或离子的电子排布式错误的是( )
A.Al 1s22s22p63s23p1 B.O2- 1s22s22p6
C.Na+ 1s22s22p6 D.Si 1s22s22p2
6、下列表达方式错误的是( )
A.甲烷的电子式
B.氟化钠的电子式
C.硫离子的核外电子排布式 1s22s22p63s23p4
D.碳-12原子符号 126CDC小 结
