人教版九年级上册 化学 第六单元 碳和碳的氧化物 复习(共46张PPT)
文档属性
| 名称 | 人教版九年级上册 化学 第六单元 碳和碳的氧化物 复习(共46张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-20 00:00:00 | ||
图片预览







文档简介
第六单元复习
碳和碳的氧化物
我会猜
真真假假两包公,双双坐入煤炉中。
真包得道上青天,假包气得脸通红。
真包公指的是__假包公指的是___。
发生反应的化学方程式为
C
CuO
引言
碳和碳的化合物可以说是化学世界里最庞大的家族。他们有超过三千万的成员。刻划玻璃用的金刚石。
写字用的铅笔芯、制汽水用的二氧化碳、制水泥用的石灰石以及煤和石油、甲烷(通常称为沼气)乙醇
(酒精)、醋酸、糖、蛋白质、塑料纤维、橡胶、有机涂料和有机粘合剂等都是碳和碳的化合物。他们是在国民经济和我们的日常生活里占有很重要的地位。
碳家族的兄弟俩
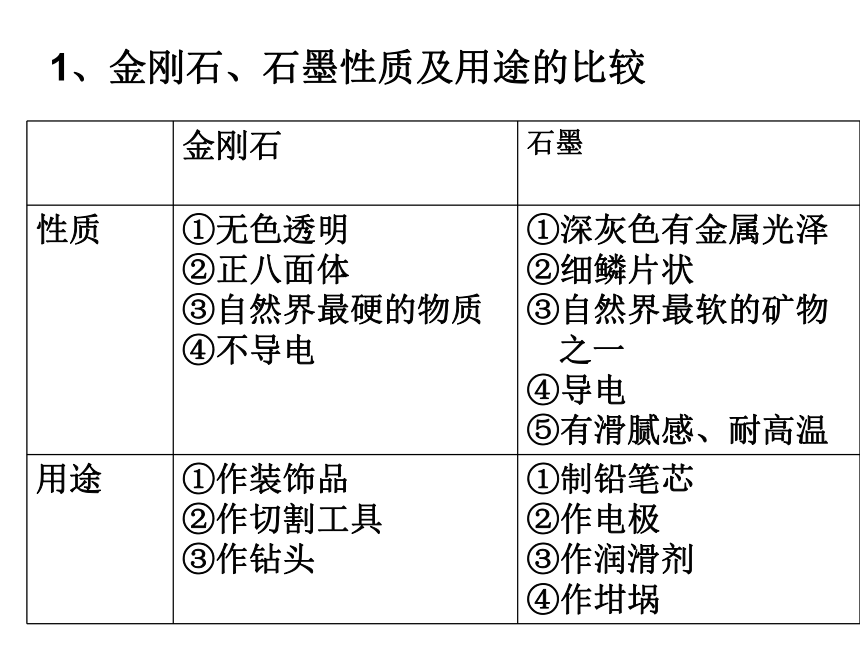
1、金刚石、石墨性质及用途的比较
金刚石 石墨
性质 无色透明
正八面体
自然界最硬的物质
不导电 深灰色有金属光泽
细鳞片状
自然界最软的矿物之一
导电
有滑腻感、耐高温
用途 作装饰品
作切割工具
作钻头 制铅笔芯
作电极
作润滑剂
作坩埚
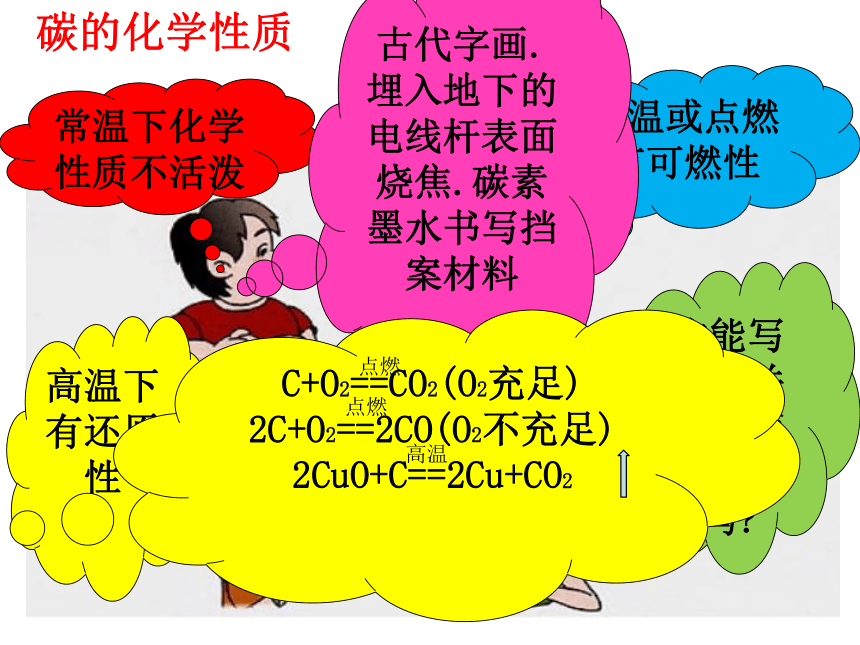
碳的化学性质
高温或点燃有可燃性
常温下化学性质不活泼
你能写出有关的反应方程式吗?
高温下有还原性
古代字画.埋入地下的电线杆表面烧焦.碳素墨水书写挡案材料
C+O2==CO2(O2充足) 2C+O2==2CO(O2不充足) 2CuO+C==2Cu+CO2
点燃
点燃
高温
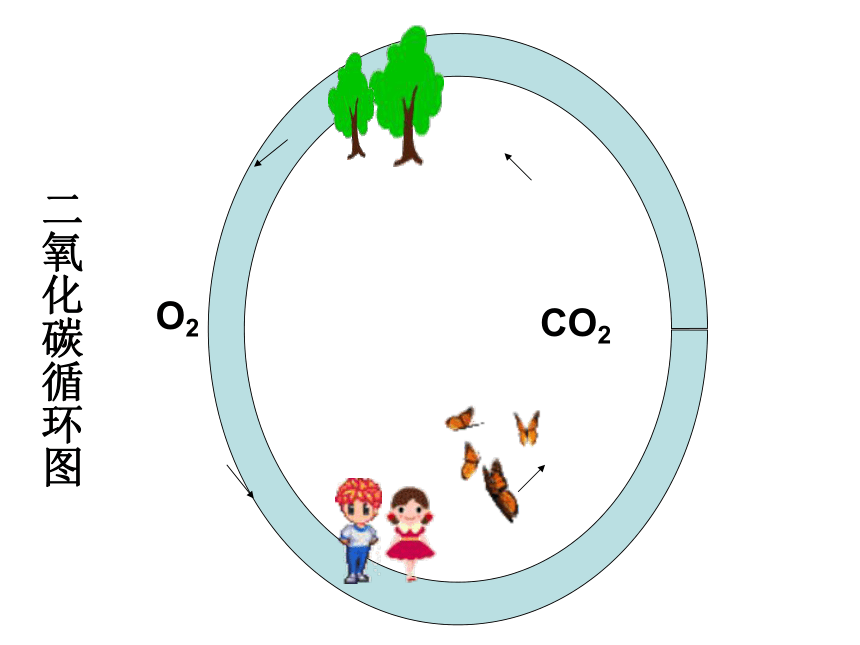
O2
CO2
二氧化碳循环图
探究实验
实验器材: 阶梯状铜片、烧杯
实验药品: 二氧化碳气体、 短蜡烛两只
实验目的: 探究CO2是否具有可燃性和助燃性.
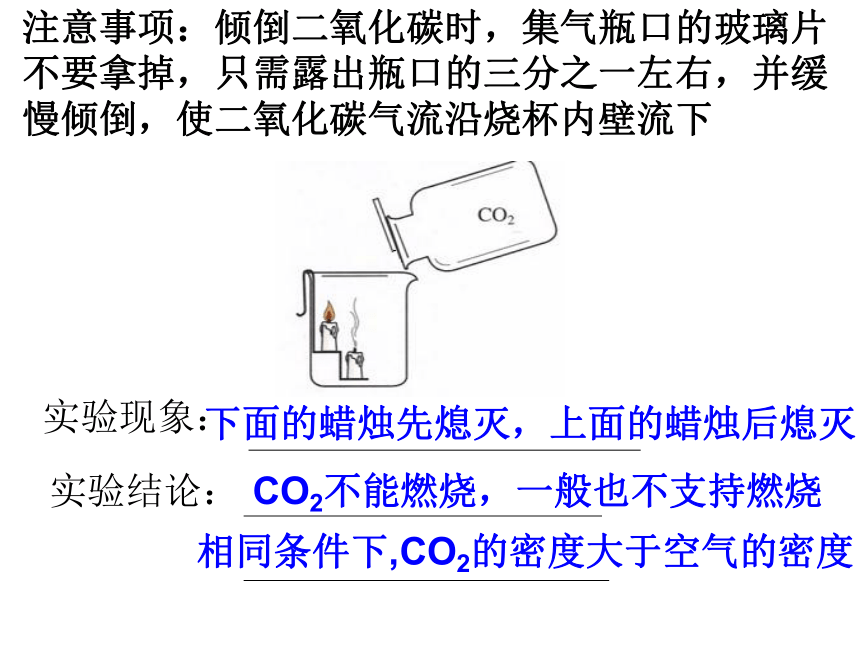
注意事项:倾倒二氧化碳时,集气瓶口的玻璃片不要拿掉,只需露出瓶口的三分之一左右,并缓慢倾倒,使二氧化碳气流沿烧杯内壁流下
下面的蜡烛先熄灭,上面的蜡烛后熄灭
CO2不能燃烧,一般也不支持燃烧
相同条件下,CO2的密度大于空气的密度
二、CO2的物理性质
1、通常情况下是___色、____气味的气体。 能溶于水,密度大于空气.它的固体叫________,升华时,吸收大量
_____,因此可作_________。
无
无
干冰
热
致冷剂
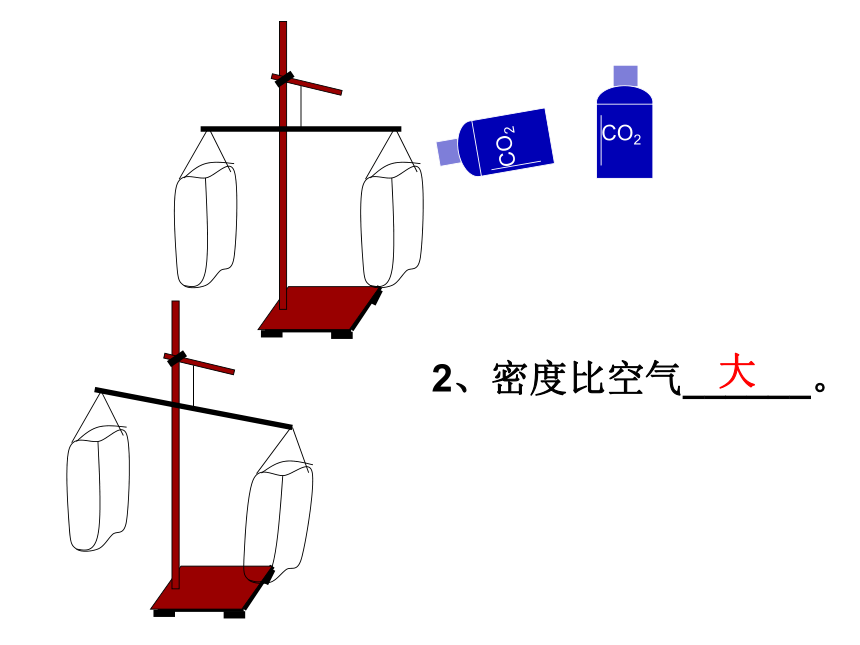
2、密度比空气______。
大
探究实验
实验器材: 饮料瓶
实验药品: 二氧化碳气体、 蒸馏水
实验目的: 探究CO2能否溶于水?
实验操作
实验现象
结 论
方案二:
CO2能溶于水
结论:
现 象:
把充满CO2气体的试管倒扣在水中
试管内液面上升
联系实际:
久未开启的放置大白菜的地窖底部二氧化碳含量较高,若贸然进去有窒息的危险。
1、为什么地窖底部二氧化碳含量较高?
2、为防不测,人们在进入地窖前,常做灯火实验,为什么?
实验器材: 喷壶、酒精灯
实验药品: 二氧化碳气体、 蒸馏水
醋酸,浸有紫色石蕊试液的滤纸葫芦
实验目的: 探究CO2能否与水反应?
实验现象:
对应的结论:
水不能使紫色石蕊变红
3、直接放入二氧化碳的葫芦不变色
CO2不能使紫色石蕊变红
4、喷水后放入二氧化碳的葫芦变红
CO2和水反应生成碳酸CO2+H2O=H2CO3
5、变红的葫芦烘干后又变为紫色
2、喷水的葫芦不变色
1、喷酸的葫芦变红色
酸能使紫色石蕊变红
2、CO2不能供呼吸。
3、CO2跟水反应。
CO2+H2O = H2CO3
二、CO2的化学性质
二、CO2的化学性质
1、CO2不能燃烧,不能支持燃烧。
2、CO2不能供呼吸。
CO2+H2O = H2CO3
二、CO2的化学性质
CO2+H2O = H2CO3
H2CO3 = CO2↑ +H2O
4、CO2与石灰水[Ca(OH)2]反应。
CO2+ Ca(OH)2 = H2O +CaCO3 ↓
此反应可用来鉴定____
CO2
5.参与光合作用
6.与C反应(氧化性)
CO2+C===2CO
高温
人工降雨
灭火
工业原料
致冷剂
光合作用
CO2的用途
我会归纳:CO的物理性质
无色无味气体
难溶于水
密度略小于空气
我会归纳:CO的化学性质
可燃性
还原性
毒性
我还能写出方程式呢!
2CO+O2==2CO2
Fe2O3+3CO==2Fe+3CO2
CuO+CO==Cu+CO2
点燃
高温
CO易与血红蛋白结合,使血红蛋白不能很好的与结合,造成生物体缺氧中毒而亡
燃烧着煤炉中发生的化学反应
你知道可燃性气体有哪些吗?
氢气
一氧化碳一
甲烷
2H2+O2== 2H2O
2CO+O2==2CO2
CH4+2O2==CO2+2H2O
点燃
点燃
点燃
怎样鉴别它们呀?
检验燃烧的产物
C
既有可燃性又有还原性的物质有哪些呢?
3、碳、氢气、一氧化碳的比较
碳 氢气 一氧化碳
化学性质 常
温 不活泼,受日光照射或与空气、水接触都不易反应 稳定.与空气、水接触,都不易起反应 稳定,与空气、水接触,都不易起反应
加
热
或
点
燃 能跟很多物质反应
可燃性
燃烧充分或燃烧不充分两种情况
②还原性
跟金属氧化物(氧化铜等)或非金属氧化物(二氧化碳等)反应
能跟很多物质发生反应
①可燃性
(跟氧气的反应)
②还原性(跟氧化铜等金属氧化物的反应) 能跟很多物质发生反应
①可燃性
(跟氧气的反应)
②还原性(跟氧化铜等金属氧化物的反应)
某混合气体,它可能是由CO、CO2、H2及N2的两种或两种以上气体的混合物,现将该混合气体依次通过下图中甲、乙、丙三个装置一段时间,反应平稳进行,甲瓶无明显现象,丙瓶中石灰水变浑浊,小橡皮泡A逐渐膨胀变大。(假设试验前,装置内空气已排尽,甲、丙两瓶中澄清石灰水均是足量的)。
(1)写出乙装置中的实验现象
黑色粉末变红
CO
CO2
收集尾气,防止污染空气
甲:检验混合物中是否存在CO2
丙:检验产物中是否存在CO2
金刚石( )
石墨( )
C60
物理性质
颜色
状态
光泽
硬度
导电性
熔点
润滑性
用途
互相转化
无色透明
深灰色不透明
正八面体形状固体
细鳞片状固体
形似足球
加工琢磨有光泽
有金属光泽
天然物中硬度最大
质软
质脆
不导电
导电
不导电
很高
很高
无
有
钻石.玻璃刀.钻头
铅笔芯.电极.润滑剂
超导体
金刚石
石墨
C
C
金刚石和石墨的物理性质不同的原因
单质的种类与元素的种类的关系
怎样证明金刚石和石墨是由碳元素组成的
无定形炭
木 炭
活性炭
焦 炭
炭 黑
燃料
除去异味.色素
防毒面具
疏松多孔
吸附性
冶炼金属
橡胶添加剂.油墨.鞋油
碳原子排列的方式不同
单质的种类多于元素的种类
可燃性
还原性
请将下列物质与相关用途连起来
A、石墨 冰箱去味剂
B、炭黑 制炭素墨水
C、活性炭 切割大理石
D、焦炭 冶炼金属
E、金刚石 干电池电极
F. C60 超导材料
碳单质的化学性质
常温
稳定
古代用墨书写的字画
埋入地下的电线杆表面烧焦
用碳素墨水书写挡案材料
原因
高温
可燃性
还原性
充分燃烧
不充分燃烧
C + O2=== CO2
2C + O2 === 2CO
2CuO + C === 2Cu + CO2
C
CuO
得氧
被氧化
氧化反应
还原剂
还原性
失氧
被还原
还原反应
氧化剂
氧化性
反应物的量不同.产物不同
点燃
点燃
信息
高温
碳的化合物
CO2
物性
无色无味气体
能溶于水
汽水
干冰
制冷剂
人工降雨
密度大于空气
化性
1.不燃烧.也不支持燃烧
灭火
2.不能供给呼吸
灯火实验
3.和水反应
4.和Ca(OH)2反应
5.参与光和作用
气体肥料
6.氧化性
CO2 + H2O == H2CO3
Ca(OH)2+CO2==CaCO3+H2O
CO2+C===2CO
高温
CO2制法
实验室
工业
原料
不用Na2CO3原因
不用稀H2SO4原因
原理
CaCO3+2HCl==CaCl2+CO2 +H2O
装置
与用H2O2溶液制取O2相同
步骤
收集
向上排空气法
密度大于空气
检验
澄清石灰水
变浑浊
是CO2
验满
燃着木条
瓶口
熄灭
已满
高温煅烧石灰石
CaCO3===CaO+CO2
怎样检验CaO中是否有CaCO3
怎样除去CaO中的CaCO3
石灰石.稀盐酸
不用浓盐酸原因
高温
查.装(先固后液).收.验
加入稀盐酸
高温煅烧
没有收集到二氧化碳的原因
收集的二氧化碳不纯的原因
没有收集满二氧化碳的原因
装置漏气
1.导管没有伸到集气瓶的底部
2.使用了浓盐酸
1.药品太少
2.装置漏气
实验室制取二氧化碳的装置
一氧化碳
物性
无色无味气体
密度略小于空气
报警器安装
难溶于水
煤炉上放盆水不能防中毒
化性
毒性
易与血红蛋白结合.使人中毒而亡
可燃性
还原性
2CO+O2===2CO2
Fe2O3+3CO===2Fe+3CO2
用途
燃料
冶炼金属
煤气
加有味气体作用?
泄露处理方法?
现象
点燃
高温
碳的其它化合物
甲烷
酒精
纯碱
小苏打
CH4
C2H5OH
Na2CO3
NaHCO3
物性
化性
物性
化性
CH4+2O2==CO2+2H2O
C2H5OH+3O2==2CO2+3H2O
无色无味气体.难溶于水.密度略小于空气
无色有特殊气味液体.能和水以任意比例互溶
(可燃性)
燃料
(可燃性)
较清洁能源
较清洁能源
燃料
点燃
点燃
木炭、一氧化碳分别还原氧化铜的两套装置的比较
看故事 想问题
看故事 想问题
我会归纳:CO的物理性质
Huanjing baohu
碳和碳的氧化物
我会猜
真真假假两包公,双双坐入煤炉中。
真包得道上青天,假包气得脸通红。
真包公指的是__假包公指的是___。
发生反应的化学方程式为
C
CuO
引言
碳和碳的化合物可以说是化学世界里最庞大的家族。他们有超过三千万的成员。刻划玻璃用的金刚石。
写字用的铅笔芯、制汽水用的二氧化碳、制水泥用的石灰石以及煤和石油、甲烷(通常称为沼气)乙醇
(酒精)、醋酸、糖、蛋白质、塑料纤维、橡胶、有机涂料和有机粘合剂等都是碳和碳的化合物。他们是在国民经济和我们的日常生活里占有很重要的地位。
碳家族的兄弟俩
1、金刚石、石墨性质及用途的比较
金刚石 石墨
性质 无色透明
正八面体
自然界最硬的物质
不导电 深灰色有金属光泽
细鳞片状
自然界最软的矿物之一
导电
有滑腻感、耐高温
用途 作装饰品
作切割工具
作钻头 制铅笔芯
作电极
作润滑剂
作坩埚
碳的化学性质
高温或点燃有可燃性
常温下化学性质不活泼
你能写出有关的反应方程式吗?
高温下有还原性
古代字画.埋入地下的电线杆表面烧焦.碳素墨水书写挡案材料
C+O2==CO2(O2充足) 2C+O2==2CO(O2不充足) 2CuO+C==2Cu+CO2
点燃
点燃
高温
O2
CO2
二氧化碳循环图
探究实验
实验器材: 阶梯状铜片、烧杯
实验药品: 二氧化碳气体、 短蜡烛两只
实验目的: 探究CO2是否具有可燃性和助燃性.
注意事项:倾倒二氧化碳时,集气瓶口的玻璃片不要拿掉,只需露出瓶口的三分之一左右,并缓慢倾倒,使二氧化碳气流沿烧杯内壁流下
下面的蜡烛先熄灭,上面的蜡烛后熄灭
CO2不能燃烧,一般也不支持燃烧
相同条件下,CO2的密度大于空气的密度
二、CO2的物理性质
1、通常情况下是___色、____气味的气体。 能溶于水,密度大于空气.它的固体叫________,升华时,吸收大量
_____,因此可作_________。
无
无
干冰
热
致冷剂
2、密度比空气______。
大
探究实验
实验器材: 饮料瓶
实验药品: 二氧化碳气体、 蒸馏水
实验目的: 探究CO2能否溶于水?
实验操作
实验现象
结 论
方案二:
CO2能溶于水
结论:
现 象:
把充满CO2气体的试管倒扣在水中
试管内液面上升
联系实际:
久未开启的放置大白菜的地窖底部二氧化碳含量较高,若贸然进去有窒息的危险。
1、为什么地窖底部二氧化碳含量较高?
2、为防不测,人们在进入地窖前,常做灯火实验,为什么?
实验器材: 喷壶、酒精灯
实验药品: 二氧化碳气体、 蒸馏水
醋酸,浸有紫色石蕊试液的滤纸葫芦
实验目的: 探究CO2能否与水反应?
实验现象:
对应的结论:
水不能使紫色石蕊变红
3、直接放入二氧化碳的葫芦不变色
CO2不能使紫色石蕊变红
4、喷水后放入二氧化碳的葫芦变红
CO2和水反应生成碳酸CO2+H2O=H2CO3
5、变红的葫芦烘干后又变为紫色
2、喷水的葫芦不变色
1、喷酸的葫芦变红色
酸能使紫色石蕊变红
2、CO2不能供呼吸。
3、CO2跟水反应。
CO2+H2O = H2CO3
二、CO2的化学性质
二、CO2的化学性质
1、CO2不能燃烧,不能支持燃烧。
2、CO2不能供呼吸。
CO2+H2O = H2CO3
二、CO2的化学性质
CO2+H2O = H2CO3
H2CO3 = CO2↑ +H2O
4、CO2与石灰水[Ca(OH)2]反应。
CO2+ Ca(OH)2 = H2O +CaCO3 ↓
此反应可用来鉴定____
CO2
5.参与光合作用
6.与C反应(氧化性)
CO2+C===2CO
高温
人工降雨
灭火
工业原料
致冷剂
光合作用
CO2的用途
我会归纳:CO的物理性质
无色无味气体
难溶于水
密度略小于空气
我会归纳:CO的化学性质
可燃性
还原性
毒性
我还能写出方程式呢!
2CO+O2==2CO2
Fe2O3+3CO==2Fe+3CO2
CuO+CO==Cu+CO2
点燃
高温
CO易与血红蛋白结合,使血红蛋白不能很好的与结合,造成生物体缺氧中毒而亡
燃烧着煤炉中发生的化学反应
你知道可燃性气体有哪些吗?
氢气
一氧化碳一
甲烷
2H2+O2== 2H2O
2CO+O2==2CO2
CH4+2O2==CO2+2H2O
点燃
点燃
点燃
怎样鉴别它们呀?
检验燃烧的产物
C
既有可燃性又有还原性的物质有哪些呢?
3、碳、氢气、一氧化碳的比较
碳 氢气 一氧化碳
化学性质 常
温 不活泼,受日光照射或与空气、水接触都不易反应 稳定.与空气、水接触,都不易起反应 稳定,与空气、水接触,都不易起反应
加
热
或
点
燃 能跟很多物质反应
可燃性
燃烧充分或燃烧不充分两种情况
②还原性
跟金属氧化物(氧化铜等)或非金属氧化物(二氧化碳等)反应
能跟很多物质发生反应
①可燃性
(跟氧气的反应)
②还原性(跟氧化铜等金属氧化物的反应) 能跟很多物质发生反应
①可燃性
(跟氧气的反应)
②还原性(跟氧化铜等金属氧化物的反应)
某混合气体,它可能是由CO、CO2、H2及N2的两种或两种以上气体的混合物,现将该混合气体依次通过下图中甲、乙、丙三个装置一段时间,反应平稳进行,甲瓶无明显现象,丙瓶中石灰水变浑浊,小橡皮泡A逐渐膨胀变大。(假设试验前,装置内空气已排尽,甲、丙两瓶中澄清石灰水均是足量的)。
(1)写出乙装置中的实验现象
黑色粉末变红
CO
CO2
收集尾气,防止污染空气
甲:检验混合物中是否存在CO2
丙:检验产物中是否存在CO2
金刚石( )
石墨( )
C60
物理性质
颜色
状态
光泽
硬度
导电性
熔点
润滑性
用途
互相转化
无色透明
深灰色不透明
正八面体形状固体
细鳞片状固体
形似足球
加工琢磨有光泽
有金属光泽
天然物中硬度最大
质软
质脆
不导电
导电
不导电
很高
很高
无
有
钻石.玻璃刀.钻头
铅笔芯.电极.润滑剂
超导体
金刚石
石墨
C
C
金刚石和石墨的物理性质不同的原因
单质的种类与元素的种类的关系
怎样证明金刚石和石墨是由碳元素组成的
无定形炭
木 炭
活性炭
焦 炭
炭 黑
燃料
除去异味.色素
防毒面具
疏松多孔
吸附性
冶炼金属
橡胶添加剂.油墨.鞋油
碳原子排列的方式不同
单质的种类多于元素的种类
可燃性
还原性
请将下列物质与相关用途连起来
A、石墨 冰箱去味剂
B、炭黑 制炭素墨水
C、活性炭 切割大理石
D、焦炭 冶炼金属
E、金刚石 干电池电极
F. C60 超导材料
碳单质的化学性质
常温
稳定
古代用墨书写的字画
埋入地下的电线杆表面烧焦
用碳素墨水书写挡案材料
原因
高温
可燃性
还原性
充分燃烧
不充分燃烧
C + O2=== CO2
2C + O2 === 2CO
2CuO + C === 2Cu + CO2
C
CuO
得氧
被氧化
氧化反应
还原剂
还原性
失氧
被还原
还原反应
氧化剂
氧化性
反应物的量不同.产物不同
点燃
点燃
信息
高温
碳的化合物
CO2
物性
无色无味气体
能溶于水
汽水
干冰
制冷剂
人工降雨
密度大于空气
化性
1.不燃烧.也不支持燃烧
灭火
2.不能供给呼吸
灯火实验
3.和水反应
4.和Ca(OH)2反应
5.参与光和作用
气体肥料
6.氧化性
CO2 + H2O == H2CO3
Ca(OH)2+CO2==CaCO3+H2O
CO2+C===2CO
高温
CO2制法
实验室
工业
原料
不用Na2CO3原因
不用稀H2SO4原因
原理
CaCO3+2HCl==CaCl2+CO2 +H2O
装置
与用H2O2溶液制取O2相同
步骤
收集
向上排空气法
密度大于空气
检验
澄清石灰水
变浑浊
是CO2
验满
燃着木条
瓶口
熄灭
已满
高温煅烧石灰石
CaCO3===CaO+CO2
怎样检验CaO中是否有CaCO3
怎样除去CaO中的CaCO3
石灰石.稀盐酸
不用浓盐酸原因
高温
查.装(先固后液).收.验
加入稀盐酸
高温煅烧
没有收集到二氧化碳的原因
收集的二氧化碳不纯的原因
没有收集满二氧化碳的原因
装置漏气
1.导管没有伸到集气瓶的底部
2.使用了浓盐酸
1.药品太少
2.装置漏气
实验室制取二氧化碳的装置
一氧化碳
物性
无色无味气体
密度略小于空气
报警器安装
难溶于水
煤炉上放盆水不能防中毒
化性
毒性
易与血红蛋白结合.使人中毒而亡
可燃性
还原性
2CO+O2===2CO2
Fe2O3+3CO===2Fe+3CO2
用途
燃料
冶炼金属
煤气
加有味气体作用?
泄露处理方法?
现象
点燃
高温
碳的其它化合物
甲烷
酒精
纯碱
小苏打
CH4
C2H5OH
Na2CO3
NaHCO3
物性
化性
物性
化性
CH4+2O2==CO2+2H2O
C2H5OH+3O2==2CO2+3H2O
无色无味气体.难溶于水.密度略小于空气
无色有特殊气味液体.能和水以任意比例互溶
(可燃性)
燃料
(可燃性)
较清洁能源
较清洁能源
燃料
点燃
点燃
木炭、一氧化碳分别还原氧化铜的两套装置的比较
看故事 想问题
看故事 想问题
我会归纳:CO的物理性质
Huanjing baohu
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
