苏教版高中化学必修2专题2第三单元第15课时 金属的腐蚀和防护(共30张PPT)
文档属性
| 名称 | 苏教版高中化学必修2专题2第三单元第15课时 金属的腐蚀和防护(共30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 878.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-04-25 00:00:00 | ||
图片预览









文档简介
课件30张PPT。 组织建设第15课时 金属的腐蚀和防护钢铁生锈金属的腐蚀在生活中非常普遍铜器生锈铜器表面生成铜绿金属跟干燥气体或非电解质液体直接接触不纯金属或合金
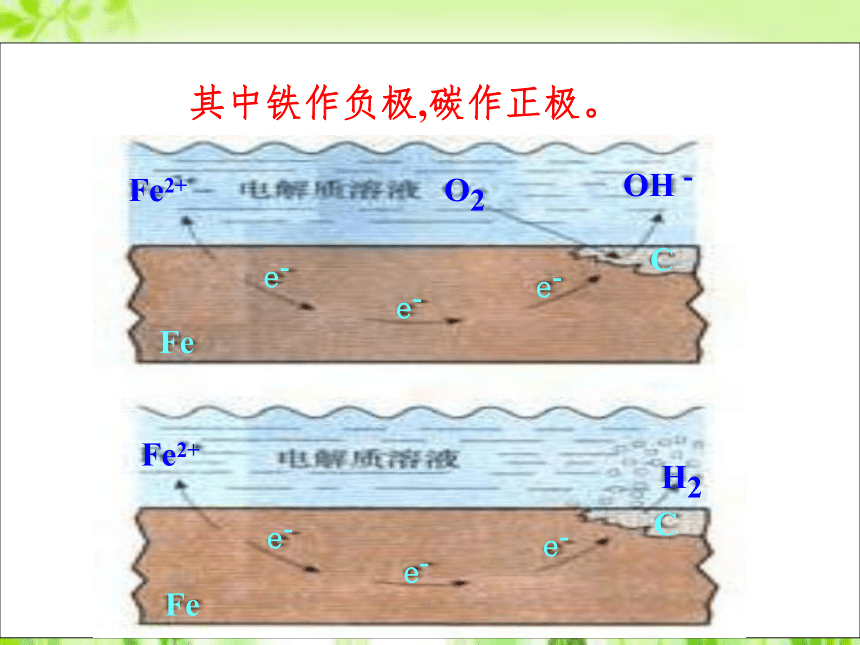
跟电解质溶液接触无电流产生有微弱电流产生金属被氧化较活泼金属被氧化与接触物质的氧化性及温度有关与电解质溶液的酸碱性及金属活性有关两者往往同时发生,电化学腐蚀更普遍化学腐蚀与电化学腐蚀的区别水膜呈酸性水膜呈弱酸性或呈中性2Fe+2H2O+O2=2Fe(OH)24Fe(OH)2+2H2O+O2=4Fe(OH)3Fe2O3·nH2O通常两种腐蚀同时存在,但以吸氧腐蚀为主Fe-2e- = Fe2+ 2Fe-4e- = 2Fe2+O2+4e-+2H2O=4OH-〖讨论〗鉴于金属发生腐蚀的原因,我们可以从哪些
方面设想解决问题的思路 ?思路一:直接隔离
即可选用适当的材料使金属与空气或其他腐蚀性试剂隔离开,以阻止金属的腐蚀。 1、给金属穿上“保护膜”
例如:①喷涂漆;②涂油脂;③表面钝化;④电镀(在钢铁表面形成铬等耐腐蚀性较强的金属镀层)等。二、金属的防护思路二:改变本质
即改变金属的内部组成结构,使其具有较强的抗腐蚀性能。 2、加入其他金属改变其组成
在钢铁中加入一定比例的铬和镍(如14%~8%Cr,7%~9%Ni),改变钢铁内部的组成和结构,可极大程度地提高钢铁抗腐蚀性能,这就是常见的“不锈钢”(合金)。 思路三:因势利导
电化学腐蚀还是用电化学方法来解决,不回避金属与氧化剂的直接接触,采用还原性更强的物质或其他替代方式来满足氧化剂对电子的需求,从而保护主体金属构件免受腐蚀。 3、电化学防护法——重点掌握牺牲阳极的阴极保护法
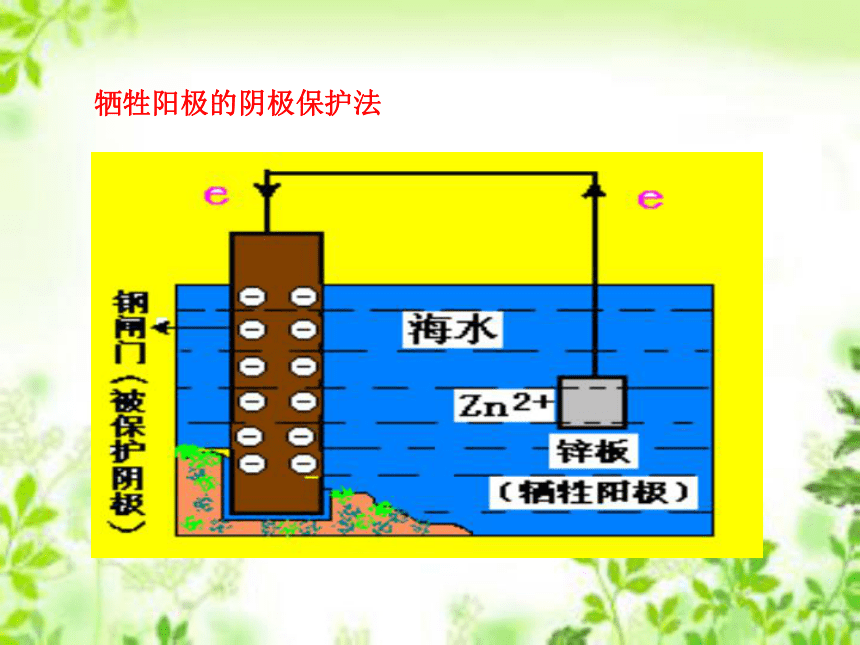
外加直流电源的阴极保护法原理:形成原电池时,让被保护金属作正极(阴极),不反应受到保护;而活泼金属作负极(阳极),反应受到腐蚀。1.牺牲阳极的阴极保护法金属的电化学防护 牺牲阳极的阴极保护法2.外加电流的阴极保护法
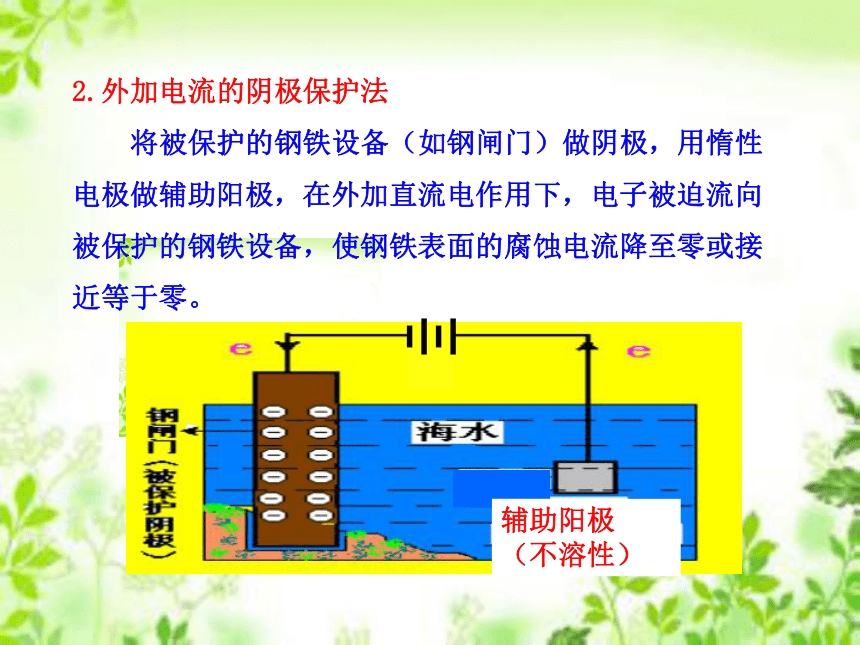
将被保护的钢铁设备(如钢闸门)做阴极,用惰性电极做辅助阳极,在外加直流电作用下,电子被迫流向被保护的钢铁设备,使钢铁表面的腐蚀电流降至零或接近等于零。金属的电化学防护 在同一电解质溶液中防腐措施由好到坏的顺序如下:
外接电源的阴极保护法>牺牲阳极的阴极保护法>有一般防腐条件保护>无防腐条件 下列各情况下,其中Fe片腐蚀由快到慢的顺序是 。(5)(2) (1)(3)(4)金属腐蚀快慢的判断
(1)与构成微电池两极的材料有关。两极材料的活动性
差别越大,氧化还原反应的速率越 ,活泼金属被
腐蚀的速度越 。
(2) 电解原理引起的腐蚀 原电池原理引起的
腐蚀 化学腐蚀 有防腐措施的腐蚀。
(3)同一种金属的腐蚀:在强电解质中______
弱电解质中 非电解质中。
(4)一般说来:原电池原理引起的腐蚀 化学
腐蚀 有防腐措施的腐蚀。>>>>>快快>>1.钢铁锈蚀过程中可能发生的变化是( )
① Fe由单质转化为+2价;
② Fe由+2价转化为+3价;
③ 产生氢气;
④产生氧气;
⑤ 杂质C被氧化除去;
⑥ Fe(OH)3失水变成Fe2O3·3H2O.
A.①②③⑥ B.①③④ C.只有①③ D.全部A2.为保护地下钢管不被腐蚀,可采用的方法是( )
A.与直流电源负极相连接
B.与直流电源的正极相连接
C.与铜板相连接
D.与锌板相连接AD3.以下现象与电化学腐蚀无关的是( )
A.黄铜(铜锌合金)制作的锣不易产生铜绿
B.生铁比纯铁容易生锈
C.铁质配件附有铜质配件,在接触处易生铁锈
D.银质物品久置表面变暗DA.潮湿疏松透气的土壤中
B.含铁元素较多的酸性土壤中
C.干燥致密不透气的土壤中
D.含碳量较高,潮湿透气的中性土壤中4.下列情况下,埋在地下的输油铸铁管道被腐蚀最慢的
是( )C5、钢铁发生吸氧腐蚀时,发生还原反应的电极反应式是( )
A、 Fe – 2e-=Fe 2+
B、 2H + + 2e- =H2 ↑
C、 4OH - - 4e-= 2H2O + O2 ↑
D、 2H2O + O2 + 4e- = 4OH - D6、如图所示,各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
A、②>①>③
B、③>②>①
C、②>③>①FeFeFeSnZnA7、下列事实不能用电化学理论解释的是 ( )
A、轮船吃水线以下的船壳上装一定数量的锌块
B、铝片不用特殊方法保护
C、纯锌与稀硫酸反应时,滴入少量的CuSO4溶液后速率加快
D、镀锌铁(在铁上镀一层锌)比镀锡耐用B 8、有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为: ( )
A.a > c > d > b
B.d > a > b > c
C.d > b > a > c
D.b > a > d > cB9、下列叙述正确的是( )
A.锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
B.镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
C.家用炒菜铁锅出现锈斑的原因是发生了化学腐蚀
D.吸氧腐蚀时正极放出氧气,析氢腐蚀时正极放出氢气
E.化学腐蚀速率超过电化学腐蚀速率,析氢腐蚀比吸氧腐蚀普遍A10、以下现象与电化学腐蚀无关的是( )
A.黄铜(铜锌合金)制作的铜制品不易被腐蚀
B.生铁比纯铁容易腐蚀
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银制奖牌久置后表面变暗
11、下列事实不能用电化学理论解释的是( )
A.轮船水线下船壳上装一偶一定数量的锌块
B.铝片不用特殊方法保存
C.纯锌与稀硫酸反应时,滴入少量的硫酸铜后速率加快
D.镀锌铁比镀锡铁耐用DB12、下列防腐措施中,属于电化学保护法的是( )
A.用氧化剂使金属表面生成一层致密稳定的氧化物保护膜
B.在金属中加入一些铬或镍制成合金
C.在轮船的船壳水线以下部分装上一些锌
D.金属表面喷漆
13、下列事实不能用电化学理论解释的是( )
A.在轮船的船壳水线以下部分装有一定量的锌块
B.镀锌的铁制品比镀锡的铁制品耐用
C.铝片不用特殊方法保护
D.粗锌跟稀硫酸反应比纯锌更快CC14、埋在地下的铸铁输油管道,在下列各种情况下,腐蚀最慢的是( )
A.在含铁元素较多的酸性土壤中
B.在潮湿疏松透气的土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多的潮湿透气的中性土壤中
15、为了避免青铜器生成铜绿,以下方法正确的是( )
A.将青铜器放在银质托盘上
B.将青铜器保存在干燥的环境中
C.将青铜器保存在潮湿的空气中
D.在青铜器的表面覆盖一层防渗的高分子膜CBD16、下列金属防护的方法不正确的是( )
A.对健身器材刷油漆以防锈
B.对某些工具的“机械转动部位”选用刷油漆方法来防锈
C.用牺牲锌块的方法来保护船身
D.自行车的钢圈上镀上一层Cr防锈B17、下列各组金属均有导线相连,并插入对应的液体中,其中能组成原电池的是( )
A. Cu | H2SO4(稀) | C
B. Cu | AgNO3(aq) | Ag
C. Zn | CCl4(稀) | Cu
D. Fe | H2SO4(稀) | Fe
18、下列各组金属均有导线相连,并插入稀硫酸溶液中,其中铁被腐蚀的速度由快到慢的顺序是( )
①Fe-Fe ②Fe-Sn ③Fe-Zn ④Cu-Fe
A. ②①③④ B. ③②④①
C. ④②③① D. ④②①③B D
跟电解质溶液接触无电流产生有微弱电流产生金属被氧化较活泼金属被氧化与接触物质的氧化性及温度有关与电解质溶液的酸碱性及金属活性有关两者往往同时发生,电化学腐蚀更普遍化学腐蚀与电化学腐蚀的区别水膜呈酸性水膜呈弱酸性或呈中性2Fe+2H2O+O2=2Fe(OH)24Fe(OH)2+2H2O+O2=4Fe(OH)3Fe2O3·nH2O通常两种腐蚀同时存在,但以吸氧腐蚀为主Fe-2e- = Fe2+ 2Fe-4e- = 2Fe2+O2+4e-+2H2O=4OH-〖讨论〗鉴于金属发生腐蚀的原因,我们可以从哪些
方面设想解决问题的思路 ?思路一:直接隔离
即可选用适当的材料使金属与空气或其他腐蚀性试剂隔离开,以阻止金属的腐蚀。 1、给金属穿上“保护膜”
例如:①喷涂漆;②涂油脂;③表面钝化;④电镀(在钢铁表面形成铬等耐腐蚀性较强的金属镀层)等。二、金属的防护思路二:改变本质
即改变金属的内部组成结构,使其具有较强的抗腐蚀性能。 2、加入其他金属改变其组成
在钢铁中加入一定比例的铬和镍(如14%~8%Cr,7%~9%Ni),改变钢铁内部的组成和结构,可极大程度地提高钢铁抗腐蚀性能,这就是常见的“不锈钢”(合金)。 思路三:因势利导
电化学腐蚀还是用电化学方法来解决,不回避金属与氧化剂的直接接触,采用还原性更强的物质或其他替代方式来满足氧化剂对电子的需求,从而保护主体金属构件免受腐蚀。 3、电化学防护法——重点掌握牺牲阳极的阴极保护法
外加直流电源的阴极保护法原理:形成原电池时,让被保护金属作正极(阴极),不反应受到保护;而活泼金属作负极(阳极),反应受到腐蚀。1.牺牲阳极的阴极保护法金属的电化学防护 牺牲阳极的阴极保护法2.外加电流的阴极保护法
将被保护的钢铁设备(如钢闸门)做阴极,用惰性电极做辅助阳极,在外加直流电作用下,电子被迫流向被保护的钢铁设备,使钢铁表面的腐蚀电流降至零或接近等于零。金属的电化学防护 在同一电解质溶液中防腐措施由好到坏的顺序如下:
外接电源的阴极保护法>牺牲阳极的阴极保护法>有一般防腐条件保护>无防腐条件 下列各情况下,其中Fe片腐蚀由快到慢的顺序是 。(5)(2) (1)(3)(4)金属腐蚀快慢的判断
(1)与构成微电池两极的材料有关。两极材料的活动性
差别越大,氧化还原反应的速率越 ,活泼金属被
腐蚀的速度越 。
(2) 电解原理引起的腐蚀 原电池原理引起的
腐蚀 化学腐蚀 有防腐措施的腐蚀。
(3)同一种金属的腐蚀:在强电解质中______
弱电解质中 非电解质中。
(4)一般说来:原电池原理引起的腐蚀 化学
腐蚀 有防腐措施的腐蚀。>>>>>快快>>1.钢铁锈蚀过程中可能发生的变化是( )
① Fe由单质转化为+2价;
② Fe由+2价转化为+3价;
③ 产生氢气;
④产生氧气;
⑤ 杂质C被氧化除去;
⑥ Fe(OH)3失水变成Fe2O3·3H2O.
A.①②③⑥ B.①③④ C.只有①③ D.全部A2.为保护地下钢管不被腐蚀,可采用的方法是( )
A.与直流电源负极相连接
B.与直流电源的正极相连接
C.与铜板相连接
D.与锌板相连接AD3.以下现象与电化学腐蚀无关的是( )
A.黄铜(铜锌合金)制作的锣不易产生铜绿
B.生铁比纯铁容易生锈
C.铁质配件附有铜质配件,在接触处易生铁锈
D.银质物品久置表面变暗DA.潮湿疏松透气的土壤中
B.含铁元素较多的酸性土壤中
C.干燥致密不透气的土壤中
D.含碳量较高,潮湿透气的中性土壤中4.下列情况下,埋在地下的输油铸铁管道被腐蚀最慢的
是( )C5、钢铁发生吸氧腐蚀时,发生还原反应的电极反应式是( )
A、 Fe – 2e-=Fe 2+
B、 2H + + 2e- =H2 ↑
C、 4OH - - 4e-= 2H2O + O2 ↑
D、 2H2O + O2 + 4e- = 4OH - D6、如图所示,各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
A、②>①>③
B、③>②>①
C、②>③>①FeFeFeSnZnA7、下列事实不能用电化学理论解释的是 ( )
A、轮船吃水线以下的船壳上装一定数量的锌块
B、铝片不用特殊方法保护
C、纯锌与稀硫酸反应时,滴入少量的CuSO4溶液后速率加快
D、镀锌铁(在铁上镀一层锌)比镀锡耐用B 8、有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为: ( )
A.a > c > d > b
B.d > a > b > c
C.d > b > a > c
D.b > a > d > cB9、下列叙述正确的是( )
A.锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
B.镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
C.家用炒菜铁锅出现锈斑的原因是发生了化学腐蚀
D.吸氧腐蚀时正极放出氧气,析氢腐蚀时正极放出氢气
E.化学腐蚀速率超过电化学腐蚀速率,析氢腐蚀比吸氧腐蚀普遍A10、以下现象与电化学腐蚀无关的是( )
A.黄铜(铜锌合金)制作的铜制品不易被腐蚀
B.生铁比纯铁容易腐蚀
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银制奖牌久置后表面变暗
11、下列事实不能用电化学理论解释的是( )
A.轮船水线下船壳上装一偶一定数量的锌块
B.铝片不用特殊方法保存
C.纯锌与稀硫酸反应时,滴入少量的硫酸铜后速率加快
D.镀锌铁比镀锡铁耐用DB12、下列防腐措施中,属于电化学保护法的是( )
A.用氧化剂使金属表面生成一层致密稳定的氧化物保护膜
B.在金属中加入一些铬或镍制成合金
C.在轮船的船壳水线以下部分装上一些锌
D.金属表面喷漆
13、下列事实不能用电化学理论解释的是( )
A.在轮船的船壳水线以下部分装有一定量的锌块
B.镀锌的铁制品比镀锡的铁制品耐用
C.铝片不用特殊方法保护
D.粗锌跟稀硫酸反应比纯锌更快CC14、埋在地下的铸铁输油管道,在下列各种情况下,腐蚀最慢的是( )
A.在含铁元素较多的酸性土壤中
B.在潮湿疏松透气的土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多的潮湿透气的中性土壤中
15、为了避免青铜器生成铜绿,以下方法正确的是( )
A.将青铜器放在银质托盘上
B.将青铜器保存在干燥的环境中
C.将青铜器保存在潮湿的空气中
D.在青铜器的表面覆盖一层防渗的高分子膜CBD16、下列金属防护的方法不正确的是( )
A.对健身器材刷油漆以防锈
B.对某些工具的“机械转动部位”选用刷油漆方法来防锈
C.用牺牲锌块的方法来保护船身
D.自行车的钢圈上镀上一层Cr防锈B17、下列各组金属均有导线相连,并插入对应的液体中,其中能组成原电池的是( )
A. Cu | H2SO4(稀) | C
B. Cu | AgNO3(aq) | Ag
C. Zn | CCl4(稀) | Cu
D. Fe | H2SO4(稀) | Fe
18、下列各组金属均有导线相连,并插入稀硫酸溶液中,其中铁被腐蚀的速度由快到慢的顺序是( )
①Fe-Fe ②Fe-Sn ③Fe-Zn ④Cu-Fe
A. ②①③④ B. ③②④①
C. ④②③① D. ④②①③B D
