北京课改版九下化学 10.4金属的化学性质 复习 课件(20张PPT)
文档属性
| 名称 | 北京课改版九下化学 10.4金属的化学性质 复习 课件(20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 816.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-07 00:00:00 | ||
图片预览








文档简介
课件20张PPT。金属的化学性质复习回顾金属的物理性质
(1) 常温下为 体(汞为液体)。
(2) 都有金属光泽,大多数为 色;而铜为 色,金为 色。
(3) 有良好的 性、 性和延展性。
(4) 多数密度 ,熔点 。固紫红 黄 导电 导热 较大 较高银白1. 金属与氧气的反应 大多数金属都能与氧气发生反应,但反应难易和剧烈程度是不同的。你学过哪些金属能与O2反应?镁、铝等在常温下就能与氧气反应。金即使在高温时也不与氧气反应。铁、铜等在常温下几乎不与氧气反应,但在高温时能与氧气反应。3Fe+2O2 = Fe3O4点燃2Mg+O2=2MgO2Cu+O2 = 2CuO△点燃MgFe金属的化学性质1.大多数金属能与氧气反应反应的剧烈程度不相同 【例】有一著名收藏家收藏的清末铝制品,至今保存十分完好,经历这么长的时间,该铝制艺术品不易锈蚀的重要原因是( )。
A.铝不易发生化学反应
B.铝不易氧化
C.铝的氧化物易发生还原反应
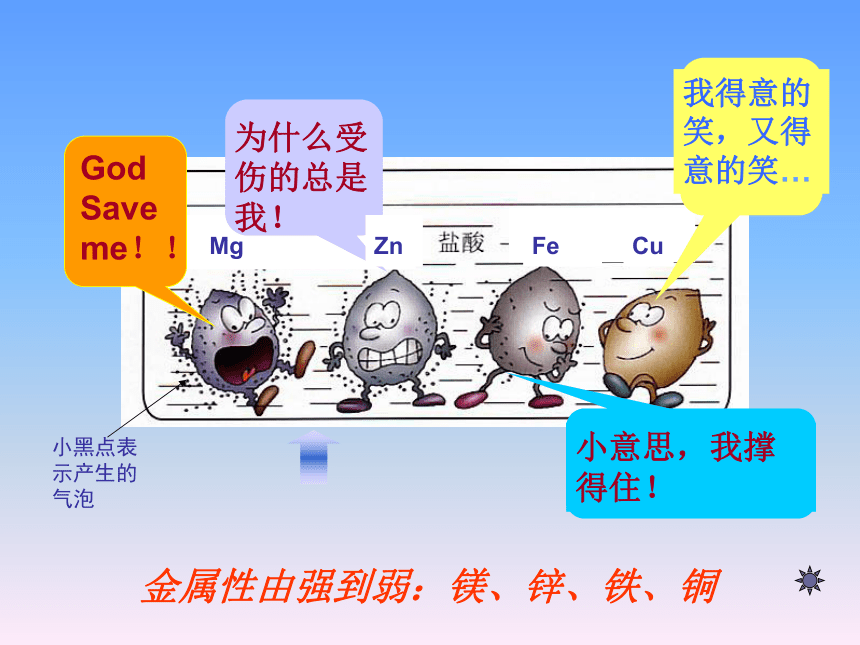
D.铝易氧化,但铝表面的氧化铝具有保护内部铝的作用 D2. 金属与酸的反应(高频考点)镁、锌、铁等较活泼金属能与酸反应放出氢气。金属性由强到弱:镁、锌、铁、铜MgZnFeCu小黑点表示产生的气泡金属活动性顺序1、在金属活动性顺序里,金属的位置越靠前,它的________________
2、在金属活动性顺序里,_____________________能置换出盐酸、稀硫酸中的氢,生成氢气。活动性越强位于氢前面的金属写出下列反应的化学方程式 【特别提醒】①并不是所有的金属都能与稀酸发生反应,只有那些在金属活动性顺序表中排在氢前面的金属才能与稀酸发生置换反应,产生氢气。②金属不能和浓硫酸和硝酸等氧化性强的酸反应生成氢气。③铁与酸或可溶性金属盐反应时,生成的化合物中铁元素为+2价,读作亚铁,溶液呈浅绿色。(重点) 【例】(13酒泉)质量相同的Mg和Al分别跟足量的稀盐酸反应,如果横坐标表示反应的时间,纵坐标表示生成氢气的质量,能正确表示两种金属反应情况的是下图中的 ( )A 方法指导 活泼金属和盐酸、硫酸的反应,产生氢气的多少可以用下面的规律来判断:
(1)等量的金属与足量的同种酸反应,金属的化合价相等时,相对原子质量小的产生的氢气多;相对原子质量相近时,化合价高的产生的氢气多。
(2)等质量的同种酸与过量的金属反应,产生的氢气质量相等。(16市一诊)将质量相等的X、Y、Z三种金属,
同时分别放入三份溶质质量分数相同且足量的稀硫酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是(已知:X、Y、Z在生成物中均为+2价) ( )
A. 放出H2的质量是Z>Y>X
B. 反应速率最大的是X
C. 金属活动性顺序是Y>X>Z
D. 相对原子质量是X>Y>ZC中考我能行3. 金属与盐溶液的反应(高频考点)条件:在金属活动性顺序中,只有排在前面的金属才能置换出排在后面的金属。2.判断下列各组物质能否发生反应?
(1)铜和硫酸锌溶液
(2)锌和硫酸铜溶液
(3)金和硫酸铜溶液
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au不反应能反应不反应 Zn + CuSO4 Cu + ZnSO4=====(16北海)向Mg(NO3)2、AgNO3、Cu(NO3)2混合液中加入一定量的铁粉,充分反应后过滤。下列情况不可能存在的是 ( )
A. 滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+、Mg2+
B. 滤纸上有Ag、Cu,滤液中有Cu2+、Fe2+、Mg2+
C. 滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+
D. 滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Fe2+、Mg2+D(15天水) 下列方程式中,正确的是:( )
A、Cu + 2AgCl = 2Ag + CuCl2
B、Zn + 2AgNO3 = 2Ag + Zn(NO3)2
C、2Na + CuSO4 = Cu + Na2SO4
D、2Fe + 3CuCl2 = 2FeCl3 + 3CuB(15兰州) 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸,X溶解并产生氢气,而Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会在Y表面有银析出,而Z没有变化。请判断X、Y、Z的金属活动性顺序是 ( )A、X>Y>Z B、X>Z>Y C、Z>Y>X D、Z>X>YA1、两种金属的验证方法(三)、设计实验证明金属活动性的强弱用实验证明Fe、Cu这两种金属的活动性顺序2、三种金属的验证方法方案二:两边金属,中间溶液
用Zn、CuSO4溶液、Ag 方案三:两边溶液,中间金属
用ZnSO4溶液、Cu、AgNO3溶液设计实验证明Zn、Fe、Ag三种金属的活动性顺序。最简单
的方法方案1: Fe、Cu、稀盐酸 方案2: Fe、 CuSO4溶液方案一: Zn、Fe、Ag、稀盐酸(但要控制变量)(五)、金属与盐溶液反应的先后次序问题:例1:锌投入到硝酸银和硝酸铜混合溶液中,谁先反应?练习1、一定量的铁粉放入硫酸铜溶液中,充分反应后过滤,滤渣中一定含 ,可能含有 。
2、向AgNO3、Zn(NO3)2的混合溶液中,加入过量的铁粉,充分
反应后过滤。则滤出的固体中一定含有的是 ;
滤液中一定含有的是 ,
一定不含 。CuFeFe、AgFe(NO3)2、Zn(NO3)2AgNO31.金属+氧气=金属氧化物2.金属+酸=盐+氢气
3.金属+盐=新金属+新盐金属的化学性质(金属越活泼,反应越容易,越剧烈)(金属越活泼,反应越容易,越剧烈)(活动性强的能把活动性弱的金属从盐溶液中置换出来)小结:
(1) 常温下为 体(汞为液体)。
(2) 都有金属光泽,大多数为 色;而铜为 色,金为 色。
(3) 有良好的 性、 性和延展性。
(4) 多数密度 ,熔点 。固紫红 黄 导电 导热 较大 较高银白1. 金属与氧气的反应 大多数金属都能与氧气发生反应,但反应难易和剧烈程度是不同的。你学过哪些金属能与O2反应?镁、铝等在常温下就能与氧气反应。金即使在高温时也不与氧气反应。铁、铜等在常温下几乎不与氧气反应,但在高温时能与氧气反应。3Fe+2O2 = Fe3O4点燃2Mg+O2=2MgO2Cu+O2 = 2CuO△点燃MgFe金属的化学性质1.大多数金属能与氧气反应反应的剧烈程度不相同 【例】有一著名收藏家收藏的清末铝制品,至今保存十分完好,经历这么长的时间,该铝制艺术品不易锈蚀的重要原因是( )。
A.铝不易发生化学反应
B.铝不易氧化
C.铝的氧化物易发生还原反应
D.铝易氧化,但铝表面的氧化铝具有保护内部铝的作用 D2. 金属与酸的反应(高频考点)镁、锌、铁等较活泼金属能与酸反应放出氢气。金属性由强到弱:镁、锌、铁、铜MgZnFeCu小黑点表示产生的气泡金属活动性顺序1、在金属活动性顺序里,金属的位置越靠前,它的________________
2、在金属活动性顺序里,_____________________能置换出盐酸、稀硫酸中的氢,生成氢气。活动性越强位于氢前面的金属写出下列反应的化学方程式 【特别提醒】①并不是所有的金属都能与稀酸发生反应,只有那些在金属活动性顺序表中排在氢前面的金属才能与稀酸发生置换反应,产生氢气。②金属不能和浓硫酸和硝酸等氧化性强的酸反应生成氢气。③铁与酸或可溶性金属盐反应时,生成的化合物中铁元素为+2价,读作亚铁,溶液呈浅绿色。(重点) 【例】(13酒泉)质量相同的Mg和Al分别跟足量的稀盐酸反应,如果横坐标表示反应的时间,纵坐标表示生成氢气的质量,能正确表示两种金属反应情况的是下图中的 ( )A 方法指导 活泼金属和盐酸、硫酸的反应,产生氢气的多少可以用下面的规律来判断:
(1)等量的金属与足量的同种酸反应,金属的化合价相等时,相对原子质量小的产生的氢气多;相对原子质量相近时,化合价高的产生的氢气多。
(2)等质量的同种酸与过量的金属反应,产生的氢气质量相等。(16市一诊)将质量相等的X、Y、Z三种金属,
同时分别放入三份溶质质量分数相同且足量的稀硫酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是(已知:X、Y、Z在生成物中均为+2价) ( )
A. 放出H2的质量是Z>Y>X
B. 反应速率最大的是X
C. 金属活动性顺序是Y>X>Z
D. 相对原子质量是X>Y>ZC中考我能行3. 金属与盐溶液的反应(高频考点)条件:在金属活动性顺序中,只有排在前面的金属才能置换出排在后面的金属。2.判断下列各组物质能否发生反应?
(1)铜和硫酸锌溶液
(2)锌和硫酸铜溶液
(3)金和硫酸铜溶液
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au不反应能反应不反应 Zn + CuSO4 Cu + ZnSO4=====(16北海)向Mg(NO3)2、AgNO3、Cu(NO3)2混合液中加入一定量的铁粉,充分反应后过滤。下列情况不可能存在的是 ( )
A. 滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+、Mg2+
B. 滤纸上有Ag、Cu,滤液中有Cu2+、Fe2+、Mg2+
C. 滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+
D. 滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Fe2+、Mg2+D(15天水) 下列方程式中,正确的是:( )
A、Cu + 2AgCl = 2Ag + CuCl2
B、Zn + 2AgNO3 = 2Ag + Zn(NO3)2
C、2Na + CuSO4 = Cu + Na2SO4
D、2Fe + 3CuCl2 = 2FeCl3 + 3CuB(15兰州) 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸,X溶解并产生氢气,而Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会在Y表面有银析出,而Z没有变化。请判断X、Y、Z的金属活动性顺序是 ( )A、X>Y>Z B、X>Z>Y C、Z>Y>X D、Z>X>YA1、两种金属的验证方法(三)、设计实验证明金属活动性的强弱用实验证明Fe、Cu这两种金属的活动性顺序2、三种金属的验证方法方案二:两边金属,中间溶液
用Zn、CuSO4溶液、Ag 方案三:两边溶液,中间金属
用ZnSO4溶液、Cu、AgNO3溶液设计实验证明Zn、Fe、Ag三种金属的活动性顺序。最简单
的方法方案1: Fe、Cu、稀盐酸 方案2: Fe、 CuSO4溶液方案一: Zn、Fe、Ag、稀盐酸(但要控制变量)(五)、金属与盐溶液反应的先后次序问题:例1:锌投入到硝酸银和硝酸铜混合溶液中,谁先反应?练习1、一定量的铁粉放入硫酸铜溶液中,充分反应后过滤,滤渣中一定含 ,可能含有 。
2、向AgNO3、Zn(NO3)2的混合溶液中,加入过量的铁粉,充分
反应后过滤。则滤出的固体中一定含有的是 ;
滤液中一定含有的是 ,
一定不含 。CuFeFe、AgFe(NO3)2、Zn(NO3)2AgNO31.金属+氧气=金属氧化物2.金属+酸=盐+氢气
3.金属+盐=新金属+新盐金属的化学性质(金属越活泼,反应越容易,越剧烈)(金属越活泼,反应越容易,越剧烈)(活动性强的能把活动性弱的金属从盐溶液中置换出来)小结:
