北京课改版九下化学 11.1对酸和碱的初步认识 课件(25张PPT)
文档属性
| 名称 | 北京课改版九下化学 11.1对酸和碱的初步认识 课件(25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 11.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-07 00:00:00 | ||
图片预览








文档简介
课件25张PPT。对酸和碱的初步认识1.掌握酸碱的概念;3.掌握常见酸的物理性质及用途。2.认识两种常见的酸碱指示剂及其应用;学习目标(1分钟)2.酸溶液具有相似的化学性质是因为酸在水溶液中能解离出________和__________,即在不同的酸溶液中都含有相同的_________;
3.碱溶液具有相似的化学性质是因为碱在水溶液中能解离出_________和___________,即在不同的碱溶液中都含有相同的___________。 学生自学,教师巡视1 (2分钟)1.2.酸溶液具有相似的化学性质是因为酸在水溶液中能解离出________和__________,即在不同的酸溶液中都含有相同的_________;
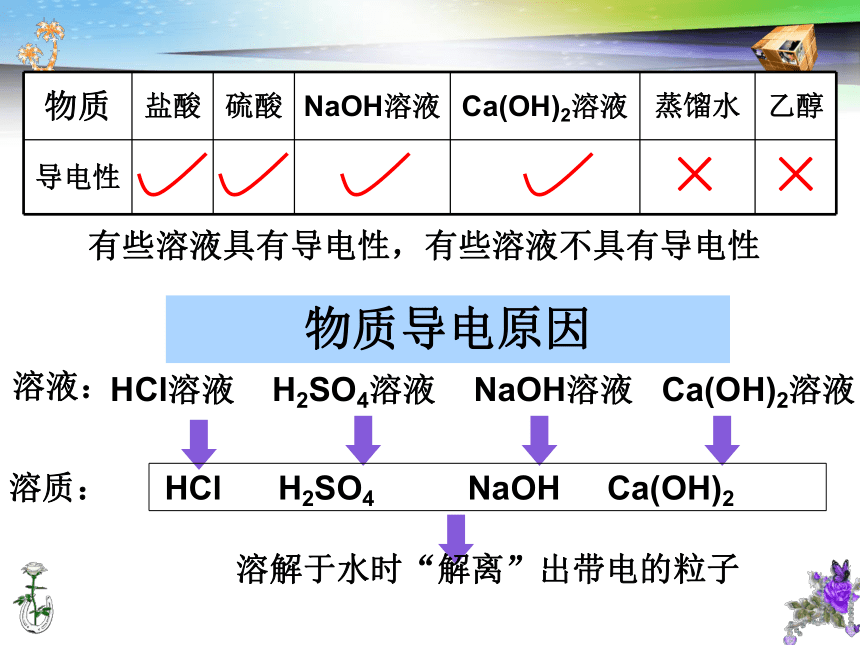
3.碱溶液具有相似的化学性质是因为碱在水溶液中能解离出_________和___________,即在不同的碱溶液中都含有相同的___________。 氢离子酸根离子氢离子金属离子氢氧根离子氢氧根离子盐酸硫酸氢氧化钠溶液氢氧化钙溶液蒸馏水乙醇1.自学检测1 2分钟××有些溶液具有导电性,有些溶液不具有导电性HCl溶液 H2SO4溶液 NaOH溶液 Ca(OH)2溶液HCl H2SO4 NaOH Ca(OH)2溶液:溶质:溶解于水时“解离”出带电的粒子物质导电原因HCl → H+ + Cl-H2SO4→ 2 H+ + SO42-NaOH → Na+ + OH-Ca(OH)2→ Ca2+ + 2 OH- 酸在水溶液中都能解离出H+和酸根离子,即在不同的酸溶液中都含有相同的H+,所以酸有一些相似的性质。碱溶液中也含有相同的OH-,所以,碱也有一些相似的性质。学生讨论,教师点拨1: 2分钟电离时产生的阳离子全部是氢离子(H+)的化合物。 电离时产生的阴离子全部是氢氧根离子(OH-)的化合物。酸碱的概念:酸:碱:NaCl=Na++Cl-K2CO3=2K++CO32-CaCl2=Ca2++2Cl-Na2CO3=2Na++CO32-盐的概念:盐:由金属离子和酸根离子构成的。
盐在水溶液中能电离出金属离子和酸根离子。学生自学,教师巡视2: (4分钟)1.化合物可分为氧化物、酸 、碱 、盐。常见的酸有 、 、 、 。
常见的碱有 、 。
2. 能跟酸或碱的溶液起作用而显示不同的颜色的物质叫
做 。简称 。
3.石蕊溶液遇酸溶液变成 色,遇碱溶液变成 色;
酚酞溶液遇酸溶液 色,遇碱溶液变成 色。上述属于酸溶液的是 ;
上述属于碱溶液的是 。 酸碱指示剂1.化合物可分为氧化物、酸 、碱 、盐。常见的酸有 、 、 、 。
常见的碱有 、 。
2. 能跟酸或碱的溶液起作用而显示不同的颜色的物质叫
做 。简称 。
3.石蕊溶液遇酸溶液变成 色,遇碱溶液变成 色;
酚酞溶液遇酸溶液 色,遇碱溶液变成 色。红色无色红色无色蓝色蓝色红色红色上述属于酸溶液的是 ;
上述属于碱溶液的是 。 食醋和盐酸石灰水和氢氧化钠4.酸碱指示剂指示剂醋酸盐酸氢氧化钠氢氧化钙硫酸碳酸红蓝不变红酸碱指示剂自学检测2.1:2分钟变红变蓝不变色变红仍为紫色仍为无色学生讨论,教师点拨1:2分钟(如NaCl溶液)★点拨:是指示剂在变色,不是酸溶液和碱溶液在变色。可以说:石蕊溶液遇酸变红 或 酸使石蕊溶液变红。
不能说:石蕊溶液使酸变红。变红变红变蓝不变色中性溶液能使石蕊溶液变红的一定是酸吗?是酸性溶液小结:酸碱指示剂:能跟酸或碱的溶液起作用而显示不同颜色的物质叫酸碱指示剂(也叫指示剂)。常用指示剂:石蕊溶液和酚酞溶液指示剂:变色规律:紫色石蕊溶液:
遇酸变红色,遇碱变蓝色遇酸不变色,遇碱变红色无色酚酞溶液: 取少量该溶液,滴入几滴石蕊试液,若溶液呈现蓝色;
或取少量该溶液,滴入几滴无色的酚酞试液,若溶液呈现红色,则说明该溶液为碱性溶液。如何用酸碱指示剂检验溶液的酸碱性?检验溶液是酸性的方法: 取少量该溶液,滴入几滴石蕊试液,若溶液呈现红色,则说明该溶液为酸性溶液。检验溶液为碱性的方法:自学检测2.2:1分钟月季花牵牛花紫萝卜美人焦胡萝卜紫包菜植物色素易溶解在酒精溶液中自制指示剂原料1.上述实验结果,哪些不可以作酸碱指示剂?2.上述实验结果,哪些可以作酸碱指示剂?代用指示剂的颜色牵牛花、月季花、紫卷心菜。
因为在酸、碱溶液里呈显不同的颜色。自学检测2.3:2分钟金盈菊花瓣汁,因为在酸、碱溶液中没有变色。学生自学,教师巡视3 (3分钟)酸物理性质及用途1.浓盐酸、浓硫酸物理性质 2. 分别盛放浓盐酸和浓硫酸的两个试剂瓶,敞口放置一段时间后(不考虑水分的蒸发),两瓶酸的质量、质量分数各有何变化?应如何保存?3.酸的用途:浓硫酸可做 。1.浓盐酸、浓硫酸物理性质无色液体瓶口出现白雾刺激性气味无色、粘稠状液体无明显现象无味有挥发性有吸水性 2. 分别盛放浓盐酸和浓硫酸的两个试剂瓶,敞口放置一段时间后(不考虑水分的蒸发),两瓶酸的质量、质量分数各有何变化?减少减小增加减小不变不变自学检测3:2分钟3.酸的用途:浓硫酸可做 。干燥剂酸物理性质密封保存应如何保存?学生讨论,教师点拨1: 4分钟 从浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气接触形成盐酸小液滴.浓盐酸瓶口为什么有白雾?浓盐酸特性: 挥发性 讨论1浓硫酸特性:吸水性用途:做某些气体的干燥剂——酸性干燥剂通入液面下H2、H2OH2讨论2哪些气体能用浓硫酸来干燥?哪些不能用?干燥原理:干燥剂只吸收水分, 但不与被干燥的气体发生反应。注意:长管进,短管出(长进短出)洗气瓶能干燥不能干燥:碱性气体:NH3酸性气体:CO2 、SO2、 HCl小 结1、盐酸(HCl):常温下是无色有刺激性气味的液体,
有挥发性。
2、浓硫酸:无色、粘稠状液体,有吸水性 能跟酸或碱的溶液起作用而显示不同的颜色的物质叫做酸碱指示剂。简称指示剂。二、酸碱指示剂:变红变蓝不变色变红仍为紫色仍为无色电离时产生的阳离子全部是氢离子(H+)的化合物叫做酸;
电离时产生的阴离子全部是氢氧根离子(OH-)的化合物叫做碱。一、酸碱的概念:三、常见的酸物理性质1.下表是四种花的提取液实验(酒精用于提取花中的色素)
⑴上表中能做酸碱指示剂的花汁是 ;
⑵将厨房中的少量白醋滴入大红花的花汁中,可以看到的现象是______;
⑶若将紫罗兰提取液滴入氯化钠溶液中,则可看到的现象是_________。 大红花、紫罗兰橙色紫色六.当堂训练 (15分钟)必做题2.能使紫色石蕊溶液变蓝的溶液,它能使无色酚酞溶液 ( )
A.变红色 B.变蓝色 C.呈无色 D.变紫色 A3.下列物质的水溶液能使紫色石蕊溶液变红色的
是 ( )
A.NaCl B.NH3 C.HCl D.NaOH C盐类、中性变成氨水
后是碱类盐酸是酸类是碱类4.下列物质的水溶液不能使紫色石蕊溶液变色的
是( )
A.NaCl B.NH3 C.HCl D.NaOH A5.下列物质露置于空气中,质量不变的是 ( )
A.石灰水 B.碳酸钙
C.浓盐酸 D.浓硫酸
6.某溶液滴加酚酞显无色,则该溶液 ( )
A. 一定是碱溶液 B .一定是酸溶液
C .一定是盐溶液 D. 可能是酸溶液BD1.小华在一张滤纸上用蘸有某溶液的玻璃棒在上面写“化学”两字,再将其悬挂于铁架台上,并在滤纸的下方放置一盛有某溶液的烧杯,过一会儿,发现滤纸上显示红色“化学”二字,则滤纸上的指示剂和烧杯中的溶液分别是( )AD(选做题)多选题2.下列检验物质导电性的实验中,不亮的灯泡是( ) A
3.碱溶液具有相似的化学性质是因为碱在水溶液中能解离出_________和___________,即在不同的碱溶液中都含有相同的___________。 学生自学,教师巡视1 (2分钟)1.2.酸溶液具有相似的化学性质是因为酸在水溶液中能解离出________和__________,即在不同的酸溶液中都含有相同的_________;
3.碱溶液具有相似的化学性质是因为碱在水溶液中能解离出_________和___________,即在不同的碱溶液中都含有相同的___________。 氢离子酸根离子氢离子金属离子氢氧根离子氢氧根离子盐酸硫酸氢氧化钠溶液氢氧化钙溶液蒸馏水乙醇1.自学检测1 2分钟××有些溶液具有导电性,有些溶液不具有导电性HCl溶液 H2SO4溶液 NaOH溶液 Ca(OH)2溶液HCl H2SO4 NaOH Ca(OH)2溶液:溶质:溶解于水时“解离”出带电的粒子物质导电原因HCl → H+ + Cl-H2SO4→ 2 H+ + SO42-NaOH → Na+ + OH-Ca(OH)2→ Ca2+ + 2 OH- 酸在水溶液中都能解离出H+和酸根离子,即在不同的酸溶液中都含有相同的H+,所以酸有一些相似的性质。碱溶液中也含有相同的OH-,所以,碱也有一些相似的性质。学生讨论,教师点拨1: 2分钟电离时产生的阳离子全部是氢离子(H+)的化合物。 电离时产生的阴离子全部是氢氧根离子(OH-)的化合物。酸碱的概念:酸:碱:NaCl=Na++Cl-K2CO3=2K++CO32-CaCl2=Ca2++2Cl-Na2CO3=2Na++CO32-盐的概念:盐:由金属离子和酸根离子构成的。
盐在水溶液中能电离出金属离子和酸根离子。学生自学,教师巡视2: (4分钟)1.化合物可分为氧化物、酸 、碱 、盐。常见的酸有 、 、 、 。
常见的碱有 、 。
2. 能跟酸或碱的溶液起作用而显示不同的颜色的物质叫
做 。简称 。
3.石蕊溶液遇酸溶液变成 色,遇碱溶液变成 色;
酚酞溶液遇酸溶液 色,遇碱溶液变成 色。上述属于酸溶液的是 ;
上述属于碱溶液的是 。 酸碱指示剂1.化合物可分为氧化物、酸 、碱 、盐。常见的酸有 、 、 、 。
常见的碱有 、 。
2. 能跟酸或碱的溶液起作用而显示不同的颜色的物质叫
做 。简称 。
3.石蕊溶液遇酸溶液变成 色,遇碱溶液变成 色;
酚酞溶液遇酸溶液 色,遇碱溶液变成 色。红色无色红色无色蓝色蓝色红色红色上述属于酸溶液的是 ;
上述属于碱溶液的是 。 食醋和盐酸石灰水和氢氧化钠4.酸碱指示剂指示剂醋酸盐酸氢氧化钠氢氧化钙硫酸碳酸红蓝不变红酸碱指示剂自学检测2.1:2分钟变红变蓝不变色变红仍为紫色仍为无色学生讨论,教师点拨1:2分钟(如NaCl溶液)★点拨:是指示剂在变色,不是酸溶液和碱溶液在变色。可以说:石蕊溶液遇酸变红 或 酸使石蕊溶液变红。
不能说:石蕊溶液使酸变红。变红变红变蓝不变色中性溶液能使石蕊溶液变红的一定是酸吗?是酸性溶液小结:酸碱指示剂:能跟酸或碱的溶液起作用而显示不同颜色的物质叫酸碱指示剂(也叫指示剂)。常用指示剂:石蕊溶液和酚酞溶液指示剂:变色规律:紫色石蕊溶液:
遇酸变红色,遇碱变蓝色遇酸不变色,遇碱变红色无色酚酞溶液: 取少量该溶液,滴入几滴石蕊试液,若溶液呈现蓝色;
或取少量该溶液,滴入几滴无色的酚酞试液,若溶液呈现红色,则说明该溶液为碱性溶液。如何用酸碱指示剂检验溶液的酸碱性?检验溶液是酸性的方法: 取少量该溶液,滴入几滴石蕊试液,若溶液呈现红色,则说明该溶液为酸性溶液。检验溶液为碱性的方法:自学检测2.2:1分钟月季花牵牛花紫萝卜美人焦胡萝卜紫包菜植物色素易溶解在酒精溶液中自制指示剂原料1.上述实验结果,哪些不可以作酸碱指示剂?2.上述实验结果,哪些可以作酸碱指示剂?代用指示剂的颜色牵牛花、月季花、紫卷心菜。
因为在酸、碱溶液里呈显不同的颜色。自学检测2.3:2分钟金盈菊花瓣汁,因为在酸、碱溶液中没有变色。学生自学,教师巡视3 (3分钟)酸物理性质及用途1.浓盐酸、浓硫酸物理性质 2. 分别盛放浓盐酸和浓硫酸的两个试剂瓶,敞口放置一段时间后(不考虑水分的蒸发),两瓶酸的质量、质量分数各有何变化?应如何保存?3.酸的用途:浓硫酸可做 。1.浓盐酸、浓硫酸物理性质无色液体瓶口出现白雾刺激性气味无色、粘稠状液体无明显现象无味有挥发性有吸水性 2. 分别盛放浓盐酸和浓硫酸的两个试剂瓶,敞口放置一段时间后(不考虑水分的蒸发),两瓶酸的质量、质量分数各有何变化?减少减小增加减小不变不变自学检测3:2分钟3.酸的用途:浓硫酸可做 。干燥剂酸物理性质密封保存应如何保存?学生讨论,教师点拨1: 4分钟 从浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气接触形成盐酸小液滴.浓盐酸瓶口为什么有白雾?浓盐酸特性: 挥发性 讨论1浓硫酸特性:吸水性用途:做某些气体的干燥剂——酸性干燥剂通入液面下H2、H2OH2讨论2哪些气体能用浓硫酸来干燥?哪些不能用?干燥原理:干燥剂只吸收水分, 但不与被干燥的气体发生反应。注意:长管进,短管出(长进短出)洗气瓶能干燥不能干燥:碱性气体:NH3酸性气体:CO2 、SO2、 HCl小 结1、盐酸(HCl):常温下是无色有刺激性气味的液体,
有挥发性。
2、浓硫酸:无色、粘稠状液体,有吸水性 能跟酸或碱的溶液起作用而显示不同的颜色的物质叫做酸碱指示剂。简称指示剂。二、酸碱指示剂:变红变蓝不变色变红仍为紫色仍为无色电离时产生的阳离子全部是氢离子(H+)的化合物叫做酸;
电离时产生的阴离子全部是氢氧根离子(OH-)的化合物叫做碱。一、酸碱的概念:三、常见的酸物理性质1.下表是四种花的提取液实验(酒精用于提取花中的色素)
⑴上表中能做酸碱指示剂的花汁是 ;
⑵将厨房中的少量白醋滴入大红花的花汁中,可以看到的现象是______;
⑶若将紫罗兰提取液滴入氯化钠溶液中,则可看到的现象是_________。 大红花、紫罗兰橙色紫色六.当堂训练 (15分钟)必做题2.能使紫色石蕊溶液变蓝的溶液,它能使无色酚酞溶液 ( )
A.变红色 B.变蓝色 C.呈无色 D.变紫色 A3.下列物质的水溶液能使紫色石蕊溶液变红色的
是 ( )
A.NaCl B.NH3 C.HCl D.NaOH C盐类、中性变成氨水
后是碱类盐酸是酸类是碱类4.下列物质的水溶液不能使紫色石蕊溶液变色的
是( )
A.NaCl B.NH3 C.HCl D.NaOH A5.下列物质露置于空气中,质量不变的是 ( )
A.石灰水 B.碳酸钙
C.浓盐酸 D.浓硫酸
6.某溶液滴加酚酞显无色,则该溶液 ( )
A. 一定是碱溶液 B .一定是酸溶液
C .一定是盐溶液 D. 可能是酸溶液BD1.小华在一张滤纸上用蘸有某溶液的玻璃棒在上面写“化学”两字,再将其悬挂于铁架台上,并在滤纸的下方放置一盛有某溶液的烧杯,过一会儿,发现滤纸上显示红色“化学”二字,则滤纸上的指示剂和烧杯中的溶液分别是( )AD(选做题)多选题2.下列检验物质导电性的实验中,不亮的灯泡是( ) A
